Первичный васкулит центральной нервной системы
Первичный васкулит (ПВ) центральной нервной системы (ЦНС) — редкое заболевание, вовлекающее исключительно сосуды головного, реже спинного мозга и их оболочек, причина которого до настоящего времени остается нераскрытой, а клиническая диагностика сопряжена с немалыми трудностями. В литературе ПВЦНС также описывается под названиями: первичный ангиит ЦНС, изолированный васкулит (ангиит) ЦНС [1—4]. Термин ПВЦНС закреплен в номенклатуре васкулитов, принятой на международной конференции, состоявшейся в 2012 г. и посвященной ее пересмотру (International Chapel Hill Consensus Conference Nomenclature of Vasculitides), и отнесен к рубрике васкулитов одного органа [5]. Термин «первичный» подразумевает, что васкулит не является вторичным по отношению к каким-либо другим заболеваниям. Ко вторичным васкулитам, с которыми необходимо дифференцировать ПВЦНС, относятся болезнь Такаясу, гигантоклеточный артериит (поражение артерий крупного калибра), узелковый периартериит, болезнь Кавасаки (поражение артерий среднего размера), васкулиты, ассоциированные с антинейтрофильными цитоплазматическими антителами, иммунокомплексные васкулиты (поражение мелких артерий), болезнь Бехчета (поражение сосудов различного калибра), а также васкулиты при системных заболеваниях (системная красная волчанка и другие ревматологические заболевания) и васкулиты, связанные с вероятной этиологией (гепатит С и В, сифилис, онкология, иммунные, лекарственные и др.
Распространенность васкулитов ЦНС с точностью неизвестна, поскольку их часто не распознают из-за неспецифичности клинических проявлений, отсутствия серологических маркеров воспаления, а также в связи с тем, что церебральная ангиография, магнитно-резонансная томография (МРТ) головного мозга и биопсия головного мозга могут давать ложноположительные и/или ложноотрицательные результаты. Данные об относительной частоте ПВЦНС и вторичных васкулитов с поражением ЦНС противоречивы. Одни авторы указывают, что частота ПВЦНС составляет 1,2% от всех васкулитов, поражающих ЦНС [11], и что они встречаются реже, чем системные васкулиты с поражением ЦНС [2, 7]. В отличие от этого данные клиники Mayo свидетельствуют о преобладании ПВЦНС среди всех васкулитов с поражением ЦНС [12].
Данные об относительной частоте ПВЦНС и вторичных васкулитов с поражением ЦНС противоречивы. Одни авторы указывают, что частота ПВЦНС составляет 1,2% от всех васкулитов, поражающих ЦНС [11], и что они встречаются реже, чем системные васкулиты с поражением ЦНС [2, 7]. В отличие от этого данные клиники Mayo свидетельствуют о преобладании ПВЦНС среди всех васкулитов с поражением ЦНС [12].
К 1986 г. в англоязычной литературе было опубликовано всего 46 наблюдений ПВЦНС [13]. В последние годы благодаря совершенствованию инструментально-лабораторной базы, они распознаются чаще, чем ранее, особенно по сравнению со вторичными васкулитами, что отражается и в росте числа публикаций, посвященных ПВЦНС [2—4, 6—10, 14—23].
По данным клиники Mayo, располагающей наибольшим числом наблюдений ПВЦНС, верифицированных с помощью ангиографии или биопсии головного мозга (101 больной к 2007 г. и 163 больных к 2015 г.), его ежегодная частота у взрослых составляет 2,4 случая на 1 млн населения [10, 20]. Возраст больных в этой серии наблюдений, а также среди еще одной большой группы больных (102 пациента), описанных французскими исследователями [24], колебался от 17 до 85 лет, составляя в среднем 48 лет. M. Lucke и R. Hajj-Ali отмечают, что пик заболевания приходится на возраст 50 лет [22]. Заболевание встречается не только у взрослых, но и у детей [6, 25]. Гендерные различия в больших сериях наблюдений, представленных в литературе американскими и французскими исследователями, не были существенны: первые отмечали небольшое преобладание женщин (56%) [19], вторые — мужчин (53%) [17]. В отдельных небольших сериях больных, упомянутых в обзоре J. Birnbaum и D. Hellman, отмечено двукратное преобладание мужчин [4]. Среди детей ПВЦНС чаще встречается у мальчиков (62—74%) [25, 26]. M. Twilt и S. Benseler отмечают отличия гендерного распределения у детей в зависимости от калибра пораженных артерий: васкулит с поражением мелких артерий чаще встречается у девочек, с поражением средних и крупных артерий — у мальчиков [6].
Возраст больных в этой серии наблюдений, а также среди еще одной большой группы больных (102 пациента), описанных французскими исследователями [24], колебался от 17 до 85 лет, составляя в среднем 48 лет. M. Lucke и R. Hajj-Ali отмечают, что пик заболевания приходится на возраст 50 лет [22]. Заболевание встречается не только у взрослых, но и у детей [6, 25]. Гендерные различия в больших сериях наблюдений, представленных в литературе американскими и французскими исследователями, не были существенны: первые отмечали небольшое преобладание женщин (56%) [19], вторые — мужчин (53%) [17]. В отдельных небольших сериях больных, упомянутых в обзоре J. Birnbaum и D. Hellman, отмечено двукратное преобладание мужчин [4]. Среди детей ПВЦНС чаще встречается у мальчиков (62—74%) [25, 26]. M. Twilt и S. Benseler отмечают отличия гендерного распределения у детей в зависимости от калибра пораженных артерий: васкулит с поражением мелких артерий чаще встречается у девочек, с поражением средних и крупных артерий — у мальчиков [6].
Одни из первых описаний ПВЦНС были сделаны в 50-е годы прошлого столетия W. Newman, A. Wolf [27] и H. Cravioto, I. Feigin [28]. Так как методом верификации ПВЦНС было патоморфологическое исследование, заболевание считалось фатальным. В 80-е годы число публикаций значительно возросло благодаря широкому применению в клинике инвазивной контрастной ангиографии, позволившей верифицировать васкулиты по характерному признаку — чередованию участков сужения и расширения артерий. Большинство описанных случаев не были верифицированы патоморфологически, что в некоторых из них не исключало гипердиагностику [23].
В 1988 г. американские ревматологи L. Calabrese, J. Mallek [13] на основе анализа 8 собственных и 40 случаев, описанных в литературе, предложили следующие диагностические критерии ПВЦНС, поражающего мелкие артерии: 1) наличие неврологического или психического дефекта, необъяснимого другими причинами; 2) наличие классических ангиографических признаков (распространенные чередующиеся участки расширения и сужения мелких артерий) или гистопатологических проявлений ПВЦНС; 3) отсутствие признаков системного васкулита или любых других заболеваний, которые могли бы вызвать такую же ангиографическую картину.
К концу ХХ века стало очевидным, что случаи ПВЦНС с доброкачественным течением, благоприятным прогнозом и ангиографическими изменениями в виде чередующихся участков сужения и расширения в действительности могут представлять собой не васкулит, а невоспалительную обратимую церебральную ангиопатию [29, 30], для обозначения которой L. Calabrese и соавт. [31] предложили термин «обратимый церебральный вазоконстрикторный синдром» (англ.: reversible cerebral vasoconstriction syndrome — RCVS). Это основное заболевание, которое может имитировать ПВЦНС.
В первой декаде 2000-х годов было предложено разделять ПВЦНС в зависимости от калибра пораженных сосудов. Васкулиты мелких артерий также обозначаются как ангиографически негативные, поскольку их верификация возможна только при биопсии головного мозга. Васкулиты средних/крупных артерий — как ангиографически позитивные [8, 10, 15]. Необходимость такого разделения продиктована отличием их клинических проявлений, течения, диагностических и лечебных подходов. Следует отметить, что понятия васкулит мелких артерий и ангиографически негативный васкулит не всегда равнозначны, так как иногда васкулит мелких артерий верифицируется при контрастной ангиографии [19]. Согласно международной номенклатуре васкулитов, принятой в 2012 г. [5], к крупным артериям относятся аорта и ее ветви, к средним — основные висцеральные артерии и отходящие от них ветви, к мелким — интрапаренхиматозные артерии, артериолы, капилляры. Применительно к головному мозгу крупными считаются внутренняя сонная артерия (ВСА) и позвоночная артерия (ПА), средними — средняя (СМА), передняя (ПМА), задняя (ЗМА) мозговые артерии, базилярная артерия (БА) и их интракраниальные ветви, мелкими — внутримозговые сосуды. Вместе с тем необходимо отметить, что до настоящего времени нет единого подхода к оценке размера сосудов головного мозга, чем, очевидно, отчасти объясняются различия данных американских и французских исследователей.
Следует отметить, что понятия васкулит мелких артерий и ангиографически негативный васкулит не всегда равнозначны, так как иногда васкулит мелких артерий верифицируется при контрастной ангиографии [19]. Согласно международной номенклатуре васкулитов, принятой в 2012 г. [5], к крупным артериям относятся аорта и ее ветви, к средним — основные висцеральные артерии и отходящие от них ветви, к мелким — интрапаренхиматозные артерии, артериолы, капилляры. Применительно к головному мозгу крупными считаются внутренняя сонная артерия (ВСА) и позвоночная артерия (ПА), средними — средняя (СМА), передняя (ПМА), задняя (ЗМА) мозговые артерии, базилярная артерия (БА) и их интракраниальные ветви, мелкими — внутримозговые сосуды. Вместе с тем необходимо отметить, что до настоящего времени нет единого подхода к оценке размера сосудов головного мозга, чем, очевидно, отчасти объясняются различия данных американских и французских исследователей.
Существенным прорывом в неинвазивной верификации васкулитов крупных и средних артерий стало использование высокоразрешающей МРТ с толщиной срезов не более 3 мм для оценки состояния артериальной стенки до и после введения контраста. С помощью этого метода T. Bley и соавт. в 2005 г. показали возможность выявления воспалительных изменений по накоплению контраста в стенке поверхностной височной артерии у больных с гигантоклеточным артериитом [32]. Причем чувствительность и специфичность МРТ и гистологических методов диагностики в этих случаях были сходными (около 80 и 100% соответственно). В 2007—2008 гг. W. Kuker и соавт. для верификации воспаления в крупных артериях мозга (интракраниальные отделы ВСА и ПА, начальные отделы СМА, ПМА, ЗМА и БА) предложили проведение мультипланарной высокоразрешающей МРТ в режиме Т1 с подавлением сигнала от жировой ткани до и после введения контраста, которая позволяет обнаружить утолщение артериальной стенки и накопление в ней контраста [33—35]. В 2010 г. T. Saam и соавт. предложили протокол проведения высокоразрешающей МРТ с подавлением сигнала не только от жировой ткани, но и от движущейся крови (режим Dark blood — черная кровь) для верификации васкулита интракраниальных и цервикальных артерий [36].
С помощью этого метода T. Bley и соавт. в 2005 г. показали возможность выявления воспалительных изменений по накоплению контраста в стенке поверхностной височной артерии у больных с гигантоклеточным артериитом [32]. Причем чувствительность и специфичность МРТ и гистологических методов диагностики в этих случаях были сходными (около 80 и 100% соответственно). В 2007—2008 гг. W. Kuker и соавт. для верификации воспаления в крупных артериях мозга (интракраниальные отделы ВСА и ПА, начальные отделы СМА, ПМА, ЗМА и БА) предложили проведение мультипланарной высокоразрешающей МРТ в режиме Т1 с подавлением сигнала от жировой ткани до и после введения контраста, которая позволяет обнаружить утолщение артериальной стенки и накопление в ней контраста [33—35]. В 2010 г. T. Saam и соавт. предложили протокол проведения высокоразрешающей МРТ с подавлением сигнала не только от жировой ткани, но и от движущейся крови (режим Dark blood — черная кровь) для верификации васкулита интракраниальных и цервикальных артерий [36].
К настоящему времени наибольшее число больных (более 100 наблюдений) с ПВЦНС, поражающим сосуды разного калибра, обследованы в клинике Mayo (США) [19] и во Франции [16, 17]. Несмотря на накопившиеся новые данные и появившиеся диагностические возможности, критерии диагностики ПВЦНС, разработанные около 30 лет назад для мелких артерий, остаются прежними и используются для артерий разного калибра. Сложность и малоизученность проблемы ПВЦНС инициировали объединение усилий исследователей разных стран для проведения международного исследования [37].
Морфологические изменения при ПВЦНСВыделяют 3 основных гистопатологических варианта ПВЦНС [38, 39]. Наиболее частым из них является гранулематозный васкулит, доля которого среди всех ПВЦНС составляет 58%. Он характеризуется наличием вокруг сосудов мононуклеарного воспаления в сочетании с образованием гранулем в разных слоях сосудистой стенки и наличием полинуклеарных клеток.
Лимфоцитарный васкулит составляет 28% всех случаев ПВЦНС и характеризуется выраженной инфильтрацией сосудистой стенки лимфоцитами, а иногда и плазматическими клетками, что ведет к ее дезорганизации и деструкции. Наличие отдельных периваскулярных мононуклеарных клеток не является основанием для диагностики лимфоцитарного васкулита. Значительная лимфоцитарная инфильтрация вещества головного мозга при лимфоцитарном васкулите отсутствует [39].
Значительная лимфоцитарная инфильтрация вещества головного мозга при лимфоцитарном васкулите отсутствует [39].
Некротизирующий васкулит встречается в 14% случаев и обычно поражает небольшие артерии мышечного типа. Морфологически изменения напоминают таковые при узелковом полиартериите и характеризуются трансмуральным фибриноидным некрозом с деструкцией внутренней эластической мембраны. Некроз сосудистой стенки является причиной внутримозговых кровоизлияний и микроаневризм. Состояние сосудистой стенки при дифференциальном диагнозе васкулита с другими причинами острых некрозов или кровоизлияний в мозге должно оцениваться вне зон этих повреждений, так как в их пределах изменения сосудистой стенки носят вторичный характер и не являются признаком васкулита [39]. Ишемические изменения в биоптатах головного мозга при ПВЦНС обнаруживаются в 40—51% случаев, чаще всего при некротизирующем васкулите, кровоизлияния — в 12% [39]. Морфологические изменения при ПВЦНС, как правило, обнаруживаются в артериях небольшого и среднего калибра и артериолах, тогда как в венах они выявляются редко [11]. В отдельных случаях находят изолированное поражение вен небольшого и среднего калибра белого вещества полушарий головного мозга и его мягкой мозговой оболочки. В наблюдении J. Mlakar и соавт. оно было представлено гранулематозным воспалением вен в виде аккумуляции эпителиоидных макрофагов с лимфоцитами, расположенными по периферии гранулемы, и отдельными гигантскими клетками типа Лангерганса, рассеянными среди макрофагов и лимфоцитов. Поскольку эндотелий вен практически был интактен, предполагалось, что патогенный антиген, вызвавший воспалительную реакцию вокруг вен, распространялся со стороны их адвентиции [42] и имел сродство к венам.
В отдельных случаях находят изолированное поражение вен небольшого и среднего калибра белого вещества полушарий головного мозга и его мягкой мозговой оболочки. В наблюдении J. Mlakar и соавт. оно было представлено гранулематозным воспалением вен в виде аккумуляции эпителиоидных макрофагов с лимфоцитами, расположенными по периферии гранулемы, и отдельными гигантскими клетками типа Лангерганса, рассеянными среди макрофагов и лимфоцитов. Поскольку эндотелий вен практически был интактен, предполагалось, что патогенный антиген, вызвавший воспалительную реакцию вокруг вен, распространялся со стороны их адвентиции [42] и имел сродство к венам.
До настоящего времени этиология и патогенез остаются недостаточно изученными [22]. В литературе широко обсуждается роль инфекции, особенно учитывая частый гранулематозный и лимфоцитарный типы воспаления, выявляемые при морфологическом исследовании. В качестве этиологических факторов придается значение вирусу ветрянки (Varicella zoster virus — VZV) [43—45], вирусу Эпштейна—Барр [46], вирусу лихорадки Западного Нила [47] и вирусу иммунодефицита человека [48]. Необходимо подчеркнуть, что патогенные агенты исполняют роль провоцирующего фактора, приводящего к развитию иммунного воспаления в сосудистой стенке, и что ПВЦНС не относится к инфекционным васкулитам. Наиболее ярко это демонстрируется на примере вируса VZV. После перенесенной общей инфекции (ветряная оспа) вирус в латентной форме персистирует в тригеминальном и цереброспинальных ганглиях. При снижении иммунитета вирус активируется и трансаксонально может достигать стенки ВСА (из тригеминального ганглия) или ПА (из верхних цереброспинальных ганглиев), инициируя в них воспалительные изменения, в генезе которых определяющая роль принадлежит иммунным реакциям. Клиническим подтверждением роли VZV в поражении церебральных артерий является повышение частоты инсультов после перенесенной VZV-инфекции.
В качестве этиологических факторов придается значение вирусу ветрянки (Varicella zoster virus — VZV) [43—45], вирусу Эпштейна—Барр [46], вирусу лихорадки Западного Нила [47] и вирусу иммунодефицита человека [48]. Необходимо подчеркнуть, что патогенные агенты исполняют роль провоцирующего фактора, приводящего к развитию иммунного воспаления в сосудистой стенке, и что ПВЦНС не относится к инфекционным васкулитам. Наиболее ярко это демонстрируется на примере вируса VZV. После перенесенной общей инфекции (ветряная оспа) вирус в латентной форме персистирует в тригеминальном и цереброспинальных ганглиях. При снижении иммунитета вирус активируется и трансаксонально может достигать стенки ВСА (из тригеминального ганглия) или ПА (из верхних цереброспинальных ганглиев), инициируя в них воспалительные изменения, в генезе которых определяющая роль принадлежит иммунным реакциям. Клиническим подтверждением роли VZV в поражении церебральных артерий является повышение частоты инсультов после перенесенной VZV-инфекции.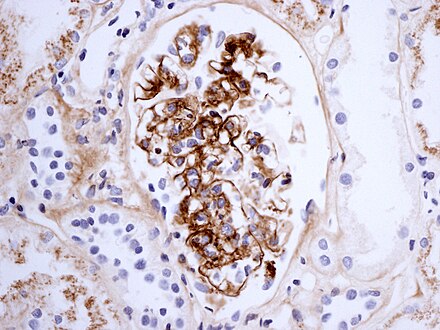 Данные иммуногистохимического исследования, обнаружившие присутствие антигена VZV в адвентиции на начальных стадиях заболевания, а позже — в медии и интиме, также подтверждают роль трансаксонально распространяющегося VZV в поражении сосудистой стенки. Ее изменение представлено утолщением интимы, миоциты которой экспрессируют актин и миозин [45]. Подтверждением иммунных механизмов служит эффект от лечения кортикостероидами и иммуносупрессантами [21].
Данные иммуногистохимического исследования, обнаружившие присутствие антигена VZV в адвентиции на начальных стадиях заболевания, а позже — в медии и интиме, также подтверждают роль трансаксонально распространяющегося VZV в поражении сосудистой стенки. Ее изменение представлено утолщением интимы, миоциты которой экспрессируют актин и миозин [45]. Подтверждением иммунных механизмов служит эффект от лечения кортикостероидами и иммуносупрессантами [21].
Значение иммунных механизмов в генезе ПВЦНС подчеркивается случаями его развития у больных с первичным и приобретенным иммунодефицитом. Предполагается, что определенное значение имеет система гистосовместимости классов I и II. Ее типирование у больной с изолированным васкулитом обеих ВСА обнаружило HLA-аллели, ассоциирующиеся с болезнью Такаясу (B52), болезнью Бехчета (В51), гигантоклеточным артериитом (DR 4), тогда как клинико-лабораторных признаков этих заболеваний у больной не было [49].
Фундаментальное значение в раскрытии триггерной роли вирусов и роли иммунной системы в развитии первичного васкулита крупных и средних артерий представляет работа C. Weyand и соавт., посвященная изучению механизмов развития воспаления в стенке крупных артерий на модели гигантоклеточного артериита, в генезе которого придается значение герпетической инфекции [50]. Отличительной чертой этих артерий является наличие в их адвентиции и медии дендритных клеток, которые осуществляют взаимодействие сосудистой стенки и иммунной системы. При васкулите они трансформируются, увеличиваются в количестве, распределяются по всей стенке и участвуют в прогрессировании заболевания. Предполагается, что стимуляция дендритных клеток осуществляется через Тoll-подобные рецепторы, причем в качестве стимула (локального или системного) рассматриваются различные инфекционные агенты. Стимуляция дендритных клеток вызывает активацию иммунной системы с притоком в артериальную стенку Т-клеток, преимущественно CD4 Т-клеток и макрофагов. Они проникают в стенку по собственным сосудам артерий (vasa vasorum), переходят в межклеточное пространство и направляются от адвентиции к интиме. В типичной ситуации высокоактивированные макрофаги, известные как гистиоциты, собираются в гранулемы, которые окружены Т-клетками.
Weyand и соавт., посвященная изучению механизмов развития воспаления в стенке крупных артерий на модели гигантоклеточного артериита, в генезе которого придается значение герпетической инфекции [50]. Отличительной чертой этих артерий является наличие в их адвентиции и медии дендритных клеток, которые осуществляют взаимодействие сосудистой стенки и иммунной системы. При васкулите они трансформируются, увеличиваются в количестве, распределяются по всей стенке и участвуют в прогрессировании заболевания. Предполагается, что стимуляция дендритных клеток осуществляется через Тoll-подобные рецепторы, причем в качестве стимула (локального или системного) рассматриваются различные инфекционные агенты. Стимуляция дендритных клеток вызывает активацию иммунной системы с притоком в артериальную стенку Т-клеток, преимущественно CD4 Т-клеток и макрофагов. Они проникают в стенку по собственным сосудам артерий (vasa vasorum), переходят в межклеточное пространство и направляются от адвентиции к интиме. В типичной ситуации высокоактивированные макрофаги, известные как гистиоциты, собираются в гранулемы, которые окружены Т-клетками. В месте повреждения сосудов при васкулите обнаруживается множество эффекторных цитокинов. Выделяют два основных кластера цитокинов, связанных с развитием воспаления сосудистой стенки и активностью заболевания. Для первого из них центром является ось IL-6/IL-17, для второго — IL-12/IFN-γ. Предполагается, что первый кластер связан с остротой процесса, учитывая его высокую чувствительность к кортикостероидной терапии. Активация второго кластера цитокинов ответственна за переход заболевания в хроническую стадию. Наблюдающаяся при этом активация макрофагов с выделением сосудистых ростковых факторов, металлопротеиназ вызывает деградацию экстраклеточного матрикса сосудистой стенки, усиливает провоспалительную активность эндотелия и пролиферацию гладкомышечных клеток. В сосудистой стенке IFN-γ запускает сигнальные пути миграции и пролиферации для гладкомышечных клеток, что приводит к сужению просвета сосуда гиперплазированной интимой, формированию неоваскулярной сети капилляров. IFN-γ может вызывать не только пролиферацию, но и апоптоз гладкомышечных клеток, т.
В месте повреждения сосудов при васкулите обнаруживается множество эффекторных цитокинов. Выделяют два основных кластера цитокинов, связанных с развитием воспаления сосудистой стенки и активностью заболевания. Для первого из них центром является ось IL-6/IL-17, для второго — IL-12/IFN-γ. Предполагается, что первый кластер связан с остротой процесса, учитывая его высокую чувствительность к кортикостероидной терапии. Активация второго кластера цитокинов ответственна за переход заболевания в хроническую стадию. Наблюдающаяся при этом активация макрофагов с выделением сосудистых ростковых факторов, металлопротеиназ вызывает деградацию экстраклеточного матрикса сосудистой стенки, усиливает провоспалительную активность эндотелия и пролиферацию гладкомышечных клеток. В сосудистой стенке IFN-γ запускает сигнальные пути миграции и пролиферации для гладкомышечных клеток, что приводит к сужению просвета сосуда гиперплазированной интимой, формированию неоваскулярной сети капилляров. IFN-γ может вызывать не только пролиферацию, но и апоптоз гладкомышечных клеток, т. е. исполнять роль сигнала, который разделяет гладкомышечные клетки на пролиферирующие и погибающие. Особенностью кластера цитокинов, связанных с Тh2-клетками, является его нечувствительность к стероидам и персистирование высокого уровня IFN-γ в крови, несмотря на иммуносупресантную терапию, что поддерживает хроническое воспаление. Дальнейшее изучение данных механизмов поможет выявить маркеры активности заболевания и эффективности проводимого лечения [50].
е. исполнять роль сигнала, который разделяет гладкомышечные клетки на пролиферирующие и погибающие. Особенностью кластера цитокинов, связанных с Тh2-клетками, является его нечувствительность к стероидам и персистирование высокого уровня IFN-γ в крови, несмотря на иммуносупресантную терапию, что поддерживает хроническое воспаление. Дальнейшее изучение данных механизмов поможет выявить маркеры активности заболевания и эффективности проводимого лечения [50].
Клинические проявления ПВЦНС разнообразны и включают головную боль (51—65%), когнитивные нарушения (36%—54%), инсульты (40%), преходящие нарушения мозгового кровообращения (26%), эпилептические приступы (20—35%), снижение уровня бодрствования (26%), психические расстройства (22%), парезы конечностей (5%), снижение зрения (11%), отек дисков зрительных нервов (4%) [17, 19, 51]. Указанная симптоматика в 68% случаев развивается остро, в остальных — имеет постепенно прогрессирующее течение.
Первыми клиническими проявлениями у 71% больных являются инсульты, стойкий неврологический дефицит, головная боль и когнитивные нарушения [19]. Иногда заболевание дебютирует эпилептическими приступами [52].
Клинические проявления зависят от калибра пораженных сосудов. Отличительной особенностью васкулита мелких артерий, верифицированного при биопсии мозга, является более частое развитие когнитивных нарушений (67—71%), чем при поражении крупных/средних артерий, верифицированном при ангиографии (36—47%) [17, 19]. H. De Boysson и соавт. [17] отмечают также более молодой возраст больных с поражением мелких артерий (41,5 года против 48,5 года при поражении артерий среднего/крупного калибров), более частое развитие у них эпилептических приступов (77% против 21%), дискинезий (35% против 9%), снижения уровня бодрствования (42% против 21%). Отличительной особенностью клинических проявлений артериита крупных/средних артерий является более частое развитие преходящих нарушений мозгового кровообращения, инсультов, очаговых неврологических нарушений, частота которых достигает 50—88% [17, 19]. M. Lucke и R. Hajj-Ali обращают внимание на то, что нарушения мозгового кровообращения развиваются в разных сосудистых бассейнах и часто сочетаются с воспалительными изменениями в цереброспинальной жидкости (ЦСЖ) [22]. Наряду с неврологической симптоматикой у 10% больных, по данным клиники Mayo, отмечаются повышенная утомляемость, снижение аппетита, потеря массы тела, артралгии, а у 14% больных — повышение температуры [19].
M. Lucke и R. Hajj-Ali обращают внимание на то, что нарушения мозгового кровообращения развиваются в разных сосудистых бассейнах и часто сочетаются с воспалительными изменениями в цереброспинальной жидкости (ЦСЖ) [22]. Наряду с неврологической симптоматикой у 10% больных, по данным клиники Mayo, отмечаются повышенная утомляемость, снижение аппетита, потеря массы тела, артралгии, а у 14% больных — повышение температуры [19].
Описания серии больных с васкулитом крупных артерий (ВСА, ПА), верифицированным накоплением контраста в их стенке, в литературе отсутствуют. Имеются лишь сообщения об отдельных пациентах, ишемические инсульты у которых имели тенденцию к рецидивам с развитием в пределах одной сосудистой системы (вертебрально-базилярной или каротидной) [49, 53]. На ранней стадии заболевания просвет артерий мог быть не стенозирован, тогда как при МРТ-исследовании выявлялось накопление контраста артериальной стенкой — признак ее воспалительных изменений [53]. После лечения стероидами одни авторы [53, 54] наблюдали исчезновение или уменьшение накопления контраста сосудистой стенкой, другие [49] отмечали его персистирование на протяжении 6 мес при положительном клиническом эффекте.
Среди ПВЦНС с поражением мелких артерий выделяют ангиит, характеризующийся отложением β-амилоидного пептида в мелких артериях коры и лептоменингеальной оболочке (ABRA) [19, 55]. Он развивается в более пожилом возрасте, чаще дебютирует когнитивными нарушениями и эпилептическими приступами, характеризуется повышением белка в ЦСЖ, частым накоплением контраста оболочками головного мозга при МРТ, хорошим эффектом от лечения стероидами (монотерапия или в сочетании с циклофосфамидом).
В рамках ПВЦНС, в основном поражающем мелкие артерии, выделяется опухолеподобная форма [15, 56]. Она развивается в более молодом возрасте (средний возраст 37 лет) и в 90% случаев проявляется эпилептическими приступами. МРТ обнаруживает одиночные или множественные очаги, накапливающие контраст, окруженные отеком и оказывающие объемное воздействие на смежные структуры головного мозга. Очень часто этот подвид ПВЦНС ошибочно рассматривается как опухоль или лимфома. Дифференциальной диагностике с опухолью помогает биопсия головного мозга и МР-спектроскопия. Лечение глюкокортикоидами в сочетании с циклофосфаном дает хороший эффект, однако у половины больных в последующем отмечаются рецидивы, требующие повторного курса лечения [56].
Лечение глюкокортикоидами в сочетании с циклофосфаном дает хороший эффект, однако у половины больных в последующем отмечаются рецидивы, требующие повторного курса лечения [56].
Течение ПВЦНС может быть как прогрессирующим, с повторными обострениями, так и монофазным. Среди 102 больных, описанных H. Boysson и соавт. [17], обострения заболевания происходили в трети случаев, причем чаще при поражении мелких, чем крупных артерий (54% против 24%). К. Maclaren и соавт. также указывают на более частые обострения при поражении мелких артерий [8]. Они происходили на фоне низких поддерживающих доз преднизолона или азатиоприна либо при отмене препаратов. В целом при поражении мелких артерий заболевание протекало тяжелее, с развитием энцефалопатии, проявляющейся когнитивными нарушениями и эпилептическими приступами, тогда как при поражении средних и крупных артерий обычно имелся очаговый неврологический дефицит, обусловленный инсультом. Функциональное состояние больных, по данным динамического наблюдения, продолжавшегося в среднем 53 мес, существенно не зависело от калибра пораженных артерий [17].
В отличие от данных H. Boysson и соавт. [17] C. Salvarani и соавт. [19—21] указывают на более тяжелое, быстро прогрессирующее течение заболевания у больных с двусторонними, множественными изменениями церебральных артерий по данным ангиографии и множественными инфарктами головного мозга на МРТ, тогда как при поражении мелких артерий течение заболевания более доброкачественное. Функциональный неврологический дефицит в среднем через год от дебюта заболевания был больше при васкулите, верифицированном ангиографически, чем при васкулите мелких артерий, включая амилоидассоциированный васкулит, встречающийся в более старшей возрастной группе.
Различия между данными французских и американских исследователей, возможно, связаны с селекцией больных, разной стандартизацией калибра артерий головного мозга (мелкие, средние, крупные), а также с преобладанием у больных, описанных H. Boysson и соавт., лимфоцитарного васкулита [17].
Как американские, так и французские исследователи указывают на зависимость течения заболевания, а именно частоты рецидивов, от проводимого лечения. Так, C. Salvarani и соавт. отметили меньшую частоту рецидивов, если в дебюте заболевания кортикостероиды сочетали с циклофосфаном, а не применяли как монотерапию (18% против 39%) [20]. H. Boysson и соавт. указывают на более редкие обострения и лучший функциональный исход, если после лечения в острой стадии заболевания продолжается поддерживающая терапия [24].
Так, C. Salvarani и соавт. отметили меньшую частоту рецидивов, если в дебюте заболевания кортикостероиды сочетали с циклофосфаном, а не применяли как монотерапию (18% против 39%) [20]. H. Boysson и соавт. указывают на более редкие обострения и лучший функциональный исход, если после лечения в острой стадии заболевания продолжается поддерживающая терапия [24].
У 10% больных ПВЦНС имеет катастрофическое течение, для которого характерно быстрое, в течение нескольких дней снижение уровня бодрствования и появление дыхательных нарушений. Если в течение первых недель не наступает летальный исход, функциональное состояние больных к концу лечения не отличается от такового при менее тяжелом течении заболевания [57].
Смертность при ПВЦНС среди 163 больных, наблюдавшихся C. Salvarani и соавт., составила 15% [19]. Чаще всего летальный исход наступал в течение первого года заболевания при гранулематозном и некротизирующем васкулите. Во французской когорте, включавшей в разные временны́е сроки 52 и 102 больных, летальный исход отмечен в 6—8% случаев соответственно. В половине случаев смерть наступала в первые надели заболевания, в остальных — при очередном обострении [16, 17].
В половине случаев смерть наступала в первые надели заболевания, в остальных — при очередном обострении [16, 17].
Она основывается на описанных выше критериях, предложенных в 1988 г. L. Calabrese и J. Mallek [13]. Несмотря на успехи, достигнутые в изучении ПВЦНС, его диагностика до настоящего времени представляет значительные трудности. На это указывает длительный временной интервал (170 дней) между дебютом заболевания и его диагностикой [14]. Диагностические трудности во многом связаны отсутствием специфичных и чувствительных лабораторно-инструментальных тестов, в связи с чем большое значение имеет комплексная оценка клинико-лабораторно-инструментальных данных.
Исследование крови. Специфичные и чувствительные для ПВЦНС серологические маркеры отсутствуют [15]. В наиболее многочисленных сериях ПВЦНС, представленных в литературе, у 18% больных отмечено повышение скорости оседания эритроцитов (СОЭ), у 27—33% — повышение С-реактивного белка, обычно небольшое. Ревматоидный и антинуклеарный факторы, антинейтрофильные цитоплазматические антитела (АНЦА), антитела к экстрагированному ядерному антигену, комплимент, криоглобулины, волчаночный антикоагулянт, ВИЧ были отрицательными или в пределах нормы [16, 19]. Среди небольших групп больных с ПВЦНС в отдельных случаях отмечали небольшое, диагностически незначимое повышение АНЦА и антинуклеарного фактора [8, 51].
Ревматоидный и антинуклеарный факторы, антинейтрофильные цитоплазматические антитела (АНЦА), антитела к экстрагированному ядерному антигену, комплимент, криоглобулины, волчаночный антикоагулянт, ВИЧ были отрицательными или в пределах нормы [16, 19]. Среди небольших групп больных с ПВЦНС в отдельных случаях отмечали небольшое, диагностически незначимое повышение АНЦА и антинуклеарного фактора [8, 51].
Исследование ЦСЖ. Небольшой лимфоцитарный плеоцитоз и/или умеренное повышение белка обнаруживают у 69—94% [10, 15, 17, 22, 51]. Чаще всего изменения выявляют при поражении мелких, чем крупных сосудов [17, 19, 51]. Так, H. de Boysson и соавт. [17] выявили их у 91% больных с васкулитом мелких артерий и 62% больных с поражением крупных/средних артерий. C. Salvarani и соавт. [19] обнаружили повышение белка более 45 мг/дл или лейкоцитов более 5 клеток/мл у 81% пациентов. Более выраженное изменение ЦСЖ отмечено при васкулите мелких артерий, чем крупных (цитоз 16 клеток по сравнению с 4 клетками; белок — 98 мг/дл по сравнению с 56 мг/дл соответственно). Синтез олигоклональных антител S. Schuster и соавт. [51] обнаружили у 35% больных. Исследование ЦСЖ на различные инфекционные агенты с помощью иммуноферментного анализа и полимеразной цепной реакции (ПЦР), а также цитологическое исследование для исключения метастатического поражения не выявляют изменений [15]. F. Pagni и соавт. описали больного с васкулитом спинного мозга, верифицированным на секции, у которого при исследовании ЦСЖ методом ПЦР было найдено большое число копий вируса Эпштейна—Барр при отсутствии признаков острой или хронической инфекции, обусловленной этим вирусом [46].
Синтез олигоклональных антител S. Schuster и соавт. [51] обнаружили у 35% больных. Исследование ЦСЖ на различные инфекционные агенты с помощью иммуноферментного анализа и полимеразной цепной реакции (ПЦР), а также цитологическое исследование для исключения метастатического поражения не выявляют изменений [15]. F. Pagni и соавт. описали больного с васкулитом спинного мозга, верифицированным на секции, у которого при исследовании ЦСЖ методом ПЦР было найдено большое число копий вируса Эпштейна—Барр при отсутствии признаков острой или хронической инфекции, обусловленной этим вирусом [46].
Церебральная ангиография является одним из методов верификации ПВЦНС. Характерные изменения представлены распространенными чередующимися участками сужения и расширения артерий, как правило, двусторонними, окклюзией отдельных сосудов, замедлением времени прохождения контраста, неоваскуляризацией, микроаневризмами, ранним заполнением венозного русла, обеднением дистальных отделов сосудистых бассейнов. Необходимо иметь в виду, что основной ангиографический признак васкулита — чередование участков сужения и расширения артерий — неспецифичен и может наблюдаться при спазме артерий, отеке сосудистой стенке, пролиферации ее клеточных элементов, в связи с чем большое значение имеет комплексный анализ ангиографических и клинических данных. Кроме того, характерные для ПВЦНС изменения выявляются в артериях среднего и крупного калибра, тогда как разрешающие способности ангиографии не позволяют обнаружить их в мелких артериях (менее 0,2 мм) [58].
Необходимо иметь в виду, что основной ангиографический признак васкулита — чередование участков сужения и расширения артерий — неспецифичен и может наблюдаться при спазме артерий, отеке сосудистой стенке, пролиферации ее клеточных элементов, в связи с чем большое значение имеет комплексный анализ ангиографических и клинических данных. Кроме того, характерные для ПВЦНС изменения выявляются в артериях среднего и крупного калибра, тогда как разрешающие способности ангиографии не позволяют обнаружить их в мелких артериях (менее 0,2 мм) [58].
Среди 129 больных с васкулитом, обследованных в клинике Mayo, изменения при ангиографии были найдены в 88% случаев, причем в 96% из них изменения были двусторонними. Частота и распространенность поражения зависели от калибра пораженных сосудов. Поражение крупных артерий (интракраниальный отдел ВСА и ПА, проксимальные отделы СМА, ПМА, ЗМА, БА) выявлялось реже (66%), чем поражение артерий меньшего калибра (дистальные отделы интракраниальных артерий и их ветви второго порядка) (91%). Кроме того, поражение крупных артерий реже было двусторонним (55%) по сравнению с артериями меньшего размера (91%) [19].
Кроме того, поражение крупных артерий реже было двусторонним (55%) по сравнению с артериями меньшего размера (91%) [19].
Нейровизуализация. Изменения вещества головного мозга, выявляемые при МРТ у больных с ПВЦНС, неспецифичны. Они включают корковые и субкортикальные инфаркты, внутримозговые кровоизлияния, накопление контраста оболочками мозга или внутримозговыми очагами, участки повышенной интенсивности сигнала в режиме Т2 или FLAIR [59, 60]. В 5% случаев выявляются изменения в спинном мозге, чаще всего в грудном отделе [60]. При псевдотуморозной форме ПВЦНС обнаруживаются очаги, иногда с зонами некроза, перифокальным отеком, объемным воздействием на смежные структуры, которые накапливают контраст и нередко ошибочно трактуются как злокачественные опухоли или абсцесс [15, 60]. Частота опухолеподобных очагов при ПВЦНС, по данным G. Boulouis и соавт., составляет 12% [61].
По данным клиники Mayo, инфаркты головного мозга при МРТ были найдены у 54% из 149 обследованных больных с ПВЦНС [19]. Чаще их выявляли при ангиографически верифицированном васкулите, т. е. при поражении артерий среднего и крупного размера (66%), чем при васкулите, подтвержденном биопсией, т. е. при поражении мелких артерий (34%). Сходные данные получены S. Schuster и соавт. [51]: инфаркты головного мозга были найдены в 85,7% случаев при поражении крупных артерий, в 29,4% случаев при поражении мелких. C. Thaler и соавт. также указывают на типичность развития инфарктов головного мозга при поражении артерий среднего и крупного калибра: в этом случае они были выявлены у 19 из 25 больных, чаще всего в бассейне СМА, в отличие от этого инфаркты отсутствовали у всех 8 больных с поражением мелких артерий [62]. G. Boulouis и соавт. обнаружили при МРТ головного мозга множественные, двусторонние инфаркты, преимущественно в системе сонных артерий у 42% из 60 больных с ПВЦНС, верифицированным биопсией или ангиографически. В 55% случаев выявляли геморрагические инфаркты и паренхиматозные кровоизлияния, в 26% — острые конвекситальные субарахноидальные кровоизлияния [61].
Чаще их выявляли при ангиографически верифицированном васкулите, т. е. при поражении артерий среднего и крупного размера (66%), чем при васкулите, подтвержденном биопсией, т. е. при поражении мелких артерий (34%). Сходные данные получены S. Schuster и соавт. [51]: инфаркты головного мозга были найдены в 85,7% случаев при поражении крупных артерий, в 29,4% случаев при поражении мелких. C. Thaler и соавт. также указывают на типичность развития инфарктов головного мозга при поражении артерий среднего и крупного калибра: в этом случае они были выявлены у 19 из 25 больных, чаще всего в бассейне СМА, в отличие от этого инфаркты отсутствовали у всех 8 больных с поражением мелких артерий [62]. G. Boulouis и соавт. обнаружили при МРТ головного мозга множественные, двусторонние инфаркты, преимущественно в системе сонных артерий у 42% из 60 больных с ПВЦНС, верифицированным биопсией или ангиографически. В 55% случаев выявляли геморрагические инфаркты и паренхиматозные кровоизлияния, в 26% — острые конвекситальные субарахноидальные кровоизлияния [61].
Почти у всех больных наряду с инфарктами головного мозга при МРТ в режиме Т2 и FLAIR в белом веществе головного мозга обнаруживаются гиперинтенсивные очаги, трактовка которых вызывает диагностические трудности [15, 51].
Накопление контраста очагами или оболочками головного мозга чаще отмечено при васкулите мелких (60—77%), чем крупных (22—29%) артерий [19, 51, 61].
Редкой нейровизуализационной находкой среди больных, описанных S. Schuster и соавт., была выраженная атрофия головного мозга, в основе которой согласно данным биопсии лежало трансмуральное воспаление очень мелких сосудов [51].
При изолированном поражении церебральных вен небольшого и среднего калибра, верифицированном на секции, МРТ головного мозга в режиме Т2 и FLAIR обнаруживает линейной формы гиперинтенсивность в проекции вен и перивенозных пространств белого вещества полушарий головного мозга [42].
Характерными нейровизуализационными признаками амилоидассоциированного ангиита с периваскулярным воспалением, отличающими его от ЦАА, является накопление контраста мягкой мозговой оболочкой с сопутствующим инфильтративным изменением белого вещества полушарий головного мозга или без него (70% против 7%), а также более редкое развитие лобарных кровоизлияний (7% против 62%) [63].
Нейровизуализационное исследование в режиме ангиографии (МРА и КТА) может выявлять чередующиеся участки сужения и расширения артерий с гладкими или неровными контурами, дву- или односторонние. Результаты исследования артерий головного мозга с помощью МРА и КТА зависят от разрешающей способности используемого оборудования. Если ранее считалось, что МРА практически не имеет диагностической значимости, то согласно данным, опубликованным в 2017 г., изменения интракраниальных артерий при МРА были выявлены в 77% случаев [61]. Несмотря на улучшение разрешающей способности МРА, ее диагностические возможности меньше, чем у инвазивной контрастной ангиографии [60, 61]. Необходимо иметь в виду неспецифичность этих изменений, в связи с чем диагноз должен основываться на комплексной оценке клинических, лабораторных и ангиографических данных [15].
Исследование сосудистой стенки ВСА, ПА, СМА, ПМА, ЗМА, БА с помощью высокоразрешающей МРТ в режиме подавлением сигнала от жировой ткани и движущейся крови до и после введения контраста при толщине срезов не более 3 мм в больших сериях больных с ПВЦНС не проводилось [33—36]. В литературе описаны лишь отдельные больные, у которых при этом исследовании выявлено накопление контраста артериальной стенкой — признак ее воспалительных изменений [49, 51, 53, 54]. Накопление контраста артериальной стенкой в некоторых случаях уменьшалось или исчезало в среднем через 7 мес, в других — персистировало на протяжении более года, что, по-видимому, связано с разным ответом на проводимое лечение [36, 64, 65]. H. Noh и соавт. [53] подчеркнули, что накопление контраста может выявляться на ранней стадии ПВЦНС, когда явные изменения просвета артерии отсутствуют и контрастная ангиография дает негативные результаты. K. Ohno и соавт. [54] пришли к заключению, что феномен накопления может использоваться не только для верификации воспаления артериальной стенки, но и для мониторирования активности заболевания: после лечения кортикостероидами и микофенолатом мофетилом 2 детей с ПВЦНС и ишемическими инсультами, обусловленными стенозами СМА и ВСА, накопление контраста их стенкой значительно уменьшилось.
В литературе описаны лишь отдельные больные, у которых при этом исследовании выявлено накопление контраста артериальной стенкой — признак ее воспалительных изменений [49, 51, 53, 54]. Накопление контраста артериальной стенкой в некоторых случаях уменьшалось или исчезало в среднем через 7 мес, в других — персистировало на протяжении более года, что, по-видимому, связано с разным ответом на проводимое лечение [36, 64, 65]. H. Noh и соавт. [53] подчеркнули, что накопление контраста может выявляться на ранней стадии ПВЦНС, когда явные изменения просвета артерии отсутствуют и контрастная ангиография дает негативные результаты. K. Ohno и соавт. [54] пришли к заключению, что феномен накопления может использоваться не только для верификации воспаления артериальной стенки, но и для мониторирования активности заболевания: после лечения кортикостероидами и микофенолатом мофетилом 2 детей с ПВЦНС и ишемическими инсультами, обусловленными стенозами СМА и ВСА, накопление контраста их стенкой значительно уменьшилось. Вместе с тем K. Fukuma и соавт. отметили, что накопление контраста артериальной стенкой не всегда свидетельствует об активности воспалительного процесса: они наблюдали его персистирование в стенке ВСА, несмотря на улучшение сигнала от кровотока по СМА и ПМА после лечения стероидами [49]. E. Obusez и соавт. полагают, что длительно персистирующее накопление контраста артериальной стенкой на фоне лечения может быть связано не с текущим воспалением, а с поствоспалительным повреждением эндотелиальных контактов [65].
Вместе с тем K. Fukuma и соавт. отметили, что накопление контраста артериальной стенкой не всегда свидетельствует об активности воспалительного процесса: они наблюдали его персистирование в стенке ВСА, несмотря на улучшение сигнала от кровотока по СМА и ПМА после лечения стероидами [49]. E. Obusez и соавт. полагают, что длительно персистирующее накопление контраста артериальной стенкой на фоне лечения может быть связано не с текущим воспалением, а с поствоспалительным повреждением эндотелиальных контактов [65].
Накопление контраста в артериальной стенке обнаруживается не только при ПВЦНС, но и при постветряночной васулопатии, саркоидозе, гигантоклеточном артериите, ревматологических заболеваниях, сифилисе, боррелиозе [33, 34, 66, 67]. Кроме того, умеренное накопление может наблюдаться при атеросклерозе, болезни моямоя и диссекции магистральных артерий головы [64].
Ультразвуковое исследование (УЗИ) экстракраниальных артерий с введением контраста. Данное исследование с введением специального контраста
Симптомы, диагностика и лечение васкулита
Васкулит (артериит) представляет собой группу заболеваний соединительной ткани, которые вызывают воспаление сосудистой стенки и некроз сосудов. Процесс этот может возникнуть в различных тканях и органах, но, как правило, чаще затрагивает почки, легкие, верхние дыхательные пути, кожа, нервная система, глазное яблоко.
Процесс этот может возникнуть в различных тканях и органах, но, как правило, чаще затрагивает почки, легкие, верхние дыхательные пути, кожа, нервная система, глазное яблоко.
ЛЕЧЕНИЕ ВАСКУЛИТА ДОСТУПНО В ФИЛИАЛАХ:
Лечение васкулита в Приморском районе
Адрес: г. Санкт-Петербург, Приморский район, ул. Репищева, 13
Лечение васкулита в Петроградском районе
Адрес: г. Санкт-Петербург, Петроградский район, ул. Ленина, 5
Лечение васкулита во Всеволожске
Адрес: г. Всеволожск, Октябрьский пр-т, 96 А
Заболевание, как правило, сопровождается осложнениями. Со стороны желудочно-кишечного тракта может открыться кишечное кровотечение. Васкулит может также привести к повреждению печени. В сердечнососудистой системе могут сформироваться такие нарушения, как кардиомиопатия, нарушение работы клапанов сердца.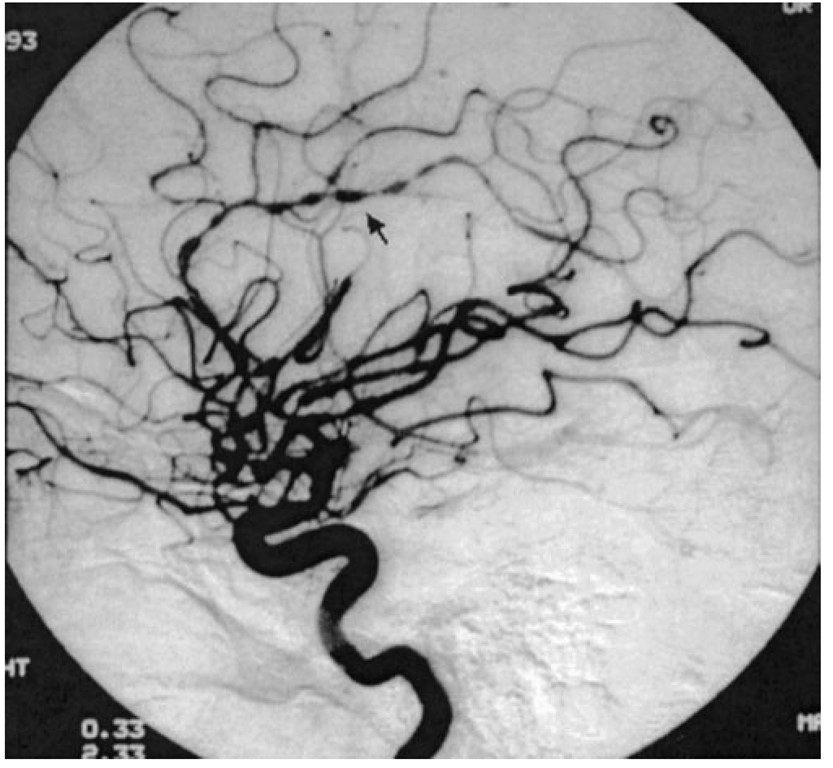 Наиболее опасным следствием васкулита является инсульт. В выделительной системе возможное осложнение — гломерулонефрит.
Наиболее опасным следствием васкулита является инсульт. В выделительной системе возможное осложнение — гломерулонефрит.
Васкулит — Причины и факторы риска
Считается, что воспаление сосудов инициируется иммунными процессами (связанными с реакцией гиперчувствительности к антигенам). Например, некоторые заболевания, классифицируемые, как системное воспаление мелких сосудов, связаны с наличием антинейтрофильных цитоплазматических антител. Аллергический васкулит провоцируется аллергическими реакциями организма. Церебральный васкулит может возникать, как осложнение инфекционного заболевания, опухолей, так и в результате изолированного поражения сосудов головного мозга.
Васкулит — типы
1. Системный васкулит мелких сосудов (артериол, капилляров и вен)
- Гранулематоз Вегенера – некротизирующий васкулит с поражением дыхательных путей, глаз, почек и других органов.
- Микроскопический полиангиит – некротизирующий васкулит с поражением лёгких и почек, без формирования гранулём
- Эозинофильный гранулематозный васкулит (Синдром Черджа-Стросса)
- Геморрагический васкулит, связанный с отложением иммуноглобулинов IgA (пурпура Шенлейна-Геноха), характерно поражение кожи, кишечника и почек, сопровождающееся артритом и артралгиями.
 Этот тип васкулита чаще возникает у детей в возрасте 4-7 лет.
Этот тип васкулита чаще возникает у детей в возрасте 4-7 лет. - Кожный лейкоцитокластический васкулит — изолированный васкулит без системного поражения
2. Системный васкулит средних сосудов (висцеральные сосуды, брыжеечная, почечная артерии и т.д.)
- Полиартериит артерий – очаговое поражение артерий, протекающее с разрывом аневризм и кровотечением, возможен инфаркт органов и тканей.
- Болезнь Кавасаки – воспаление сосудов с кожно-слизистым лимфатическим синдромом, может поражать коронарные артерии.
3. Системный васкулит крупных сосудов (аорта и крупные ветви)
- Гигантоклеточный артериит (болезнь Хортона) – гранулематозный артериит, сочетается с ревматической полимиалгией (боли в плечевом и тазовом поясе), у пациентов старше 50 лет.
- Артериит Такаясу – прогрессирующее воспаление аорты, часто возникает у молодых женщин.
4. Смешанные васкулиты (синдром Бехчета)
Кроме того, васкулит разделяют на:
- Первичный — причина заболевания неизвестна
- Вторичный — изменения в сосудах вызваны другими заболеваниями (например, ревматоидный артрит, системная красная волчанка) или являются побочным эффектом от применения лекарственных препаратов
Симптомы васкулита
Проявления васкулита зависят от особенностей течения заболевания.
При узелковом периартериите может возникать боль в мышцах, резкие боли в животе, рвота, высокая температура, снижение массы тела. Гранулематоз Вегенера вызывает гнойные и кровянистые выделения из носа, слизистая носа покрывается язвами, может появиться кашель с кровью. Гигантоклеточный артериит сопровождается слабостью, лихорадкой, головными болями, снижением массы тела. Могут возникать язвы на половых органах, стоматит, воспаления глаз (синдром Бехчета)
При васкулитах, поражающих кожу, возникает сыпь на ногах и других частых тела. При нарушении нервной системы нарушается чувствительность.
Лечение заболевания осложняется при сахарном диабете, гипертонии и венозной недостаточности.
Диагностика васкулита
Для диагностики заболевания необходимо обратиться к ревматологу и провести клинический анализ крови, мочи, ангиографию (исследование сосудов), рентген грудной клетки.
Васкулит – лечение
Лечение системного васкулита (СПб) в первую очередь сопровождается иммуносупрессивной (подавляющей) терапией, а также применяются лекарства для улучшения кровотока в сосудах. В случаях тяжёлого течения болезни применяется плазмаферез (метод очистки крови от крупных частиц, таких как иммунные комплексы). Часто лечение васкулита требует консультации нефролога, окулиста, ларинголога, невропатолога, дерматолога и хирурга.
В случаях тяжёлого течения болезни применяется плазмаферез (метод очистки крови от крупных частиц, таких как иммунные комплексы). Часто лечение васкулита требует консультации нефролога, окулиста, ларинголога, невропатолога, дерматолога и хирурга.
В нашей клинике Вы можете пройти обследование у ревматолога, получить квалифицированную консультацию врачей других направлений и провести диагностику заболеваний с использованием современного оборудования.
Приём ведут врачи:
Выберите филиал“Династия” на Новочеркасском пр-те, Красногвардейский район“Династия” на Ленина, Петроградский район“Династия” на Репищева, Приморский район“Династия” во ВсеволожскеВыездная служба
Стоимость лечения васкулита:
| Наименование услуг | Цена в рублях | |
| Санкт-Петербург | Всеволожск | |
| Первичный прием ревматолога 1 ступени | 1850 | — |
| Повторный прием ревматолога 1 ступени | 1650 | — |
| Первичный прием ревматолога, ведущего специалиста | 2500 | 2000 |
| Повторный прием ревматолога, ведущего специалиста | 2300 | 1800 |
| МАНИПУЛЯЦИИ | ||
| Капилляроскопия | 1500 | — |
ЗАПИСЬ НА ЛЕЧЕНИЕ ВАСКУЛИТА
Ваша заявка отправлена
Менеджер свяжется с вами для уточнения деталей
Мы ценим ваше обращение в наш медицинский центр «Династия»
Васкулит геморрагический
Одно из самых распространенных геморрагических заболеваний, в основе которого лежит множественный микротромбоваскулит, поражающий сосуды кожи и внутренних органов.
Причины и факторы риска. Геморрагический васкулит относится к иммунокомплексным заболеваниям, при которых микрососуды подвергаются асептическому воспалению с более или менее глубоким повреждением стенок, тромбированием и образованием циркулирующих иммунных комплексов. Причиной развития данной патологии является образование в кровотоке циркулирующих иммунных комплексов. Данные вещества оседают на внутренней поверхности кровеносных сосудов, вызывая тем самым их неспецифическое повреждение.
Факторы, способные спровоцировать заболевание:
-
вирусные и бактериальные (стрептококковые) инфекции,
-
прививки,
-
лекарственная аллергия,
-
пищевые продукты,
-
паразитарные инвазии,
-
холод.

Болезнь нередко встречается в детском возрасте и среди детей моложе 14 лет (частота 23-25 на 10 000).
Симптомы.
-
Крапивница и другие аллергические сыпи. Могут поражаться сосуды любой области, в том числе легких, мозга и его оболочек.
-
Кожный синдром: симметричное поражение конечностей, ягодиц, реже — туловища. Возникает папулезно-геморрагическая сыпь, иногда с волдырями. Высыпания однотипные, сначала имеют отчетливую воспалительную основу, в тяжелых случаях осложняются центральными некрозами и покрываются корочками, надолго оставляют пигментацию. При надавливании элементы сыпи не исчезают.
-
Суставной синдром: возникает часто вместе с кожным или спустя несколько часов (дней) в виде болей разной интенсивности в крупных суставах: коленных, локтевых, тазобедренных. Через несколько дней боль проходит, но при новой волне высыпаний может возникнуть опять.
 В ряде случаев суставное поражение бывает стойким и упорным, напоминает ревматоидный полиартрит.
В ряде случаев суставное поражение бывает стойким и упорным, напоминает ревматоидный полиартрит.
-
Абдоминальный синдром: чаще наблюдается в детском возрасте (у 54-72% больных), приблизительно у 1/3 он преобладает в клинической картине, в ряде случаев предшествует кожным изменениям, что очень затрудняет диагностику. Основной признак — сильные боли в животе, постоянные или схваткообразные, иногда настолько интенсивные, что больные не находят себе места в постели и в течение многих часов кричат. Боль обусловлена кровоизлияниями в стенку кишки.
Диагностика. Диагноз ставится на основании клинических данных и не требует дополнительных исследований для подтверждения. В анализе периферической крови обнаруживают разной степени выраженности лейкоцитоз, увеличенное СОЭ, нейтрофилез (увеличение количества нейтрофильных лейкоцитов), эозинофилия (увеличение количества эозинофилов), тромбоцитоз (увеличение количества тромбоцитов). Учитывая частое поражение почек, всем больным необходимо систематически делать анализы мочи.
Учитывая частое поражение почек, всем больным необходимо систематически делать анализы мочи.
При абдоминальном синдроме сравнительная диагностика может вызывать определенные сложности — это связано с тем, что сам геморрагический васкулит может стать причиной ряда хирургических заболеваний органов брюшной полости. Трудности дифференциальной диагностики в подобной ситуации приводят к тому, что часть больных геморрагическим васкулитом подвергается необоснованным хирургическим вмешательствам.
Лечение. Обязательным условием терапии является госпитализация и соблюдение постельного режима не менее 3 недель, затем его постепенно расширяют, так как возможны обострения.
Больному следует всячески избегать:
-
Охлаждения;
-
Дополнительной аллергизации больных пищевыми продуктами и лекарственными препаратами. Из рациона исключают какао, кофе, шоколад, цитрусовые, свежие ягоды (земляника, клубника) и блюда из них, а также индивидуально непереносимые виды пищи;
-
Применения антибиотиков, сульфаниламидов и других аллергизирующих препаратов (в том числе всех витаминов), способных поддерживать геморрагический васкулит или способствовать его обострению.

Малоаллергизирующие антибиотики (цепорин, рифампицин) назначают лишь при фоновых или сопутствующих острых инфекционных заболеваниях (например, крупозной пневмонии). Суставной синдром, увеличение температуры тела, лейкоцитоз и повышение СОЭ не являются показанием для назначения антибиотиков и других антибактериальных препаратов, поскольку они характеризуются иммунным асептическим воспалением.
Больному назначаются:
-
Энтеросорбенты: активированный уголь, холестирамин или полифепан внутрь.
-
Желудочные капли,
-
Антигистаминные препараты,
-
Пантотенат кальция, рутин, средние дозы аскорбиновой кислоты,
-
Часто применяется фитотерапия.
Эффективность вышеперечисленных препаратов в лечении данной патологии остается весьма сомнительной.
Наблюдение. Заболевание переходит в состояние ремиссии и требует диспансерного наблюдения.
Куда обращаться?
При обнаружении подозрительных симптомов необходимо обратиться за первичной консультацией к врачу-специалисту
Также на первичный прием к специалисту можно записаться в поликлинике по месту прикрепления. Для этого необходим паспорт и полис ОМС.
Геморрагический васкулит – что это за болезнь, 💉 лечение, симптомы и 🔬 диагностика на МЕД Zoon
Геморрагический васкулит (по МКБ-10 «аллергическая пурпура») – заболевание, связанное с иммунопатологическим воспалением стенок кровеносных сосудов любых органов с множественным микротромбообразованием. Болезни чаще подвержены дети (мальчики вдвое чаще, чем девочки) в возрасте 5-14 лет. Неправильное и несвоевременное лечение приводит к осложнениям, при которых поражаются почки, сердце, головной мозг.
Классификация
Синонимы заболевания – капилляротоксикоз, болезнь Шенлейна-Геноха. Единой, общепринятой классификации не существует. На практике разделение геморрагического васкулита используется по следующим признакам.
Единой, общепринятой классификации не существует. На практике разделение геморрагического васкулита используется по следующим признакам.
| Признаки классификации | Форма | Пояснения |
| По клиническому течению | острая фаза | характерна для начального этапа заболевания или периода обострения |
| фаза стихания | период, когда пациент начинает чувствовать себя лучше | |
| По характеру течения | острый геморрагический васкулит | длительность до 2 месяцев |
| затяжной | до 6 месяцев | |
| хронический | более 6 месяцев | |
| По степени тяжести клинических проявлений | легкая | больной чувствует себя удовлетворительно, отмечается в небольшом количестве сыпь на теле, могут появиться несильные боли в суставах |
| средняя | сыпь обильная, состояние пациента ухудшается; суставные боли могут сочетаться с артритом, часто появляется чувство дискомфорта, боли в животе; содержание в моче эритроцитов может повышаться | |
| тяжелая | сыпь обильная, отмечаются некротические участки; в органах желудочно-кишечного тракта могут начаться кровотечения; в моче появляется кровь; не исключена острая почечная недостаточность | |
| По форме воспаления | геморрагический васкулит кожи | поражаются только кожные покровы |
| кожно-суставная форма | кроме кожи, поражаются и суставы, чаще крупные; при геморрагическом васкулите ног они могут отекать | |
| абдоминальная форма | поражается кожа и органы желудочно-кишечного тракта; отмечаются дискомфорт и боли в брюшной полости | |
| почечный васкулит | поражаются почки; высыпаний на коже не бывает |
Причины
Этиология заболевания до конца не изучена, признается лишь то обстоятельство, что природа геморрагического васкулита – инфекционно-аллергическая.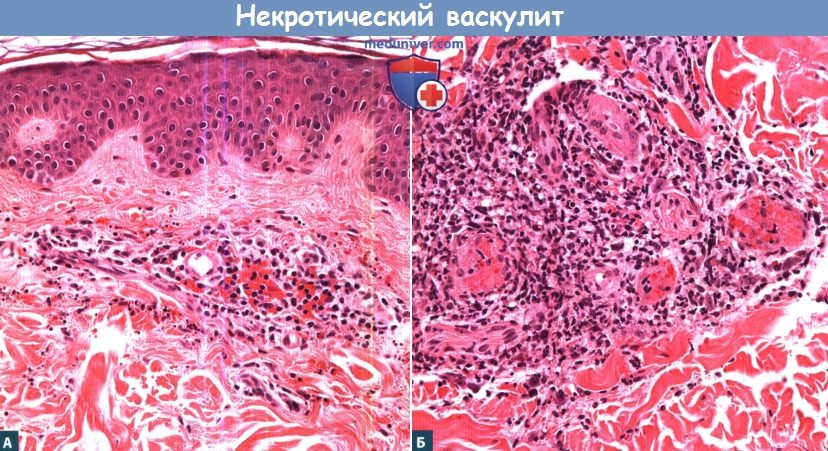 Чаще заболевание развивается, когда стоит холодная и сырая погода.
Чаще заболевание развивается, когда стоит холодная и сырая погода.
Замечено влияние респираторных инфекций на развитие болезни: как правило, первые признаки васкулита начинают давать знать о себе через неделю-месяц после перенесенного тяжелого инфекционного заболевания. Толчком могут послужить трахеобронхит, тонзиллит, ринофарингит.
Зафиксированы случаи, когда появление патологии провоцировал прием антибиотиков, особенно пенициллиновой группы, или антиаритмических средств. Сообщается также о таком провоцирующем факторе, как профилактическая вакцинация, если она была проведена непосредственно после перенесенного острого респираторного заболевания.
Отклонения в работе иммунной системы тоже могут вызвать заболевание. В группу риска входят и люди с аллергической зависимостью – будь это медикаментозная, пищевая, или холодовая аллергия.
Геморрагический васкулит может вызываться укусами насекомых, переохлаждением, ожогами и другими травмами. Фоном развития болезни могут послужить также беременность, сахарный диабет, наличие злокачественных опухолей, цирроз печени, снижение иммунных функций.
Обратите внимание! Геморрагический васкулит не относится к числу распространенных болезней: в среднем из ста тысяч человек им заболевают 14. У детей до трех лет эта патология встречается очень редко.
Патогенез
В наш организм постоянно проникают чужеродные микроорганизмы – антигены. Когда человек здоров, их успешно нейтрализуют иммунные антитела, а остатки антигенов разрушаются и утилизируются мононуклеарными фагоцитами – группой долгоживущих клеток.
Если антителам не удается справиться со своими функциями, на фоне избыточного количества антигенов образуются циркулирующие иммунные комплексы. Передвигаясь в общем кровеносном потоке, они осаждаются на внутренней поверхности стенок сосудов, повреждают их, что вызывает асептический воспалительный процесс.
Наиболее подвержены такому поражению микрососуды кожи, суставов, брыжейки кишечника и почек. Нарушается сосудистая проницаемость, формируются микротромбозы, что и приводит к развитию геморрагического васкулита.
Симптомы (признаки)
Начинается заболевание, как правило, с повышения температуры тела до субфебрильных (37-38 градусов) или фебрильных (38-39) значений. Практически у всех больных на коже появляется симметричная мелкопятнистая или пятнисто-папулезная геморрагическая сыпь. Чаще всего она возникает на местах сгибания ног (реже – рук), в зоне крупных суставов, ягодиц. При тяжелом течении болезни сыпь могут сопровождать некроз (омертвение) ткани и язвы.
Две трети случаев связаны с поражением суставов, чаще коленных и голеностопных. Боли могут быть кратковременными, иногда длятся несколько дней, наблюдаются отеки, покраснение кожи, движения в суставах становятся ограниченными, но их деформации не происходит.
Перечисленные клинические проявления могут сопровождаться абдоминальным синдромом: появляются боли в животе, иногда напоминающие кишечную колику; точно обозначить болевую точку пациенты затрудняются; присутствуют тошнота, рвота, нарушение стула. Боль возникает несколько раз в день, проходит или самостоятельно, или с началом лечения.
Примерно четверть случаев заболевания характерна тем, что у пациентов развивается почечный синдром. Анализы показывают кровь в моче, появляются признаки гломерулонефрита – болезни, характерной поражением клубочков почек.
Другие органы геморрагическим васкулитом поражаются редко. Одышка и кашель с кровяными прожилками в мокроте могут свидетельствовать о геморрагической пневмонии. Не исключено также развитие геморрагического перикардита, миокардита, кровоизлияния в эндокард.
Головокружение, раздражительность, головные боли, как правило, сопровождают поражение сосудов головного мозга, которое чревато развитием геморрагического менингита.
У детей сыпь появляется реже, чем у взрослых. Сердце и почки также подвергаются поражению нечасто, в основном страдают органы пищеварения и суставы. Ранняя диагностика заболевания у детей позволяет делать благоприятные прогнозы. Но поскольку точные причины болезни по-прежнему остаются под вопросом, здоровью детей даже после полного выздоровления следует уделять больше внимания.
Обратите внимание! Уже первые признаки заболевания должны стать поводом для посещения врача. Для начала нужно показаться терапевту. Чтобы подтвердить или опровергнуть диагноз, он может отправить пациента на консультацию к ревматологу, в отдельных случаях в этом принимают участие нефролог и хирург.
Диагностика
Признаки заболевания видны по результатам общего и биохимического анализа крови: повышается содержание лейкоцитов, увеличивается СОЭ (скорость оседания эритроцитов), происходят иммунологические нарушения. Также проводится коагулограмма – исследование, позволяющее понять, насколько хорошо происходит свертывание крови.
Анализ мочи при заболевании геморрагическим васкулитом показывает содержание в ней крови, белка. Скрытое кровотечение желудочно-кишечного тракта определяется с помощью анализа кала.
Состояние почек, брюшной полости проверяется посредством УЗИ и УЗДГ (ультразвуковая допплерография). По показаниям может проводиться гастроскопия (осмотр стенок пищевода с помощью эндоскопического обследования), бронхоскопия (оценивается состояние трахеи и бронхов).
Врач осматривает кожные покровы пациента, проверяя, нет ли высыпаний.
Лечение
При наступлении острой фазы болезни пациентам предписывается постельный режим с соблюдением гипоаллергенной диеты и ограничением употребления жидкости и соли. Исключается прием препаратов (в том числе антибиотиков), усиливающих сенсибилизацию – повышенную чувствительность организма к аллергенам.
При любых клинических проявлениях заболевания назначаются дезагреганты – лекарственные препараты, блокирующие образование тромбов в сосудах, а также активаторы фибринолиза, растворяющие уже появившиеся тромбы.
Терапия геморрагического васкулита кожи проводится с применением кортикостероидов (препаратов, обладающих противовоспалительным действием). Если ожидаемого эффекта нет, могут использоваться цитостатики, замедляющие процесс деления клеток.
Примерно в 50% случаев врачам удается полностью вылечить геморрагический васкулит кожи, для остальных пациентов удается перевести болезнь в стадию ремиссии, которая через какое-то время может вновь обратиться в острую форму.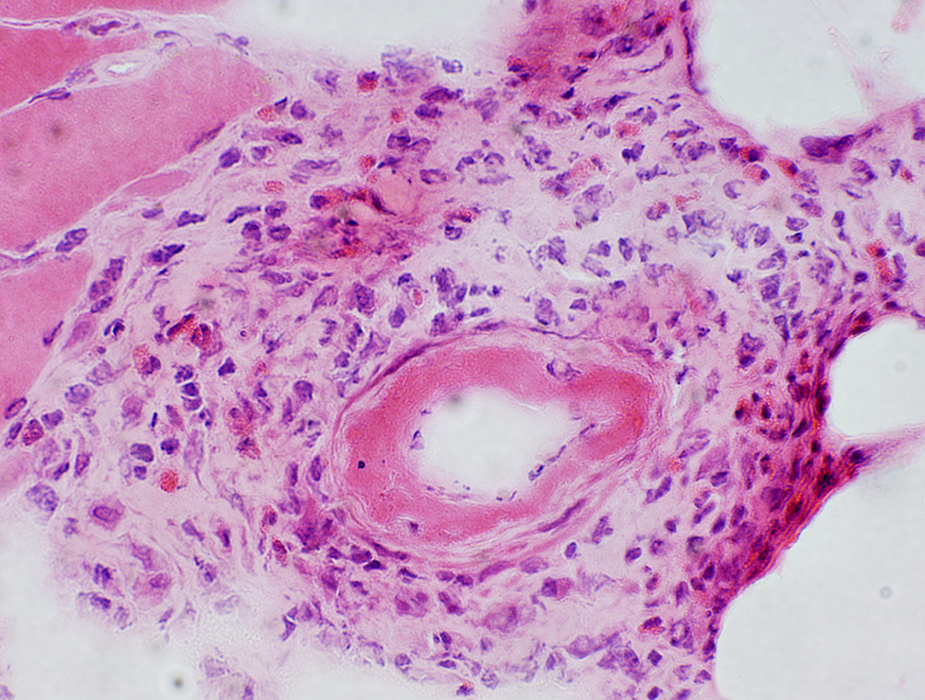
Боли летучего характера в суставах снимаются с помощью противовоспалительных препаратов (индометацин, ибупрофен), могут назначаться также производные аминохинолина – лекарства, применяемые при ревматических заболеваниях и системных заболеваниях соединительной ткани.
При поражении почек для лечения используются цитостатики, глюкокортикоиды – стероидные гормоны, производимые корой надпочечников. Может назначаться электрофорез с никотиновой кислотой и гепарином на область почек. Тяжелая стадия болезни не исключает применение гемодиализа или трансплантацию почки.
Абдоминальный синдром предполагает использование глюкокортикоидных лекарственных препаратов. При кишечной непроходимости или сквозном повреждении кишечных стенок требуется хирургическое вмешательство.
При тяжелом течении геморрагического васкулита может использоваться такой способ лечения, как экстракорпоральная гемокоррекция. Суть метода заключается в том, что взятую у пациента из вены кровь с помощью специальных микрофильтров освобождают от патологических субстанций, наполняют ее препаратами, призванными подавить болезнь, затем кровь возвращается в организм.
Осложнения
Серьезным осложнением при заболевании геморрагическим васкулитом считается развитие почечной недостаточности. Не исключены желудочно-кишечные кровотечения, при этом наблюдается кровавая рвота, в каловых массах появляется кровь. Могут появиться легочные кровотечения, в отдельных случаях возникает геморрагический инсульт с кровоизлиянием в головной мозг.
Потеря большого количества крови может стать угрозой для жизни и вызвать анемическую кому.
При абдоминальном синдроме заболевание может привести к инвагинации кишечника, перитониту, тромбозу брыжеечных сосудов, некрозу части тонкого кишечника.
Профилактика
Для предупреждения геморрагического васкулита проводится санация хронических инфекционных очагов ЛОР органов, при появлении глистных инвазий надо применять дегельминтизацию. Нельзя бесконтрольно принимать лекарственные препараты.
Инфекции и васкулиты | Ревматология
Аннотация
Васкулит может быть связан с инфекцией, иммунизацией или противомикробными препаратами. Инфекции являются причиной ряда различных типов васкулита. И наоборот, у пациентов с васкулитом могут развиться инфекции, которые иногда имитируют рецидив. Цель этого обзора состоит в том, чтобы обобщить различные аспекты взаимосвязи между васкулитом и инфекцией, а также задействованные физиопатологические механизмы в свете наших текущих знаний о животных моделях.В настоящее время причинно-следственная связь между инфекцией и васкулитом установлена лишь в нескольких случаях, и многие механизмы остаются гипотетическими. Эта взаимосвязь далее оценивается с точки зрения клинических проявлений и терапевтических возможностей на основе сообщений о случаях заболевания и данных проспективных наблюдений.
Инфекции являются причиной ряда различных типов васкулита. И наоборот, у пациентов с васкулитом могут развиться инфекции, которые иногда имитируют рецидив. Цель этого обзора состоит в том, чтобы обобщить различные аспекты взаимосвязи между васкулитом и инфекцией, а также задействованные физиопатологические механизмы в свете наших текущих знаний о животных моделях.В настоящее время причинно-следственная связь между инфекцией и васкулитом установлена лишь в нескольких случаях, и многие механизмы остаются гипотетическими. Эта взаимосвязь далее оценивается с точки зрения клинических проявлений и терапевтических возможностей на основе сообщений о случаях заболевания и данных проспективных наблюдений.
Введение
Взаимосвязь между инфекцией и васкулитом сложна [1]. Принимая во внимание примеры исторических заболеваний, таких как туберкулезный или сифилитический аортит, долгое время предполагалось, что инфекции являются триггерными факторами для многих типов васкулита. Однако причинно-следственная связь была достоверно установлена только в нескольких случаях с использованием эпидемиологического подхода (например, PAN и HBV; криоглобулинемия и HCV). Однако в большинстве случаев эта связь остается гипотетической без формальных доказательств. Физиопатология этой взаимосвязи остается плохо изученной.
Однако причинно-следственная связь была достоверно установлена только в нескольких случаях с использованием эпидемиологического подхода (например, PAN и HBV; криоглобулинемия и HCV). Однако в большинстве случаев эта связь остается гипотетической без формальных доказательств. Физиопатология этой взаимосвязи остается плохо изученной.
Модели васкулита на животных
За васкулит ответственны как иммунные, так и аутоиммунные механизмы. Недавно было обнаружено, что антитела, такие как ANCA и/или некоторые ключевые компоненты апоптоза, участвуют в патогенезе различных типов васкулита на животных моделях.Важным вкладом в эту область стало использование мышиной модели ANCA-ассоциированного васкулита [2]. Хууген и др. [2] использовали модель пассивного переноса антител к МПО, полученных на мышах с нокаутом МПО. Они перенесли анти-MPO IgG наивным мышам C57BL/6 (контрольные мыши получили антитела против BSA). Через час после введения анти-МПО некоторым мышам также внутрибрюшинно вводили бактериальный липополисахарид (ЛПС). Клинические проявления (гематурия и лейкоцитурия) и патологические изменения (некротический полулунный гломерулонефрит) были более тяжелыми у мышей, получавших ЛПС, что свидетельствует о том, что ЛПС является усугубляющим фактором анти-МПО васкулита [2].
Клинические проявления (гематурия и лейкоцитурия) и патологические изменения (некротический полулунный гломерулонефрит) были более тяжелыми у мышей, получавших ЛПС, что свидетельствует о том, что ЛПС является усугубляющим фактором анти-МПО васкулита [2].
Некоторые авторы недавно сообщили о тяжелом гранулематозном васкулите легких после внутривенной инъекции Fas-лиганда на мышиной модели животных [3].
Существуют также некоторые другие экспериментальные модели васкулита на животных, которые предполагают, что инфекция может быть триггером васкулита и/или влиять на различные иммунные механизмы. К ним относятся парвовирусная инфекция алеутских норок, приводящая к васкулиту, сходному с PAN человека, и эпидемическая коронавирусная инфекция лошадей, которая сопровождается эндотелиальной инфекцией с локальным воспалением и фибриноидным некрозом [4, 5].
Кроме того, при введении стрептококковых токсинов в ушные артерии кроликов индуцировался васкулитный синдром [6]. Было показано, что Chlamydia pneumoniae вызывает аортальный васкулит у кроликов [7], а РНК-вирус и/или вирус герпеса вызывают аортит и/или болезнь Бехчета у инбредных линий мышей [8, 9].
Васкулит крупных сосудов был описан у мышей, у которых отсутствовала чувствительность к INF-γ, а иммуногистохимические исследования показали, что заражение мышей вирусом γ-герпеса 68 сопровождалось тяжелым панартериитом [10].Однако, хотя вирус γ-герпеса 68 обладает высокой тропностью к средам эластических артерий (участок, который, по-видимому, допускает персистенцию патогенов), этот васкулит ограничивается IFN-γ [10].
Недавно Paessler et al. [11] описал модель восточного лошадиного энцефалита на животных. Заражение золотистых хомяков вирусом восточного конского энцефалита, ответственным за самые тяжелые арбовирусные заболевания человека в США, приводило к гистологическим данным васкулита с мозговыми микрокровоизлияниями, сходными с таковыми, описанными у людей.
Механизмы васкулита
В первичный васкулит, связанный с инфекциями, могут быть вовлечены несколько механизмов [12, 13].
Полисахариды Candida и фрагменты грамположительных и грамотрицательных микроорганизмов могут активировать альтернативный путь, а также приводить к воспалительной реакции, характерной для васкулита [14–16].(i) Тип III или иммунно-комплексная реакция, при которой антигенами являются инфекционные агенты или их антигенные части [14]: после достижения зоны эквивалентности иммунные комплексы выпадают в осадок и захватываются стенками сосудов, стимулируя иммунный ответ, приводящий к повреждению сосудов.
Васкулит, возникающий в результате отложения циркулирующих иммунных комплексов, представлен ПАН, ассоциированным с HBV-инфекцией, криоглобулинемией, связанной с системными васкулитами, в основном следствием HCV-инфекции, и HSP, возникающим в результате отложения в мезангии и сосудах IgA-образующих комплексов.
Гистология в основном выявляет отложение иммунных комплексов, образованных вирусными антигенами и антителами, ответственными за активацию классического пути комплемента и за рекрутирование нейтрофилов (т.е. PAN, связанный с HBV-инфекцией).
Сообщалось о криоглобулинемии у ВИЧ-1-инфицированных пациентов [17], и считается, что она связана с повышенным риском смерти и/или неоплазии [18].
Однако продукция циркулирующих криоглобулинов, по-видимому, не связана с ВИЧ-инфекцией, но сильно коррелирует с коинфекцией ВГС и циррозом печени [19].
Недавно были изучены особенности криоглобулинемического васкулита у пациентов с коинфекцией ВИЧ и ВГС. Следовательно, у пациентов с коинфекцией было более выраженное воспаление печени и более высокая гаммаглобулинемия, но более низкий уровень криоглобулина [20].Более того, анти-ВГС-терапия оказалась полезной в этой популяции [20].
Сопутствующая ВИЧ-инфекция значительно снижает клиническое и иммунологическое выражение криоглобулинемии, за исключением пациентов с коинфекцией с высокой вирусной нагрузкой для обоих вирусов [21].
Криоглобулинемия была дополнительно изучена у пациентов с коинфекцией в отношении количества клеток CD4 Aaron et al. , и полученные данные свидетельствуют о том, что клеточно-опосредованный иммунитет может способствовать выработке криоглобулинов, ассоциированных с ВГС [22].
Например, при ГКА воздействие антигенов (вероятно, инфекционных, но нет четких доказательств, подтверждающих эти данные) запускает управляемый Т-клетками процесс, ведущий к васкулиту. Дендритные клетки сосудистой стенки являются мощными антигенпрезентирующими клетками и, следовательно, способны активировать CD4 + Т-клетки, которые в дальнейшем будут нести ответственность за привлечение макрофагов и моноцитов к стенке сосуда [23].(ii) Клеточная гиперчувствительность: воздействие антигена может привлекать лимфоциты, которые высвобождают цитокины, вызывая повреждение тканей и дальнейшую активацию макрофагов и лимфоцитов (ГКА).
Эти клетки высвобождают несколько цитокинов (IL-1 и -6), а резидентные Т-клетки выделяют IFN-γ, который является ключевым провоспалительным цитокином, участвующим в патогенезе ГКА. Устойчивое воспаление, опосредованное Т-клетками, макрофагами и провоспалительными цитокинами, приводит к утолщению интимы и окклюзии сосудов. Фактор роста тромбоцитов и фактор роста эндотелия сосудов также играют важную роль в последующем развитии закупоривающего просвет артериита.
(iii) Нарушение иммунной регуляции (некоторые васкулиты у пациентов с ВИЧ на поздних стадиях заболевания): при большинстве васкулитных синдромов наблюдается аномальная экспрессия молекул адгезии и цитокинов в эндотелии сосудов как проявление эндотелиальной дисфункции, которая может быть вызвана различные раздражители (включая инфекционные агенты, иммунные комплексы и антитела против эндотелиальных клеток).

(iv) Прямая инвазия эндотелиальных клеток может быть основным патогенным процессом при инфекциях, вызванных ЦМВ, простым герпесом, риккетсиями, грибами и бактериями [15, 16].
(v) Последние данные предполагают другие механизмы развития васкулита в контексте инфекции [24]. Цитокины, такие как TNF и различные IL, продуцируются непосредственно при стимуляции инфекционными агентами. Впоследствии происходит рекрутирование нейтрофилов в мелкие сосуды, что приводит к развитию васкулита. Васкулит, связанный с инфекцией, вызванной стрептококком и стафилококком, был связан с этим механизмом повреждения сосудов.
Первичный васкулит и инфекция
ПАН
PAN и его ассоциация с HBV — классический пример первичного васкулита, связанного с инфекционным агентом [25, 26].Не существует надежной животной модели УПА, связанной с ВГВ, но вирусологические исследования и исследования распространенности подтверждают формальную причинно-следственную связь.
О связи между УПА и ВГВ сообщалось часто (10-54%) [27-30], обычно в течение первых 6 месяцев после инфицирования ВГВ. За последние годы произошло значительное снижение HBV-PAN [31], в первую очередь благодаря вакцинации против HBV и полному скринингу крови перед трансфузией. Были отмечены незначительные клинические отличия HBV-PAN по сравнению с неинфекционным PAN, включая резкое начало, более мягкое благоприятное клиническое течение и сероконверсию с последующим полным выздоровлением.Биология HBV-PAN выявляет постоянную репликацию вируса, HBsAg (7-36% случаев) и непостоянные иммунные комплексы. Менее 10% случаев УПА связаны с ВГС. В ретроспективном исследовании были обнаружены важные клинико-патологические особенности и терапевтические различия между HCV-PAN-васкулитом и HCV-криоглобулинемией [32].
О некоторых других инфекционных агентах сообщается в PAN, но без официальных данных о доказательствах (Таблица 1).
Таблица 1.Инфекционные агенты и ПАН
Инфекционный агент
. | Частота ассоциации (ссылки) . | Дополнительные данные . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HBV | STROL [27-30] | Распространенные исследования, вирусологические | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STREPTOCOCCUS β-HAEMOLYTICUS | Возможен [33-35] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klebsiella | слабый [36] | Anecdotal Case отчеты | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S слабого [36] | Anectotal Case отчеты | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yersinia | Anectotal Case Reports | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HIV | S слабого [38-40] | Anectotal Case Reports | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parvovirus B19 | Слабый [41, 42] | Anecdotal Case | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| VZV | слабый [43] | Anecdotal отчеты | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Эхинококк | Слабый [44, 45] | Анекдоты TAL CASE сообщает | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [44, 46] | 1 Anecdotal Case | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ascaris | S слабого [44, 45]Anecdotal Case | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Инфекционный агент
. | Частота ассоциации (ссылки) . | Дополнительные данные . | |||
|---|---|---|---|---|---|
| HBV | STROL [27-30] | Распространенные исследования, вирусологические | |||
| STREPTOCOCCUS β-HAEMOLYTICUS | Возможен [33-35] | ||||
| Klebsiella | слабый [36] | Anecdotal Case отчеты | |||
| S слабого [36] | Anectotal Case отчеты | ||||
| Yersinia | Anectotal Case Reports | ||||
| HIV | S слабого [38-40] | Anectotal Case Reports | |||
| Parvovirus B19 | Слабый [41, 42] | Anecdotal Case | |||
| VZV | слабый [43] | Anecdotal отчеты | |||
| Эхинококк | Слабый [44, 45] | Анекдоты TAL CASE сообщает | |||
2102 | |||||
| Ascaris | Scown [44, 45] | Anecdotal Case |

Инфекционные агенты и ПАН
| Инфекционный агент . | Частота ассоциации (ссылки) . | Дополнительные данные . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| HBV | STROL [27-30] | Распространенные исследования, вирусологические | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| STREPTOCOCCUS β-HAEMOLYTICUS | Возможен [33-35] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klebsiella | слабый [36] | Anecdotal Case отчеты | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S слабого [36] | Anectotal Case отчеты | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yersinia | Anectotal Case Reports | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HIV | S слабого [38-40] | Anectotal Case Reports | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parvovirus B19 | Слабый [41, 42] | Anecdotal Case | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| VZV | слабый [43] | Anecdotal отчеты | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Эхинококк | Слабый [44, 45] | Анекдоты TAL CASE сообщает | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [44, 46] | 1 Anecdotal Case | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ascaris | S слабого [44, 45]Anecdotal Case | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Инфекционный агент
. | Частота ассоциации (ссылки) . | Дополнительные данные . | ||
|---|---|---|---|---|
| HBV | STROL [27-30] | Распространенные исследования, вирусологические | ||
| STREPTOCOCCUS β-HAEMOLYTICUS | Возможен [33-35] | |||
| Klebsiella | слабый [36] | Anecdotal Case отчеты | ||
| S слабого [36] | Anectotal Case отчеты | |||
| Yersinia | Anectotal Case Reports | |||
| HIV | S слабого [38-40] | Anectotal Case Reports | ||
| Parvovirus B19 | Слабый [41, 42] | Anecdotal Case | ||
| VZV | слабый [43] | Anecdotal отчеты | ||
| Эхинококк | Слабый [44, 45] | Анекдоты TAL CASE отчеты | ||
2 | 1 Anecdotal Case | |||
| ASCARIS | Scire [44, 45] | Anecdotal Case |
должно быть сделано между PAN и PAN, связанной с HBV, поскольку существуют важные различия в патогенезе с дальнейшими последствиями для лечения и прогноза.
ИНФ-α и видарабин, использованные в проспективном неконтролируемом исследовании, привели к улучшению выживаемости и сероконверсии более чем в 50% случаев [47]. Кроме того, Guillevin et al. [48, 49] продемонстрировали, что краткосрочные кортикостероиды, плазмаферез и противовирусная терапия при ВГВ-ПАН были эффективными и безопасными.
Криоглобулинемия
Большинство случаев криоглобулинемии связаны с ВГС, и эта связь была установлена в течение нескольких лет [50].Дальнейшие исследования показали, что смешанная криоглобулинемия часто встречается при хронической инфекции ВГС и преимущественно II типа [51]. Данные серологических и вирусологических исследований подтверждают патофизиологическую роль ВГС-инфекции при криоглобулинемии: положительные тесты на ВГС (80-90% пациентов), циркулирующая РНК ВГС, ВГС в очагах поражения и РНК ВГС в криопреципитате.
Кроме того, Sansonno et al. [52] показали, что уровни РНК ВГС в циркулирующих лимфоцитах у пациентов со смешанной криоглобулинемией значительно выше, чем у пациентов без криоглобулинемии.
Последние данные идентифицировали генотип 1b ВГС как генотип, наиболее часто связанный с криоглобулинемией, в то время как генотипы 2–3 связаны с криоглобулинемией у пациентов с коинфекцией ВИЧ-ВГС. Симптомы криоглобулинемии, связанные с ВГС, в основном кожные, ревматологические и почечные. Однако корреляции между оценкой активности болезни печени и криоглобулинемией нет. Зарегистрированная распространенность криоглобулинов составила 45,7% у пациентов с ВГС, а распространенность симптомов, связанных с наличием криоглобулинов, составила 27% [53].
Криоглобулинемия также может быть вторичной по отношению к HBV-инфекции, и связь между HBV и криоглобулинемией была установлена с момента обнаружения HBV при криоглобулинемии III типа [54].
Levo [55] обнаружил маркеры HBV (HBsAg или его антитела) в криопреципитатах у двух третей (74% или 14/19) их пациентов со смешанной криоглобулинемией, не связанной с лимфопролиферативным заболеванием или ЗСТ. В образцах сыворотки 3 из 25 сывороток были положительными на HBsAg (12%), а 12 имели анти-HBV-антитела (48%) [55].
HBV и HCV имеют схожие эпидемиологические характеристики, но несколько случаев криоглобулинемии, связанной с HBV-инфекцией, описанные в литературе, не позволяют точно определить роль коинфекции с HCV [56].
В серии из 154 последовательных пациентов распространенность криоглобулинов оказалась значительно выше ( P <0,001) у пациентов с ВГС (46%), чем у пациентов с ВГВ (13,4%) [57].
Иногда сообщалось о криоглобулинемии после инфицирования ВИЧ, ЦМВ, ВЭБ и парвовирусом B19, но это были лишь спорадические сообщения, и нельзя было сделать формального заключения [57–59] (таблица 2).
Таблица 2.Инфекционные агенты и криоглобулинемия
| Инфекционный агент . | Частота ассоциации . | Дополнительные данные . |
|---|---|---|
| Распространенность и вирусологические исследования | ||
| CMV | S слабого [61-63] | Анекдотальные корпусы |
| EBV | ||
| Парвовирус B19 | Слабая [59, 63, 65] | Отдельные случаи |
Инфекционный агент
. | Частота ассоциации . | Дополнительные данные . | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Распространенность и вирусологические исследования | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CMV | S слабого [61-63] | Анекдотальные корпусы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| EBV | Таблица 2 Инфекционные агенты и криоглобулинемия
|
 Этот тип васкулита чаще возникает у детей в возрасте 4-7 лет.
Этот тип васкулита чаще возникает у детей в возрасте 4-7 лет.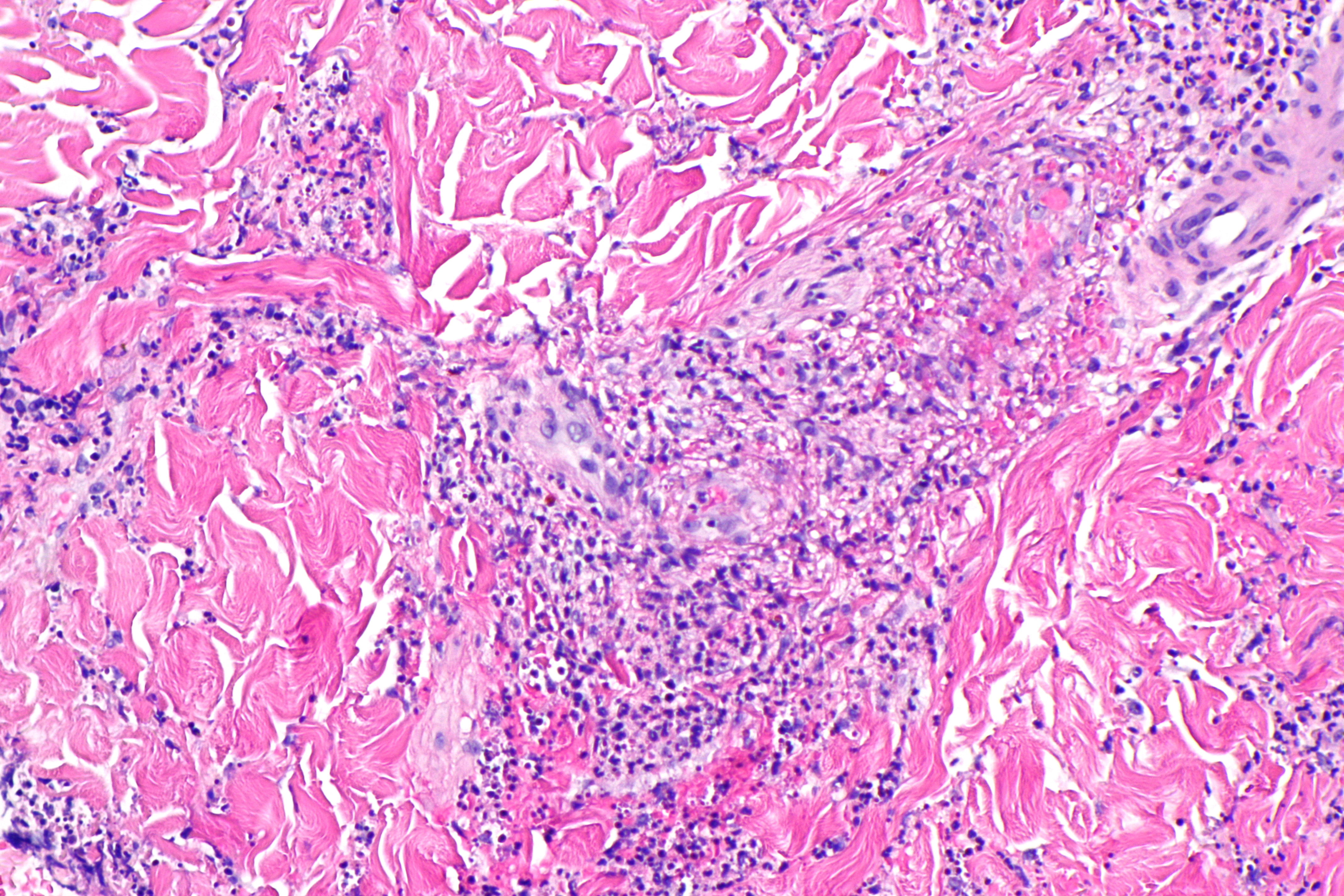
 В ряде случаев суставное поражение бывает стойким и упорным, напоминает ревматоидный полиартрит.
В ряде случаев суставное поражение бывает стойким и упорным, напоминает ревматоидный полиартрит.




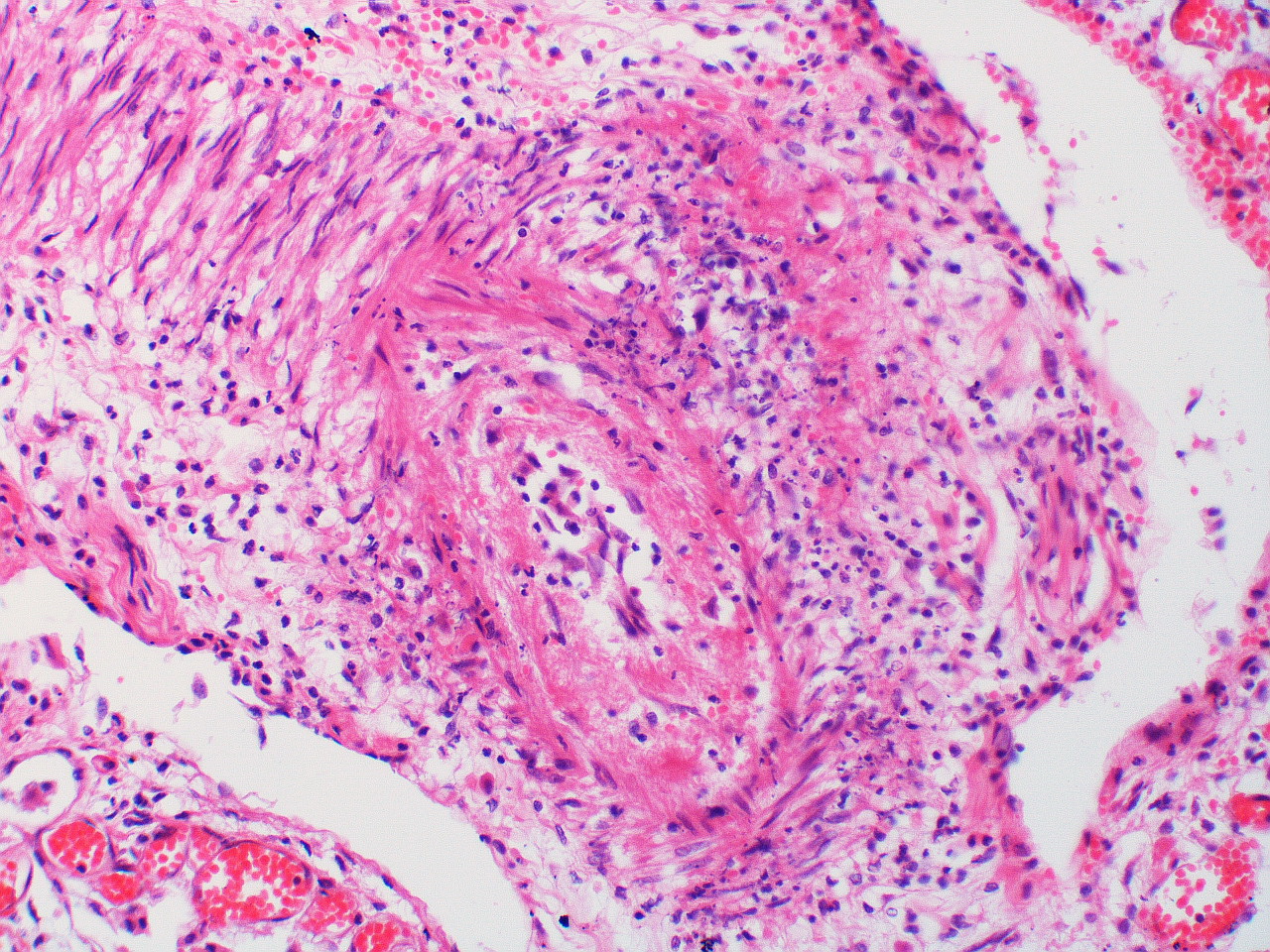
 Однако в настоящее время некоторые новые методы лечения, такие как введение моноклональных антител против CD20, также обсуждаются в качестве лечения этих пациентов [68].
Однако в настоящее время некоторые новые методы лечения, такие как введение моноклональных антител против CD20, также обсуждаются в качестве лечения этих пациентов [68].
 aureus : несмотря на выработку суперантигенных токсинов при назальном носительстве S. aureus , систематическая ошибка репертуара периферических Т-лимфоцитов не обнаружена.
aureus : несмотря на выработку суперантигенных токсинов при назальном носительстве S. aureus , систематическая ошибка репертуара периферических Т-лимфоцитов не обнаружена.
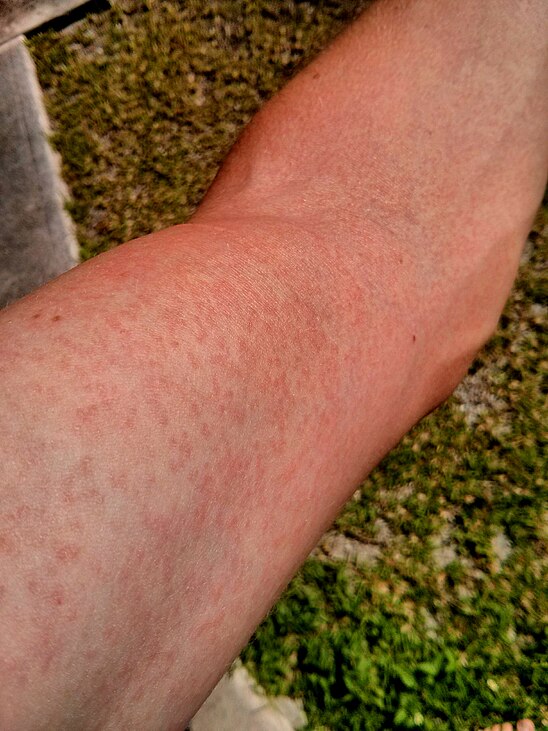

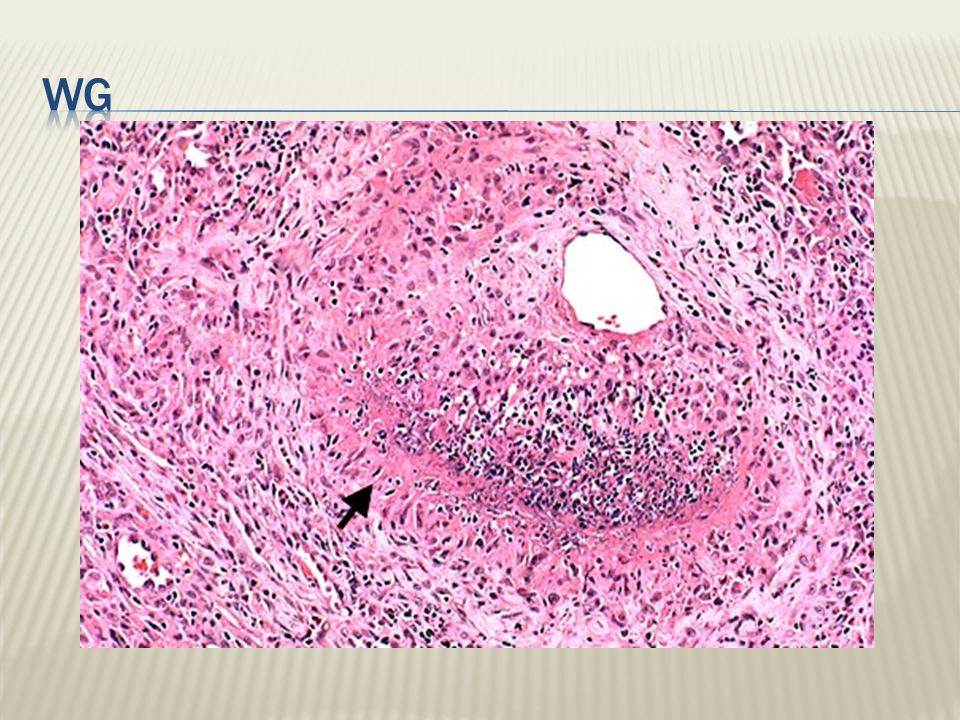



 Молекулярные методы не позволяют обнаружить циркулирующие консервативные микробные последовательности при БК, что позволяет предположить, что антигенный стимул может возникать из отдаленного места и/или может быть фактором хозяина, участвующим в провоспалительном каскаде.
Молекулярные методы не позволяют обнаружить циркулирующие консервативные микробные последовательности при БК, что позволяет предположить, что антигенный стимул может возникать из отдаленного места и/или может быть фактором хозяина, участвующим в провоспалительном каскаде.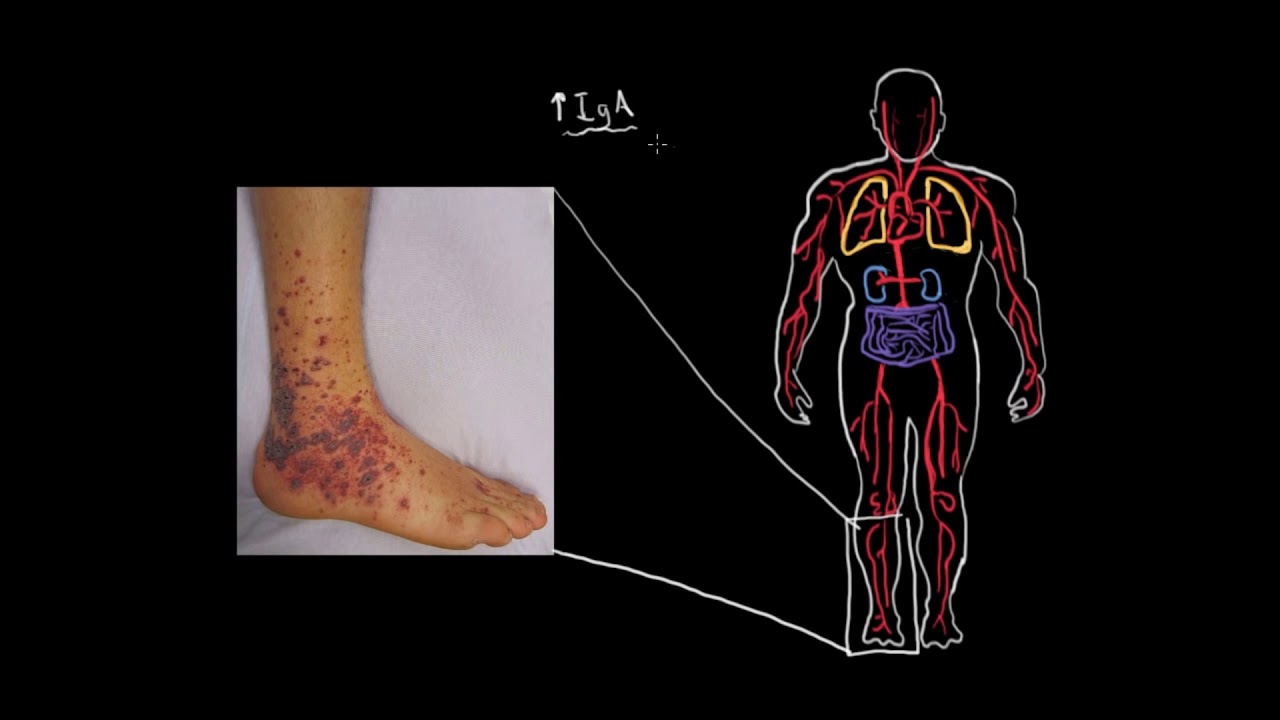
 [108] сообщили, что блокатор ФНО (этанерцепт) может предотвратить развитие артериита, что указывает на роль провоспалительных цитокинов в патогенезе БК.
[108] сообщили, что блокатор ФНО (этанерцепт) может предотвратить развитие артериита, что указывает на роль провоспалительных цитокинов в патогенезе БК.