Препараты железа в лечении анемии у онкологических больных
В последние годы анемия привлекает к себе пристальное внимание ученых, так как является частым осложнением опухолевых заболеваний и противоопухолевой цитотоксической терапии. На фоне лекарственного лечения частота анемии среднетяжелой (Нb 8—10 г/л) и тяжелой (Нb 6,5—8 г/л) степени достигает 75%, что отрицательно сказывается на качестве жизни пациентов [1]. Кроме того, анемия ведет к тканевой гипоксии, снижает чувствительность опухоли к химиотерапии и лучевой терапии и является независимым прогностическим фактором, определяющим выживаемость онкологических больных [2].
В течение многих лет единственным методом лечения тяжелого анемического синдрома в онкологии была гемотрансфузия (ГТ), а точнее, переливание донорской эритроцитарной массы. ГТ и сейчас используется при необходимости быстрого повышения уровня гемоглобина, хотя обладает множеством побочных эффектов и, по данным американских авторов, существенно увеличивает риск тромбоэмболии и смерти [3].
Создание и внедрение в практику лечения онкологических больных рекомбинантных человеческих эритропоэтинов (ЭПО) значительно снизило количество ГТ и обусловленных ими осложнений. При этом отмечено положительное влияние ЭПО на качество жизни пациентов [4]. Однако, являясь единственным патогенетическим методом лечения анемии, ЭПО не всегда позволяют достичь желаемого результата. Одной из причин этого может быть дефицит железа.
Спорные вопросы, касающиеся использования ЭПО у онкологических больных, достаточно подробно освещены в ряде отечественных публикаций [5, 6]. Целью данного обзора является оценка роли дефицита железа и препаратов для его коррекции в лечении анемии у онкологических больных.
Железо является функциональным компонентом большого числа ферментов, играющих важную роль в основных метаболических процессах. По мнению M. Aapro и соавт. [7], дефицит железа у онкологических больных составляет 30—60%.
Этиопатогенетические механизмы развития анемии при злокачественных опухолях многофакторны и сложны. Активация иммунной системы и гиперэкспрессия провоспалительных цитокинов (интерлейкины-1 и 6, фактор некроза опухоли, интерферон-гамма и др.) нарушает продукцию эндогенного эритропоэтина, эритроцитов и метаболизма железа [8—10].
Активация иммунной системы и гиперэкспрессия провоспалительных цитокинов (интерлейкины-1 и 6, фактор некроза опухоли, интерферон-гамма и др.) нарушает продукцию эндогенного эритропоэтина, эритроцитов и метаболизма железа [8—10].
Гепсидин — гормон, синтезируемый печенью, открыт и описан A. Krause и соавт. [11] как LEAP — liver expressed antimicrobial peptide. Установлено, что гиперпродукция интерлейкина-6 способствует повышенному синтезу гепсидина. Циркулируя в плазме, гепсидин взаимодействует с транспортным белком ферропортином, подавляет всасывание железа в кишечнике, высвобождение его и макрофагов из депо, что приводит к дефициту железа в костном мозге и развитию анемии [12]. При том, что количество железа в организме может быть достаточным и даже повышенным, возникает так называемый функциональный дефицит железа (ФДЖ) [13, 14].
Таким образом, существует дефицит железа абсолютный и функциональный. Функциональный дефицит железа характеризуется нормальным или высоким уровнем ферритина в сыворотке (≤800 нг/мл), насыщением трансферрина <20%, увеличением пропорции гипохромных эритроцитов и ретикулоцитов, низким уровнем среднего объема эритроцитов (MCV <80 fl), низким содержанием гемоглобина в эритроците (МСН <27 pg). Может возникать в результате возросших потребностей костного мозга в железе после стимуляции эритропоэза ЭПО.
Может возникать в результате возросших потребностей костного мозга в железе после стимуляции эритропоэза ЭПО.
Абсолютный дефицит железа у онкологических больных может развиваться в результате недостаточного поступления с пищей и недостаточной его абсорбции в желудочно-кишечном тракте, а также повышенной потребности организма при ряде клинических ситуаций (хирургическое вмешательство, желудочно-кишечное кровотечение и др.) Развитию железодефицитной анемии предшествуют стадии простого дефицита железа и железодефицитного эритропоэза. Простой дефицит железа характеризуется сниженной концентрацией ферритина в сыворотке (<30 нг/мл) и железа в костном мозге при нормальном уровне гемоглобина. Клинически отмечается утомляемость, снижение работоспособности, изменение настроения и ухудшение когнитивной функции. Железодефицитный эритропоэз развивается при дефиците железа, доступного для включения в протопорфириновую группу гемоглобина. Отмечается снижение уровня гемоглобина, низкий уровень железа в сыворотке, увеличение свободного протопорфирина в эритроцитах, повышение общей железосвязывающей способности сыворотки, низкое насыщение трансферрина (<15%).
В онкологии лечение анемии при абсолютном дефиците начинают с применения препаратов железа. При функциональном дефиците железа их сочетают со стимуляторами эритропоэза. При уровне ферритина ≥800 мг/мл и насыщении трансферрина — 20% препараты железа не вводятся.
В клинической практике для внутривенного введения используются следующие препараты: карбоксимальтозат железа (феринжект), сахарат железа (венофер), глюконат железа (ферлицит), декстран железа (феррум-лек, космофер). Все они представляют собой сферические железо-углеводные коллоидные комплексы, включающие железо-(III)-оксигидроксидное ядро, сходное по структуре с ферритином, которое покрыто углеводной оболочкой. Оболочка придает комплексу стабильность и замедляет выделение железа.
Карбоксимальтозат железа (феринжект) характеризуется медленным физиологическим высвобождением железа из стабильного комплекса с углеводом, что определяет его низкую токсичность. Феринжект после внутривенного введения захватывается ретикулоэндотелиальной системой и распределяется на железо и карбоксимальтозу. После однократного внутривенного введения препарата в дозах от 100 до 1000 мг максимальная его концентрация в сыворотке (37—333 мкг/мл) достигается через 15 мин — 1,21 ч.
Таким образом, больные со злокачественными опухолями часто страдают анемией, которая может быть железодефицитной. Для лечения этих состояний используют средства, стимулирующие эритропоэз и гемотрансфузии. Одновременно необходимо возмещение дефицита железа.
Впервые эффективность комбинации ЭПО с препаратами железа была выявлена в нефрологии, причем было установлено преимущество именно внутривенных форм железа по сравнению с пероральными. В последнее десятилетие проведен ряд исследований по оценке такого лечения у онкологических больных с анемией, индуцированной химиотерапией.
В исследовании М. Auerbach и соавт. [17] 157 пациентов, получавших эритропоэтин альфа еженедельно в течение 6 нед, были рандомизированы на три группы: 1-я — дополнительно вводился декстран железа внутривенно струйно или капельно; 2-я — получала препарат железа внутрь, 3-я — была контрольной. Все пациенты имели исходный уровень Нb≤105 г/л и низкое насыщение трансферрина ≤19%. При оценке через 6 нед лечения в контрольной группе средний уровень Нb ≤105 г/л (анемия сохраняется), во 2-й группе Нb — 112 г/л, целевой уровень не достигнут, существенной разницы с контролем нет. В 1-й группе достигнут максимальный уровень гемоглобина — 119—122 г/л, отличий при струйном и капельном введении нет. Дополнительно оценивали частоту гематологического ответа — процент больных, достигших уровень Нb ≥120 г/л или имевших увеличение Нb≥20 г/л. Гематологический ответ достоверно превышал показатели 2-й группы и контроля: 68, 36 и 25% соответственно (р<0,01).
В исследовании D. Henry и соавт. [18] 187 пациентов получали лечение эритропоэтином альфа 1 раз в неделю в течение 12 нед. Из них 129 были рандомизированы на три группы: 1-я — получала дополнительно глюконат железа внутривенно; 2-я — сульфат железа внутрь; 3-я — была контрольной. Включались больные с исходным уровнем Нb ≤110 г/л и насыщением трансферрина ≤15%. При оценке через 8 нед лечения прирост уровня Нb в 1-й группе составил 24 г/л, а во 2-й и 3-й — 16—15 г/л. Гематологический ответ в 1-й группе составил 73%, во 2-й и 3-й группе соответственно 45 и 41%. Разница статистически достоверна как между 1-й и 2-й группами (р=0,009), так и между 1-й и контролем (р=0,0044).
В 2008 г. L. Bastit и соавт. [19] опубликовали результаты крупного (n=396) открытого рандомизированного исследования III фазы. Пациенты с исходным уровнем Hb ≤105 г/л и насыщением трансферрина ≥15% получали лечение дарбэпоэтином альфа по 500 мкг 1 раз в 3 нед в течение 16 нед. Сравнивались две группы: исследовательская — дополнительно внутривенно 1 раз в неделю вводился сахарат железа; контрольная — железо вводилось перорально или не вводилось. Частота гематологического ответа в исследовательской группе составила 86%, а в контрольной — 73%. Дополнительно оценивалась потребность в заместительных гемотрансфузиях, которая в группе комбинированного лечения достоверно различалась с контролем (9% против 20% соответственно, р=0,005).
Частота гематологического ответа в исследовательской группе составила 86%, а в контрольной — 73%. Дополнительно оценивалась потребность в заместительных гемотрансфузиях, которая в группе комбинированного лечения достоверно различалась с контролем (9% против 20% соответственно, р=0,005).
В исследовании P. Pedrazzoli и соавт. [20] 149 больным дарбэпоэтин вводился по 150 мкг 1 раз в нед с внутривенным железом или без него. Авторы показали достоверное преимущество комбинированного лечения с включением внутривенного железа. Интересные данные получили М. Hedenus и соавт. [21], оценившие не только гематологический ответ, но и количество израсходованного ЭПО. Было установлено, что комбинированное применение ЭПО с внутривенным железом в среднем на 25% снижает расход ЭПО по сравнению с контролем.
В литературе имеются публикации, указывающие на возможность достижения целевого уровня гемоглобина и снижения потребности в гемотрансфузиях у онкологических больных с анемией при использовании только внутривенных форм железа. В 2010 г. Р. Dangsuvan и соавт. [22] опубликовали результаты локального исследования (n=44), в котором сравнивался сахарат железа и пероральные препараты у пациенток с анемией на фоне химиотерапии без дополнительного введения ЭПО. Потребность в заместительных гемотрансфузиях в группе внутривенного сахарата железа составила 22,7%, с пероральным препаратом железа — 63,6%. Опубликованы данные, показавшие эффективность внутривенных препаратов железа для лечения анемии у онкологических больных без применения средств, стимулирующих эритропоэз. В 2010 г. Т. Steinmetz и соавт. [23] опубликовали результаты исследования по оценке эффективности и переносимости карбоксимальтозата железа у онкологических больных с анемией и абсолютным или функциональным дефицитом железа. Оценка эффективности проведена у 420 пациентов, которые были рандомизированы в группу внутривенного железа без средств стимулирующих эритропоэз (n=347), и группу, получавших этот же препарат в комбинации со стимуляторами эритропоэза (n=73).
В 2010 г. Р. Dangsuvan и соавт. [22] опубликовали результаты локального исследования (n=44), в котором сравнивался сахарат железа и пероральные препараты у пациенток с анемией на фоне химиотерапии без дополнительного введения ЭПО. Потребность в заместительных гемотрансфузиях в группе внутривенного сахарата железа составила 22,7%, с пероральным препаратом железа — 63,6%. Опубликованы данные, показавшие эффективность внутривенных препаратов железа для лечения анемии у онкологических больных без применения средств, стимулирующих эритропоэз. В 2010 г. Т. Steinmetz и соавт. [23] опубликовали результаты исследования по оценке эффективности и переносимости карбоксимальтозата железа у онкологических больных с анемией и абсолютным или функциональным дефицитом железа. Оценка эффективности проведена у 420 пациентов, которые были рандомизированы в группу внутривенного железа без средств стимулирующих эритропоэз (n=347), и группу, получавших этот же препарат в комбинации со стимуляторами эритропоэза (n=73). Через 5 нед лечения гемоглобин в обеих группах повысился до 11—12 г/л. Нежелательные явления (в основном тошнота и диарея), возможно связанные с карбоксимальтозатом железа, составили 2,3%. Препарат в обоих случаях эффективно повышал и стабилизировал уровень гемоглобина у онкологических больных [23].
Через 5 нед лечения гемоглобин в обеих группах повысился до 11—12 г/л. Нежелательные явления (в основном тошнота и диарея), возможно связанные с карбоксимальтозатом железа, составили 2,3%. Препарат в обоих случаях эффективно повышал и стабилизировал уровень гемоглобина у онкологических больных [23].
Анемия часто встречается у больных со злокачественными новообразованиями и связана как с основным заболеванием, так и с его лечением: цитотоксическая и лучевая терапия оказывают прямое подавляющее действие на кроветворение. Анемия при злокачественных опухолях по патогенезу ассоциируется с анемией при хронических заболеваниях и нередко сочетается с дефицитом железа — функциональным или абсолютным. Результаты международных исследований показали необходимость использования внутривенных форм железа с гемостимулирующей терапией ЭПО для лечения анемии, возникшей на фоне химиотерапии. Одновременно существуют указания на эффективность внутривенного железа в монотерапии при функциональном его дефиците. Это явилось основанием для включения в международные рекомендации (NCCN, ESMO) по проведению гемостимулирующей терапии у онкологических больных внутривенных форм железа [15, 24]. При отсутствии дефицита железа (ферритин >800 нг/мл и насыщение трансферрина ≥20%) вводить его не рекомендуется, как и пациентам с признаками активной инфекции [15]. Целевой уровень гемоглобина при лечении анемии не должен превышать 12,0 г/дл (120 г/л), его достижение сопровождается улучшением качества жизни пациентов и, возможно, результатов противоопухолевого лечения и выживаемости. Надеемся, что дальнейшее проведение хорошо спланированных международных исследований позволит ответить на многие вопросы, еще существующие в этой проблеме.
Это явилось основанием для включения в международные рекомендации (NCCN, ESMO) по проведению гемостимулирующей терапии у онкологических больных внутривенных форм железа [15, 24]. При отсутствии дефицита железа (ферритин >800 нг/мл и насыщение трансферрина ≥20%) вводить его не рекомендуется, как и пациентам с признаками активной инфекции [15]. Целевой уровень гемоглобина при лечении анемии не должен превышать 12,0 г/дл (120 г/л), его достижение сопровождается улучшением качества жизни пациентов и, возможно, результатов противоопухолевого лечения и выживаемости. Надеемся, что дальнейшее проведение хорошо спланированных международных исследований позволит ответить на многие вопросы, еще существующие в этой проблеме.
Недавно в клинической практике появился новый препарат для внутривенного введения — железа карбоксимальтозат (феринжект), показавший высокую эффективность как в комбинации с ЭПО, так и в монорежиме. Феринжект не требует проведения тест-дозы, обладает хорошей переносимостью и минимальным риском развития аллергических реакций.
Препараты железа в лечении анемии, индуцированной химиотерапией
Статья в формате PDF.
Одним из наиболее частых симптомокомплексов, ассоциированных со злокачественным опухолевым процессом, является анемия, которая может развиваться как в результате основного заболевания, так и в качестве побочного эффекта противоопухолевого лечения, в частности химиотерапии, причем второй вариант встречается значительно чаще.
Анемия имеет место более чем в трети случаев злокачественных новообразований, а среди пациентов, получающих химиотерапию, ее частота достигает 90%. При этом, с одной стороны, химиотерапия приводит к снижению уровня гемоглобина (Hb) при всех видах онкопатологии, а с другой – уровень гемоглобина перед началом химиотерапии непосредственно влияет на ее результативность. Таким образом, коррекция анемии, вызванной применением химиопрепаратов, повышает эффективность противоопухолевого лечения, выживаемость пациентов и качество их жизни.
Как патологический процесс, анемия характеризуется уменьшением количества эритроцитов, концентрации гемоглобина в единице объема крови (≤12 г/дл) и развитием тканевой гипоксии, что оказывает дополнительное неблагоприятное влияние на выживаемость онкологических больных. Кроме того, гипоксия опухолевой ткани может ассоциироваться с резистентностью к химиотерапии и лучевой терапии, а также с усилением генетических мутаций и ангиогенеза опухоли, которые в значительной мере затрудняют контроль ее роста. В многочисленных исследованиях подтверждена связь гипоксии опухолевой ткани и низких показателей Hb с ухудшением прогноза течения злокачественного процесса.
В онкологической практике многие врачи рассматривают развитие умеренной анемии у пациентов как неизбежное явление; считается, что снижение уровня Hb до 10 г/дл или даже до 8 г/дл не наносит значимого вреда состоянию таких больных. Однако результаты многих исследований по изучению взаимосвязи анемии и качества жизни опровергают данную точку зрения, показывая, что значение анемии для прогноза онкологических больных явно недооценено. Применение в онкологической практике современных химиопрепаратов, агрессивного сочетания химиотерапии с лучевой терапией, использование высоких доз интерферонов и интерлейкинов увеличивают эффективность лечения, но вместе с тем существенно ухудшают качество жизни пациентов. Интенсификация стратегий требует активной поддерживающей терапии, в первую очередь адекватной коррекции анемии; при этом улучшение состояния пациента может рассматриваться как резерв повышения результативности лечения онкопатологии.
Применение в онкологической практике современных химиопрепаратов, агрессивного сочетания химиотерапии с лучевой терапией, использование высоких доз интерферонов и интерлейкинов увеличивают эффективность лечения, но вместе с тем существенно ухудшают качество жизни пациентов. Интенсификация стратегий требует активной поддерживающей терапии, в первую очередь адекватной коррекции анемии; при этом улучшение состояния пациента может рассматриваться как резерв повышения результативности лечения онкопатологии.
Распространенность анемии у больных со злокачественными опухолями изучали в крупном многоцентровом исследовании ECAS (European Cancer Anaemia Survey), в котором приняли участие 15 367 пациентов из 750 клиник. Результаты испытания показали, что на момент установления первичного диагноза анемию зарегистрировали у 39,3% пациентов, а за 6 мес на фоне противоопухолевого лечения соответствующий показатель возрос до 67,0%. У пациенток с опухолями репродуктивной системы частота анемии составляет 81%, при раке легкого – 77%, при лимфопролиферативных заболеваниях – 73%, новообразованиях желудочно-кишечного тракта – 61%, опухолях головы и шеи – 51%. В целом частота и степень тяжести анемии зависят от типа опухоли, стадии онкологического заболевания и его длительности, характера лечения.
В целом частота и степень тяжести анемии зависят от типа опухоли, стадии онкологического заболевания и его длительности, характера лечения.
К дополнительным факторам риска развития анемии также относят низкий исходный уровень Hb, рефрактерность болезни к противоопухолевой терапии, женский пол (Ludwig H. et al., ECAS, 2004).
Анемия у онкологических больных имеет мультифакторное происхождение. Основными этиопатогенетическими механизмами развития анемии являются угнетение эритропоэза и уменьшение реутилизации железа в костном мозге, сокращение срока жизни и усиление разрушения эритроцитов на фоне противоопухолевого лечения, кровопотери в результате осложнений течения злокачественного процесса. Так, подавление эритропоэза происходит вследствие инфильтрации костного мозга опухолевыми клетками (при гемобластозах), действия различных цитокинов. Для опухолевого процесса характерна гиперпродукция провоспалительных цитокинов, в частности интерлейкина‑6 (ИЛ‑6) и фактора некроза опухоли (ФНО). Данные цитокины обладают плейоморфным негативным влиянием на различные этапы эритропоэза, длительность жизни эритроцитов, обмен железа. Например, ФНО тормозит утилизацию железа, разрушает мембрану эритроцитов, участвует в супрессии ранних эритроидных клеток.
Данные цитокины обладают плейоморфным негативным влиянием на различные этапы эритропоэза, длительность жизни эритроцитов, обмен железа. Например, ФНО тормозит утилизацию железа, разрушает мембрану эритроцитов, участвует в супрессии ранних эритроидных клеток.
В этиопатогенезе анемии при онкологических заболеваниях важная роль принадлежит ИЛ‑6; одним из его эффектов является повышенный синтез в печени гепсидина – пептида, регулирующего обмен железа и эритропоэз. Гепсидин является негативным регулятором поступления железа из клеток, блокируя его выход из макрофагов и снижая абсорбцию в тонком кишечнике. Таким образом, хроническая активация иммунной системы при неопластических процессах сопровождается вторичным повышением концентрации гепсидина и недостаточной реутилизацией железа костным мозгом при достаточных запасах в организме. Подобное состояние характерно для функционального дефицита железа.
Непосредственно угнетают кроветворение лучевая терапия и химиотерапия: препараты, содержащие платину, обладают нефротоксичностью, провоцируя снижение синтеза эндогенного эритропоэтина; цитостатики вызывают миелосупрессию, при этом наблюдается кумулятивный эффект их повторного применения, что усугубляет анемию. Лимфопролиферативные заболевания сопровождаются аутоиммунным гемолизом. Хронические скрытые кровотечения и дефицит витаминов и железа характерны для неоплазий желудочно-кишечного тракта.
Лимфопролиферативные заболевания сопровождаются аутоиммунным гемолизом. Хронические скрытые кровотечения и дефицит витаминов и железа характерны для неоплазий желудочно-кишечного тракта.
По данным литературы, в целом частота железодефицита у онкологических больных составляет от 32 до 60%. Абсолютный дефицит развивается в результате недостаточного поступления алиментарного железа, снижения его абсорбции в желудочно-кишечном тракте, а также повышения потребности организма в железе при хирургических вмешательствах, кровотечениях. Функциональный дефицит железа прежде всего связан с усилением эритропоэза на фоне лечения эритропоэтином (ЭПО) либо стимуляции костного мозга, а также блокированием выхода железа из макрофагов и эпителиоцитов кишечника при повышенной экспрессии острофазового пептида гепсидина. У онкологических больных чаще всего встречается сочетание патогенетических и клинических признаков абсолютного и функционального дефицита железа.
С учетом всего вышеизложенного анемия при онкологических заболеваниях может быть определена как сложное патологическое состояние, развивающееся вследствие специфики основного заболевания и усугубляющееся в процессе его лечения. Помимо анемии, вызванной миелосупрессией, повышенным гемолизом и кровотечением, развиваются анемия хронического заболевания и железодефицит. Клинические последствия анемии у онкологических больных – снижение эффективности химиотерапии и вероятности успеха лучевой терапии.
Помимо анемии, вызванной миелосупрессией, повышенным гемолизом и кровотечением, развиваются анемия хронического заболевания и железодефицит. Клинические последствия анемии у онкологических больных – снижение эффективности химиотерапии и вероятности успеха лучевой терапии.
Анемия проявляется рядом симптомов, обусловленных развитием клеточной гипоксии в тканях и органах с последующим нарушением их функций. Степень выраженности этих симптомов зависит от уровня Hb, сопутствующей патологии, физиологического статуса пациента. Следует подчеркнуть, что анемия может быть одним из первых признаков онкологического заболевания. Ее первичными функциональными симптомами считаются выраженная слабость, утомляемость, одышка, тахикардия, значительное снижение работоспособности при обычных нагрузках. При этом слабость относят к основным жалобам таких пациентов, частота ее встречаемости достигает 75% и коррелирует с уровнем Hb. В условиях доступности адекватного обезболивания именно слабость и повышенная утомляемость отмечаются больными как наиболее частый симптом, существенно ухудшающий качество их жизни и являющийся одной из причин отказа от химиотерапии. Помимо этого, слабость вследствие побочных эффектов химиопрепаратов усиливается при развитии тошноты, рвоты, диареи.
Помимо этого, слабость вследствие побочных эффектов химиопрепаратов усиливается при развитии тошноты, рвоты, диареи.
Гематологически анемия, связанная с онкологическими заболеваниями, является гипопролиферативной, она может быть нормоцитарной и нормохромной, микроцитарной и гипохромной или макроцитарной. Макроцитарная анемия часто связана с недостаточностью функции костного мозга, тогда как микроцитарная чаще развивается вследствие гемолиза или нарушений метаболизма железа. В большинстве случаев анемия у онкологических больных характеризуется снижением уровня Hb (≤12 г/дл), нарушением утилизации железа, накоплением его в ретикулоэндотелиальной системе, что проявляется снижением уровня сывороточного железа и низкой степенью насыщения трансферрина (≤15%) при повышении уровня ферритина. В различных публикациях критерии диагностики железодефицитной анемии у онкологических больных отличаются между собой. В частности, рекомендации NCCN (National Comprehensive Cancer Network) за 2012 год предлагают диагностировать абсолютный дефицит железа при снижении уровня ферритина ≤30 нг/мл и степени насыщения трансферрина ≤15%. При данном варианте течения анемии лечение целесообразно начинать с препаратов железа. Функциональный дефицит диагностируют при более высоком (до 800 нг/мл) уровне ферритина и степени насыщения трансферрина ≤20%; в этом случае препараты железа применяют со стимуляторами эритропоэза.
При данном варианте течения анемии лечение целесообразно начинать с препаратов железа. Функциональный дефицит диагностируют при более высоком (до 800 нг/мл) уровне ферритина и степени насыщения трансферрина ≤20%; в этом случае препараты железа применяют со стимуляторами эритропоэза.
Стратегия коррекции анемии у онкологических больных предусматривает необходимость определения статуса дефицита железа (абсолютный или функциональный) для выбора оптимальной тактики комплексного лечения. Основными вариантами лечения анемии, индуцированной химиотерапией, являются гемотрансфузии, терапия ЭПО и препаратами железа. Гемотрансфузия позволяет быстро восполнить дефицит эритроцитов и достичь повышения Hb и гематокрита, однако связана с риском развития быстрых и отсроченных посттрансфузионных реакций и осложнений, а также с опасностью инфицирования вирусами гепатита В и С, ВИЧ, бактериальной контаминации, иммуносупрессии, перегрузки железом. При повторных трансфузиях могут отмечаться гемолитические реакции, связанные с развитием сенсибилизации к редким антигенам эритроцитов. Кроме того, существенный недостаток быстрой коррекции Hb при гемотрансфузии – кратковременность эффекта.
Кроме того, существенный недостаток быстрой коррекции Hb при гемотрансфузии – кратковременность эффекта.
Альтернативой гемотрансфузии выступает использование экзогенных стимуляторов эритропоэза, которые компенсируют абсолютное или относительное снижение продукции эндогенного ЭПО. В настоящее время в онкологической практике ЭПО применяются в сочетании с препаратами железа для внутривенного введения.
Данная тактика является абсолютно патогенетически оправданной, так как у онкологических больных запасы железа ограничены и при активации эритропоэза быстро истощаются. Кроме того, у таких пациентов чаще встречается функциональный дефицит железа вследствие хронической стимуляции иммунной системы в условиях злокачественного процесса, повышенной экспрессии цитокинов и усиления синтеза гепсидина. Внутривенное введение транспортной формы железа (III) и доставка его в органы эритропоэза позволяют обойти «блокаду» макрофагов и эпителиоцитов кишечника, вызываемую гепсидином. В нескольких рандомизированных клинических исследованиях продемонстрировано, что внутривенное введение препаратов трехвалентного железа позволяет повысить частоту ответа на лечение ЭПО с 25-70 до 68-93%. Имеются данные, что применение препаратов железа для внутривенного введения ассоциируется со снижением затрат на лечение онкологических больных вследствие уменьшения доз ЭПО и потребности в гемотрансфузиях.
Имеются данные, что применение препаратов железа для внутривенного введения ассоциируется со снижением затрат на лечение онкологических больных вследствие уменьшения доз ЭПО и потребности в гемотрансфузиях.
При анемии, индуцированной химиотерапией, внутривенное введение препаратов железа является методом выбора, если необходимо достичь быстрого восполнения железодефицита и увеличения уровня Hb. Кроме того, анорексия, тошнота и рвота не позволяют принимать препараты железа перорально.
Один из основных аргументов против внутривенного введения препаратов железа – риск развития аллергических реакций вплоть до анафилаксии. Сахарат железа для внутривенного ведения реже других препаратов этой группы вызывает реакции гиперчувствительности, поэтому может применяться в дозе 200 мг/кг болюсом без дополнительного разведения с индивидуальным подбором дозы. Сахарат железа характеризуется низкой токсичностью; повторные его введения можно проводить каждые 1-3 нед, что хорошо подходит для пациентов онкологического профиля с анемией, индуцированной химиотерапией.
В Украине для лечения абсолютного и функционального железодефицита успешно применяется препарат железа для внутривенного введения Суфер («Юрия-Фарм»), 1 мл которого содержит комплекс гидроксида железа (III) с сахарозой, эквивалентный 20 мг железа. Суфер – высокоэффективное лекарственное средство для внутривенного введения с благоприятным профилем безопасности, применяющееся с целью коррекции абсолютного или функционального дефицита железа. Накопленный положительный опыт дает возможность рекомендовать Суфер для коррекции анемии, индуцированной химиотерапией.
В заключение можно отметить, что благодаря достижениям современной медицины и возможности длительного применения паллиативной терапии выживаемость, а также качество жизни онкологических больных повышаются. Однако в целом значимость проблемы дефицита железа как при онкологических, так и при многих других заболеваниях все еще остается недооцененной. Поэтому изучение влияния дефицита железа у пациентов онкологического профиля и расширение возможностей коррекции данного состояния представляется перспективным направлением для дальнейших исследований.
Подготовила Наталия Позднякова
СТАТТІ ЗА ТЕМОЮ Онкологія та гематологія
19.01.2022 Онкологія та гематологія Терапія та сімейна медицина Паліативна допомога: акцент на знеболюванніЗа визначенням Всесвітньої організації охорони здоров’я (ВООЗ), паліативна допомога – це підхід, що дозволяє поліпшити якість життя пацієнтів (дітей і дорослих) та їхніх сімей і вирішити проблеми, пов’язані із загрозливим для життя захворюванням, запобігаючи стражданням і полегшуючи їх шляхом раннього виявлення, ретельного оцінювання й купірування болю та інших фізичних симптомів, а також включає надання психосоціальної і духовної підтримки (ВООЗ, 2002). 23 листопада відбулася науково-практична школа-семінар «Паліативний пацієнт: допоможемо провести життя з рідними, а не з болем».
…
23 листопада відбулася науково-практична школа-семінар «Паліативний пацієнт: допоможемо провести життя з рідними, а не з болем».
…
Високі показники гіпердіагностики є основною перепоною для організованого скринінгу раку передміхурової залози (РПЗ). Цю проблему можна вирішити застосуванням магнітно-резонансної томографії (МРТ) із цільовою біопсією, однак досі не з’ясовано, чи придатний такий метод для організованого скринінгу РПЗ. …
…
Лечении анемии
Питание больных с анемией должно быть полноценным и в нем должно быть достаточно большое количество не только белков и углеводов, но и непосредственно самого железа. Железо в еде делится на два вида – это гемовое и негемовое. Первое содержится в различных мясных и рыбных продуктах, и на его всасываемость посторонние продукты практически не влияют. Немного сложнее все со вторым видом железа, хотя его и можно найти в различных растительных продуктах – таких как яблоки, гранат, сухофрукты, зелень в свежем виде и так далее. По сравнению с гемовым это железо всасывается гораздо хуже.
Установлено, что лечение анемии происходит гораздо эффективнее, когда в организме присутствует аскорбиновая кислота. Поэтому на Вашем столе должны постоянно быть соответствующие продукты, богатые витамином С.
А вот те продукты, которые препятствуют всасыванию железа и от которых, следовательно, Вам стоит отказаться – это свежая зелень, сыр, а также различные напитки, в том числе кофе и чай.
Помимо богатой диеты больным необходимы и витамины, и лучше бы если бы это был целый специально подобранный витаминный комплекс.
Ни для кого, наверное, не секрет, что к полноценной диете для лечения анемии так же необходимы и лекарственные препараты, содержащие в себе железо, так как разнообразная диета играет лишь вспомогательную роль и дополняет действие медикаментов.
Рекомендации ВОЗ по лечению анемии являются следующими:
- Для профилактики понижения гемоглобина абсолютно все беременные женщины должны получать железо и фолиевую кислоту в профилактических дозах.
- Если результат анализа крови показал, что у беременной все же снизился гемоглобин, то тогда дозу железа ей увеличивают вдвое.
- Желательно, чтобы препараты железа употреблялись исключительно внутрь, а медикаменты для инъекций использовались только в самых тяжелых случаях.

- Пить железо нужно долгое время, а именно не менее двух месяцев.
Лечение анемии в клинике «Скандинавия»
Клиника «Скандинавия» готова предложить своим клиентам услуги по лечению анемии. Для Вас только лучшие специалисты и оборудование по приемлемым ценам. Для того, чтобы получить консультацию, Вам достаточно оставить свою заявку на нашем сайте, либо связаться с нами по контактному телефону 600-77-77.
Как принимать препараты железа — статьи Lab4u.RU
Делать или не делать, пить или не пить лекарство, сдавать или не сдавать анализ. Мы всегда стоим перед выбором и часто боимся ошибиться. Железно можно сказать, что с железом ошибаться нельзя.
В организме взрослого человека содержится около 3–4,5 г железа. Больше половины железа представлено гемом в составе гемоглобина, треть запасается в депо в виде ферритина и гемосидерина. При этом дефицит железа – наиболее распространенное дефицитное состояние во всем мире, скрытно приводящее к анемии.
Основные причины дефицита железа:
Снижение поступления железа в организм в связи с нарушением его всасывания при заболеваниях желудочно-кишечного тракта, голодании, отказе или уменьшение потребления продуктов питания, содержащих железо.
Увеличение потерь железа при хронических, повторных кровопотерях (маточных, желудочных, кишечных, и др.), а также при остром объемном кровотечении.
Повышенное расходование железа организмом у детей в периоды роста, у женщин во время беременности и последующего грудного вскармливания ребёнка.
Какие анализы показывают железодефицит
Анализы рекомендовано сдавать в утренние часы, с 8 до 11 утра, так как уровень железа в сыворотке в утренние часы выше. Также их стоит сдавать при отсутствии воспаления, которое способствует понижению уровня трансферрина и повышению уровня ферритина.
Содержание железа в сыворотке смотрят через 5-7 дней после приема витаминно-минеральных комплексов и БАДов, содержащих железо, или недолгого приема препаратов железа.
Как лечат железодефицит
Необходимо выявить и устранить причину железодефицита, скорректировать питание. Если эти меры не помогают, а потери железа значительные, врач может назначить лекарственные препараты на основе железа.Длительность курса лечения препаратами железа с целью восстановления и пополнение запасов железа в депо:
- при скрытом железодефиците 1-2 месяца,
- при анемии легкой степени 3 мес,
- при анемии средней степени 4,5 мес,
- при тяжелой анемии 6 мес.
Конечно, в первую очередь, используют препараты железа в виде таблеток, капель, капсул, сиропов. Если врач назначил вам препараты железа, необходимо настроиться на длительное и комфортное лечение. Этому поможет соблюдение простых правил.
Дозировку препарата также определяют по наличию анемии (это полная лечебная доза) и вида иона железа, который входит в лекарственный препарат.
Какие препараты железа бывают
Железо в препаратах может быть представлено двух- или трехвалентным ионом, обозначаемым Fe2+ или Fe3+, входящим в состав солей или сложных комплексов (например, гидроксид полимальтозного комплекса).
При использовании солей железа можно столкнуться с проблемой его всасывания. К сожалению, не все железо из препарата всасывается в желудочно-кишечном тракте. Более того, этот процесс плохо контролируется, поскольку зависит от состояния желудочно-кишечного тракта, принимаемой пищи, других лекарственных препаратов. Поэтому возможна как нехватка поступающего железа, так и его передозировка. К тому же, не все формы выпуска лекарств удобны к применению, некоторые таблетки если разжевать, то часто окрашивается эмаль зубов и надолго остается металлический привкус во рту. Трехвалентные препараты железа обычно лишены этих побочных свойств.
Как повысить эффективность лечения
Для снижения вероятности побочных эффектов препараты солей железа принимают до еды.
Всасываемость железа выше при одновременном приеме с аскорбиновой и янтарной кислотами, фруктозой, цистеином. Это свойство используется в некоторых комбинированных препаратах.
Всасывание железа уменьшается под влиянием некоторых веществ из пищи или лекарств. Так, его уменьшают танин (крепкозаваренный чай), соли кальция (в молоке или препаратах), магний и марганец (в минеральных комплексах или антацидных препаратах, типа фосфалюгеля), тетрациклиновые антибиотики, фосфорная и фитиновые кислоты (семена злаковых, бобовые). Это влияние сглаживается при использовании препаратов на основе трехвалентного железа.
Всасывание железа повышается при тяжелом железодефиците. Поэтому стоит внимательнее относится к назначенной дозировке. Врачи часто отталкиваются от лечебной дозы в 200 мг иона железа/сутки. Если вы понимаете, что препарат железа вам не подходит из-за развития побочных реакций, трудностей приема, отсутствия улучшения самочувствия, скажите об этом врачу. Ни в коем случае не меняйте дозировку препарата самостоятельно. Превышение дозы может привести к передозировке и отравлению, снижение дозы — к бесполезному приему и отсутствию эффекта.
Ни в коем случае не меняйте дозировку препарата самостоятельно. Превышение дозы может привести к передозировке и отравлению, снижение дозы — к бесполезному приему и отсутствию эффекта.
Как оценивают эффективность лечения
В первые дни лечения препаратами железа оцениваются физические ощущения.
При лечении анемии, на 5-8-й день лечения определяют ретикулоцитарный криз (увеличение числа ретикулоцитов по сравнению с исходным значением, обычно на 2–3% или 20–30‰).
Через 4 недели лечения оценивают прирост гемоглобина. Повышение концентрации гемоглобина к концу первого месяца лечения препаратами железа на 10 г/л говорит о правильно подобранной дозе и эффективности терапии. После восстановления гемоглобина терапию продолжают для насыщения депо железа, при этом доза препарата снижается в 2 раза.
При скрытом дефиците железа применяют половинные дозы препаратов на протяжении 4-8 недель. Насыщение депо определяется с помощью комплексного биохимического исследования (ферритин, трансферрин, ОЖСС).
В Lab4U вы можете сдать анализы для выявления железодефицита и контролировать эффективность терапии со скидкой до 50%.
ИсточникиИнтерпретацию результатов анализов, выбор дальнейшего обследования и лечения осуществляет лечащий врач.
6 лучших препаратов железа — Рейтинг 2021
Обновлено: 24.02.2021 17:56:38*Обзор лучших по мнению редакции expertology.ru. О критериях отбора. Данный материал носит субъективный характер, не является рекламой и не служит руководством к покупке. Перед покупкой необходима консультация со специалистом.
По данным ВОЗ, более 2 млрд. человек в мире страдают от анемии, вызванной недостатком железа. Большая часть из них – женщины и дети. В России анемия есть у 12% женщин детородного возраста, а от скрытого дефицита железа страдает едва ли не половина фертильных женщин. Причина этого – особенности женской физиологии в сочетании с недостаточным поступлением элемента с пищей. Среди детей каждый третий имеет либо клинически выраженную анемию, либо скрытый дефицит железа.
Среди детей каждый третий имеет либо клинически выраженную анемию, либо скрытый дефицит железа.
В организм оно поступает с пищей, но усваивается довольно плохо, особенно из растительных продуктов. Если из мяса человек может усвоить до 20% содержащегося железа, то из растений – не более 5%. Именно поэтому ВОЗ считает вегетарианок находящимися в группе риска по железодефицитным анемиям беременных и рекомендует им препараты железа в профилактических целях с самых ранних сроков. Пожалуй, это единственная группа людей, которым подобные средства назначают для профилактики.
Другая группа, которой они могли бы понадобиться – женщины с обильными менструациями. Их суточная потребность в железе – 3 мг, тогда как с пищей в сутки может усвоиться не более 2 мг этого вещества. Но на практике, если железодефицит еще не развился, для его профилактики бывает достаточно витаминно-минерального комплекса с содержанием железа – даже в недорогом отечественном «Компливите» есть 5 мг этого элемента.
Поэтому обычно показанием для применения препаратов железа становится диагностированная анемия – недостаток гемоглобина в крови.
Признаки недостатка железа в организме
Большая часть железа в организме находится в виде гемоглобина – особого вещества, которое связывает кислород из воздуха и отдает его в ткани, взамен выводя из них углекислоту. Поэтому о количестве железа в крови чаще всего судят по уровню гемоглобина. Нормальное содержание гемоглобина в крови для мужчин 130–170 г/л, женщин 120–150 г/л (во время беременности норма снижается до 110–140, так как в этот период кровь разжижается), для детей от года до 14 лет – 110–150 г/л.
Но на практике нормальные показатели гемоглобина далеко не гарантируют нормального содержания железа в организме. Полноценный кислородный обмен жизненно важен для всех органов и систем: головной мозг погибает без кислорода за 5 – 6 минут. Организм всеми силами будет поддерживать нормальный уровень гемоглобина, пока не будут исчерпаны все резервы. Поэтому о дефиците железа обычно судят по другим показателям.
Поэтому о дефиците железа обычно судят по другим показателям.
|
показатель |
норма для женщин |
норма для мужчин |
|
ферритин |
10–120 мкг/л |
20–250 мкг/л |
|
трансферрин |
2–4 г/л |
2–4 г/л |
|
% насыщения трансферрина |
15–50 |
20–55 |
|
сывороточное железо |
80,9–30,4 мкмоль/л |
11,6–30,4 мкмоль/л |
Снижение любого из этих показателей говорит о скрытом дефиците железа в организме.
По мере того, как проблема нарастает, появляются и признаки, которые можно обнаружить самостоятельно:
- сухие, секущиеся волосы, чрезмерная потеря волос;
- ломкие ногти,
- «заеды» в углах губ, трещины, сухость кожи вокруг рта;
- нарушение сна: днем – сонливость, ночью бессонница;
- язык становится гладким, исчезают сосочки;
- извращение вкуса – желание есть мел, землю, резину и другие несъедобные вещи;
- быстрая утомляемость, мышечная слабость.
Эти симптомы связаны с недостатком макроэлемента в тканях: он необходим не только для нормального кислородного обмена, но и для мышц (15% всего железа организма находится в составе мышечного белка миоглобина), многих обменных процессов.
Рейтинг лучших препаратов железа
Лучшие препараты железа для беременных
Как уже упоминалось, до 50% женщин фертильного возраста имеют скрытый дефицит железа. После наступления беременности ситуация ухудшается. 320–500 мг этого вещества уходит на прирост гемоглобина и возросший клеточный метаболизм, 100 мг — на построение плаценты, 50 мг — на увеличение размеров матки, 400–500 мг — на потребности плода. Таким образом, всего за беременность расходуется дополнительно 1200–1140 мг железа. Особенно активно оно тратится на 16–20 неделе беременности, когда у плода запускается процесс кроветворения. К этому времени ежедневная потребность женщины в железе возрастает до 6 мг в день.
После наступления беременности ситуация ухудшается. 320–500 мг этого вещества уходит на прирост гемоглобина и возросший клеточный метаболизм, 100 мг — на построение плаценты, 50 мг — на увеличение размеров матки, 400–500 мг — на потребности плода. Таким образом, всего за беременность расходуется дополнительно 1200–1140 мг железа. Особенно активно оно тратится на 16–20 неделе беременности, когда у плода запускается процесс кроветворения. К этому времени ежедневная потребность женщины в железе возрастает до 6 мг в день.
Для профилактики дефицита железа, как уже упоминалось, обычно бывает достаточно витаминно-минеральных комплексов. Но если анемия уже развилась, необходимые дозировки железа становятся гораздо выше: от 100 до 300 мг в сутки.
Выбирая лучшие препараты железа для включения в рейтинг мы следовали рекомендациям ВОЗ, согласно которым для лечения анемии, в том числе у беременных, предпочтительней средства, содержащие двухвалентное железо. Именно в такой форме оно лучше всего усваивается в желудочно-кишечном тракте. При домашнем использовании пероральные (для приема через рот) лекарства лучше инъекционных. Во-первых, чтобы их использовать не нужен медперсонал или люди, обладающие специальными навыками, во-вторых, исключается вероятность постинъекционных осложнений. Поэтому мы не стали вносить в рейтинг средства для инъекций, оставив их для специалистов, работающих в условиях медицинских учреждений.
Именно в такой форме оно лучше всего усваивается в желудочно-кишечном тракте. При домашнем использовании пероральные (для приема через рот) лекарства лучше инъекционных. Во-первых, чтобы их использовать не нужен медперсонал или люди, обладающие специальными навыками, во-вторых, исключается вероятность постинъекционных осложнений. Поэтому мы не стали вносить в рейтинг средства для инъекций, оставив их для специалистов, работающих в условиях медицинских учреждений.
Все пероральные препараты железа не рекомендуется сочетать с едой, так как чай, кофе, продукты, богатые кальцием, снижают их усвояемость. По той же причине нельзя сочетать их с препаратами магния и алюминия (большинство средств от изжоги).
Судить об эффективности терапии нужно не раньше чем через 3 недели, продолжительность приема – от месяца до полугода: такой долгий срок нужен для того, чтобы обновились депо организма и красные кровяные клетки (средний срок жизни эритроцита – 120 дней).
Тотема
Рейтинг: 4.8
Содержит железо, медь и марганец. Последние два вещества нужны, чтобы улучшить усвоение железа: они входят в состав транспортных белков. Кроме того, они способствуют усилению антиоксидантной защиты: ионы двухвалентного железа могут активировать процесс перекисного окисления липидов на поверхности слизистой оболочки желудка и таким образом спровоцировать нежелательные явления (изжога, тошнота, диарея).
Выпускается в виде раствора для приема внутрь, который нужно растворить в стакане воды или яблочного сока. В сутки необходимо от 2 до 4 ампул. Чтобы уменьшить вероятность нежелательных явлений, рекомендуется начинать с минимальной дозировки и постепенно ее увеличивать.
Поскольку раствор может окрасить эмаль зубов, пить его лучше через трубочку, а сразу после употребления – чистить зубы.
Достоинства
- хорошо усваиваемая форма,
- комплексный состав,
-
доступная цена.

Недостатки
- неприятный вкус,
- неудобно вскрывать ампулы.
Ферро–Фольгамма
Рейтинг: 4.7
В составе, кроме двухвалентной соли железа, цианокобаламин (витамин В12), фолиевая и аскорбиновая кислота. Витамин В12 и фолиевая кислота улучшают кроветворение, а витамин С способствует лучшему всасыванию железа, а кроме того это сильный антиоксидант. По отзывам врачей, это средство повышает гемоглобин в среднем на 2,5 мг в сутки, поэтому самочувствие пациенток улучшается довольно быстро. Тем не менее, курс лечения необходимо завершить полностью, иначе результаты окажутся временными.
Выпускается в капсулах, которые нужно принимать по 1 – 2 х 3 раза в день.
Достоинства
- быстро нормализует уровень гемоглобина,
- удобная форма выпуска.
Недостатки
-
возможны побочные эффекты.

Фенюльс
Рейтинг: 4.5
Еще один комплекс, сочетающий двухвалентное железо с витаминами: содержит витамины группы В (В1, В2, В3, В5, В6), нормализующие обмен веществ, который нередко нарушается при дефиците железа; и С. Капсулы лекарства содержат микрогранулы, из которых железо и витамины высвобождаются постепенно, что уменьшает раздражение слизистой оболочки желудка и, следовательно, вероятность появления побочных эффектов.Принимать по 1 – 2 капсулы в день, в зависимости от тяжести анемии.
Достоинства
- обычно достаточно 1 таблетки в сутки,
- замедленное всасывание уменьшает выраженность побочных явлений,
- низкая цена.
Гино-тардиферон
Рейтинг: 4.4
Содержит соль железа и фолиевую кислоту, нормализующую кроветворение и формирование нервной системы плода. Рекомендуется по 1 – 3 таблетки в день, в зависимости от тяжести анемии. После восстановление гемоглобина до нормы дозировку нужно снизить до 1 таблетки в день, далее, стандартный для большинства препаратов железа курс от 1 до 3 месяцев.
Рекомендуется по 1 – 3 таблетки в день, в зависимости от тяжести анемии. После восстановление гемоглобина до нормы дозировку нужно снизить до 1 таблетки в день, далее, стандартный для большинства препаратов железа курс от 1 до 3 месяцев.
Принимая препараты железа нужно помнить, что все они окрашивают стул в черный цвет, и сделанный в это время анализ на скрытую кровь дает ложноположительный результат, так как он измеряет именно железо в кале (которого в норме не должно быть). Очень осторожно к таким средствам нужно относиться людям, страдающим гастритом, гастроэнтероколитом и другими воспалительными заболеваниями ЖКТ, так как они раздражают слизистую оболочку.
Лучшие препараты железа для детей
Если при выборе лекарства для взрослых прежде всего учитывается эффективность и безопасность, то когда речь идет о средстве для детей на первый план выходит приверженность ребенка к лечению. Ни одна мать не выдержит долго, если лекарство в малыша каждый раз придется в прямом смысле запихивать с боем.
Есть и еще один нюанс: форма выпуска. Таблетки нельзя назначать детям до 3 лет, а лекарства в капсулах запрещены для детей младше 7 из опасения, что ребенок поперхнется таблеткой или капсулой. То есть препараты для детей – это капли или сиропы. Но двухвалентное железо имеет ярко выраженный металлический привкус, который не могут скрыть никакие добавки – и дети часто отказываются их принимать. К тому же, двухвалентное ионное железо при всех его достоинствах, раздражает слизистую желудочно-кишечного тракта, и нежный детский организм реагирует на это тошнотой и рвотой куда чаще, чем взрослые.
Поэтому в рейтинг лучших препаратов железа для детей мы включили средства, содержащие трехвалентное железо – но в особой, современной форме: гидроокись железа с полимальтозным комплексом. Это крупная молекула, состоящая из железного «ядра», окруженного полимальтозной (полисахаридной) оболочкой. Таким образом макроэлемент непосредственно не взаимодействует с клетками желудочно-кишечного тракта и не раздражает их; не проявляет свой характерный вкус в каплях, жидкостях и сиропах; не взаимодействует с другими веществами. Всасывание такого железа медленней, чем двухвалентного, но в целом усвояемость оказывается достаточной для эффективной терапии.
Всасывание такого железа медленней, чем двухвалентного, но в целом усвояемость оказывается достаточной для эффективной терапии.
Еще одно преимущество подобных препаратов – ими невозможно отравиться из-за замедленного всасывания, и это очень важно, когда дело касается ребенка.
Дозировка лекарств, содержащих гидроокись железа с полимальтозным комплексом: 3 – 5 мг активного железа на кг массы тела. Более точные указания даст лечащий врач: заниматься самолечением, когда речь идет о детях, не слишком разумно.
Мальтофер капли
Рейтинг: 4.9
В 1 мл раствора (20 каплях) содержится 50 мг железа, то есть в 1 капле – 2,5 мг. Таким образом, их очень просто дозировать: 1-2 капли на килограмм веса ребенка в сутки, в зависимости от тяжести анемии. Суточную дозу можно принять за 1 раз, смешав капли с соком или любым безалкогольным напитком. Средство не имеет возрастных ограничений.
Достоинства
- безопасность,
-
удобный способ дозировки.

Недостатки
- содержит сахар
Феррум-Лек сироп
Рейтинг: 4.6
В 1 мерной ложке сиропа – 50 мг активного железа. Точно так же, как и предыдущее средство, лекарство можно смешивать с любым безалкогольным напитком или добавлять в детское питание. Из-за того, что минимальное количество сиропа, которое можно отмерить – половина мерной ложки, детям до года препарат не рекомендуется.
Достоинства
- безопасность,
- низкая цена.
Недостатки
- только для детей старше года.
| Оцените статью | |
Всего голосов: 4, рейтинг: 5 |
 Перед покупкой необходима консультация со специалистом.
Перед покупкой необходима консультация со специалистом.Железосодержащие добавки для лечения анемии
Железо — это минерал, необходимый для жизни. Железо играет ключевую роль в создании эритроцитов, которые переносят кислород. Вы можете получить железо из пищи и пищевых добавок. Если вам не хватает железа, у вас может развиться анемия, низкий уровень эритроцитов. Однако большинство людей в США получают железо из пищи.
Почему люди принимают железо?
Железосодержащие добавки чаще всего используются при определенных видах анемии.Анемия может вызвать усталость и другие симптомы. Если у вас есть симптомы анемии, обратитесь за помощью к своему врачу. Не пытайтесь лечить его самостоятельно.
Добавки железа часто назначают для лечения анемии, вызванной:
В группу риска дефицита железа могут входить недоношенные дети, маленькие дети, девочки-подростки и беременные женщины, а также люди с определенными заболеваниями, включая хроническую сердечную недостаточность , болезнь Крона, глютеновая болезнь и язвенный колит. Добавки железа обычно рекомендуются беременным женщинам или женщинам детородного возраста для предотвращения анемии. Прежде чем принимать добавку железа, спросите своего лечащего врача, подходит ли она вам.
Добавки железа обычно рекомендуются беременным женщинам или женщинам детородного возраста для предотвращения анемии. Прежде чем принимать добавку железа, спросите своего лечащего врача, подходит ли она вам.
Сколько железа нужно принимать?
Рекомендуемая диетическая норма (RDA) включает железо, которое вы получаете как из пищи, которую вы едите, так и из любых пищевых добавок, которые вы принимаете.
Категория | Рекомендуемые диетические пособие (RDA) | ||
ДЕТИ | |||
7-12 месяцев | 11 мг / сут | ||
1-3 лет | 70027 | ||
10 мг / день | |||
9-13 лет | 8 мг / день | ||
|
| ||
14-18 лет | 15 мг / день | ||
19-50 лет | 18 мг/день | ||
51 год и старше | 8 мг/день | ||
Беременные | 27 мг / день | грудное вскармливание | младше 19 лет : 10 мг / день |
мужчин | |||
11 мг / день | |||
19 лет и до | 8 мг /день | ||
Строгим вегетарианцам может потребоваться более высокий уровень железа.
В высоких дозах железо токсично. Для взрослых и детей в возрасте 14 лет и старше верхний предел — самая высокая доза, которую можно безопасно принимать — составляет 45 мг в день. Детям до 14 лет не следует принимать более 40 мг в день.
Американская академия педиатрии предлагает, начиная с 4-месячного возраста, доношенным детям, находящимся на грудном вскармливании, давать перорально 1 мг/кг железа в день. Это должно продолжаться до тех пор, пока в рацион не будут введены железосодержащие продукты прикорма, такие как каши, обогащенные железом.Стандартная смесь для детского питания, содержащая 12 мг/л железа, может удовлетворить потребности ребенка в железе до 1 года.
Спросите у своего лечащего врача, сколько добавок железа вы или ваш ребенок должны принимать, если таковые имеются.
Можно ли получать железо естественным путем из продуктов питания?
Для большинства людей хорошее питание обеспечивает достаточное количество железа. Природные пищевые источники железа включают:
- Мясо, рыбу и птицу
- Овощи, такие как шпинат, капуста и брокколи
- Сухофрукты и орехи
- Фасоль, чечевицу и горох
Во многие продукты также добавляют железо обогащенные продукты, такие как хлопья и обогащенный хлеб.
Железо животного происхождения лучше усваивается организмом. Однако вы можете помочь своему организму усваивать железо растительного происхождения, употребляя в пищу фрукты или овощи с высоким содержанием витамина С (например, красный сладкий перец, киви, апельсины).
Каковы риски приема железа?
- Побочные эффекты. Прием в обычных дозах препаратов железа может вызвать расстройство желудка, изменение стула и запор.
- Риски. Не начинайте принимать железосодержащие добавки, если только ваш лечащий врач не скажет вам, что они вам нужны.Это особенно верно, если у вас есть хронические заболевания. Женщины, которые планируют забеременеть, также должны проконсультироваться с врачом, прежде чем начинать ежедневный прием добавок железа.
- Взаимодействие. Железо может взаимодействовать со многими различными лекарствами и добавками. К ним относятся антациды и ингибиторы протонной помпы, некоторые антибиотики, кальций и другие.
 Убедитесь, что ваш врач знает обо всех рецептурных и безрецептурных лекарствах, которые вы принимаете, если они предлагают вам принимать добавки железа.
Убедитесь, что ваш врач знает обо всех рецептурных и безрецептурных лекарствах, которые вы принимаете, если они предлагают вам принимать добавки железа. - Передозировка. Передозировка железом является частой причиной отравления детей. Это может быть фатальным. Признаки передозировки железа включают сильную рвоту и диарею, желудочные спазмы, бледность или синюшность кожи и ногтей, а также слабость. Рассматривайте эти признаки как неотложную медицинскую помощь. Позвоните в токсикологическую службу и немедленно обратитесь за медицинской помощью.
Сульфат железа: лекарство для лечения железодефицитной анемии
Если вам или вашему ребенку прописали сульфат железа, следуйте инструкциям врача о том, как и когда его принимать.
Если вы покупаете сульфат железа в аптеке, следуйте инструкциям на упаковке.
Сульфат железа выпускается в виде таблеток по 200 мг или капель, которые нужно глотать.
Капли содержат 125 мг сульфата железа в 1 мл.
Капли могут быть легче для детей и людей, которым трудно глотать таблетки.
Сколько я возьму?
Доза сульфата железа зависит от того, почему вы его принимаете и от того, принимаете ли вы таблетки, капсулы или капли.
Для детей в возрасте до 18 лет врач будет использовать возраст, вес и результаты крови вашего ребенка, чтобы определить правильную дозу.
Для лечения анемии
Обычная доза для взрослых:
- таблетки : одна таблетка 200 мг, принимать 2-3 раза в день
- капли : 4 мл, принимать один или два раза в день
Для профилактики анемии
Обычная доза для взрослых:
- таблетки : одна таблетка 200 мг один раз в день
- капли : 2.от 4 до 4,8 мл в день
Как принимать
Сульфат железа лучше всего работает, когда вы принимаете его натощак. Однако, если он вызывает расстройство желудка, вы можете принимать его во время или после еды.
Однако, если он вызывает расстройство желудка, вы можете принимать его во время или после еды.
Врач (или фармацевт) может порекомендовать принимать сульфат железа с апельсиновым соком или добавкой витамина С. Считается, что витамин С увеличивает количество железа, усваиваемого организмом.
Таблетку или капсулу проглотить целиком, запив стаканом воды. Не рассасывайте, не жуйте и не держите таблетку во рту, так как это может вызвать язвы во рту или окрасить зубы.
Не принимайте его с чаем, кофе, яйцами, молочными продуктами и продуктами из сои, так как они могут уменьшить количество железа, попадающего в ваш организм. Когда вы принимаете сульфат железа (или когда вы едите продукты с высоким содержанием железа), оставьте 2-часовой перерыв, прежде чем есть эти продукты или напитки.
Если вам трудно глотать таблетки, сообщите об этом своему врачу или фармацевту.
Если вы принимаете сульфат железа в виде капель, к нему прилагается пластиковый шприц или пипетка, которые помогут вам отмерить правильную дозу.
Если у вас его нет, попросите его у фармацевта. Не используйте кухонную чайную ложку, так как она не даст вам нужного количества лекарства.
Что, если я забуду взять его?
Если вы забыли принять дозу, примите другую, как только вспомните. Если почти пришло время принять следующую дозу, то вообще не принимайте пропущенную дозу.
Не принимайте двойную дозу, чтобы компенсировать пропущенную дозу.
Если вы часто забываете о дозах, может помочь установка будильника, чтобы напомнить вам.Вы также можете обратиться к своему фармацевту за советом о других способах запомнить свое лекарство.
Что, если я возьму слишком много?
Если вы идете в отделение неотложной помощи, не садитесь за руль. Попросите кого-нибудь отвезти вас или вызовите скорую помощь.
Возьмите с собой пакет с сульфатом железа или листовку внутри него и оставшееся лекарство.
Фумарат железа: лекарство для лечения железодефицитной анемии
Если вам или вашему ребенку прописали фумарат железа, следуйте инструкциям своего врача о том, как и когда его принимать.
Если вы покупаете фумарат железа в аптеке, следуйте инструкциям на упаковке.
Таблетки фумарата железа выпускаются двух видов: 210 мг и 322 мг.
Капсулы фумарата железа по 305 мг.
Жидкий фумарат железа содержит 140 мг фумарата железа в 5 мл ложке (140 мг/5 мл).
Жидкость может быть легче для детей и людей, которым трудно глотать таблетки или капсулы.
Сколько я возьму?
Доза фумарата железа зависит от того, почему вы его принимаете и от того, принимаете ли вы таблетки, капсулы или жидкость.
Для лечения анемии
Обычная доза фумарата железа для взрослых и детей старше 12 лет: 2 раза в день
Детям до 12 лет назначает врач возраст или вес вашего ребенка, чтобы определить правильную дозу.
Для профилактики анемии
Обычная доза фумарата железа для взрослых и детей старше 12 лет: день
Для детей в возрасте до 12 лет врач назначит возраст или вес вашего ребенка, чтобы определить правильную дозу.
Как принимать
Фумарат железа лучше всего действует, когда вы принимаете его натощак. Принимать за 30 минут до еды или через 2 часа после еды. Но если он вызывает расстройство желудка, вы можете принимать его во время или сразу после еды.
Ваш врач (или фармацевт) может порекомендовать принимать фумарат железа с апельсиновым соком или добавкой витамина С. Считается, что витамин С увеличивает количество железа, усваиваемого организмом.
Глотать таблетки или капсулы только со стаканом воды или сока.Не принимайте их с молоком, так как молоко препятствует попаданию железа в ваш организм.
Если вы принимаете фумарат железа в виде жидкости, к нему прилагается пластиковый шприц или ложка, которые помогут вам отмерить правильную дозу. Если у вас его нет, попросите его у фармацевта. Не используйте кухонную чайную ложку, так как вы не получите нужное количество.
Фумарат железа не представляет опасности, если он был назначен вашему ребенку и вы следуете указаниям врача или инструкциям на упаковке.
Что, если я забуду взять его?
Если вы обычно принимаете:
- один раз в день – принимайте, как только вспомните. Но если до следующей дозы осталось менее 12 часов, пропустите пропущенную дозу.
- 2 раза в день – если вы помните в течение 4 часов о пропущенной дозе, примите ее, как только вспомните.
 Если вы помните более чем через 4 часа после пропущенной дозы, пропустите пропущенную дозу, а затем примите следующую, как обычно.
Если вы помните более чем через 4 часа после пропущенной дозы, пропустите пропущенную дозу, а затем примите следующую, как обычно. - 3 раза в день – пропустите пропущенную дозу и принимайте следующую дозу как обычно.
Не принимайте двойную дозу, чтобы компенсировать пропущенную дозу.
Если вы часто забываете дозы, может помочь установка будильника, чтобы напомнить вам. Вы также можете обратиться к фармацевту за советом о других способах запомнить свое лекарство.
Что, если я возьму слишком много?
Если вы идете в отделение неотложной помощи, не садитесь за руль. Попросите кого-нибудь отвезти вас или вызовите скорую помощь.
Возьмите с собой пакетик фумарата железа или листок-вкладыш и оставшееся лекарство.
Каков режим дозирования препаратов железа для лечения анемии?
Автор
Джозеф Э. Маакарон, доктор медицинских наук Научный сотрудник, отделение внутренней медицины, отделение гематологии/онкологии, Медицинский центр Американского университета Бейрута, Ливан,
Маакарон, доктор медицинских наук Научный сотрудник, отделение внутренней медицины, отделение гематологии/онкологии, Медицинский центр Американского университета Бейрута, Ливан,
Раскрытие информации: ничего не подлежит раскрытию.
Соавтор (ы)
Али Т. Тахер, доктор медицины, доктор медицинских наук, FRCP , профессор медицины, доцент кафедры внутренних болезней, отделение гематологии/онкологии, директор по исследованиям, онкологический центр NK Basile, Медицинский центр Американского университета в Бейруте, Ливан
Раскрытие информации: Нечего раскрывать.
Марсель Э. Конрад, доктор медицины Заслуженный профессор медицины (в отставке), Медицинский колледж Университета Южной Алабамы
Марсель Э. Конрад, доктор медицины, является членом следующих медицинских обществ: Альфа Омега Альфа, Американская ассоциация содействия развитию науки , Американская ассоциация банков крови, Американское химическое общество, Американский колледж врачей, Американское физиологическое общество, Американское общество клинических исследований, Американское общество гематологов, Ассоциация американских врачей, Ассоциация военных хирургов США, Международное общество гематологов, Общество для экспериментальной биологии и медицины, SWOG
Раскрытие информации: партнер не получал никаких финансовых интересов ни за что.
Главный редактор
Emmanuel C Besa, MD Почетный профессор, медицинский факультет, отделение гематологических злокачественных новообразований и трансплантации гемопоэтических стволовых клеток, Онкологический центр Kimmel, Медицинский колледж Джефферсона Университета Томаса Джефферсона
Emmanuel C Besa, MD является членом следующих медицинских общества: Американская ассоциация онкологического образования, Американское общество клинической онкологии, Американский колледж клинической фармакологии, Американская федерация медицинских исследований, Американское общество гематологии, Нью-Йоркская академия наук,
Раскрытие информации: Нечего раскрывать.
Благодарности
Jose A Perez Jr, MD, MBA, MSEd Консультант, медицинский факультет, методистская больница; Адъюнкт-профессор клинической медицины, Медицинский колледж Вейла Корнелла,
webmd.com»> Jose A Perez Jr, MD, MBA, MSEd является членом следующих медицинских обществ: Американского колледжа руководителей врачей, Американского колледжа врачей, Общества общей внутренней медицины и Общества больничной медицины.Раскрытие информации: Нечего раскрывать.
Рональд А. Захер, MB, BCh, MD, FRCPC Профессор внутренней медицины и патологии, директор Центра крови Хоксворта, Академический медицинский центр Университета Цинциннати
Рональд А. Захер, MB, BCh, MD, FRCPC является членом следующих медицинских обществ: Американской ассоциации развития науки, Американской ассоциации банков крови, Американской клинической и климатологической ассоциации, Американского общества клинической патологии, Американского общества Гематология, Колледж американских патологов, Международное общество переливания крови, Международное общество тромбоза и гемостаза и Королевский колледж врачей и хирургов Канады
webmd.com»> Раскрытие информации: Glaxo Smith Kline Honoraria Выступления и преподавание; Членство в совете Talecris HonorariaФрансиско Талавера, PharmD, PhD Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Заработная плата Medscape
Индивидуальное лечение железодефицитной анемии у взрослых
Am J Med.Авторская рукопись; Доступен в PMC 2009 ноября 1.
Опубликовано в окончательной редактированной форме AS:
PMCID: PMC2582401
NIHMSID: NIHMS77765
, MD, A, C , MD C и, MD C , *Michael Alleyne
a Национальный институт рака, Национальные институты здоровья, Бетесда, Мэриленд
c Национальный институт диабета, заболеваний органов пищеварения и почек, Национальные институты здравоохранения, Бетесда, Бетесда
Макдональд К.
 Horne
Horneb Служба гематологии и отделение лабораторной медицины, Клинический центр им. В.Г. Магнусона, Национальные институты здравоохранения, Бетесда, Мэриленд
Jeffery L. Miller
c Национальный институт диабета, болезней органов пищеварения и почек, Национальный Institutes of Health, Bethesda, Maryland
a Национальный институт рака, National Institutes of Health, Bethesda, Maryland
b Служба гематологии и отделение лабораторной медицины, W.Клинический центр Г. Магнусона, Национальные институты здравоохранения, Бетесда, Мэриленд
c Национальный институт диабета, болезней органов пищеварения и почек, Национальные институты здравоохранения, Бетесда, Мэриленд
* Автор, ответственный за корреспонденцию: Джеффри Л. Миллер, доктор медицинских наук, руководитель отдела молекулярной геномики и терапии, отделение молекулярной медицины, NIDDK, Национальный институт здравоохранения, здание 10, комната 9N311, 10 Center Drive, Bethesda, MD 20892-1801, тел. 301-480-1908, факс.301-435-5148, vog.hin@f7mjОкончательная отредактированная версия этой статьи доступна по адресу Am J Med См. другие статьи в PMC, в которых цитируется опубликованная статья.
301-480-1908, факс.301-435-5148, vog.hin@f7mjОкончательная отредактированная версия этой статьи доступна по адресу Am J Med См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Дефицит железа является одним из наиболее распространенных заболеваний, поражающих человечество, а железодефицитная анемия продолжает представлять серьезную проблему общественного здравоохранения во всем мире. Особенно часто встречается у женщин детородного возраста в связи с беременностью и менструальной кровопотерей. Дополнительные группы пациентов включают пациентов с другими источниками кровопотери, недоеданием или нарушением всасывания в кишечнике.Железодефицитная анемия остается достаточно распространенной, несмотря на широкие возможности диагностики заболевания и доступность лекарственных препаратов железа. Следовательно, необходимы новые подходы для эффективного управления этими группами пациентов. В этом обзоре обсуждаются диагностика и лечение железодефицитной анемии с акцентом на учет индивидуальных особенностей пациента. Предлагается, чтобы все пациенты участвовали в самолечении, помогая своему врачу определить переносимую суточную дозу железа, состав и график приема.Циклы дозирования рекомендуются для заместительной терапии железом в зависимости от переносимой суточной дозы и общего дефицита железа. Каждый цикл состоит из перорального приема 5000 мг элементарного железа в течение как минимум одного месяца с соответствующим последующим наблюдением. Такой подход должен помочь врачам и их пациентам в реализации индивидуальной стратегии лечения пациентов с железодефицитной анемией.
Предлагается, чтобы все пациенты участвовали в самолечении, помогая своему врачу определить переносимую суточную дозу железа, состав и график приема.Циклы дозирования рекомендуются для заместительной терапии железом в зависимости от переносимой суточной дозы и общего дефицита железа. Каждый цикл состоит из перорального приема 5000 мг элементарного железа в течение как минимум одного месяца с соответствующим последующим наблюдением. Такой подход должен помочь врачам и их пациентам в реализации индивидуальной стратегии лечения пациентов с железодефицитной анемией.
Ключевые слова: железо, анемия, гепсидин, циклы дозирования
Введение
Железо имеет решающее значение для роста всех клеток.Поэтому неудивительно, что железодефицитная анемия независимо увеличивает заболеваемость и смертность. 1 По оценкам, во всем мире насчитывается 3,5 миллиарда человек с дефицитом железа, подавляющее большинство из которых проживает в развивающихся странах. 2 Примечательно, что дефицит железа также является наиболее распространенной причиной анемии в Соединенных Штатах. 3 Наличие в анамнезе хронической усталости или кровопотери должно насторожить врача, чтобы он рассмотрел диагноз дефицита железа. Иногда более тонкие истории выпадения волос или пикацизма (аппетит к веществам, не подходящим в качестве источника пищи, таким как лед, глина, почва или бумажные изделия) дают первоначальное подозрение на железодефицитную анемию.Классические хрестоматийные признаки синдрома Пламмера-Винсона (дисфагия, перепонка пищевода и атрофический глоссит с железодефицитной анемией) и койлонихия (ложкообразные ногти) редко встречаются в развитых странах. Даже при отсутствии явных признаков и симптомов врач может установить вероятный диагноз железодефицитной анемии с помощью рутинного анализа крови.
2 Примечательно, что дефицит железа также является наиболее распространенной причиной анемии в Соединенных Штатах. 3 Наличие в анамнезе хронической усталости или кровопотери должно насторожить врача, чтобы он рассмотрел диагноз дефицита железа. Иногда более тонкие истории выпадения волос или пикацизма (аппетит к веществам, не подходящим в качестве источника пищи, таким как лед, глина, почва или бумажные изделия) дают первоначальное подозрение на железодефицитную анемию.Классические хрестоматийные признаки синдрома Пламмера-Винсона (дисфагия, перепонка пищевода и атрофический глоссит с железодефицитной анемией) и койлонихия (ложкообразные ногти) редко встречаются в развитых странах. Даже при отсутствии явных признаков и симптомов врач может установить вероятный диагноз железодефицитной анемии с помощью рутинного анализа крови.
После постановки диагноза железодефицитной анемии врач должен определить причину и разработать план лечения. Как показано на рисунке, железодефицитная анемия возникает в результате множества причин, которые можно разделить на четыре основные категории, связанные с потреблением или потерей железа. В подавляющем большинстве случаев причиной железодефицитной анемии является анемия, которую можно предотвратить и обратить путем увеличения приема препаратов железа или снижения потерь железа. Однако тот факт, что более трех миллионов женщин в этой стране продолжают страдать железодефицитной анемией 4 , свидетельствует о том, что общие терапевтические подходы остаются неоптимальными. Возможно, потребуется переосмыслить общие подходы к лечению, чтобы снизить заболеваемость железодефицитной анемией. В этом обзоре концепции накопления и кинетики железа объединены с обзором пероральных добавок железа, чтобы предоставить клиницистам индивидуальные стратегии лечения железодефицитной анемии.
В подавляющем большинстве случаев причиной железодефицитной анемии является анемия, которую можно предотвратить и обратить путем увеличения приема препаратов железа или снижения потерь железа. Однако тот факт, что более трех миллионов женщин в этой стране продолжают страдать железодефицитной анемией 4 , свидетельствует о том, что общие терапевтические подходы остаются неоптимальными. Возможно, потребуется переосмыслить общие подходы к лечению, чтобы снизить заболеваемость железодефицитной анемией. В этом обзоре концепции накопления и кинетики железа объединены с обзором пероральных добавок железа, чтобы предоставить клиницистам индивидуальные стратегии лечения железодефицитной анемии.
Таблица 1
Причины дефицита железа у взрослых.
| Причины | Примеры |
|---|---|
| Повышенная потеря железа | Острое кровотечение
|
| Пониженный уровень железа в рационе | Вегетарианская диета Недоедание Деменция, психическое заболевание |
| Снижение всасывания железа | Антацидная терапия или высокий рН желудка Целиакия Воспалительные заболевания кишечника Частичная гастрэктомия |
| Повышенная потребность в железе | Беременность Лактация |
Кинетика железа и развитие анемии
У большинства взрослых в организме содержится не менее 3000 мг (45 мг/кг) элементарного железа. Женщины обычно имеют более низкие уровни, чем мужчины, из-за потери железа во время менструаций, беременности и лактации. В этом пуле общего железа тела примерно две трети содержится в геме (в основном включенном в гемоглобин эритроцитов) и одна треть в запасных формах ферритина или гемосидерина. Чтобы поддерживать адекватные запасы железа для синтеза гема, 20 мг железа ежедневно перерабатываются из стареющих эритроцитов, которые удаляются из кровообращения, в новые клетки костного мозга. 5 Железо из этих старых клеток загружается макрофагами на трансферрин для доставки в костный мозг.Для компенсации потерь с мочой, потом и стулом требуется около 1-2 мг дополнительного пищевого железа в день. Гормон гепсидин регулирует гомеостаз железа, регулируя опосредованное ферропортином высвобождение железа из энтероцитов и макрофагов. 6 Если поступления с пищей недостаточно для возмещения 1–2 мг/сут облигатной потери железа или для возмещения дополнительной потери из-за кровотечения, разовьется дефицит железа.
Женщины обычно имеют более низкие уровни, чем мужчины, из-за потери железа во время менструаций, беременности и лактации. В этом пуле общего железа тела примерно две трети содержится в геме (в основном включенном в гемоглобин эритроцитов) и одна треть в запасных формах ферритина или гемосидерина. Чтобы поддерживать адекватные запасы железа для синтеза гема, 20 мг железа ежедневно перерабатываются из стареющих эритроцитов, которые удаляются из кровообращения, в новые клетки костного мозга. 5 Железо из этих старых клеток загружается макрофагами на трансферрин для доставки в костный мозг.Для компенсации потерь с мочой, потом и стулом требуется около 1-2 мг дополнительного пищевого железа в день. Гормон гепсидин регулирует гомеостаз железа, регулируя опосредованное ферропортином высвобождение железа из энтероцитов и макрофагов. 6 Если поступления с пищей недостаточно для возмещения 1–2 мг/сут облигатной потери железа или для возмещения дополнительной потери из-за кровотечения, разовьется дефицит железа.
Фундаментальное значение имеет понимание того, что запасы железа истощаются до того, как возникает железодефицитный эритропоэз.Таким образом, лабораторные показатели, связанные с истощением запасов железа, обычно предшествуют возникновению анемии (4). Три года диеты с тяжелым дефицитом железа (менее 1-2 мг/сут с пищей X 1000 дней) или более острая двухлитровая кровопотеря (0,4 мг элементарного железа на мл цельной крови) приведут к полной потере запасов железа. обычно около 1 грамма железа в виде ферритина и гемосидерина). Потеря запасов железа отражается в крови снижением уровня ферритина и снижением уровня железа, связанного с трансферрином.По мере того, как запасы железа становятся более истощенными, доступность железа, связанного с трансферрином, для эритроидного предшественника вызывает снижение продукции гема и гемоглобина. Это отражается в снижении количества эритроцитов и среднего объема эритроцитов. Количество эритроцитов обычно становится ненормальным раньше, чем средний объем эритроцитов, который остается в пределах нормы до тех пор, пока гемоглобин не достигнет примерно 10 г/дл..gif) Кроме того, ширина распределения эритроцитов увеличивается, потому что более мелкие железодефицитные клетки смешиваются с нормоцитарными клетками.При отсутствии терапии продукция эритроцитов остается недостаточной и развивается анемия. Важно отметить, что многие пациенты с железодефицитной анемией имеют нормальные показатели эритроцитов, потому что количество эритроцитов становится ненормальным до того, как произойдут значительные изменения в морфологии эритроцитов. 7 В этих случаях для подтверждения диагноза железодефицитной анемии может потребоваться более специализированное тестирование уровня железа. 8
Кроме того, ширина распределения эритроцитов увеличивается, потому что более мелкие железодефицитные клетки смешиваются с нормоцитарными клетками.При отсутствии терапии продукция эритроцитов остается недостаточной и развивается анемия. Важно отметить, что многие пациенты с железодефицитной анемией имеют нормальные показатели эритроцитов, потому что количество эритроцитов становится ненормальным до того, как произойдут значительные изменения в морфологии эритроцитов. 7 В этих случаях для подтверждения диагноза железодефицитной анемии может потребоваться более специализированное тестирование уровня железа. 8
Таблица 2
Лабораторные нарушения при дефиците железа.
| Лабораторный тест | Лабораторный результат | |
|---|---|---|
| Ferritin | <40 мкг / л | |
| <15% | ||
| > 450 мкг/дл | ||
| Количество эритроцитов | < 4 × 10 6 / мм 3 | |
| Средний объем эритроцитов | < 80 фл | |
| Гемоглобин | < 13 г/дл мужчины
< 12 г/дл женщины во время менструации |
Пищевые добавки железа
После того, как дефицит железа диагностирован и его основная причина устранена, следующей задачей является восстановление запасов железа. При средней абсорбции 10% железа в лекарственной форме суточная потребность в элементарном железе составляет 10 мг для детей, взрослых мужчин и женщин в постменопаузе (для обеспечения организма 1 мг), 20 мг для молодых небеременных женщин.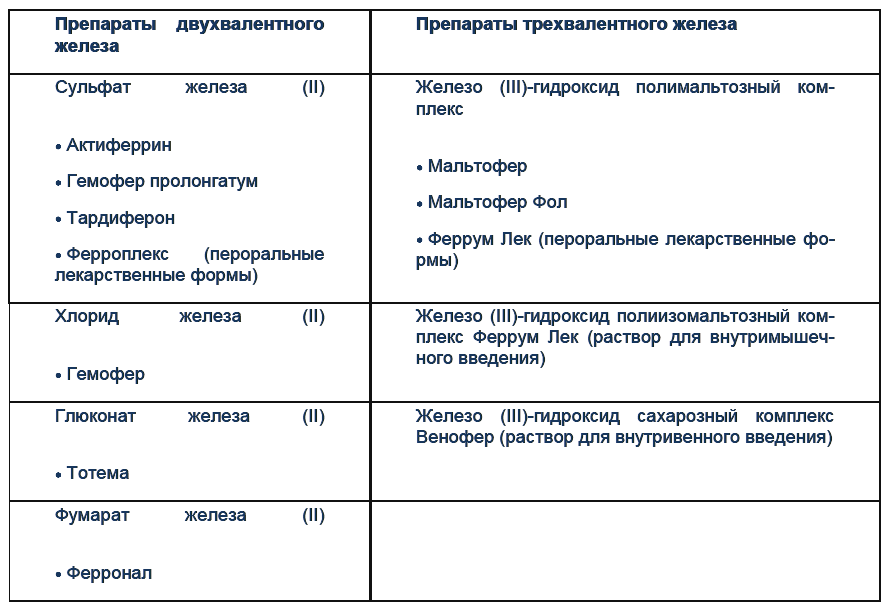 и 30 мг у беременных. 9 Конечно, пациентам с нарушением всасывания железа, например, перенесшим желудочное шунтирование, требуется больше. 10
и 30 мг у беременных. 9 Конечно, пациентам с нарушением всасывания железа, например, перенесшим желудочное шунтирование, требуется больше. 10
Если диетический анамнез предполагает дефицит, пациентам следует рекомендовать дополнить свой рацион продуктами, богатыми гемовым железом, такими как красное мясо (содержащее гемоглобин и миоглобин) или печень. Негемовое железо, которое преобладает в крупах, яичном желтке и зеленых листовых овощах, не усваивается эффективно. Известно, что витамин С увеличивает усвоение железа, и его можно увеличить в рационе, добавив цитрусовые.Напротив, чай подавляет всасывание железа, поэтому пациентам с дефицитом железа следует подождать 1-2 часа после еды, прежде чем пить чай, или, в качестве альтернативы, исключить чай из своего рациона. Оптимальное лечение может потребовать направления к зарегистрированному диетологу или диетологу для более тщательной оценки питания и консультирования. В то время как диетический обзор и консультирование важны, диета сама по себе обычно недостаточна в качестве источника замещения железа у большинства пациентов с железодефицитной анемией. 11
11
Лекарственные препараты железа
Препараты железа обычно содержат одну из трех солей железа: сульфат железа, глюконат железа и фумурат железа.Однако важно понимать, что таблетка сульфатной соли содержит в два раза больше железа, чем таблетка двух других солей, хотя разная молекулярная масса соединений скрывает этот факт (). Следовательно, требуется в два раза больше таблеток глюконата железа или фумурата железа, чтобы обеспечить количество элементарного железа в таблетках сульфата железа.
Таблица 3
Распространенные пероральные препараты железа.




 Убедитесь, что ваш врач знает обо всех рецептурных и безрецептурных лекарствах, которые вы принимаете, если они предлагают вам принимать добавки железа.
Убедитесь, что ваш врач знает обо всех рецептурных и безрецептурных лекарствах, которые вы принимаете, если они предлагают вам принимать добавки железа. Если вы помните более чем через 4 часа после пропущенной дозы, пропустите пропущенную дозу, а затем примите следующую, как обычно.
Если вы помните более чем через 4 часа после пропущенной дозы, пропустите пропущенную дозу, а затем примите следующую, как обычно.
 Пероральное железо можно давать в виде таблеток или эликсиров. Среди таблетированных препаратов есть таблетки с неэнтеросолюбильным покрытием, а также препараты с энтеросолюбильным покрытием и препараты с пролонгированным высвобождением. Таблетки железа, не покрытые кишечнорастворимой оболочкой, чаще всего используются в качестве начального лечения из-за их более низкой стоимости. Препараты железа с отсроченным высвобождением и с энтеросолюбильным покрытием рекомендуются, поскольку они лучше переносятся, чем таблетки без энтеросолюбильного покрытия. Однако они менее эффективны, так как могут содержать меньше железа и их железо может не высвобождаться в двенадцатиперстной кишке, где железо всасывается.Фактически, пациенты, которые безуспешно лечились препаратами железа с кишечнорастворимой оболочкой и препаратами пролонгированного действия, могут хорошо реагировать на введение солей железа без кишечнорастворимой оболочки. 12
Пероральное железо можно давать в виде таблеток или эликсиров. Среди таблетированных препаратов есть таблетки с неэнтеросолюбильным покрытием, а также препараты с энтеросолюбильным покрытием и препараты с пролонгированным высвобождением. Таблетки железа, не покрытые кишечнорастворимой оболочкой, чаще всего используются в качестве начального лечения из-за их более низкой стоимости. Препараты железа с отсроченным высвобождением и с энтеросолюбильным покрытием рекомендуются, поскольку они лучше переносятся, чем таблетки без энтеросолюбильного покрытия. Однако они менее эффективны, так как могут содержать меньше железа и их железо может не высвобождаться в двенадцатиперстной кишке, где железо всасывается.Фактически, пациенты, которые безуспешно лечились препаратами железа с кишечнорастворимой оболочкой и препаратами пролонгированного действия, могут хорошо реагировать на введение солей железа без кишечнорастворимой оболочки. 12  Различия в абсорбции, скорее всего, связаны с потребностью кислотности в двенадцатиперстной кишке и верхних отделах тощей кишки для растворимости железа. Для железа, высвобождаемого за пределами этих мест, щелочная среда снижает абсорбцию. 13 В идеале пациентам не следует принимать препараты железа в течение 1–2 часов после приема антацидов. Ингибирование всасывания железа другими препаратами, снижающими кислотность желудка, такими как блокаторы Н3, может быть еще более длительным. Всасывание также замедляется при приеме тетрациклинов, молока и фосфатсодержащих газированных напитков, таких как безалкогольные напитки. Даже соли кальция, фосфора и магния, содержащиеся в железосодержащих поливитаминных таблетках, ухудшают усвоение элементарного железа. 14 По этой причине поливитаминные препараты никогда не следует рекомендовать в качестве единственной терапии железодефицитной анемии.Таблетки железа рекомендуется принимать между приемами пищи или перед сном, чтобы избежать подщелачивающего эффекта пищи и воспользоваться пиковой выработкой желудочной кислоты поздно ночью.
Различия в абсорбции, скорее всего, связаны с потребностью кислотности в двенадцатиперстной кишке и верхних отделах тощей кишки для растворимости железа. Для железа, высвобождаемого за пределами этих мест, щелочная среда снижает абсорбцию. 13 В идеале пациентам не следует принимать препараты железа в течение 1–2 часов после приема антацидов. Ингибирование всасывания железа другими препаратами, снижающими кислотность желудка, такими как блокаторы Н3, может быть еще более длительным. Всасывание также замедляется при приеме тетрациклинов, молока и фосфатсодержащих газированных напитков, таких как безалкогольные напитки. Даже соли кальция, фосфора и магния, содержащиеся в железосодержащих поливитаминных таблетках, ухудшают усвоение элементарного железа. 14 По этой причине поливитаминные препараты никогда не следует рекомендовать в качестве единственной терапии железодефицитной анемии.Таблетки железа рекомендуется принимать между приемами пищи или перед сном, чтобы избежать подщелачивающего эффекта пищи и воспользоваться пиковой выработкой желудочной кислоты поздно ночью.

 поднять гемоглобин цельной крови на 2-3 г/дл). 15 Для дальнейшего пополнения запасов железа некоторые рекомендуют продолжать этот режим в течение нескольких дополнительных месяцев. 16 К сожалению, этот подход часто не работает. До 20 процентов пациентов испытывают дискомфорт в желудочно-кишечном тракте при приеме 180 мг элементарного железа в день по этой схеме 17 , а 30 процентов некоторых групп пациентов могут самостоятельно прекратить прием препарата. 18 Основными препятствиями на пути к успешной пероральной терапии препаратами железа являются дозозависимые побочные эффекты со стороны верхних отделов желудочно-кишечного тракта, такие как тошнота и дискомфорт в эпигастрии, которые возникают примерно через час после приема внутрь.Побочные эффекты со стороны желудочно-кишечного тракта, такие как запор и диарея, в меньшей степени зависят от дозы и лечатся специфическими для симптомов препаратами (например, цитратом магния при запорах). 19 Если у пациента быстро возникают запоры или тошнота после обычно рекомендуемой дозы 150-200 мг элементарного железа в день, применяется снижение дозы.
поднять гемоглобин цельной крови на 2-3 г/дл). 15 Для дальнейшего пополнения запасов железа некоторые рекомендуют продолжать этот режим в течение нескольких дополнительных месяцев. 16 К сожалению, этот подход часто не работает. До 20 процентов пациентов испытывают дискомфорт в желудочно-кишечном тракте при приеме 180 мг элементарного железа в день по этой схеме 17 , а 30 процентов некоторых групп пациентов могут самостоятельно прекратить прием препарата. 18 Основными препятствиями на пути к успешной пероральной терапии препаратами железа являются дозозависимые побочные эффекты со стороны верхних отделов желудочно-кишечного тракта, такие как тошнота и дискомфорт в эпигастрии, которые возникают примерно через час после приема внутрь.Побочные эффекты со стороны желудочно-кишечного тракта, такие как запор и диарея, в меньшей степени зависят от дозы и лечатся специфическими для симптомов препаратами (например, цитратом магния при запорах). 19 Если у пациента быстро возникают запоры или тошнота после обычно рекомендуемой дозы 150-200 мг элементарного железа в день, применяется снижение дозы. Изменения солей железа (и, следовательно, элементарного железа на таблетку) и составов обычно пробуют, и большинство из них включает снижение дозы за счет удлинения интервала между приемами. 19 Эти меры по снижению дозы могут позволить пациентам с непереносимостью железа продолжить пероральную терапию и избежать парентеральной терапии.
Изменения солей железа (и, следовательно, элементарного железа на таблетку) и составов обычно пробуют, и большинство из них включает снижение дозы за счет удлинения интервала между приемами. 19 Эти меры по снижению дозы могут позволить пациентам с непереносимостью железа продолжить пероральную терапию и избежать парентеральной терапии. 21
21  Количество всасываемого железа уменьшается по мере устранения дефицита железа. Следовательно, невозможно предсказать точный процент железа, который будет абсорбироваться у отдельных пациентов, но предполагается, что примерно 10–20 % пероральной дозы железа будет абсорбироваться в начале терапии. 22 Таким образом, в этом обзоре для оценки общей дозы, необходимой для заместительной терапии железом, будет использоваться расчетное среднее значение 10% пероральной дозы железа.
Количество всасываемого железа уменьшается по мере устранения дефицита железа. Следовательно, невозможно предсказать точный процент железа, который будет абсорбироваться у отдельных пациентов, но предполагается, что примерно 10–20 % пероральной дозы железа будет абсорбироваться в начале терапии. 22 Таким образом, в этом обзоре для оценки общей дозы, необходимой для заместительной терапии железом, будет использоваться расчетное среднее значение 10% пероральной дозы железа.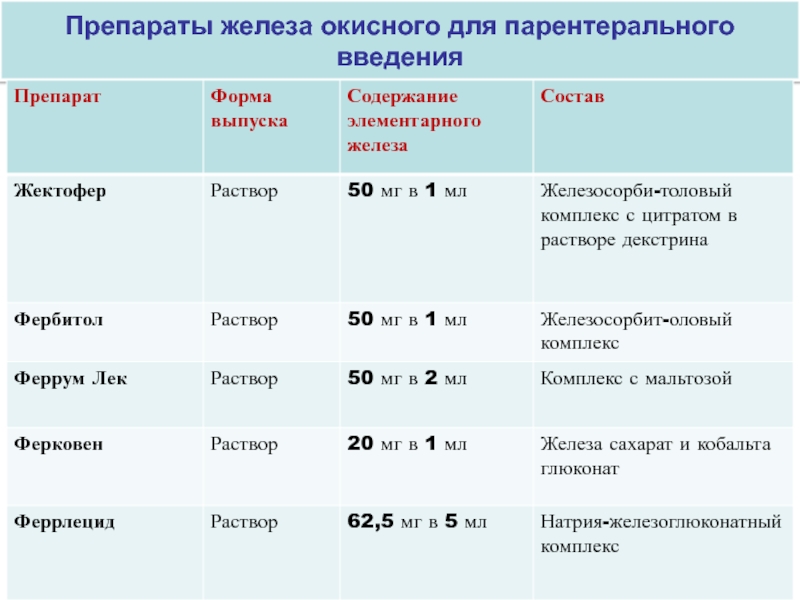 23 Если анемия нетяжелая и нет таких осложняющих явлений, как продолжающаяся кровопотеря или энтеропатии, для коррекции анемии могут не потребоваться дополнительные циклы приема препаратов железа. Повторная оценка анемии после завершения первого цикла дозирования 5000 мг должна быть выполнена, чтобы определить, необходимы ли дополнительные добавки железа. У пациентов с более тяжелой анемией можно рассчитать альтернативную дозу на основе уровня гемоглобина (1). Если прогнозируется постоянный дефицит железа у пациента (т.г. меноррагия), можно легко разработать поддерживающую дозировку препаратов железа. Ключевой особенностью стратегии циклического дозирования, предложенной здесь, является то, что несколько факторов, включая причину железодефицитной анемии, общий дефицит железа, препараты железа для замены и прогнозируемую продолжительность заместительной терапии, объединяются для реализации индивидуального терапевтического плана.
23 Если анемия нетяжелая и нет таких осложняющих явлений, как продолжающаяся кровопотеря или энтеропатии, для коррекции анемии могут не потребоваться дополнительные циклы приема препаратов железа. Повторная оценка анемии после завершения первого цикла дозирования 5000 мг должна быть выполнена, чтобы определить, необходимы ли дополнительные добавки железа. У пациентов с более тяжелой анемией можно рассчитать альтернативную дозу на основе уровня гемоглобина (1). Если прогнозируется постоянный дефицит железа у пациента (т.г. меноррагия), можно легко разработать поддерживающую дозировку препаратов железа. Ключевой особенностью стратегии циклического дозирования, предложенной здесь, является то, что несколько факторов, включая причину железодефицитной анемии, общий дефицит железа, препараты железа для замены и прогнозируемую продолжительность заместительной терапии, объединяются для реализации индивидуального терапевтического плана.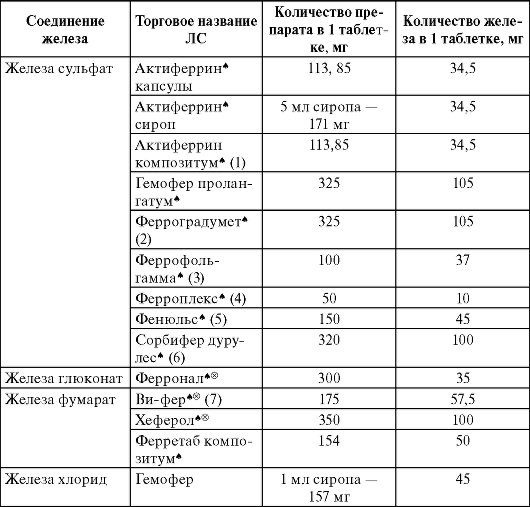

 Пациенты могут быть обследованы в начале курса заместительной терапии железом, чтобы подтвердить соответствующий ответ ретикулоцитов. Соображения относительно недостаточного ответа включают текущую кровопотерю, мальабсорбцию, которые могут быть анатомическими или ингибирующими факторами, например.антациды или чай, неверный диагноз или несоблюдение режима лечения. 19 Несоблюдение пациентом режима лечения следует выяснить по анамнезу, но в случае неопределенности следует исключить другие причины. Как правило, комплаентные пациенты, которые не реагируют на терапию препаратами железа, могут быть направлены к гематологу для дальнейшей оценки анемии или к гастроэнтерологу на предмет возможной мальабсорбции или скрытой кровопотери.
Пациенты могут быть обследованы в начале курса заместительной терапии железом, чтобы подтвердить соответствующий ответ ретикулоцитов. Соображения относительно недостаточного ответа включают текущую кровопотерю, мальабсорбцию, которые могут быть анатомическими или ингибирующими факторами, например.антациды или чай, неверный диагноз или несоблюдение режима лечения. 19 Несоблюдение пациентом режима лечения следует выяснить по анамнезу, но в случае неопределенности следует исключить другие причины. Как правило, комплаентные пациенты, которые не реагируют на терапию препаратами железа, могут быть направлены к гематологу для дальнейшей оценки анемии или к гастроэнтерологу на предмет возможной мальабсорбции или скрытой кровопотери.
 MMWR Morb Mortal Wkly Rep. 1998; 47 (RR3): 1–29. [PubMed] [Google Scholar]4.Looker AC, Dallman PR, Carroll MD, et al. Распространенность дефицита железа в США. ДЖАМА. 1997; 277: 973–976. [PubMed] [Google Scholar]5. Хини М.М., Эндрюс Н.К. Гомеостаз железа и наследственные нарушения перегрузки железом: обзор. Hematol Oncol Clin North Am. 2004; 18:1379–1403. [PubMed] [Google Scholar]6. Кемна Э.Х., Тьялсма Х., Виллемс Х.Л., Свинкелс Д.В. Гепсидин: от открытия к дифференциальной диагностике. Гематология. 2008;93:90–97. [PubMed] [Google Scholar]7. Farley PC, Foland J. Железодефицитная анемия.Как диагностировать и исправить. Последипломная мед. 1990; 87: 89–101. [PubMed] [Google Scholar]8. Кук Джей Ди. Диагностика и лечение железодефицитной анемии. Best Pract Res Clin Haematol. 2005; 18: 319–332. [PubMed] [Google Scholar]9. Институт медицины. Совет по продовольствию и питанию. Референсные нормы потребления витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка.
MMWR Morb Mortal Wkly Rep. 1998; 47 (RR3): 1–29. [PubMed] [Google Scholar]4.Looker AC, Dallman PR, Carroll MD, et al. Распространенность дефицита железа в США. ДЖАМА. 1997; 277: 973–976. [PubMed] [Google Scholar]5. Хини М.М., Эндрюс Н.К. Гомеостаз железа и наследственные нарушения перегрузки железом: обзор. Hematol Oncol Clin North Am. 2004; 18:1379–1403. [PubMed] [Google Scholar]6. Кемна Э.Х., Тьялсма Х., Виллемс Х.Л., Свинкелс Д.В. Гепсидин: от открытия к дифференциальной диагностике. Гематология. 2008;93:90–97. [PubMed] [Google Scholar]7. Farley PC, Foland J. Железодефицитная анемия.Как диагностировать и исправить. Последипломная мед. 1990; 87: 89–101. [PubMed] [Google Scholar]8. Кук Джей Ди. Диагностика и лечение железодефицитной анемии. Best Pract Res Clin Haematol. 2005; 18: 319–332. [PubMed] [Google Scholar]9. Институт медицины. Совет по продовольствию и питанию. Референсные нормы потребления витамина А, витамина К, мышьяка, бора, хрома, меди, йода, железа, марганца, молибдена, никеля, кремния, ванадия и цинка. Вашингтон, округ Колумбия: Издательство Национальной академии; 2001. [PubMed] [Google Scholar]10.Любовь AL, Биллетт HH. Ожирение, бариатрическая хирургия и дефицит железа: правда, правда, правда и родственные связи. Am J Гематол. 2008; 83: 403–409. [PubMed] [Google Scholar] 11. Кросби У.Х. Обоснование лечения железодефицитной анемии. Arch Intern Med. 1984; 144: 471–472. [PubMed] [Google Scholar] 12. Бейтлер Э. Уильямс Гематология. Седьмой. Глава 40. США: McGraw-Hill; Нарушения обмена железа; стр. 511–553. [Google Академия] 13. Прован Д. Механизмы и лечение железодефицитной анемии. Бр Дж Гематол. 1999; 105 (Приложение 1): 19–26.[PubMed] [Google Scholar] 14. Стэнг Дж, Стори М, редакторы. Руководящие принципы для службы питания подростков. 2005. [Google Scholar] 15. Кук Джей Ди. Железодефицитная анемия. Baillieres Clin Haematol. 1994; 7: 787–804. [PubMed] [Google Scholar] 16. Мэсси А. Микроцитарная анемия. Дифференциальная диагностика и лечение железодефицитной анемии. Медицинские клиники Северной Америки.
Вашингтон, округ Колумбия: Издательство Национальной академии; 2001. [PubMed] [Google Scholar]10.Любовь AL, Биллетт HH. Ожирение, бариатрическая хирургия и дефицит железа: правда, правда, правда и родственные связи. Am J Гематол. 2008; 83: 403–409. [PubMed] [Google Scholar] 11. Кросби У.Х. Обоснование лечения железодефицитной анемии. Arch Intern Med. 1984; 144: 471–472. [PubMed] [Google Scholar] 12. Бейтлер Э. Уильямс Гематология. Седьмой. Глава 40. США: McGraw-Hill; Нарушения обмена железа; стр. 511–553. [Google Академия] 13. Прован Д. Механизмы и лечение железодефицитной анемии. Бр Дж Гематол. 1999; 105 (Приложение 1): 19–26.[PubMed] [Google Scholar] 14. Стэнг Дж, Стори М, редакторы. Руководящие принципы для службы питания подростков. 2005. [Google Scholar] 15. Кук Джей Ди. Железодефицитная анемия. Baillieres Clin Haematol. 1994; 7: 787–804. [PubMed] [Google Scholar] 16. Мэсси А. Микроцитарная анемия. Дифференциальная диагностика и лечение железодефицитной анемии. Медицинские клиники Северной Америки. 1992; 76: 549–565. [PubMed] [Google Scholar] 17. Римон Э., Каганский Н., Каганский М. и др. Не даем ли мы слишком много железа? Терапия низкими дозами железа эффективна у восьмидесятилетних.Am J Med. 2005; 118:1142–1147. [PubMed] [Google Scholar] 18. Боннар Дж., Голдберг А., Смит Дж. А. Принимают ли беременные женщины железо? Ланцет. 1969; 1: 457–458. [PubMed] [Google Scholar] 19. Бейтлер Э., Хоффбранд А.В., Кук Д.Д. Дефицит железа и перегрузки. Гематология Программа Am Soc Hematol Educ. 2003: 40–61. [PubMed] [Google Scholar] 20. Wiltink WF, Ybema HJ, Leijnse B, Gerbrandy J. Тест на переносимость железа. Измерение всасывания и использования терапевтической дозы железа. Клин Чим Акта. 1966; 13: 701–707.[PubMed] [Google Scholar] 21. Гершко С., Хоффбранд А.В., Керет Д. и соавт. Роль аутоиммунного гастрита, Helicobacter pylori и целиакии в рефрактерной или необъяснимой железодефицитной анемии. Гематология. 2005; 90: 585–595. [PubMed] [Google Scholar] 22. Горолл А.Х., Малли А.Г. Кабинетная оценка и ведение взрослого пациента.
1992; 76: 549–565. [PubMed] [Google Scholar] 17. Римон Э., Каганский Н., Каганский М. и др. Не даем ли мы слишком много железа? Терапия низкими дозами железа эффективна у восьмидесятилетних.Am J Med. 2005; 118:1142–1147. [PubMed] [Google Scholar] 18. Боннар Дж., Голдберг А., Смит Дж. А. Принимают ли беременные женщины железо? Ланцет. 1969; 1: 457–458. [PubMed] [Google Scholar] 19. Бейтлер Э., Хоффбранд А.В., Кук Д.Д. Дефицит железа и перегрузки. Гематология Программа Am Soc Hematol Educ. 2003: 40–61. [PubMed] [Google Scholar] 20. Wiltink WF, Ybema HJ, Leijnse B, Gerbrandy J. Тест на переносимость железа. Измерение всасывания и использования терапевтической дозы железа. Клин Чим Акта. 1966; 13: 701–707.[PubMed] [Google Scholar] 21. Гершко С., Хоффбранд А.В., Керет Д. и соавт. Роль аутоиммунного гастрита, Helicobacter pylori и целиакии в рефрактерной или необъяснимой железодефицитной анемии. Гематология. 2005; 90: 585–595. [PubMed] [Google Scholar] 22. Горолл А.Х., Малли А.Г. Кабинетная оценка и ведение взрослого пациента. Первичная медико-санитарная помощь. Глава 82: 607–608. [Google Академия] 23. Кук Д.Д., Флауэрс Ч., Скикне Б.С. Количественная оценка содержания железа в организме. Кровь. 2003; 101:3359–3364. [PubMed] [Google Scholar]
Первичная медико-санитарная помощь. Глава 82: 607–608. [Google Академия] 23. Кук Д.Д., Флауэрс Ч., Скикне Б.С. Количественная оценка содержания железа в организме. Кровь. 2003; 101:3359–3364. [PubMed] [Google Scholar]


 Некоторые эксперты рекомендуют дозы 150–200 мг элементарного железа в день, при этом доза распределяется в течение дня. Однако недавние исследования показывают, что это не может быть оптимальным режимом. Доля железа, абсорбируемая из высоких доз перорального железа, низка, а неабсорбированное железо может вызвать раздражение кишечника, воспаление и дисбактериоз, что снижает комплаентность. В недавних исследованиях с использованием профилей гепсидина в сыворотке и стабильных изотопов железа для количественной оценки всасывания железа у молодых женщин мы показали, что: (а) пероральные дозы железа ≥60 мг у женщин с дефицитом железа и дозы ≥100 мг у женщин с ЖДА стимулируют острое повышение уровня гепсидина, которое сохраняется через 24 часа после введения дозы, но проходит через 48 часов; (b) поэтому, чтобы максимизировать фракционное всасывание железа, пероральные дозы ≥60 мг следует назначать через день; (c) циркадное увеличение гепсидина в плазме усиливается утренней дозой железа; поэтому дозы железа не следует давать днем или вечером после утренней дозы.
Некоторые эксперты рекомендуют дозы 150–200 мг элементарного железа в день, при этом доза распределяется в течение дня. Однако недавние исследования показывают, что это не может быть оптимальным режимом. Доля железа, абсорбируемая из высоких доз перорального железа, низка, а неабсорбированное железо может вызвать раздражение кишечника, воспаление и дисбактериоз, что снижает комплаентность. В недавних исследованиях с использованием профилей гепсидина в сыворотке и стабильных изотопов железа для количественной оценки всасывания железа у молодых женщин мы показали, что: (а) пероральные дозы железа ≥60 мг у женщин с дефицитом железа и дозы ≥100 мг у женщин с ЖДА стимулируют острое повышение уровня гепсидина, которое сохраняется через 24 часа после введения дозы, но проходит через 48 часов; (b) поэтому, чтобы максимизировать фракционное всасывание железа, пероральные дозы ≥60 мг следует назначать через день; (c) циркадное увеличение гепсидина в плазме усиливается утренней дозой железа; поэтому дозы железа не следует давать днем или вечером после утренней дозы. Если важна скорость ответа Hb, объединенный анализ наших данных, проведенный для этого обзора, показывает, что общее всасывание железа также выше, если двойная целевая суточная доза железа принимается через день. Таким образом, эти исследования показывают, что переход от ежедневного приема к режиму через день, а также от разделенных до утренних однократных доз увеличивает всасывание железа и может уменьшить побочные эффекты. Таким образом, предоставление утренних доз 60–120 мг железа в виде соли двухвалентного железа, принимаемого с аскорбиновой кислотой через день, может быть оптимальным режимом перорального дозирования для женщин с дефицитом железа и легкой ЖДА.
Если важна скорость ответа Hb, объединенный анализ наших данных, проведенный для этого обзора, показывает, что общее всасывание железа также выше, если двойная целевая суточная доза железа принимается через день. Таким образом, эти исследования показывают, что переход от ежедневного приема к режиму через день, а также от разделенных до утренних однократных доз увеличивает всасывание железа и может уменьшить побочные эффекты. Таким образом, предоставление утренних доз 60–120 мг железа в виде соли двухвалентного железа, принимаемого с аскорбиновой кислотой через день, может быть оптимальным режимом перорального дозирования для женщин с дефицитом железа и легкой ЖДА.