Нужно ли лечить streptococcus agalactiae. Гемолитический стрептококк группы в
Инфекция Streptococcus agalactiae (S. agalactiae). Неонатальная заболеваемость S. Agalactiae- инфекцией, ее клинические проявления. Методы специфической иммунопрофилактики S. Agalactiae-инфекции.
Садова Н.В., Заплатников А.Л., Шипулина О.Ю., Подкопаев В.Н., Фомина С.Г., Скачкова Т.С., Домоно ва Э.А., Сафонова А.П.
Одним из частых бактериальных заболеваний перинатального периода является инфекция, вызванная Streptococcus agalactiae (S. agalactiae). У женщин в период беременности S. agalactiae; инфекция может протекать как бессимптомно, так и клинически значимо с развитием бактериемии, эндометрита, хориоамнионита, воспаления мочевых и родовых путей, а у новорожденных детей проявляться локализованными и инвазивными поражениями .
S. agalactiae относится к стрептококкам группы В, которые являются грамположительными инкапсулированными факультативными анаэробами, не образующими спор. Главным фактором вирулентности S. agalactiae является полисахаридная капсула. Из белковых факторов патогенности особо отмечают С5а пептидазу, бета–гемолизин, С протеины (альфа– и бета–), гиалуронидазу, Sip белок, CAMP фактор (В–белок), а также комплекс протеаз, гемолизин, адгезины и др. .
Установлено, что 15–40% женщин являются носителями S. agalactiae, колонизирующей слизистые влагалища или прямой кишки . Рождение детей от S. agalactiae–инфицированных женщин в 50% сопровождается вертикальной трансмиссией возбудителя. Передача инфекции от инфицированной матери происходит, как правило, незадолго до родов или непосредственно во время родов. В постнатальный период, особенно в ближайшие часы и сутки после рождения, ребенок также может инфицироваться, однако это случается значительно реже по сравнению с пре– и интранатальной контаминацией. Отмечено, что S. agalactiae– инфицирование новорожденных не всегда приводит к развитию инфекционного процесса. Факторами риска реализации инфекции у ребенка, рожденного от S. agalactiae–инфицированной женщины, являются: возраст беременной (12 часов), задержка внутриутробного развития и наличие S. agalactiae– инфекции у ранее рожденных детей .
Неонатальная заболеваемость S. agalactiae– инфекцией до недавнего времени составляла 1–4 на 1000 живорожденных детей, среди которых в 75% случаев имела место манифестация в 1–7–е сутки жизни. При этом на 100 инфицированных беременных женщин рождался 1 ребенок с тяжелой S. agalactiae–инфекцией . Благодаря активному использованию в акушерской практике рекомендаций по профилактике S. agalactiae– инфекции, удалось существенно снизить уровень инфицированности новорожденных, а также частоту инвазивных форм заболевания у детей первого месяца жизни. Так, в странах, где проводится антибактериальная профилактика перинатальной S. agalactiae–инфекции, заболеваемость в ранний неонатальный период удалось снизить более чем на 80%, а показатели неонатальной заболеваемости в целом не превышают 0,3 случая на 1000 живорожденных детей .
Клиническими проявлениями перинатальной S. agalactiae–инфекции у женщин являются послеродовые инфекции эндометрия, мочевыводящих путей, головного мозга, а также сепсис и осложнения кесарева сечения. У новорожденных выделяют локализованные и инвазивные формы перинатальной S. agalactiae–инфекции. При этом в зависимости от времени манифестации выделяют заболевания с ранним (до 7 дня жизни) и поздним (после 7 суток жизни) дебютом. S. agalactiae– инфекция у новорожденных наиболее часто протекает в виде инвазивных форм с бактериемией, поражением легких, мозговых оболочек. Нередко при этом заболевание приобретает септический характер, особенно у недоношенных и маловесных детей, у которых сепсис отмечен в 77–88% среди всех случаев S. agalactiae–инфекции. Именно в этой группе пациентов S. agalactiae– инфекция протекает наиболее тяжело и нередко заканчивается летально . Особо следует отметить, что в подавляющем большинстве случаев дети при этом рождаются в нормальном состоянии, однако уже через несколько часов клиническая картина резко меняется.
Манифестация ранних форм, как правило, дебютирует цианозом и респираторными нарушениями (апноэ, тахипноэ). Возможна также молниеносная форма заболевания, при которой очень быстро появляются все признаки септического шока . В клинических анализах крови при этом нередко обнаруживают лейкопению. При позднем дебюте (после 7–го дня жизни) S. agalactiae– инфекция также может протекать в виде сепсиса или менингита . Клинически при этом чаще регистрируют напряжение родничков, лихорадку, угнетение сознания вплоть до комы и тонико– клонические судороги. Реже отмечаются другие проявления инфекции: омфалит, отит, синусит, конъюнктивит, артрит, остеомиелит, поражения кожи, мочевой системы, эндокардит, миокардит.
В связи с низкой специфичностью клинических проявлений S. agalactiae–инфекции у новорожденных детей особое значение в верификации этиологии заболевания приобретают лабораторные методы диагностики (классические бактериологические, серологические, молекулярно– биологические) . При бактериоскопии обнаруживают типичные грамположительные кокки, образующие короткие цепочки. Для выявления S. agalactiae в биологических жидкостях организма (в крови, ликворе, моче, трахео–бронхиальном аспирате) методом бактериологических посевов необходимо использовать среды, обогащенные кровью или сывороткой, т.к. выделение S. agalactiae на обычных средах, как правило, не превышает 10–12%. Серологические методы диагностики имеют значение лишь в плане ретроспективного подтверждения диагноза, а также для выявления напряженности пассивного иммунитета, трансплацентарно полученного от матери. При этом к факторам высокого риска реализации S. agalactiae–инфекции в неонатальный период относят указание на серонегативность или низкие титры специфических антител у инфицированных беременных женщин.
В последние годы все большую значимость приобретают молекулярно–биологические методы диагностики. Быстрота получения результатов при использовании полимеразной цепной реакции (ПЦР) в сочетании с высокой чувствительностью и специфичностью делают ПЦР незаменимым методом верификации инфекционных заболеваний, особенно в неонатологической практике . Так, нами в пилотном исследовании было проведено изучение чувствительности ПЦР в детекции генома S. agalactiae в сравнении с методом бактериологических посевов. При исследовании аспирата из трахеи у 62 новорожденных, находящихся в отделении неонатальной реанимации и интенсивной терапии в связи с тяжелыми инфекциями неонатального периода, у 9 детей (14,5%) методом ПЦР удалось выявить геном S. agalactiae, в то время как при параллельно выполненных бактериологических посевах результаты были отрицательными. Вероятно, негативные результаты бактериологического исследования были обусловлены массивной антибиотикотерапией, проводимой детям с первых дней жизни, что могло привести к изменению культурально– морфологических характеристик возбудителя и снижению числа жизнеспособных микроорганизмов.
Методы специфической иммунопрофилактики S. agalactiae–инфекции до настоящего времени не разработаны, поэтому для предупреждения перинатальной S. agalactiae–инфекции используют антибиотикопрофилактику (АБ–профилактика). Разработанные в 2002 г. рекомендации СDC предусматривают обязательное обследование на S. agalactiae–носительство всех беременных женщин на сроке 35–37 недель . При выделении возбудителя из влагалища и/или заднепроходного канала женщине в период родов назначают антибиотики в тех случаях, когда имеются определенные факторы риска. К факторам риска при этом относят следующие состояния: предыдущий ребенок перенес инвазивную S. agalactiae– инфекцию, во время настоящей беременности имели место S. agalactiae–бактериурия, угроза преждевременных родов (до 37 нед.), безводный промежуток больше 12 часов, лихорадка в родах.
В случае выявления у S. agalactia– инфицированной женщины одного из указанных выше факторов риска, для профилактики перинатальной S. agalactiae–инфекции в период родов назначают антибиотик.
Для АБ–профилактики рекомендовано использовать бензилпенициллин, который вводят внутривенно в дозе 5 млн. ЕД с момента начала родовой деятельности, переходя в дальнейшем на дозу 2,5 млн. ЕД каждые 4 часа до окончания родов. Альтернативой бензилпенициллину является ампициллин, который вводят также внутривенно, первоначально в дозе 2 г на введение, а затем – по 1 г каждые 4 часа. При аллергии к пенициллинам их заменяют клиндамицином или эритромицином, но чаще в этих случаях рекомендуют цефазолин (вначале
dbdd.ru
определение, проведение анализов, причины и лечение
Стрептококк у мужчин выявляется чаще всего в мазке из зева, носа или во время анализа мочи. Он выступает нормальным обитателем носовой полости, рта и кишечника, в связи с этим диагностическую ценность играет комбинация его высокого титра с клиническим проявлением инфекционного заболевания.
Определение
Streptococcus agalactiae у мужчин (или по-другому стрептококк агалактия) является условной патогенной бактерией, относящейся к группе гемолитических стрептококков. В норме данный микроскопический организм имеется в человеческом теле в малом количестве, но не вызывает болезни и никак не угрожает здоровью.
Род стрептококков сегодня насчитывает свыше двадцати видов бактерий. Одна часть этих микроскопических существ является представителями здоровой микрофлоры человека, а другая вызывает заболевания. Сами бактерии имеют микроскопические размеры, у них шаровидная форма, они достаточно длительное время сохраняются в пыли, на различных предметах, могут переносить низкие температуры, а при температуре более пятидесяти шест градусов погибают лишь через тридцать минут.
Причины Streptococcus agalactiae у мужчин
Стрептококковую инфекцию вызывают бактерии данной группы, которые способны разрушать эритроциты, вызывая в человеческом организме воспалительный процесс. Streptococcus agalactiae у мужчин может доставлять неприятности абсолютно по тем же причинам, что и у дам.
В большей степени все, как правило, напрямую зависит от гормонального фона, а также от способности организма человека противостоять инфекции. Главной опасностью для здоровья человека при развитии стрептококковой инфекции служат яды с токсинами, которые выделяются болезнетворными микроорганизмами при размножении. Возбудитель может попадать в мужской организм следующими способами:
- Передача паразита может осуществляться при питании зараженными продуктами.
- Проникновение нередко происходит на фоне интимного контакта. Половой партнер, передающий инфекцию, может быть носителем или больным. Стрептококк способен активно размножаться во влагалище женщин, а при интимном контакте патогены попадают на половой орган мужчины. Также стрептококки способны размножаться в уретре.
- Алиментарным способом. Заражение часто наступает из-за нарушения правил личной гигиены. Стрептококки из прямой кишки попадают на половые органы.
- Возбудитель может проникать внутрь организма при стоматологическом осмотре либо хирургическом вмешательстве, если таковые осуществляются с применением инструментов, не прошедших необходимую дезинфекцию.
- Если инфекция у собеседника локализована в дыхательных путях, заразиться можно при поцелуе, чихании или кашле больного (слюна должна попасть на кожу или в дыхательные пути здорового человека).
- Бытовой путь. Стрептококки способны длительное время жить на различных поверхностях. Поэтому заразиться можно, если пользоваться предметами быта (посудой, полотенцем, бельем) больного.

Проведение исследований
Для анализ на Streptococcus agalactiae у мужчин, как правило, берут следующие биологические материалы:
- Мазок из ротоглотки (при болезнях верхних дыхательных каналов).
- Мазок из уретры (при патологиях мочеполовой системы).
- Исследование мокроты из носа.
- Взятие соскоба поверхности кожи (при развитии рожистого заболевания).
Также проводятся следующие исследования:
- Сдача крови и мочи.
- Биохимическое исследование крови.
- Проведение бактериологического посева.
- Ультразвуковое исследование внутренних органов.
- Проведение рентгенографии легких и электрокардиографии.
Методы терапии
Лечение Streptococcus agalactiae у мужчин сводят к уничтожению ее источника. Курс терапии стрептококка, как правило, основывается на использовании антибиотиков пенициллиновой группы, а также препаратов, которые укрепляют иммунитет. На период лечения рекомендуют правильно питаться, снизив физические нагрузки, ведя здоровый образ жизни и соблюдая гигиену.
Для общего лечения Streptococcus agalactiae у мужчин используется «Бензилпенициллин», «Феноксиметилпенициллин», «Амоксициллин», «Аугументин», «Азитромицин», «Цефуроксим», «Цефтриаксон», «Цефотаксим», «Кларитромицин» и «Эритромицин». В рамках местной терапии применяют «Биопарокс», «Шексорал» или «Хлоргексидин». Любые назначения выполняет доктор, самолечением заниматься не рекомендуется.

Укрепление иммунитета
В целях укрепления иммунной системы и стимулирования работы организма при инфекционном заболевании часто назначаются «Иммунал», «ИРС-19», «Имудон», «Имунорикс», «Лизобакт». Природным иммуностимулятором выступает аскорбиновая кислота, большое количество которой присутствует в шиповнике, лимоне, киви, клюкве, облепихе, смородине, петрушке, калине.
Восстановление здоровой микрофлоры кишечника
При использовании антибактериальных препаратов микрофлора, которая необходима для нормального функционирования системы пищеварения, обычно значительно угнетается. В целях ее восстановления в обязательном порядке назначают прием пробиотиков:
- «Аципол».
- «Бифидумабактерин».
- «Бифиформ».
- «Линекс».
Детоксикация организма
У мужчин Streptococcus agalactiae group B (группы В) — выявляется редко. В основном, он обнаруживается у новорожденных, беременных и рожениц, вызывая во всех случаях (особенно у младенцев) тяжелые заболевания. Мужчины могут им заразиться при половом контакте. Эти бактерии отравляют мужской организм разными ядами и ферментами, являющимися продуктами их жизнедеятельности. Этими элементами усложняется течение болезни, а также вызывается немалое количество малоприятных проявлений.
Для вывода из организма токсинов бактерий необходимо выпивать много жидкости (около трех литров в сутки), полоскать ротоглотку раствором фурациллина, либо также подойдет слабо-соляное средство. Из препаратов для вывода патогенов из организма можно выделить «Атоксил», «Альбумин» и «Энтеросгель».

Антигистаминные препараты
Применение антибактериальных лекарств иногда сопровождается некоторыми аллергическими реакциями. Чтобы они не переросли в осложнение, назначают антигистаминные средства:
- «Кларитин».
- «Супрастин».
- «Цетрин» и другие.
Симптоматическая терапия
В целях облегчения симптоматики при наличии Streptococcus agalactiae в мазке у мужчин назначаются различные препараты (по показаниям). При возникновении тошноты и рвоты прописывают «Мотилиум», «Пипольфен», «Церукал». При повышенной температуре требуются прохладные компрессы на лоб, на шею или в области подмышек. Среди препаратов стоит выделить «Парацетамол», «Ибупрофен». При заложенности носа подойдут сосудосуживающие лекарства «Нокспрей», «Фармазолин» и их аналоги.
Норма Streptococcus agalactiae у мужчин
Направление на прохождение микробиологического посева и изучение микрофлоры мочеполовых каналов у мужчин доктор дает в том случае, если возникают симптомы раздражения в уретре. Представителями здоровой мужской микрофлоры являются: стрептококки, пептококки, микрококки, бациллярные микроорганизмы, стафилококки и лактобактерии.
Количество каждого вида микроорганизмов в пределах нормы может указывать на здоровье мочеполовой мужской системы. Если анализ показал, что Streptococcus agalactiae содержится в количестве 10 в 4 степени КОЕ/мл — это норма. Появление патогенных микроскопических организмов либо значительный рост численности какого-либо из участников биоценоза сообщает о сбоях в иммунитете или заболевании.

Мазок берется после специальной подготовки с помощью стерильного тампона. Его доставляют в лабораторию не позже двух часов с момента забора анализа. Наибольшую долю в нормальном составе мужской микрофлоры имеет пептококк, тоже являющийся стрептококком, только не имеющим никаких патогенных свойств. В результате анализа он может насчитывать количество колониеобразующих единиц до десяти в пятой степени от общего числа микроскопических организмов.
Отсутствие патогенных представителей гонококка, трихомонады в сочетании с присутствием нормальных представителей в приемлемых соотношениях свидетельствует об отсутствии дисбактериоза и хорошем состоянии иммунитета.
Что значит Streptococcus agalactiae в мазке у мужчин?
Когда мазок сообщает о стрептококковой инфекции
Если в мазке обнаружен стрептококк выше нормы, а на фоне этого дополнительно присутствует симптоматика раздражения и нагноения, то можно предположить, что в организме зародилась стрептококковая инфекция. Упомянутые ранее пептококки выступают аналогами лактобактерий нормального женского биоценоза. Пептококки у мужчин также представляют стрептококки, которые способствуют восстановлению организма и поддержке нормального уровня кислотности.
Возрастание числа стрептококков прочих видов (патогенных в том числе) сообщает о присутствии источника инфекции или воспалительном процессе непосредственно в исследуемом органе. Причинами возникновения стрептококковой агалактии в мазке из уретры у мужчин, как уже отмечалось ранее, бывает ослабленный иммунитет, несоблюдение гигиены, половой акт с больным партнером.

Развитие очагов хронических инфекций в организме, например, фарингит, может спровоцировать болезни, которые вызывает стрептококк у взрослых в различных органах или системах. В особенности это может проявляться при ослаблении иммунитета на фоне переохлаждения, гиповитаминоза, при сахарном диабете, гипотиреозе.
Легкомысленное отношение к выбору полового партнера и к личной гигиене зачастую приводит к тому, что стрептококк начинает активно размножаться в половых органах мужчин и в уретре. Мазок пациента в таком случае будет указывать на стрептококк в качестве ведущего микроорганизма.
Антибактериальные препараты убивают не только патогенные бактерии, но и полезные. Поэтому употребление антибиотиков в период лечения инфекционных патологий любой локализации требуется сочетать с пробиотиками, противогрибковыми средствами и пребиотиками. Попадание на слизистую возбудителя половых инфекций тоже ведет к нарушению иммунитета, а вместе с тем к дополнительному обсеменению стрептококками.
Что означает Streptococcus agalactiae у мужчин 10 в 6 степени? Об этом далее.

Почему стрептококк появляется у мужчин в моче
Нормальное содержание в моче Streptococcus agalactiae у мужчин — 10 в 4 степени КОЕ/мл. Увеличенная концентрация бактерий в урине выявляется при наличии инфекции или по причине некорректного забора биологического материала. Рассматриваемые патогенные возбудители активно начинают развиваться в периоды ослабления иммунитета, во время пребывания пациента в стрессовом состоянии или в качестве сопутствующего заболевания.
Такие колонии очень часто локализуются в пределах кишечника, горла или мочеполовой системы. Streptococcus agalactiae в моче у мужчин в концентрациях выявляется при патологиях мочевыводящих путей, которые возникают в качестве первичного заболевания или являются сопутствующими при других недугов.
Таким образом, высокая концентрация таких бактерий в анализе мочи может свидетельствовать о наличии в мужском организме стрептококковой инфекции. Возбудителем вызывается целый ряд серьезных заболеваний, которые затрагивают многие органы с системами. Недуги, которые спровоцированы этим микроорганизмом, пациенту доставляют дискомфорт. В отдельных случаях они могут даже угрожать жизни.
fb.ru
Стрептококк агалактия (streptococcus agalactiae)
Стрептококки – это род грамположительных анаэробных бактерий, которые получают электроны из органических веществ. Их классифицируют по разным признакам, таким как тип гемолиза эритроцитов. Неполный гемолиз характерен для группы А, а полный – для группы В. Интересно, что единственным представителем второй категории является streptococcus agalactiae.
Человеку, не имеющему отношения к науке, подобное название практически ни о чём не скажет. Именно поэтому многие путают данный микроорганизм, ошибочно называют его стафилококком агалактия или стрептококком галактика. На деле же верное название – стрептококк агалактия. В переводе на русский слово обозначает «отсутствие молока». Микроорганизм назвали таким образом, потому что изначально его нашли у коров, страдающих от мастита.
Общая информация
О существовании streptococcus agalactiae чаще всего узнают женщины после того, как врач возьмет у них мазок из влагалища. Данный микроорганизм обычно оседает в кишечнике или мочеполовой системе, приводя к развитию инфекций. Стрептококк группы В выглядит как цепочка из эллипсовидных или шарообразных структур. Хотя организм относится к анаэробам, он способен существовать в том числе и в присутствии кислорода.
Стрептококки могут присутствовать в здоровой женской микрофлоре. Если показатели не превышают 10 в 4 степени КОЕ/мл, то они считаются нормальными. Однако если что-либо спровоцирует усиленное развитие клеток, то вокруг разрастающейся колонии появится область полного гемолиза эритроцитов.
По мере развития агалактия вырабатывает ряд токсинов. Во-первых, это стрептолизин, который разрушает ткани вокруг патогена. Во-вторых, появляется лейкоцидин, влияющий на иммунные клетки таким образом, что микробы спокойно избегают их. Синтезируется некротоксин, провоцирующий некроз тканей, а также вещества вроде стрептокиназы, амилазы и протеиназы, которые помогают агалактии распространяться дальше.
Пути передачи

Микроб способен попасть в человеческий организм после начала половой жизни. Классическими местами развития являются урогенитальный тракт, носоглотка и прямая кишка.
Известны следующие пути передачи:
- Половой;
- Пищевой;
- Контактно-бытовой;
- Воздушно-капельный;
- Вертикальный.
Стрептококк часто попадает в человеческое тело во время приема пищи, если не были соблюдены санитарно-гигиенические нормы, включая мытье рук, овощей или качественной жарки мяса. В этом случае патоген добирается до ротовой полости и органов ЖКТ, затрагивается носоглотка. Нередко заразиться можно посредством слюны, которая попадает во внешнюю среду. Например, кашель, чихание или даже разговор с больным человеком может в будущем стать причиной инфекции.
Обратите внимание. Мужчины в случае заражения становятся носителями, которые передают патоген партнершам.
Высока вероятность заболеть у тех людей, которые не используют барьерные контрацептивы во время интимной близости. Таким образом агалактия быстро распространяется по мочеполовой системе. Наконец, если женщина родит ребенка, будучи при этом зараженной стрептококком, она передаст возбудителя своему малышу.
Как проявляется болезнь?

Небольшое количество патологических клеток не приводит к серьёзной симптоматике. В этом случае лактобактерии влагалища или иммунитет подавляют деятельность возбудителя. Однако если по каким-либо причинам иммунная система ослабнет, произойдет активация стрептококка.
Обычно подобное наблюдается на фоне:
- Гормональных изменений;
- Несоблюдения гигиенических норм;
- Сахарного диабета;
- ВИЧ;
- Проведения спринцевания.
Основная проблема подобного заболевания в том, что чаще всего агалактия не вызывает каких-либо симптомов. У больных не развивается воспалительный процесс, а потому заметить неладное очень трудно. Ситуация особенно осложняется во время беременности, когда рост прогестерона угнетает местный иммунитет.
По мере продвижения патогена к другим органом неприятные симптомы все же могут проявиться. У мужчин о значительном количестве вредоносных клеток можно судить по слизистым выделениям, жжению уретры и боли при мочеиспускании. У женщин проявляется разнообразная симптоматика цистита. В особо тяжелых случаях он сопровождается головной болью и слабостью. Обычно температуры нет, но в редких случаях она возможна.
Потенциальная опасность
Наибольшую опасность стрептококк агалактия представляет для беременных женщин, а точнее для их будущих детей. Патоген всегда находят в мазках во время плановых осмотров в период вынашивания, своего пика клетки обычно достигают к 36 неделе. В этот момент врачи должны уделить особенно пристальное внимание показателям, и, в случае необходимости, принять меры по обезвреживанию возбудителя.
Вероятность осложнений значительно возрастает, если:
- Есть угроза преждевременных родов;
- Будущей матери меньше двадцати лет;
- Раньше у пациентки наблюдались случаи инфицирования детей;
- Стрептококк появился в моче.
Streptococcus agalactiae может спровоцировать инфекцию мочевыделительных путей, послеродовой эндометрит, эндокардит, менингит, хориоамниотит.
Редко, но возбудитель способен приводить к воспалению плодных оболочек, из-за чего бывают задержки в развитии плода, ранние роды и самопроизвольный аборт.
Слабые и недоношенные младенцы сильно подвержены заражению во время родов. Патоген попадает в кровь и приводит к развитию пневмонии, менингита и других заболеваний. Риск заболеть сохраняется и после родов, если ребенок будет контактировать с носителями. Особую опасность представляют 4-5 недели жизни.
Стрептококковая инфекция всегда очень тяжело переносится маленькими детьми. Если ребенок не будет находиться под наблюдением специалистом, заболевание вероятней всего окончится летальным исходом. Также возможны случаи неполного выздоровления, в результате которых дети страдают от проблем с функционированием нервной системы.
Диагностика и лечение

Беременные женщины регулярно сдают мазки из цервикального канала в плановом порядке. В результате и, в случае необходимости, проводят культуральное исследование. Для более точной диагностики проводятся скрининг-тесты и ПЦР. Последнее используется и после родов (берется образец с кожи ребенка), такое исследование позволяет выявить ДНК патогена.
Стандартные методы воздействия:
- Если женщина не беременна или только планирует зачатие, серьёзного лечения обычно не требуется. В первом случае применяются местные средства, а во втором врачи вообще рекомендуют выжидать, пока не появятся симптомы.
- Если они так и не появятся, а затем женщина забеременеет, то на 35-37 неделе необходимо будет провести вторичную диагностику.
- Местные средства используются и в том случае, если s agalactiae была выявлена у кормящей матери.
В остальных случаях лечение проводится с помощью антибиотиков. Если анализы показали, что патогена стало более 10 в 5 степени КОЕ/мл, то используются пенициллины, макролиды и цефалоспорины.
Лечение во время беременности начинают только после двенадцатой недели. В этот момент женщине прописывают лекарства для приема внутрь.
В качестве средств местного воздействия используется свечи. Если у беременной выявлена очень высокая концентрация стрептококка, а ранее не было проведено санации влагалища, то используется антибактериальная терапия в родах. Такие процедуры значительно уменьшают вероятность передачи патогена ребенку, вплоть до 1-2%.
Профилактика

Чтобы защитить себя и будущего ребенка от стрептококковой инфекции, женщины должны соблюдать ряд правил. В первую очередь, они включают в себя следование гигиеническим нормам и слежение за чистотой собственного дома. Важно правильно питаться, насыщая свой рацион полезными микроэлементами, чтобы иммунитет оставался сильным.
Защитным силам организма будет способствовать отказ от вредных привычек, регулярные занятия спортом и правильный подбор одежды. На иммунитете негативно сказывается сильное переохлаждение. Необходимо выбирать медицинские учреждения с хорошим уровнем санитарии и избегать контакта с больными людьми.
Если они все же присутствуют, то должны быть изолированы, а места их пребывания продезинфицированы. В дальнейшем необходимо регулярно сдавать мазки, чтобы вовремя выявить болезнь.
yachist.ru
что такое, норма, признаки патологии
Streptococcus agalactiae в мазке у женщин не всегда указывает на воспалительный процесс. У 15–40% женщин детородного возраста встречается бактерионосительство, когда микроорганизм является элементом влагалищной микрофлоры и не причиняет беспокойства. Но стрептококк агалактия относится к условно-патогенным микроорганизмам, поэтому при благоприятных условиях начинает размножаться, вызывая воспаление мочеполовой сферы. Женщине следует знать, что это такое – стрептококковое носительство и как проявляется стрептококковая инфекция.
 Streptococcus agalactiae в мазке у женщин – не всегда признак заболевания
Streptococcus agalactiae в мазке у женщин – не всегда признак заболеванияПатология и норма
Количество streptococcus agalactiae в мазке у женщин, не превышающее 104 колонеобразующих единиц в миллилитре секрета, – вариант нормы, микроб безопасен для женского здоровья.
Повышение содержания бактерий во влагалищной слизи указывает на развитие неспецифического воспаления, вызванного b-гемолитическим стрептококком группы В.
Создают условия для активного размножения стрептококковых бактерий:
- снижение иммунитета;
- частые простудные инфекции;
- гормональные отклонения;
- эндокринные патологии;
- несоблюдение гигиены;
- самолечение антибиотиками;
- дисбактериоз кишечника или влагалища;
- прием гормонов или цитостатиков;
- стрессы;
- тесное белье, плохо пропускающее воздух;
- переохлаждения;
- незащищенный секс.
При беременности у носительниц streptococcus agalactiae размножение колоний происходит почти всегда.
Провоцируют активность микроорганизмов естественные изменения в организме, связанные с усилением секреции прогестерона и ослаблением иммунитета.
Патологическим отклонением, требующим лечения, считается показатель 105 и больше КОЕ/мл.
Чтобы избежать осложнений, при выявлении инфекции необходимо сразу начинать медикаментозную терапию.
Симптомы streptococcus agalactiae
В большинстве случаев бактериальная инфекция не вызывает характерных симптомов. Несмотря на активное размножение условно-патогенной микрофлоры, женщина не испытывает дискомфорта.
Клинические проявления появляются, когда стрептококковая активность сопровождается выбросом токсинов:
- Стрептолизин. Разрушающе действует на ткани.
- Лейкодин. Нарушает местный иммунитет.
- Некротоксин. Становится причиной некроза.
- Стрептококковые ферменты. Вещества помогают streptococcus agalactiae распространяться в окружающие ткани.
Местная интоксикация продуктами жизнедеятельности условно-патогенных микроорганизмов приводит к появлению симптомов воспаления мочеполовой сферы. Клиника зависит от локализации воспалительного процесса.
Уретрит и цистит
Из влагалища стрептококк агалактия попадает в уретральный канал и постепенно поднимается вверх к мочевому пузырю, вызывая симптомы цистита:
- острая боль внизу живота;
- частые позывы в туалет;
- рези и жжение при мочеиспускании;
- неудовлетворение после опорожнения пузыря.
Моча становится мутной с примесью хлопьев.
Острое течение цистита сопровождается головной болью, общей слабостью и снижением жизненного тонуса. Высокая температура бывает редко.
Бактериальный вагиноз
Во влагалищном секрете отмечается содержание стрептококка.
Инфекционный процесс вызывает:
- тянущую боль в паху;
- отечность и гиперемию половых губ;
- зуд и жжение промежности;
- желтоватые или коричневатые выделения.
При вагинозе женщины испытывают болезненный дискомфорт при сексе и стараются избегать интимной связи.
 Женщине следует знать, что это такое – стрептококк агалактия и какие симптомы он может вызвать
Женщине следует знать, что это такое – стрептококк агалактия и какие симптомы он может вызватьОсобенности лечебного процесса
Для лечения применяют антибиотикотерапию. Подбирают препараты, способные уничтожать стрептококки из следующих групп:
- цефалоспорины;
- пенициллины;
- макролиды.
При бессимптомном течении и при слабо выраженных проявлениях болезни 7–10-дневный лечебный курс помогает избавить женщину от streptococcus agalactiae.
Для устранения сильно выраженной симптоматики дополнительно могут назначаться симптоматические препараты:
- анальгетики;
- спазмолитики;
- антигистаминные;
- жаропонижающие.
Беременным системная антибиотикотерапия проводится редко из-за риска повлиять на развитие плода. Для подавления активности микроорганизмов применяют вагинальные свечи с антибактериальным эффектом.
В качестве общеукрепляющего средства назначают витамины.
Препараты повышают иммунную защиту и организм быстрее подавляет бактериальную активность.
Опасность стрептококка агалактия
Опасен streptococcus agalactiae тем, что большинство воспалительных процессов мочеполовой сферы протекает бессимптомно и может перейти в хроническую форму. Это негативно отразится на репродуктивной функции женщины и может стать причиной бесплодия.
Стрептококковая инфекция у беременных опасна для плода и будущей мамы. У женщины может развиться:
- послеродовый эндометрит;
- инфекция мочевыводящих путей.
У женщин с streptococcus agalactiae повышается риск выкидыша и рождения ребенка с низкой массой тела.
Инфицирование младенца происходит во время прохождения по родовым путям или в предродовом периоде, когда выход слизистой пробки снижает естественную защиту плода. У новорожденного могут быть следующие осложнения:
- неонатальный сепсис;
- пневмония;
- менингит.
Осложнения развиваются обычно на 2–3 сутки после рождения.
Обследование беременных позволяет избежать опасных для ребенка последствий.
Своевременное лечение отклонений streptococcus agalactiae в мазке у беременных предупредит заражение ребенка.
 Патология или норма streptococcus agalactiae определяют в помощью лабораторного исследования мазка
Патология или норма streptococcus agalactiae определяют в помощью лабораторного исследования мазкаStreptococcus agalactiae в мазке может быть неактивным и не вредить женскому здоровью. Но бактерия относится к условно-патогенным и при снижении защитных сил организма вызывает воспалительный процесс, который чаще протекает бессимптомно.
Если во влагалищном секрете обнаружен стрептококк агалактия, нужно внимательнее относиться к своему здоровью и не пренебрегать ежегодным осмотром у гинеколога.
Своевременное выявление бактериальной активности и грамотно подобранное лечение позволят быстро устранить признаки воспаления и уничтожить колонии микроорганизмов.
Читайте также: полип уретры у женщины
www.baby.ru
Streptococcus agalactiae — Гинекология — Здоровье Mail.ru
Здравствуйте! Установлено, что инфекция, вызванная стрептококками группы В (СГВ–инфекция), может приводить к бактериемии (наличию бактерий в крови), эндометриту (воспалительному процессу во внутреннем слизистом слое тела матки), хориоамниониту (воспалению плодных оболочек (хориона и амниона), возникающему вследствие инфицирования во время беременности и родов), воспалению мочевых и родовых путей у женщины, а также вызывать локализованные и инвазивные формы заболевания у новорожденных детей. Это одни из основных возбудителей инфекционного эндокардита, они могут вызывать кариес. Стрептококки группы В были впервые идентифицированы, как возбудители мастита у коров. Группа представлена одним видом – Streptococcus agalactiae. Стрептококки группы В – это грамположительные аэроб¬ные диплококки. Все штаммы стрептококков группы В обладают группоспецифическим полисахаридом. На основании особенностей структуры полисахаридных антигенов капсулы различают 9 серотипов СГВ: Iа,Ib, II, III, IV, V, VI, VII, VIII. К настоящему времени общепризнано, что главным фактором вирулентности СГВ является полисахаридная капсула. При этом установлено, что наибольшее количество заболеваний новорожденных обусловлено III серотипом СГВ. Идентифицирован поверхностный белок FbsA стрептококков группы В, который обладает способностью связывать человеческий фибриноген. Наряду с белком FbsA, одновременно в двух независимых исследованиях был выявлен еще один белок СГВ, способный связывать фибриноген и обозначенный, как FbsB или Fgag. Два из них были условно обозначены sspBl и sspB2. Установлено, что наличие у штаммов СГВ потенциальных адгезинов (в особенности sspB2) представляет значительную опасность, приводя к инфицированию плаценты, плацентарной недостаточности и преждевременным родам, а также приводя к развитию задержки внутриутробного развития плода и асфиксии (удушью) в родах. По данным массовых обследований, отмечено, что 15–40% женщин являются носителями СГВ, которые контаминируют (заселяют) слизистые влагалища или прямой кишки. Установлено также, что до 50% детей, рожденных инфицированными женщинами через естественные родовые пути, колонизируются СГВ. Передача инфекции от инфицированной матери плоду происходит, как правило, незадолго до родов или непосредственно во время родов. В постнатальный период, особенно в ближайшие часы и сутки после родов, ребенок также может инфицироваться, однако это случается значительно реже по сравнению с пре– и интранатальной контаминацией. Отмечено, что инфицирование новорожденных СГВ не всегда приводит к развитию инфекционного процесса. Так, к факторам риска по реализации СГВ–инфекции у ребенка, рожденного от СГВ–инфицированной женщины, относят: возраст беременной менее 20 лет, ранее случавшиеся выкидыши или медицинские аборты, амнионит, преждевременные роды (12 часов), задержку внутриутробного развития и наличие СГВ–инфекции у ранее рожденных детей. До широкого внедрения в акушерскую практику антибактериальной профилактики СГВ неонатальная заболеваемость стрептококковой (группы В) инфекцией составляла 1–4 на 1000 живорожденных детей, среди которых в 75% случаев имела место (в первые 7 суток жизни) ранняя манифестация. При этом было отмечено, что на 100 инфицированных беременных женщин рождался 1 ребенок с тяжелой СГВ–инфекцией. Следует особо подчеркнуть, что благодаря активному использованию в акушерской практике рекомендаций по профилактике СГВ–инфекции, удалось существенно снизить уровень инфицированности новорожденных. В результате этого значимо уменьшилась частота инвазивных форм СГВ–инфекции у детей первого месяца жизни. Так, заболеваемость СГВ–инфекцией в ранний неонатальный период в последние годы удалось снизить более чем на 80%, а показатели неонатальной заболеваемости в целом не превышают 0,3 случаев на 1000 живорожденных детей. Лучше избавиться от этой инфекции. Лечение назначают согласно полученной антибиотикограмме. Ваш лечащий доктор поможет Вам в этом. Эта инфекция может быть передана и половым путем, но может быть и Вашей индивидуальной особенностью. Партнеру лучше пройти предварительное обследование. Всего Вам доброго!health.mail.ru
STREPTOCOCCUS AGALACTIAE ИНФЕКЦИЯ
Инфекция Streptococcus agalactiae (S. agalactiae). Неонатальная заболеваемость S. Agalactiae- инфекцией, ее клинические проявления. Методы специфической иммунопрофилактики S. Agalactiae-инфекции.
Садова Н.В., Заплатников А.Л., Шипулина О.Ю., Подкопаев В.Н., Фомина С.Г., Скачкова Т.С., Домонова Э.А., Сафонова А.П.
Одним из частых бактериальных заболеваний перинатального периода является инфекция, вызванная Streptococcus agalactiae (S. agalactiae). У женщин в период беременности S. agalactiae; инфекция может протекать как бессимптомно, так и клинически значимо с развитием бактериемии, эндометрита, хориоамнионита, воспаления мочевых и родовых путей, а у новорожденных детей проявляться локализованными и инвазивными поражениями [1–13].
S. agalactiae относится к стрептококкам группы В, которые являются грамположительными инкапсулированными факультативными анаэробами, не образующими спор. Главным фактором вирулентности S. agalactiae является полисахаридная капсула. Из белковых факторов патогенности особо отмечают С5а пептидазу, бета–гемолизин, С протеины (альфа– и бета–), гиалуронидазу, Sip белок, CAMP фактор (В–белок), а также комплекс протеаз, гемолизин, адгезины и др. [2,14–16].
Установлено, что 15–40% женщин являются носителями S. agalactiae, колонизирующей слизистые влагалища или прямой кишки [1,2,6,8]. Рождение детей от S. agalactiae–инфицированных женщин в 50% сопровождается вертикальной трансмиссией возбудителя. Передача инфекции от инфицированной матери происходит, как правило, незадолго до родов или непосредственно во время родов. В постнатальный период, особенно в ближайшие часы и сутки после рождения, ребенок также может инфицироваться, однако это случается значительно реже по сравнению с пре– и интранатальной контаминацией. Отмечено, что S. agalactiae– инфицирование новорожденных не всегда приводит к развитию инфекционного процесса. Факторами риска реализации инфекции у ребенка, рожденного от S. agalactiae–инфицированной женщины, являются: возраст беременной (<20 лет), выкидыши или медицинские аборты в анамнезе, амнионит, преждевременные роды (<37 недель), лихорадка в родах (более 37,5°С), длительный безводный период (>12 часов), задержка внутриутробного развития и наличие S. agalactiae– инфекции у ранее рожденных детей [6,8].
Неонатальная заболеваемость S. agalactiae– инфекцией до недавнего времени составляла 1–4 на 1000 живорожденных детей, среди которых в 75% случаев имела место манифестация в 1–7–е сутки жизни. При этом на 100 инфицированных беременных женщин рождался 1 ребенок с тяжелой S. agalactiae–инфекцией [4–6]. Благодаря активному использованию в акушерской практике рекомендаций по профилактике S. agalactiae– инфекции, удалось существенно снизить уровень инфицированности новорожденных, а также частоту инвазивных форм заболевания у детей первого месяца жизни. Так, в странах, где проводится антибактериальная профилактика перинатальной S. agalactiae–инфекции, заболеваемость в ранний неонатальный период удалось снизить более чем на 80%, а показатели неонатальной заболеваемости в целом не превышают 0,3 случая на 1000 живорожденных детей [8].
Клиническими проявлениями перинатальной S. agalactiae–инфекции у женщин являются послеродовые инфекции эндометрия, мочевыводящих путей, головного мозга, а также сепсис и осложнения кесарева сечения. У новорожденных выделяют локализованные и инвазивные формы перинатальной S. agalactiae–инфекции. При этом в зависимости от времени манифестации выделяют заболевания с ранним (до 7 дня жизни) и поздним (после 7 суток жизни) дебютом. S. agalactiae– инфекция у новорожденных наиболее часто протекает в виде инвазивных форм с бактериемией, поражением легких, мозговых оболочек. Нередко при этом заболевание приобретает септический характер, особенно у недоношенных и маловесных детей, у которых сепсис отмечен в 77–88% среди всех случаев S. agalactiae–инфекции. Именно в этой группе пациентов S. agalactiae– инфекция протекает наиболее тяжело и нередко заканчивается летально [3,8]. Особо следует отметить, что в подавляющем большинстве случаев дети при этом рождаются в нормальном состоянии, однако уже через несколько часов клиническая картина резко меняется.
Манифестация ранних форм, как правило, дебютирует цианозом и респираторными нарушениями (апноэ, тахипноэ). Возможна также молниеносная форма заболевания, при которой очень быстро появляются все признаки септического шока [3– 10]. В клинических анализах крови при этом нередко обнаруживают лейкопению. При позднем дебюте (после 7–го дня жизни) S. agalactiae– инфекция также может протекать в виде сепсиса или менингита [8]. Клинически при этом чаще регистрируют напряжение родничков, лихорадку, угнетение сознания вплоть до комы и тонико– клонические судороги. Реже отмечаются другие проявления инфекции: омфалит, отит, синусит, конъюнктивит, артрит, остеомиелит, поражения кожи, мочевой системы, эндокардит, миокардит.
В связи с низкой специфичностью клинических проявлений S. agalactiae–инфекции у новорожденных детей особое значение в верификации этиологии заболевания приобретают лабораторные методы диагностики (классические бактериологические, серологические, молекулярно– биологические) [2,11,17,18]. При бактериоскопии обнаруживают типичные грамположительные кокки, образующие короткие цепочки. Для выявления S. agalactiae в биологических жидкостях организма (в крови, ликворе, моче, трахео–бронхиальном аспирате) методом бактериологических посевов необходимо использовать среды, обогащенные кровью или сывороткой, т.к. выделение S. agalactiae на обычных средах, как правило, не превышает 10–12%. Серологические методы диагностики имеют значение лишь в плане ретроспективного подтверждения диагноза, а также для выявления напряженности пассивного иммунитета, трансплацентарно полученного от матери. При этом к факторам высокого риска реализации S. agalactiae–инфекции в неонатальный период относят указание на серонегативность или низкие титры специфических антител у инфицированных беременных женщин.
В последние годы все большую значимость приобретают молекулярно–биологические методы диагностики. Быстрота получения результатов при использовании полимеразной цепной реакции (ПЦР) в сочетании с высокой чувствительностью и специфичностью делают ПЦР незаменимым методом верификации инфекционных заболеваний, особенно в неонатологической практике [17,18]. Так, нами в пилотном исследовании было проведено изучение чувствительности ПЦР в детекции генома S. agalactiae в сравнении с методом бактериологических посевов. При исследовании аспирата из трахеи у 62 новорожденных, находящихся в отделении неонатальной реанимации и интенсивной терапии в связи с тяжелыми инфекциями неонатального периода, у 9 детей (14,5%) методом ПЦР удалось выявить геном S. agalactiae, в то время как при параллельно выполненных бактериологических посевах результаты были отрицательными. Вероятно, негативные результаты бактериологического исследования были обусловлены массивной антибиотикотерапией, проводимой детям с первых дней жизни, что могло привести к изменению культурально– морфологических характеристик возбудителя и снижению числа жизнеспособных микроорганизмов.
Методы специфической иммунопрофилактики S. agalactiae–инфекции до настоящего времени не разработаны, поэтому для предупреждения перинатальной S. agalactiae–инфекции используют антибиотикопрофилактику (АБ–профилактика). Разработанные в 2002 г. рекомендации СDC предусматривают обязательное обследование на S. agalactiae–носительство всех беременных женщин на сроке 35–37 недель [6]. При выделении возбудителя из влагалища и/или заднепроходного канала женщине в период родов назначают антибиотики в тех случаях, когда имеются определенные факторы риска. К факторам риска при этом относят следующие состояния: предыдущий ребенок перенес инвазивную S. agalactiae– инфекцию, во время настоящей беременности имели место S. agalactiae–бактериурия, угроза преждевременных родов (до 37 нед.), безводный промежуток больше 12 часов, лихорадка в родах.
В случае выявления у S. agalactia– инфицированной женщины одного из указанных выше факторов риска, для профилактики перинатальной S. agalactiae–инфекции в период родов назначают антибиотик.
Для АБ–профилактики рекомендовано использовать бензилпенициллин, который вводят внутривенно в дозе 5 млн. ЕД с момента начала родовой деятельности, переходя в дальнейшем на дозу 2,5 млн. ЕД каждые 4 часа до окончания родов. Альтернативой бензилпенициллину является ампициллин, который вводят также внутривенно, первоначально в дозе 2 г на введение, а затем – по 1 г каждые 4 часа. При аллергии к пенициллинам их заменяют клиндамицином или эритромицином, но чаще в этих случаях рекомендуют цефазолин (вначале – 2 г на введение внутривенно, затем по 1 г каждые 8 часов внутривенно до окончания родов). При высоком риске развития анафилаксии на бета–лактамные антибиотики может быть использован ванкомицин, который рекомендуют вводить внутривенно по 1 г каждые 12 часов до окончания родов. Анализ результатов проведенных исследований показал, что благодаря АБ– профилактике удалось существенно снизить не только неонатальную заболеваемость S. agalactiae–инфекцией (регресс более чем на 80%), но и частоту развития инвазивных форм, что определило значительное улучшение прогноза заболевания [6,8].
В тех случаях, когда женщине во время родов АБ– профилактика S. agalactiae–инфекции проведена не была, а у новорожденного имеются факторы риска (мать – носитель S. agalactiae, возраст матери менее 20 лет, отягощенный акушерский анамнез, преждевременные роды, лихорадка в родах, длительный безводный период, S. agalactiae–инфекции у ранее рожденных детей, а также признаки задержки внутриутробного развития у самого ребенка), следует как можно быстрее начать этиотропную терапию. Выбор стартовой АБ–терапии при этом проводится эмпирически. В связи с тем, что S. agalactiae высокочувствителен к бета–лактамным антибиотикам, при подозрении на S. agalactiae–инфекцию препаратом выбора является ампициллин. Однако учитывая, что клиническая картина неспецифична и имеется вероятность иной этиологии заболевания, ампициллин комбинируют с гентамицином. При этом предпочтителен внутривенный путь введения антибиотиков. В тех случаях, когда развивается неонатальный S. agalactiae–сепсис, ампициллин назначают из расчета 200 мг/кг/сутки [3,8]. При менингите дозы антибиотиков увеличивают, ампицилин при этом вводят из расчета 300 мг/кг/сутки. При выделении S. agalactiae и его генома лечение продолжают выбранной комбинацией антибиотиков до улучшения состояния, а в дальнейшем переходят на монотерапию ампициллином. При неинвазивных формах S. agalactiae–инфекции продолжительность монотерапии составляет 10 суток, при S. agalactiae–неосложненных менингитах – 14 суток, при S. agalactiae–артритах и остеомиелитах – 3–4 недели, при S. agalactiae–эндокартите и S. agalactiae–вентрикулите – не менее 4 недель [6,8].
Таким образом, в настоящее время имеются все возможности для снижения заболеваемости и летальности от перинатальной S. agalactiae– инфекции. Для этого необходимо у всех беременных женщин на сроке 35–37 недель проводить скрининг на S. agalactiae–носительство. При его подтверждении и наличии факторов риска (предыдущий ребенок в неонатальном периоде перенес S. agalactiae–инфекцию, наличие у женщины S. agalactiae–бактериурии, преждевременные роды, длительный безводный период, лихорадка в родах) женщине в родах должны быть назначены антибиотики для профилактики перинатальной S. agalactiae–контаминации ее ребенка. Строгое выполнение указанных рекомендаций позволяет достоверно снизить риск вертикального инфицирования и значительно уменьшает частоту инвазивных форм S. agalactiae–заболеваний у новорожденных детей.
Литература
- Оганян К.А. Течение и исход беременности при колонизации мочеполового тракта женщин стрептококками группы В и D. Автореф. дисс. канд. мед. наук.– СПБ, 2008, 24
- Покровский В.И., Поздеев О.К. Семейство Streptococcaceae/ Медицинская микробиология. ГЭОТАР Медицина, М, 1999: 193–206.
- Шабалов Н. П. Внутриутробные инфекции/ Неонатология. В 2 т. – С–Пб.: Специальная литература, 1996, Т. 2: 43–76.
- Baltimore R.S. Huie S.M., Meek J.I., Schuchat A. Early–onset neonatal sepsis in the era of group В streptococcal prevention. 2001. Vol. 108: 1094–8.
- Boyer K.M.: Neonatal group В streptococcal infections // Current Opinion Pediatrics, 1995, 7: 13–18.
- Centers for Disease Control and prevention(CDC). Prevention of perinatal group В streptococcal disease: Revised Guidelines fromCDC // Morb. Mortal. Wkly Rep. 2002.Vol.51: 10–22
- Kenyon S.L., Taylor PJ., Tarnow–Mordi W. Broad–spectrum antibiotics for preterm, prelabour rupture of fetal membranes, ORACLE Collaborative Group // Lancet. Vol. 357:979–88.
- Red Book: Report of the Committee on Infectious Diseases. 27h ed. Elk Grove Village, IL: American Academy of Pediatrics, 2006; 992.
- Weisner A.M., Johnson A.P., Lamagni T.L. et al. Characterization of group В streptococci recovered from infants with invasive disease in England and Wales // Clin Infect Dis. 2004. Vol. 38: 1203–1208.
- Nandyal RR. Update on group B streptococcal infections: perinatal and neonatal periods. J Perinat Neonatal Nurs. 2008, 22, 3: 230—37. 11. Шуляк Б.Ф. Инфекция стрептококка группы В, методы ее лабораторной диагностики и профилактики. Медицинский алфавит. 2010, №2: 47–53
- Gardam M.A., Low D.E., Saginur R. Group B streptococcal necrotizing fasciitis and streptococcal toxic shock–like syndrome in adults. Arch Intern Med, 1998, 158: 1704–08.
- Sendi P., Johansson L., Norrby–Teglund A. Invasive group B Streptococcal disease in non– pregnant adults: a review with emphasis on skin and soft–tissue infections. 2008, 36, 2, 100–11.
- Дмитриев А.В., Шаклеина Е.В. Молекулярная эпидемиология патогенных стрептококков группы В // Ж. микроб. эпидемиол. и иммунол. 2003: 83–92.
- Fischetti V.A. Gram–Positive Pathogens, American Society Microbiology, Washington, D.C, 2000. 511 p.
- Jacobsson K. A Novel family of fibrinogen– binding proteins in Streptococcus agalactiae // Vet. 2003. Vol. 96: 103–113.
- Эйдельштейн И.А., Сехин С.В., Иванчик Н.В. и др. Валидация тест–системы на основе ПЦР в режиме реального времени для выявления Streptococcus agalactiae в сравнении с микробиологическим методом. Молекулярная диагностика. М., 2010, 3: 346–348.
- Сафонова А.П., Пиксасова О.В., Скачкова Т.С. и др. Разработка методики выявления и количественного определения ДНК Streptococcus agalactiae на основе ПЦР в режиме реального времени. II Ежегодный Всероссийский Конгресс по инфекционным болезням. М, 2010: 282.
medprosvita.com.ua
Streptococcus agalactiae у мужчин и женщин: норма, симтомы, лечение
Streptococcus agalactiae вызывает у новорожденных детей тяжелые заболевания и в определенных случаях опасен для взрослых пациентов. Болезни, вызванные этой бактерией, отличаются тяжелым течением и высокой летальностью, что позволяет специалистам называть агалактию наиболее патогенным стрептококком.
СодержаниеПоказать
О стрептококках
загрузка…
Стрептококки – грамположительные анаэробные бактерии. Их особенность – способность образовывать цепочки различной длины. В организме человека они вырабатывают токсины, способные растворять кровь, чем объясняется их патогенность.
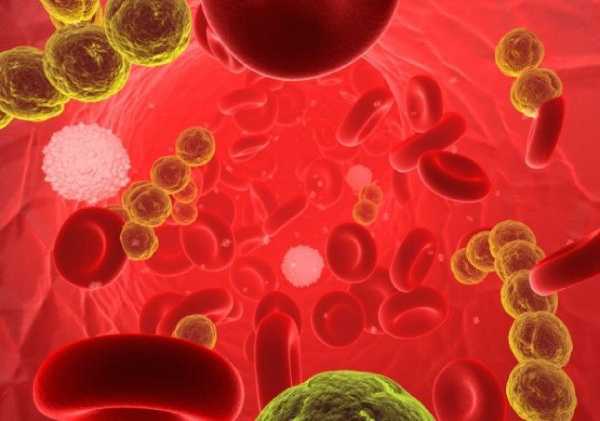
Медики делят стрептококки на несколько групп, которые обозначаются буквами латинского алфавита. Группа В состоит из несколько десятков видов стрептококка. В медицинском отношении опасен только один – агалактия.
Характеристика вида агалактия
Стрептококк группы Б агалактия – представитель условнопатогенных бактерий. Множество видов этих микроорганизмов живут в человеческом организме, до поры до времени не проявляя себя.

Агалактия распространена повсеместно. В природе она находится в различных млекопитающих, птицах, холоднокровных животных. Инфекция передается между людьми и от животных к людям.
В организме человека агалактия может находиться в толстой кишке, влагалище, уретре, изредка в горле. Изначально бактерии поселяются в прямой кишке, откуда периодически переходят на влагалище, урогенитальный тракт, на кожу. Такая колонизация у здоровых людей протекает бессимптомно.
У мужчин стрептококк агалактия обитает в кишечнике и (как патология) в мочеполовом тракте, активизируясь после приема антибиотиков или при падении иммунитета. Причинами появления стрептококков в мочеполовых путях мужчины являются:
- дисбактериоз кишечника;
- половой акт с женщиной носительницей бактерий;
- анальный половой акт.
Около 25% женщин являются носителями стрептококков во влагалище и при этом даже не догадываются о своем носительстве, так как симптомы никак не проявляются. Неприятных ощущений не возникает, а инфекция обостряется только при беременности или сильном снижением иммунитета.
Врачи отмечают, что в последние годы заболевания, вызванные агалактией, стали чаще регистрироваться у пожилых людей. У новорожденных, наоборот, заболеваемость снижается. Это связано с профилактикой инфекции в роддомах и увеличением пожилого народонаселения.
Инфекции, вызываемые бактерией
Сильно размножившись, агалактия становится причиной разнообразных болезней.
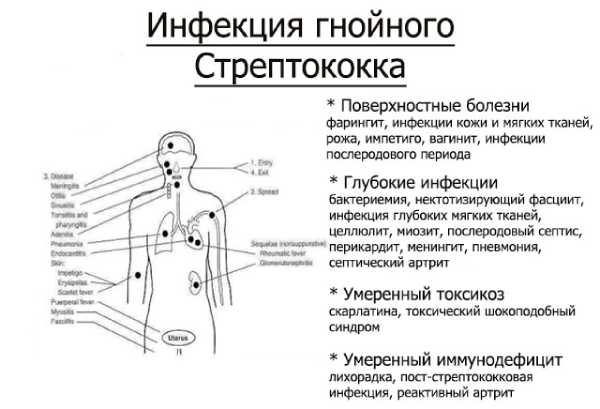
Наиболее чувствительны к стрептококку:
- новорожденные;
- беременные;
- диабетики;
- люди старше 65 лет;
- люди с проблемным иммунитетом.
В определенных условиях бактерии group B могут создавать тяжелые инфекции: поражать кожу, центральную нервную систему, сердце и легкие, реже другие органы и ткани.
Агалактия способна взаимодействовать с вирусом гриппа и вызывать воспаление легких на фоне вирусной болезни.
У пожилых людей агалактия вызывает болезни кожи и костей, сепсис и уросепсис, воспаление легких, воспаление брюшины. Нередко пожилые люди страдают от инфекции многократно.
Беременность и заражение
Носительство агалактия во влагалище не является постоянным. У беременных женщин репродуктивного возраста она выявляется чаще чем у пожилых и девочек-подростков.
Редко какая современная мама, только что выписавшаяся с малышом из роддома, не знает, что это такое – стрептококк агалактия. Повезло тем, кто вылечился от этой инфекции еще до родов.
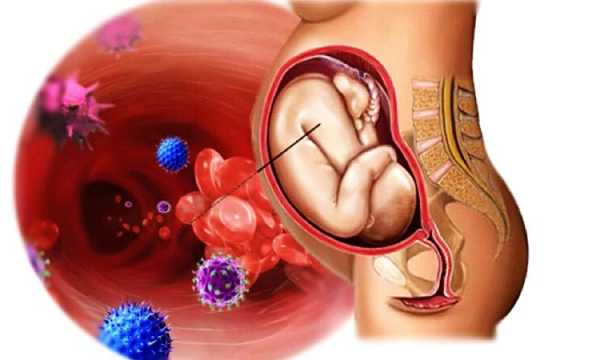
загрузка…
У беременных агалактия вызывает самопроизвольные преждевременные роды, пиелонефрит и другие инфекции мочеполовых путей, приводит к осложнениям процесса родов вплоть до необходимости кесарева сечения. У только что родивших женщин стрептококк способен вызвать менингит, мастит, эндометрит. Попадая в организм новорожденного, агалактия становится причиной сепсиса, менингита, пневмонии.
Стрептококк группы Б – главная причина развития тяжелых инфекций новорожденных в первую неделю жизни. Ребенок заражается во время родов и в раннем послеродовом периоде. 20 % детей, выживших после стрептококкового менингита, остаются инвалидами. В редких случаях агалактия приводит к смерти новорожденного.
Факторы риска:
- присутствие бактерий на шейке матки роженицы;
- обширная колонизация;
- у роженицы уже появлялись дети с инфекцией;
- аномально долгий безводный промежуток;
- острый цистит, обусловленный агалактией;
- недоношенность;
- кесарево сечение,
- введение инородных тел в матку во время беременности.
Диагностика
Что говорят врачи о паразитах
Доктор медицинских наук, профессор Гандельман Г. Ш.:
Занимаюсь обнаружением и лечением паразитов уже много лет. С уверенностью могу сказать, что паразитами заражены практически все. Просто большинство из них крайне трудно обнаружимы. Они могут быть где угодно — в крови, кишечнике, легких, сердце, мозге. Паразиты в буквальном смысле пожирают вас изнутри, заодно отравляя организм. В итоге, появляются многочисленные проблемы со здоровьем, сокращающие жизнь на 15-25 лет.
Основная ошибка — затягивание! Чем раньше начать выводить паразитов, тем лучше. Если же говорить о лекарствах, то тут всё проблематично. На сегодняшний день существует только один действительно эффективный антипаразитный комплекс, это Toximin. Он уничтожает и выметает из организма всех известных паразитов — от головного мозга и сердца до печени и кишечника. На такое не способен больше ни один из существующих сегодня препаратов.
В рамках Федеральной программы, при подаче заявки до 12 октября. (включительно) каждый житель РФ и СНГ может получить одну упаковку Toximin БЕСПЛАТНО!
Чтобы поставить диагноз, нужно выделить возбудителя или выявить его ДНК. Для исследования берут кровь, мокроту, околоплодные воды, больные ткани, соскобы из матки, цервикального канала, со слизистой оболочки влагалища, ректальный мазок и из зева.
Если есть подозрение на инфекцию на анализ берут биологический материал сразу нескольких видов. Как правило, у женщин, ждущих ребенка, бактерию обнаруживают в мазке из влагалища и ануса на сроке 34-36 недель.

Золотой стандарт диагностики – культуральный метод. Он выявляет бактерию за 4-5 дней. Метод полимеразной цепной реакции обнаруживает ДНК агалактий, но не позволяет проверить их реакцию на антибиотики.
Когда обследование на бактерию является обязательным:
- у роженицы ранее уже была диагностирована стрептококковая инфекция;
- обнаружение в моче беременной бактерий;
- время между отхождением вод и родами более 18 часов;
- у роженицы была температура выше 38.
В норме стрептококк агалактия может встречаться:
- в кишечнике 10 в 5-10 в 6 степени;
- в носоглотке 10 в 4 степени;
- у женщин во влагалище 10 в 4 степени;
- у мужчин в урогенитальных органах – норма отрицательный результат
- серологическое исследования крови результат отрицательный, то есть ДНК стрептококка в крови не обнаружено.
Превышающие эти цифры показатели говорят о развитии инфекции. При исследовании мазка у женщин необходимость лечения наступает при выявлении стрептококка в 10 в 5 степени КОЕ/мл. Необходимо лечить не только женщину, но ее полового партнера.
Лечение и профилактика
загрузка…
Существуют факторы риска, способствующие заражению бактерией новорожденных детей:
- возраст беременной менее 20 лет;
- рождение на сроке 28 и менее недель.
Стрептококки, в отличие от большинства других патогенных бактерий, очень плохо приспосабливаются к медикаментам. Поэтому они погибают от антибиотиков, к которым другие микроорганизмы давно приобрели резистентность.
Самые эффективные препараты для лечения инфекции по-прежнему – антибиотики пенициллинового ряда. Для лечения стрептококковых инфекций выписывают:
- Ампициллин;
- Линкомицин;
- Клиндамицин;
- Оксациллин.
Агалактия чувствительна также к препаратам с широким спектром действия:
- Тиенпенему;
- Секуропену;
- Пициллину.
Большинство штаммов агалактии устойчивы к тетрациклину, метронидазолу. Бактерии никак не реагируют на нистатин и антибиотики из групп полимиксины и аминогликозиды, поэтому популярные при лечении смешанных вагинитов и молочницы вагинальные свечи Полижинакс не помогут при стрептококковой инфекции.
Терапевтическия действия в родах
загрузка…
Давно решен вопрос, чем лечить стрептококк у беременных. Из-за того, что любые антибиотики отрицательно влияют на плод, женщине прокапывают лекарство непосредственно во время родов – для предотвращения инфицирования новорожденного.
Для исследования беременных женщин используют такие биологические материалы:
- вагинально-ректальный мазок;
- моча;
- кровь из вены.
Примерно у семи процентов беременных женщин стрептококки обнаруживаются в анализе мочи. Врачебная стратегия в этом случае предполагает использование антибиотиковой терапии в родах, чтобы предотвратить заражение при прохождении ребенка по родовым путям и избежать негативного воздействия лекарств на его внутриутробное развитие.
Отображается ли присутствие бактерий в анализе крови? Серологические тесты выявляют в плазме антитела к бактериям. По ним можно делать выводы о перенесенной или текущей стрептококковой инфекции.
Стрептококковая инфекция во время беременности:
У новорожденных для обнаружения агалактии исследуют:
- меконий;
- мазки из ротоглотки и ануса;
- при наличии признаков инфекции – кровь из вены;
- при подозрении на менингит – пробу спинномозговой жидкости.
Для профилактики стрептококковых инфекций, вызванных agalactiae, нужно поддерживать высокий общий уровень здоровья, соблюдать правила личной гигиены, не заниматься незащищенным сексом с непроверенными партнерами, поддерживать естественный иммунитет приемом витаминов и ведением здорового образа жизни.
загрузка…
otparazitoff.ru