Сравнительная характеристика некроза и апоптоза
Признак | Апоптоз | Некроз |
Индукция | Активируется физиологическими или патологическими стимулами | Различная в зависимости от повреждающего фактора |
Распространенность | Одиночная клетка | Группа клеток |
Биохимические изменения | Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. | Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. |
Распад ДНК | Внутриядерная конденсация с расщеплением на фрагменты | Диффузная локализация в некротизированной клетке |
Целостность клеточной мембраны | Сохранена | Нарушена |
Морфология | Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином | Набухание и лизис клеток |
Воспалительный ответ | Нет | Обычно есть |
Удаление погибших клеток | Поглощение (фагоцитоз) соседними клетками | Поглощение (фагоцитоз) нейтрофилами и макрофагами |
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез).
Гормон-зависимой инволюции органов у взрослых (отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации).
Возрастной и физиологической инволюции органов (тимус, атрофия мышц при длительном отсутствии нагрузки)
Гибели отдельных клеток в опухолях (в основном при ее регрессии, но также и в активно растущей опухоли).
Гибели клеток иммунной системы (В-, и Т-лимфоцитов, после истощения запасов цитокинов, гибели аутореактивных Т-клеток при развитии в тимусе).
Патологической атрофии гормон – зависимых органов (атрофии предстательной железы после кастрации, истощении лимфоцитов в тимусе при терапии глюкокортикоидами).
Гибели клеток, вызванных действием цитотоксических Т-клеток (при отторжении трансплантата, болезни “трансплантат против хозяина”).
Повреждении клеток при некоторых вирусных заболеваниях (при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени – тельца Каунсильмана).
Регуляция апоптоза
Как уже отмечалось, апоптоз это генетически контролируемая смерть клетки. В настоящее время выявлено большое число генов, которые кодируют вещества, необходимые для регуляции апоптоза. Многие из этих генов сохранились в ходе эволюции — от круглых червей до насекомых и млекопитающих. Некоторые из них обнаруживаются также в геноме вирусов. Таким образом, основные биохимические процессы апоптоза в разных экспериментальных системах (исследования ведутся на круглых червях и мухах) являются идентичными, поэтому результаты исследований можно прямо переносить на другие системы (например, организм человека).Воздействие внешних факторов. Апоптоз может регулироваться действием многих внешних факторов, которые ведут к повреждению ДНК. При невосстановимом повреждении ДНК путем апоптоза происходит элиминация потенциально опасных для организма клеток. В данном процессе большую роль играет ген супрессии опухолей р53. К активации апоптоза приводят вирусные инфекции, нарушение регуляции клеточного роста, повреждение клетки и потеря контакта с окружающими или основным веществом ткани. Апоптоз – это защита организма от персистенции поврежденных клеток, которые могут оказаться потенциально опасными для многоклеточного организма.
Ингибиторы апоптоза:факторы роста, клеточный матрикс, некоторые интерлейкины (например IL-lβ), для эндокринных желез тропные гормоны, для ряда клеток организма половые гормоны, недостаток тироксина, некоторые вирусные белки;
Активаторы апоптоза: недостаток факторов роста, недостаток тропных гормонов, потеря связи с матриксом, глюкокортикоиды, повышенная секреция тироксина, фактор некроза опухоли α, FAS-лиганды, некоторые вирусы, свободные радикалы, ионизирующая радиация.
При воздействии активаторов или отсутствии ингибиторов происходит активация эндогенных протеаз и эндонуклеаз. Это приводит к разрушению цитоскелета, фрагментации ДНК и нарушению функционирования митохондрий. Клетка сморщивается, но клеточная мембрана остается интактной, однако повреждение ее приводит к активации фагоцитоза. Погибшие клетки распадаются на апоптотические тельца. Воспалительная реакция на апоптотические клетки не возникает
Автономный механизм апоптоза. При развитии эмбриона различают три категории автономного апоптоза: морфогенетический, гистогенетический и филогенетический.
Морфогенетический апоптоз участвует в разрушении различных тканевых зачатков: разрушение клеток в межпальцевых промежутках; гибель клеток приводит к разрушению избыточного эпителия при слиянии небных отростков, когда формируется твердое небо; гибель клеток в дорсальной части нервной трубки во время смыкания. Нарушение морфогенетического апоптоза в этих трех локализациях приводят к развитию синдактилии, расщеплению твердого неба и spina bifida.
Гистогенетический апоптоз
Филогенетический апоптоз участвует в удалении рудиментарных структур у эмбриона (например, пронефроса).
Все факторы, усиливающие или ослабляющие апоптоз, могут действовать: прямо на механизм гибели клетки, опосредованно, путем влияния на регуляцию транскрипции.
В некоторых случаях влияние этих факторов на апоптоз является решающим (например, при глюкокортикоид-зависимом апоптозе тимоцитов), а в других не имеет особой важности (например, при Fas- и ФНО-зависимом апоптозе).
В процессе регуляции принимает участие большое количество веществ.
Наиболее изученными из них являются белок p53 и белки из семейства bcl-2.
р53является одним из наиболее мощных регуляторов апоптоза. Активируясь в ответ на самые разные неблагоприятные воздействия (повреждения ДНК, гипоксия, потеря контактов клетки с субстратом, перманентная нерегулируемая стимуляция митогенного сигнала и многие другие, р53 осуществляет на транскрипционном уровне одновременно и активацию генаBах, и репрессию генаBс12. Кроме того, р53 повышает экспрессию ряда геновPIG, продукты которых вызывают оксидативный стресс и, как следствие, нарушения проницаемости митохондриальной и ядерной мембран, а также трансактивирует некоторые киллерные рецепторы, в частностиFasиKILLER/DR5. Таким образом, активация р53 дает мощный апоптогенный сигнал, в реализации которого задействованы различные механизмы индукции «казнящих» каспаз. Важно подчеркнуть, что р53-зависимый апоптоз элиминирует из организма не только поврежденные клетки, но и клетки, в которых наблюдается нерегулируемая стимуляция пролиферации, вызываемая, например, конститутивной активацией онкогена МYС и/или транскрипционного фактораE2F. Стабилизация р53 при активации онкогенов связана с индуцируемымE2Fповышением транскрипции генаpl9ARF, продукт которого препятствует Мdm2-зависимой деградации р53. Естественно, что инактивирующие мутации р53 илиpl9ARF, нарушающие работу этого защитного механизма, будут резко увеличивать вероятность появления постоянно пролиферирующих клеточных клонов, а, следовательно, и вероятность последующего развития из них злокачественных опухолей.
До последнего времени считалось, что нерепарируемые повреждения ДНК приводят клетку к гибели в результате нарушения функций всех биохимических систем из-за невозможности полноценной транскрипции генов, содержащих дефекты в матрице ДНК, Исследования последних лет привели к формированию принципиально новых представлений о механизме гибели клеток, имеющих повреждения ДНК, как о процессе, осуществляемом в соответствии с определенной генетической программой. В индукции этой программы при наличии повреждений в ДНК клетки важная роль принадлежит белку р53. Этот белок с молекулярной массой 53 кД локализован в ядре клетки и является одним из транскрипционных факторов, повышенная экспрессия которого приводит к репрессии ряда генов, регулирующих транскрипцию и причастных к задержке клеток в фазе клеточного цикла G1. При повреждении ДНК под действием ионизирующего излучения или УФ-излучения, ингибиторов топоизомеразыII, гипоксия, потеря контактов клетки с субстратом, перманентная нерегулируемая стимуляция митогенного сигнала и некоторых других воздействиях происходит активация экспрессии гена р53. Блок клеточного цикла в фазахG1 иOF2 до репликации ДНК и митоза, соответственно, делает возможной репарацию поврежденной ДНК и предотвращает тем самым появление мутантных клеток. Если нее активность репарационных систем недостаточна и повреждения ДНК сохраняются, то в таких клетках индуцируется программируемая клеточная гибель, или апоптоз, что приводит к защите организма от присутствия клеток с поврежденной ДНК, т.е. мутантных и способных к злокачественной трансформации.
Так карбоксильный конец белка р53 может неспецифически связываться с концами молекул ДНК и катализировать ренатурацию и перенос нитей. На уровне транскрипции белок р53 трансактивирует гены, участвующие в блокаде клеточного цикла — p2lwari(ингибитор большинства циклинзависимых киназ) и взаимодействует либо с комплексами, определяющими синтез и репарацию ДНК, либо с белками, модулирующими апоптоз (Вах,Fas). Кроме перечисленных механизмов, белок р53 может ингибировать синтез ДНК по независимым от транскрипции механизмам, связываясь с ДНК и предотвращая инициацию репликации или образование репликационной вилки либо образуя комплексы белок — белок с белками, участвующими в синтезе ДНК, репарации ДНК и в апоптозе (рис. 2.3).
р53 осуществляет на транскрипционном уровне одновременно и активацию гена Bах, и репрессию генаBс12. Кроме того, р53 повышает экспрессию ряда геновPIG, продукты которых вызывают оксидативный стресс и, как следствие, нарушения проницаемости митохондриальной и ядерной мембран, а также трансактивирует некоторые киллерные рецепторы, в частностиFasиKILLER/DR5. Таким образом, активация р53 дает мощный апоптогенный сигнал, в реализации которого задействованы различные механизмы индукции «казнящих» каспаз. Важно подчеркнуть, что р53-зависимый апоптоз элиминирует из организма не только поврежденные клетки, но и клетки, в которых наблюдается нерегулируемая стимуляция пролиферации, вызываемая, например, конститутивной активацией онкогена МYС и/или транскрипционного фактораE2F. Стабилизация р53 при активации онкогенов связана с индуцируемымE2Fповышением транскрипции генаpl9ARF, продукт которого препятствует Мdm2-зависимой деградации р53. Естественно, что инактивирующие мутации р53 илиpl9ARF, нарушающие работу этого защитного механизма, будут резко увеличивать вероятность появления постоянно пролиферирующих клеточных клонов, а, следовательно, и вероятность последующего развития из них злокачественных опухолей.
Таким образом, при действии генотоксических агентов р53 не только увеличивает время репарации ДНК, но также защищает организм от клеток с опасными мутациями. Блокирование процесса апоптоза, происходящее на разных стадиях канцерогенеза, приводит к снижению способности трансформированных клеток активировать программу клеточной гибели, что определяет прогрессию опухолевого заболевания.
Bcl-2 ген впервые был описан как ген, который транслоцируется в клетках фолликулярной лимфомы и ингибирует апоптоз. При дальнейших исследованиях оказалось, что Bcl-2 является мультигеном, который обнаруживается даже у круглых червей. Гомологичные гены были также обнаружены в некоторых вирусах. Все вещества, относящиеся к данному классу делятся на активаторы и ингибиторы апоптоза.
К ингибиторам относятся: bcl-2, bcl-xL, Mcl-1, bcl-w, аденовирусный E1B 19K, Эпштейн-Барр-вирусный BHRF1.
К активаторам относятся bax, bak, Nbk/Bik1, Bad, bcl-xS.
Члены этого семейства взаимодействуют друг с другом. Одним из уровней регуляции апоптоза является взаимодействие белок-белок. Белки семейства bcl-2 формируют как гомо- так и гетеродимеры. Например, bcl-2-ингибиторы могут образовать димеры bcl-2-активаторами. Таким образом, жизнеспособность клеток зависит от соотношения активаторов и ингибиторов апоптоза. Например, bcl-2 взаимодействует с bax; при преобладании первого жизнеспособность клетки повышается, при избытке второго – уменьшается. К тому же белки семейства bcl-2 могут взаимодействовать с белками, не относящимися к этой системе. Например, bcl-2 может соединятся с R-ras, который активирует апоптоз. Другой белок, Bag-1, усиливает способность bcl-2 ингибировать апоптоз.
В настоящее время принято считать, что гены, участвующие в регуляции роста и развития опухолей (онкогены и гены-супрессоры опухолей), играют регулирующую роль в индукции апоптоза. К ним относятся:
Bcl-2 онкоген, который ингибирует апоптоз, вызванный гормонами и цитокинами, что приводит к повышению жизнеспособности клетки;
Белок bax формирует димеры bax-bax, которые усиливают действие активаторов апоптоза. Отношение bcl-2 и bax определяет чувствительность клеток к апоптотическим факторам и является “молекулярным переключателем”, который определяет, будет ли происходить рост или атрофия ткани.
c-myc онкоген, чей белковый продукт может стимулировать либо апоптоз, либо рост клеток (при наличии других сигналов выживания, например, bcl-2).
Ген р53, который в норме активирует апоптоз, но при мутации или отсутствии (что обнаружено в некоторых опухолях) повышает выживаемость клеток. Установлено, что р53 необходим для апоптоза при повреждении клетки ионизирующим излучением, однако при апоптозе, вызванном глюкокортикоидами и при старении, он не требуется.
Значение белков-регуляторов апоптоза в развитии организма и патологических процессах
Вcl-2 требуется для поддержания жизнеспособности лимфоцитов, меланоцитов, эпителия кишечника и клеток почек во время развития эмбриона.
Вcl-x необходим для ингибирования смерти клеток в эмбриогенезе, особенно в нервной системе.
Bax необходим для апоптоза тимоцитов и поддержания жизнеспособности сперматозоидов во время их развития.
р53 является геном супрессии опухолей, поэтому в эмбриогенезе особой роли не играет, но обязательно необходим для супрессии опухолевого роста.
Усиленный синтез белка, кодируемого bcl-2 геном, приводит к подавлению апоптоза и, соответственно, развитию опухолей; данный феномен обнаружен в клетках В-клеточной фолликулярной лимфомы.
При лимфопролиферативных заболеваниях и похожей на системную красную волчанку болезни у мышей наблюдается нарушение функции Fas-лиганда или Fas-рецептора.
Повышенный синтез Fas-лиганда предупреждает отторжение трансплантата.
Апоптоз является частью патологического процесса при инфицировании клетки аденовирусами, бакуловирусами, ВИЧ и вирусами гриппа.
Ингибирование апоптоза в клетке-хозяине наблюдается при персистировании инфекции, в латентном периоде, а при усиленной репликации аденовирусов, бакуловирусов, возможно герпесвирусов, вируса Эпштейн-Барра и ВИЧ наблюдается активация апоптоза в клетках иммунной системы, что способствует распространению вируса.
studfiles.net
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА НЕКРОЗА И АПОПТОЗА — КиберПедия
Тема 9. АПОПТОЗ
Апоптоз — программированная клеточная гибель, генетически контролируемый процесс, который запускается специфическими сигналами и избавляет организм от ослабленных, ненужных или повреждённых клеток.
Апоптоз – это биохимически специфический тип гибели клетки, который характеризуется активацией нелизосомных эндогенных эндонуклеаз, которые расщепляют ядерную ДНК на маленькие фрагменты. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые тут же фагоцитируются окружающими клетками.
Посредством апоптоза удаляются нежелательные и дефектные клетки организма. При снижении апоптоза происходит накопление клеток, пример – опухолевый рост. При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани, пример – атрофия.
Апоптоз – в отличие от некроза – никогда не сопровождается воспалительной реакцией.
Погибшая клетка при апаптозе, т.е. ее фрагменты– апоптосомомыпоглощаются соседними клетками.
Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, которые выглядят относительно нормальными, располагаются более компактно.
СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА НЕКРОЗА И АПОПТОЗА
| Признак | Апоптоз | Некроз |
| Индукция | Активируется физиологическими или патологическими стимулами | Различная в зависимости от повреждающего фактора |
| Распространенность | Одиночная клетка | Группа клеток |
| Биохимические изменения | Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. | Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты |
| Распад ДНК | Внутриядерная конденсация с расщеплением на фрагменты | Диффузная локализация в некротизированной клетке |
| Целостность клеточной мембраны | Сохранена | Нарушена |
| Морфология | Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином | Набухание и лизис клеток |
| Воспалительный ответ | Нет | Обычно есть |
| Удаление погибших клеток | Поглощение (фагоцитоз) соседними клетками | Поглощение (фагоцитоз) нейтрофилами и макрофагами |
ПОСЛЕДОВАТЕЛЬНОСТЬ УЛЬТРАСТРУКТУРНЫХ ИЗМЕНЕНИЙ ПРИ АПОПТОЗЕ (СПРАВА) И НЕКРОЗЕ (СЛЕВА)
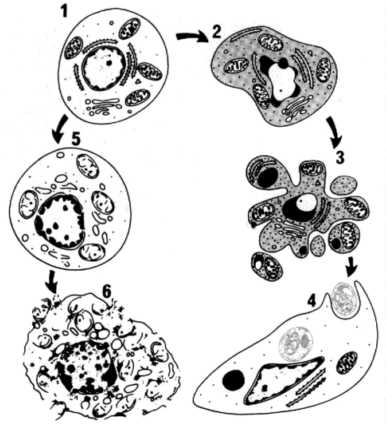
1– нормальная клетка; 2 – начало апоптоза; 3 – фрагментация апоптотической клетки; 4 – фагоцитоз апоптотических телец окружающими клетками; 5 – гибель внутриклеточных структур при некрозе; 6 – разрушение клеточной мембраны
Предполагается, что нарушение формы и объема клетки происходит в результате активации в апоптотических клетках трансглютаминазы. Этот фермент вызывает прогрессивное образование перекрестных связей в цитоплазматических белках, что приводит к формированию своеобразной оболочки под клеточной мембраной, подобно ороговевающим клеткам эпителия.
Механизм апоптоза
TNF-αи Fas-L (CD178) запускают каскад биохимических реакций, финальным этапом которых является дефрагментация хромосом и гибель клетки. На поверхности клеток организма имеются специальные рецепторы для TNF-α, это TNF-RI и TNF-RII, а для Fas-лиганда рецептор Fas/APO-1 CD95).
TNF-R и Fas/APO-1(CD95) имеют гомологию в экстрацеллюлярных доменах части рецептора.
Связывание TNF-α и Fas-лигандов с рецепторами апоптоза активирует интрацеллюлярные «домены смерти» (DED — death effector domain) этих рецепторов: DED, DED1 и DED2 приводит к активации
— каспаз(3,6,7,8,9)высвобождающие измитохондрий цитохром C — Bax проапоптозных белков (ингибиторов Bсl-антиапоптозныхбелков) — протеаз ICE/CED-3семейства
Периферическое деление Т-клеток инициирует взаимодействие либо Fas рецептора с его лигандом (FasL), либо ФНО с рецептором ФНО.
Последующая цепь передачи сигналов активирует ИЛ-1β-конвертируюшие ферментоподобные протеазы (ICE, от англ. IL-1β converting enzymelike proteases), которые опосредуют запрограммированную клеточную гибель (апоптоз).
В свою очередь активные ICE начинают взаимодействовать с рядом внутриклеточных субстратов: —поли-(АДФ-рибозо)полимеразой (PARP), участвующей в репарации ДНК и модификации активности некоторых ядерных белков, —ламином В1, —топоизомеразой I -и Р-актином.
Все члены семейства ICE/CED-3 протеаз расщепляют субстраты. Специфическое расщепление PARP, ламина В1, топоизомеразы I и Р-актина под действием ICE-подобных протеаз на большие и малые фрагменты приводит клетку к гибели, так как большие фрагменты этих субстратов и являются активными нуклеазами, которые разрезают хромосомы на фрагменты. Активация протеаз ICE/CED-3 семейства может происходить и под действием фосфолипидов, например, церамидов.
Свободный сфингозин образуемый из церамидов в результате его гидролиза церамидазой так же активирует ICE-подобные протеазы и ускоряет апоптоз.
Тироксин
Важная роль в осуществлении апоптоза принадлежит тироксину (Т4).
Он регулирует функционирование протеиновой тирозинкиназы, важного элемента реализации сигнала смерти. При недостатке этого гормона щитовидной железы происходит подавление апоптоза.
IL-lβ блокирует апоптоз. ICE-подобные протеазы взаимодействуют с IL-lβ, а не с PARP, ламином В1, топоизомеразой I и Р-актином. В результате чего не происходит образования активных нуклеаз, и клетка избегает апоптоза.
На взаимодействие TNF-α и Fas-лигандов с TNF-R и Fas/APO-1(CD95) и проведение апоптотического сигнала оказывают влияние Bclи Bax белки.
Так белки Bcl семейства: Bcl-2, Bcl-xL и Bcl-xS блокируют выход цитохрома-С из митохондрий и таким образом предотвращают превращение про-каспазы-9 в активную форму, отменяют атоптотический сигнал.
Bcl белки регулируют проницаемость мембран митохондрий, предотвращают выход цитохрома-С, ингибируют каспазы.
Bcl-2 ген впервые был описан как ген, который транслоцируется в клетках фолликулярной лимфомы и ингибирует апоптоз
В свою очередь Bax белки способствуют выходу цитохрома С из митохондрий и образованию активной каспазы-9, которая инициирует продолжение и активацию апоптотическог каскада, начавшегося с присоединения TNF-α или Fas-лигандов к TNF-R и Fas/APO-1(CD95).
Быть или не быть апоптозу зависит от соотношения Bcl и Bax белков в митохондриях: —— преобладание экспрессии белков Bcl семейства блокирует запуск апоптоза, — а преобладание экспрессии Baxбелков способствует реализации сигнала смерти.
Регуляция апоптоза
Апоптоз может регулироваться:
1. внешними факторами,
2. автономными механизмами.
Снижение апоптоза
Продукт р53 гена следит за целостностью генома при митозе. При нарушении целостности генома клетка переключается на апоптоз. Наоборот, белок bcl-2 ингибирует апоптоз. Таким образом, недостаток р53 или избыток bcl-2 приводит к накоплению клеток: эти нарушения наблюдаются в различных опухолях. Изучение факторов регулирующих апоптоз имеет важное значение в разработке лекарственных препаратов, усиливающих гибель клеток злокачественных новообразований.
Аутоиммунные заболевания могут отражать нарушения в индукции апоптоза лимфоидных клеток, способных реагировать с собственными антигенами. Например, при системной красной волчанке наблюдается нарушение Fas-рецепторов на клеточной поверхности лимфоцитов, что ведет к активации апоптоза. Некоторые вирусы повышают свою выживаемость путем ингибирования апоптоза инфицированных клеток, например, вирус Эпштейна-Барра может воздействовать на обмен bcl-2.
Ускорение апоптоза
Ускорение апоптоза доказано при синдроме приобретенного иммунодефицита (СПИД), нейротрофических заболеваниях и некоторых заболеваниях крови, при которых наблюдается дефицит каких-либо форменных элементов.
Иммунитет к вирусам
Все вирусы являются облигатными внутриклеточными патогенами. Защита организма от вирусных инфекций направлена в первую очередь на замедление репликации вируса, а затем на устранение инфекции.
Ответом на вирусы может быть
-выработка интерферона,
-антительный ответ
-и клеточно-опосредованный иммунитет.
Важным начальным механизмом зашиты является выработка интерферонов различных типов, таких как
-IFNα — лейкоцитами,
-IFNβ — фибробластами
-и IFNβ — Т- и NK-клетками.
Интерфероны являются противовирусными белками или гликопротеинами, вырабатываемыми многими типами клеток организма млекопитающих в ответ на вирусную инфекцию (или другие индукторы, такие как двухцепочечная РНК).
Интерфероны выступают в качестве раннего защитного механизма.
Вырабатываемые инфицированными клетками IFNα и IFNβ перемещаются к соседним клеткам и активируют гены, которые препятствуют репликации вируса.
Эти интерфероны также стимулируют продукцию молекул МНС I класса и протеозомных белков, которые увеличивают способность инфицированных вирусами клеток презентировать пептиды вирусов Т-клеткам.
ПРОТЕАСО́МА (от англ. protease — протеиназа и лат. soma — тело) — очень крупная мультисубъединичная протеаза, присутствующая в клетках эукариот, архей и некоторых бактерий.
В эукариотических клетках протеасомы содержатся и в ядре, и в цитоплазме.
Основная функция протеасомы — протеолитическая деградация ненужных и повреждённых белков до коротких пептидов (4—25 аминокислотных остатков), которые затем могут быть расщеплены до отдельных аминокислот.
Более того, IFNα и IFNβ активируют NK-клетки, которые распознают и убивают инфицированные вирусом клетки организма, уменьшая таким образом продукцию вирусов.
Натуральные киллеры характеризуются способностью убивать определенные клетки опухолей in vitro без предварительной сенсибилизации и обеспечивают раннюю защиту клеток от вирусов.
Позднее в процессе инфекции, когда становятся доступными антитела к вирусным антигенам, NK-клетки могут устранять клетки организма, инфицированные вирусами, посредством антителозависимой клеточно-опосредованной цитотоксичности(АЗКЦ).
Они также продуцируют IFNγ — сильный активатор макрофагов, который помогает примировать иммунную систему к выработке адаптивных иммунных ответов.
Белки системы комплемента повреждают оболочку некоторых вирусов, обеспечивая определенную степень защиты при ряде вирусных инфекций.
Гуморальный ответ приводит к выработке антител к вирусным белкам.
Некоторые антитела могут предотвращать проникновение вирусов в другие клетки.
Такие антитела называют нейтрализующими.
Из них наиболее активным изотипом противовирусных антител является IgG.
Опсонизация представляет собой конвергенцию гуморального и клеточного механизмов иммунитета.
Соединившись посредством своего Fab-фрагмента с вирусным антигеном на поверхности инфицированной клетки, IgG соединяется также с Fc-рецепторами клеток некоторых популяций, таких как NK-клетки, макрофаги и ПМЯ клетки(полиморфно ядерные).
Эти клетки могут фагоцитировать и/или повреждать инфицированную вирусом клетку (АЗКЦ).
Антитела к белкам вируса могут предотвращать инфекцию, вмешиваясь в процесс прикрепления вируса к клетке организма.
Выработка секреторного IgA может защитить организм, предотвращая инфицирование эпителиальных клеток слизистых поверхностей.
Антитела также могут вмешиваться в развитие вирусной инфекции путем агглютинации вирусных частиц, а также активируя комплемент на поверхности вирусов и способствуя фагоцитозу вирусных частиц макрофагами.
Ответ со стороны антител призван ограничить распространение вирусов и способствовать разрушению инфицированных клеток организма посредством АЗКЦ.
Таким образом, эффективный ответ со стороны антител на вирусы включает выработку антител, которые:
• нейтрализуют (или препятствуют проявлению) способность к инфицированию вирусом чувствительных клеток организма;
• фиксируют комплемент и способствуют повреждению комплементом вирионов;
• ингибируют ферменты вируса;
• способствуют опсонизации вирусных частиц;
• способствуют АЗКЦ клеток, инфицированных вирусами.
Инфицирование эпителия респираторного тракта вирусом гриппа ведет к его размножению в эпителиальных клетках и распространению на прилежащие клетки эпителия.
Соответствующий и достаточный иммунный ответ будет включать действие антител на поверхности эпителия.
Это действие может осуществляться посредством секреции в данном месте IgA или экстравазации IgG или IgM.
Однако некоторые вирусные заболевания, такие как корь и полиомиелит, начинаются с инфицирования эпителия слизистых оболочек (респираторного или кишечного тракта соответственно), но основные патогенетические эффекты проявляются после гематогенного распространения и достижения других тканей-мишеней.
Антитела, находящееся на поверхности эпителия, могут защищать от вируса, но то же самое могут сделать и антитела, циркулирующие в крови.
Однако как только вирус прикрепляется к клетке, он обычно не может быть вытеснен антителом.
Таким образом, эффективный ответ со стороны антител обычно бывает недостаточным для устранения вирусной инфекции, особенно когда вирус расположен внутри клеток организма.
Для устранения развившейся вирусной инфекции обычно требуется эффективный клеточно-опосредованный ответ специфическими CD4+— и CD8+-Т-клетками.
CD4+-Т-клетки вырабатывают важные цитокины, стимулирующие воспалительные реакции в местах вирусной инфекции и активирующие функцию макрофагов.
Цитотоксические CD8+-Т-клетки (цитотоксические Т-лимфоциты — ЦТЛ) являются основными эффекторными клетками в противовирусных реакциях. CD8+-T-клетки могут распознавать вирусные антигены в составе молекул МНС I класса и убивать клетки организма, содержащие вирусы.
Поскольку молекулы МНС I класса экспрессируются большинством типов клеток организма, CD8+-Т-клетки могут распознавать многие типы инфицированных клеток.
Однако при некоторых инфекциях, вызванных нецитопатическими вирусами, такими как вирус гепатита В, CD8+-Т-клетки могут вызывать повреждение ткани.
Нецитопатические Вирусы — вирусы с низкой репликативной активностью и наличием мутаций в вирусном геноме, приводящие к нарушению синтеза вирусных антигенов и к подавлению их экспрессии.
Поэтому хроническая инфекция, вызванная вирусом гепатита В, может привести к развитию хронического воспаления и повреждению клеток печени, что вызывает фиброз и прогрессирующую недостаточность органа.
Иммунитет к бактериям
Защита организма от бактериальных патогенов достигается посредством различных механизмов, включающих как гуморальный, так и клеточный иммунитет.
Антибактериальная защита включает лизис бактерий посредством антител и комплемента, опсонизацию и фагоцитоз с последующим удалением фагоцитированных бактерий печенью, селезенкой и другими компонентами ретикуло-эндотелиальной системы.
Бактерии и их продукты эндоцитируются АПК, такими как макрофаги и дендритные клетки, и процессируются.
Пептиды, получающиеся в результате такого процессирования, презентируются T-клетками в молекулах МНС II класса.
Этот процесс усиливает ответ организма, поскольку Т-клетки вырабатывают цитокины, активирующие макрофаги и привлекающие дополнительные воспалительные клетки.
Бактериальные патогены в зависимости от состава их клеточных стенок и мембран можно условно разделить на четыре класса:
—громположительные,
-грамотрицательные,
-микобактерии
—и спирохеты.
Некоторые грамположительные и грамотрицательные бактерии создают полисахаридные капсулы.
Другой важной характеристикой бактериальных патогенов является их принадлежность к внутриклеточнымили внеклеточнымпатогенам.
Грамположительные бактерии
Грамположительные бактерии имеют плотную клеточную стенку, состоящую из сложного перекрестно соединенного пептидогликана, позволяющего бактериям окрашиваться кристаллическим фиолетовым (отсюда название «грамположительные»).
Кроме толстого слоя пептидогликана клеточная стенка грамположительных бактерий содержит тейхоивые кислоты, углеводороды и белки.
Тейхоевые кислотыиммуногенны и составляют основные антигенные детерминанты грамположительных бактерий.
ТЕЙХОЕВЫЕ КИСЛОТЫ (от греч. τειχος, «стена») — линейные углеводные фосфатсодержащие гетерополимеры.
Этот тип клеточной стенки обеспечивает их толстым защитным слоем, который делает бактерии резистентными к лизису системой комплемента.
В защите против грамположительных бактерий участвуют специфические антитела,ответственные за обеспечение опсонинами и фагоцитирующими клетками, такими как нейтрофилы и макрофаги.
Они захватывают и разрушают бактерии.
Опсонизацияи фагоцитозсвязаны с действием IgG и IgM, как самостоятельным, так и совместным с СЗb.
Альтернативный путь активации комплемента может запускаться непосредственно бактериальной стенкой грамположительного возбудителя и приводить к депонированию опсонинов комплемента на поверхности клетки, а также выработке медиаторов воспалительной реакции.
Хотя система комплемента и непосредственно не участвует в лизисе грамположительных бактерий, она обеспечивает появление опсонинов и медиаторов воспаления, которые играют основную роль в защите организма.
Грамотрицательные бактерии
Грамотрицательные бактерии не окрашиваются кристаллическим фиолетовым.
Слоистая структура их клеточной стенки состоит из наружной и внутренней мембран, разделенных тонким слоем пептидогликана в периплазматическом пространстве.
Таким образом, грамположительные и грамотрицательные бактерии сильно отличаются по структуре клеточной стенки.
Наружная мембрана грамотрицательной бактерии содержит липополисоха-рид(ЛПС), известный так же как эндотоксин.
Полисахаридная часть ЛПС обладает антигенными детерминантами, которые обусловливают антигенную специфичность.
Многие штаммы грамотрицательных бактерий содержат варианты с различными структурами ЛПС, которые серологически могут быть определены как серотипы.
Для человека ЛПС является сильным токсином и может вызвать
-сердечно-сосудистый коллапс,
-гипотензию и шок в период инфекции, вызванной грамотрицательными бактериями.
Альтернативный путь комплемента может быть активирован непосредственно ЛПС, находящимся на стенке грамотрицательной бактерии или на ее полисахаридной капсуле, действующей на СЗ.
Активация альтернативного пути ведет к выработке хемотаксических молекул СЗа и С5а, а также опсонина СЗb, что может привести к бактериологическому действию со стороны мембраноатакующего комплекса С5 — С9. Способность системы комплемента лизировать некоторые грамотрицательные бактерии напрямую является важным отличием от грамположительных бактерий, которые невосприимчивы к опосредованному комплементом лизису благодаря толстому слою пептидогликана.
Защиту от грамотрицательных бактерий обеспечивают
—система комплемента,
-специфические антитела
—и фагоцитирующие клетки.
Микобактерии
Стенки микобактерии отличаются от стенок грамположительных и грамотрицательных бактерий.
Они характеризуются высоким содержанием липида, который затрудняет окрашивание бактерий.
Другим свойством стенки микобактерии является кислотоустойчивость, которая позволяет им удерживать краситель после обработки кислотой.
Растут микобактерии медленно.
Они обладают гидрофобными поверхностями, что обусловливает их скопление в группы.
Компоненты микобактериальных стенок в период инфекции вызывают сильные иммунные ответы, такие как реакции гиперчувствительности замедленного типа(ГЗТ), которые и дают основание для проведения туберкулинового теста.
Реакции гиперчувствительности на белки микобактерии могут быть вовлечены в патогенез микобактериальных инфекций.
Микобактерии вызывают сильный антительный ответ, хотя роль гуморального иммунитета в защите от микобактерии не определена.
Основными механизмами зашиты от микобактерии являются макрофагии клеточно-опосредованный иммунитет.
Спирохеты
Спирохеты являются спиралевидными микроорганизмами.
К их числу принадлежат возбудители сифилиса (Treponema pallidum) и болезни Лайма (Borrelia burgdorferi).
Спирохеты не обладают такими стенками, как грамположительные, грамот-рицательные бактерии и микобактерии.
Вместо этого у них есть тонкая наружная мембрана, содержащая небольшое число белков.
В защите организма от спирохет важную роль играют
—комплемент,
-специфические антитела
—и клеточно-опосредованный иммунитет.
Иммунитет к паразитам
К паразитам относится разнородная группа патогенов, таких как одноклеточные простейшиеи гельминты.
Многие паразиты характеризуются разнообразием тканевых стадий, которые могут различаться по клеточному расположению и антигенному составу, создавая, таким образом, серьезную проблему для иммунной системы.
Разнообразие паразитов таково, что обобщения относительно эффективных механизмов зашиты от них организма сделать трудно.
Однако ясно, что врожденныеи адаптивные механизмы чрезвычай-
но важны для защиты от паразитарных инфекций.
Некоторые паразиты являются простейшими одноклеточными эукариотами, которые могут существовать как в метаболически активной форме, называемой трофозоитом, так и в неактивной тканевой форме, известной как циста. Среди заболеваний, вызванных простейшими, можно назвать
-амебиаз,
-малярию,
-лейшманиоз.
-трипаносомоз
-и токсоплазмоз.
Защита от простейших осуществляется такими механизмами, как врожденный и адаптивный гуморальный и клеточный иммунитет, однако их относительная важность может изменяться в зависимости от конкретного патогена.
Некоторые паразиты из простейших, например трипаносомы, способны активировать систему комплемента по альтернативному пути.
Активация комплементавместе с фагоцитозом, осуществляемым нейтрофилами и макрофагами (компонентами врожденной иммунной системы), обеспечивает существенную степень зашиты от многих паразитарных патогенов.
Для многих протозойных(т.е простейшими) инфекций, таких как амебиаз, малярия и трипаносомоз, гуморальный иммунитет в форме антител опосредует защиту от инфекции.
Однако для остальных протозойных инфекций, таких как лейшманиоз и токсоплазмоз, более важен клеточный иммунитет.
Другими паразитами являются многоклеточные черви, называемые гельминтами.
В отличие от других патогенных микроорганизмов гельминты являются крупными макроскопическими организмами величиной от 1 см до 10 м.
Это является особой проблемой для защитных сил организма.
Для борьбы с гельминтозами необходимо сложное взаимодействие между тканевыми и иммунными реакциями.
Существует общее мнение, что такие компоненты врожденной иммунной системы, как эозинофилыи тучные клетки,являются важными эффекторными клетками для борьбы с гельминтами, но многие аспекты реакции организма на червей остаются тайной.
Считается, что IgE, специфичный к антигенам гельминта, играет важную роль в защите организма, примируя эозинофилы к АЗКЦ.
Гельминтозы часто сопровождаются повышенным содержанием эозинофилов в крови и IgE в сыворотке крови.
ЗАЩИТНАЯ РОЛЬ IgE
Защитные эффекты аллергических реакций можно наблюдать в тех случаях, когда сенсибилизирующий антиген является производным многочисленных червей-паразитов, таких как гельминты.
Иммунный ответ на присутствие гельминтов способствует стимуляции IgE.
В результате перекрестного связывания антигенов паразита IgE, фиксированным на поверхности тучных клеток (и эозинофилов), высвобождаются гистамин и другие медиаторы, участвующие в анафилактической реакции.
В результате увеличения проницаемости, вызванной высвобождением гистамина, к месту заражения паразитами поступают компоненты сыворотки крови, содержащие в том числе антитела IgG.
Эти антитела прикрепляются к поверхности гельминта.
Затем эозинофилы прикрепляются к гельминтам, покрытым IgG, посредством своих мембранных рецепторов к Fc-фрагментам и высвобождают содержимое своих гранул.
Как указывалось ранее, эозинофилы также экспрессируют низкоаффинные Fc-рецепторы к IgE, которые способствуют связыванию этих клеток с гельминтами, покрытыми IgE.
Основной составляющей содержимого гранул, высвобождаемых эозинофилами, является ГОБ, который покрывает поверхность гельминта и приводит, пока еще неизвестно, каким образом, к гибели паразита и его последующему выведению из организма.
ГОБ главный основной (щелочной) белок, т.е. катионный белок.
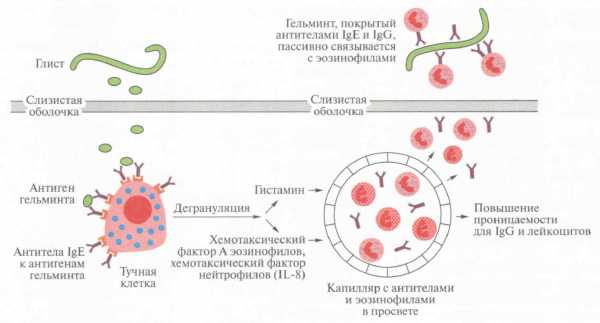 |
| Повреждение гельминта эозинофилами, мигрировавшими в участок поражения и активированными после дегрануляции тучных клеток, опосредованной IgE и антигенами Р. Койко и др., ИММУНОЛОГИЯ, «АКАДЕМИЯ», 2008. |
Иммунитет к грибам
Грибковые патогены являются эукариотами, которые могут вызывать тяжелые инфекции в основном у индивидуумов с нарушениями иммунитета.
Грибы вызывают повреждение ткани, вырабатывая протеолитические ферменты и инициируя воспалительные реакции.
Наиболее распространенным грибковым патогеном является Candida albicans.
Этот организм обычно является безвредным комменсалом(нахлебником), но может вызывать заболевания, когда обычные механизмы защиты нарушены, как, например, при нарушении целостности кожных покровов при хирургическом вмешательстве или катетеризации.
В другую группу риска по развитию тяжелых заболеваний, вызванных С. albicans, входят лица с транзиторным истощением нейтрофилов, вызванным проводимой химиотерапией.
Тот факт, что условием для развития большинства тяжелых кандидозных инфекций является нарушение целостности кожных покровов или истощение нейтрофилов, указывает на основную роль врожденных механизмов защитыв предотвращении системных заболеваний.
В то же время у больных с далеко зашедшей ВИЧ-инфекцией наблюдается кандидоз слизистых оболочек, что указывает на важность клеточно-опо-средованного иммунитетадля зашиты от этого возбудителя.
Другие грибы, такие как Histoplasma capsulatumи Cryptococcus neoformans, в тех местах, где они обнаруживаются в почве, поступают в организм при вдыхании.
Изучение распространенности бессимптомного носительства выявило высокий уровень инфицированности при очень низкой заболеваемости, что подтверждалось реакциями со стороны антител и положительными кожными пробами.
Таким образом, похоже, что первоначальное проникновение этих микробов в организм привело к появлению адаптивного иммунного ответа, защищающего от инфекции.
Некоторые грибы, такие как Histoplasma capsulatum, выживают внутри макрофагов и являются внутриклеточными патогенами.
Один из грибковых патогенов Cryptococcus neoformans имеет полисахаридную капсулу, ответственную за вирулентность.
Грибы отличаются от бактерий другим типом клеточной стенки, которая состоит из перекрестно связанных полисахаридов.
Клетки гриба обычно не подвержены лизису со стороны системы комплемента.
Реакция организма на грибковые инфекции включает как гуморальный, так и клеточный ответы.
Общепризнанно, что основной формой защиты от патогенных грибов является клеточно-опосредованный иммунитет.
Необходимость в нормальной функции Т-клеток для защиты от грибов особенно наглядно демонстрируется склонностью больных СПИДом к развитию угрожающих жизни инфекций, вызванных такими грибами, как Histoplasma capsulatum и Cryptococcus neoformans.
Исторически сложилось мнение, что иммунитет, опосредованный антителами, не имеет существенного значения для борьбы с грибами.
Однако за последние годы были сообщения о нескольких защитных моноклональных антителах против Cryptococcus albicans и Cryptococcus neoformans.
Таким образом, похоже, что и клеточный, и гуморальный иммунные механизмы участвуют в защите от грибов.
• МЕХАНИЗМЫ, С ПОМОЩЬЮ КОТОРЫХ ПАТОГЕНЫ ИЗБЕГАЮТ ИММУННОГО ОТВЕТА
Инкапсулированные бактерии
Полисахаридные капсулыявляются важными факторами вирулентностидля ряда патогенов человека, таких как Streptococcus pneumoniae (пневмококк), Haemophilus influenzae, Neisseria meningitides (менингококк) и Crypticoccus neoformans.
Эти антифагоцитарные капсулызащищают патогены от захвата и киллинга фагоцитарными клетками организма.
Поскольку бактерии устраняются РЭС в селезенке и печени, эти органы играют решающую роль в защите от инкапсулированных патогенов.
Индивидуумы с ослабленной функцией РЭС в результате заболевания (например, серповидно-клеточная анемия) или хирургического удаления селезенки особенно подвержены действию инкапсулированных бактерий.
Механизм действия антител против инкапсулированных патогенов включает фагоцитозс помощью опсонинови киллинг, осуществляемый нейтрофилами и макрофагами.
Антитела к капсулярным полисахаридам действуют путем стимуляции фагоцитоза непосредственно через Fc-рецепторы или не напрямую — активацией комплемента.
Токсины
Симптомы заболевания некоторых бактериальных инфекций вызываются факторами вирулентности,называемыми токсинами.
Бактериальные токсины являются белками.
Дифтерийный токсин может способствовать бактериальной инфекции, повреждая слизистые оболочки.
Bacillus anthracis — патоген, вызывающий сибирскую язву, вырабатывает токсины, приводящие к апоптозу макрофагов.
Основной механизм такого ускользания от иммунологического контроля включает действие так называемого летального токсина.
Этот токсин подавляет протеинкиназу макрофага, которая необходима для транскрипции антиапоптозных генов вслед за активацией клетки.
ПРОТЕИНКИНА́ЗЫ — подкласс ферментов киназ (фосфотрансфераз). Протеинкиназы модифицируют другие белки путем фосфорилирования остатков аминокислот, имеющих гидроксильные группы
Большинство токсинов являются высокоиммуногенными и вызывают сильный гуморальный и клеточный иммунные ответы.
Специфические антитела могут прикрепляться к бактериальным токсинам и нейтрализовать их.
Защита от токсинов преимущественно связана с IgG, хотя IgA может также играть важную роль в нейтрализации определенных экзотоксинов (например, секретируемых токсинов), таких как холерный энтеротоксин.
Поскольку экзотоксины плотно связываются со своими тканями-мишенями, они обычно не могут быть вытеснены при последующем назначении антитоксина.
Суперантигены
Взаимодействие определенных токсинов с иммунной системой может иметь серьезные иммунологические последствия, если токсины способны связываться с Т-клеточными рецепторами большого числа Т-клеток.
Эти токсины называют суперантигенами.
Одним из них является стафилококковый токсин синдрома токсического шока.
Суперантигены стимулируют большое количество Т-клеток, которые пролиферируют, синтезируют цитокины, а затем погибают посредством апоптоза, что приводит к потере важных иммунных клеток.
Проявляется этот феномен
—гипотензией,
-гиповолемией
—и органной недостаточностью,
которые могут привести к смерти.
Описаны также суперантигены для В-клеток, которые, связываясь с клетками, нарушают экспрессию определенных семейств генов иммуноглобулинов.
Антигенное разнообразие
Патогены могут избегать действия иммунной системы путем создания разновидностей, отличающихся по антигенному составу.
Этот механизм называют антигенным разнообразием.
Классическими примерами патогенов, использующих этот механизм, являются вирус гриппа, ВИЧ, Streptococcus pneumoniae, трипаносомы и стрептококки группы А.
В случае со стрептококком группыА М-белок, обусловливающий вирулентность, предотвращает фагоцитоз посредством механизма, способствующего отложению фибриногена на поверхности бактерии.
М-белки вызывают образование защитных антител, но отличаются антигенным разнообразием, и стрептококковая инфекция, вызванная одним штаммом, не приводит к появлению резистентности к другим штаммам.
М-белок и Миомезин и ассоциированы с миозиновыми филаментами в области центральной «голой» зоны филамента.
Антигенное разнообразие вирусов гриппа обеспечивается наличием у них сегментированного РНК-генома.
При его переформировании получаются вирионы, экспрессирующие новые комбинации двух основных поверхностных антигенов:
—гемагглютинина
-и белков поверхностной нейроаминидазы.
НЕРАМИНИДАЗА – фермент гидролизирует ацетилнейраминовой кислоты.
Результатом точечных мутаций в геноме вируса гриппа является антигенный дрейф,обеспечивающий антигенные изменения у гемагглютинина и нейроаминидазы.
Антигенный сдвигпоявляется, когда вирус гриппа экспрессирует новую аллель гемагглютинина или белка нейроаминидазы, что приводит к значительным антигенным изменениям и появлению нового штамма вируса.
В результате антигенных дрейфа и сдвига вирус гриппа быстро изменяется, и одна инфекция гриппа не приводит к появлению резистентности к последующей инфекции.
Более того, поскольку каждая эпидемия обладает антигенными отличиями, вакцина против гриппа должна обновляться каждый год.
У ВИЧ антигенная изменчивость in vivoпроявляется очень быст
cyberpedia.su
Апоптоз
Апоптоз (греч. аpo – удаление, прекращение; греч. рtosis – падение) –запрограммированная смерть клетки, представляет собой процесс, посредством которого внутренние или внешние факторы, активируя генетическую программу, приводят к гибели клетки и ее эффективному удалению из ткани.
Апоптоз – это биохимически специфический тип гибели клетки, характеризуется активацией нелизосомных эндогенных эндонуклеаз, которые расщепляют ядерную ДНК на маленькие фрагменты. Морфологически апоптоз проявляется гибелью единичных, беспорядочно расположенных клеток, что сопровождается формированием округлых, окруженных мембраной телец (“апоптотические тельца”), которые фагоцитируются окружающими клетками.
Это энергозависимый процесс, посредством которого удаляются нежелательные и дефектные клетки организма. Он играет большую роль в морфогенезе и является механизмом постоянного контроля размеров органов. При снижении апоптоза происходит накопление клеток (опухолевый рост). При увеличении апоптоза наблюдается прогрессивное уменьшение количества клеток в ткани (атрофия).
Морфологические проявления апоптоза
Апоптоз имеет свои отличительные морфологические признаки. Апоптоз определяется в единичных клетках или небольших группах клеток. Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина.
Наиболее четко морфологические признаки выявляются при электронной микроскопии (рис.6)
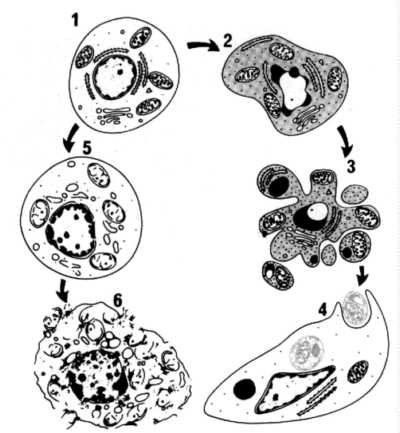
Рис. 6. Последовательность ультраструктурных изменений
При апоптозе (справа) и некрозе (слева)
1 – нормальная клетка; 2 – начало апоптоза; 3 – фрагментация апоптотической клетки; 4 – фагоцитоз апоптотических телец окружающими клетками; 5 – гибель внутриклеточных структур при некрозе; 6 – разрушение клеточной мембраны.
Для клетки, подвергающейся апоптозу характерно (рис.6):
Сжатие клетки.Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, располагаются более компактно.
Конденсация хроматина.Это наиболее характерное проявление апоптоза. Хроматин конденсируется по периферии, под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро же может разрываться на два или несколько фрагментов.
Формирование в цитоплазме полостей и апоптотических телец.В клетке первоначально формируются глубокие впячивания поверхности с образованием полостей, что приводит к фрагментации клетки и формированию окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с или без фрагментов ядра.
Фагоцитозапоптотических клеток или телец осуществляется окружающими здоровыми клетками. Апоптотические тельца быстро разрушаются в лизосомах, а окружающие клетки либо мигрируют, либо делятся, чтобы заполнить освободившееся после гибели клетки пространство.
Таблица 2
Сравнительная характеристика некроза и апоптоза
Признак | Апоптоз | Некроз |
Индукция | Активируется физиологическими или патологическими стимулами | Различная в зависимости от повреждающего фактора |
Распространенность | Одиночная клетка | Группа клеток |
Биохимические изменения | Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. | Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. |
Распад ДНК | Внутриядерная конденсация с расщеплением на фрагменты | Диффузная локализация в некротизированной клетке |
Целостность клеточной мембраны | Сохранена | Нарушена |
Морфология | Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином | Набухание и лизис клеток |
Воспалительный ответ | Нет | Обычно есть |
Удаление погибших клеток | Поглощение (фагоцитоз) соседними клетками | Поглощение (фагоцитоз) нейтрофилами и макрофагами |
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез).
Гормон-зависимой инволюции органов у взрослых (отторжение эндометрия во время менструального цикла, атрезии фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации).
Удалении некоторых клеток при пролиферации клеточной популяции
Гибели отдельных клеток в опухолях (в основном при ее регрессии, но также и в активно растущей опухоли).
Гибели клеток иммунной системы (В-, и Т-лимфоцитов, после истощения запасов цитокинов, гибели аутореактивных Т-клеток при развитии в тимусе).
Патологической атрофии гормон – зависимых органов (атрофии предстательной железы после кастрации, истощении лимфоцитов в тимусе при терапии глюкокортикоидами).
Гибели клеток, вызванных действием цитотоксических Т-клеток (при отторжении трансплантата, болезни “трансплантат против хозяина”).
Повреждении клеток при некоторых вирусных заболеваниях (при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени – тельца Каунсильмана).
studfiles.net
Сходство некроза и апоптоза
1. Разновидности смерти клеток в живом организме
2. Встречается и в норме и в патологии
Основная биологическая рольапоптоза – установление нужного равновесия м/у процессами пролиферации и гибели клеток.
Отличие апоптоза от некроза
1. Апоптоз распространяется только на отдельные клетки или группы клеток
Некроз распространяется от части клеток до целого органа
2. При апоптозе отсутствует демаркационное (отграничестельное) воспаление.
Апоптозные тельца отличаются небольшими размерами примерно с малый лимфоцит, у них высокое ядерно-цитоплазматическое соотношение, округлые контуры, конденсированные цитоплазма и хроматин. Каждое апоптозное тельце имеет фрагмент ядра, ограниченный 2-х контурной ядерной мембраной и индивидуальный набор органелл.
Апоптознае тельца – объекты фагоцитоза, которые развиваются очень быстро
30. Иммунопатологические процессы, определение, классификация. Морфологические изменения органов иммунной системы при антигенной стимуляции.
1) реакции гиерчувствительности
2) аутоимунные болезни
3) иммунодефицитные состояния (Крайним проявлением недостаточности иммунной системы. Они могут быть первичными, обусловленными гипоплазией (аплазией) иммунной системы наследственные и врожденные иммунодефицитные синдромы, или вторичными, возникающими в связи с болезнью или проводимым лечением приобретенные иммунодефицитные синдромы.
4) Амилоидоз
Иммунопатологические процессы — это реакции организма, развивающиеся в результате нарушений иммунитета.
Иммунопатологи́ческие проце́ссы — патологические изменения органов иммунной системы и нарушения иммунного ответа.
Основными формами нарушения иммунного ответа являются его недостаточность (иммунодефицит) и чрезмерная выраженность (аллергия).
К иммунной системе относятся органы и ткани, в которых происходит созревание (дифференцировка) Т- и В-лимфоцитов. Выделяют первичные и вторичные органы иммунной системы.
I. Первичные органы иммунной системы
-Тимус
-Костный мозг
-Сквамозные (многослойные плоские) эпителии покровных тканей.
II. Вторичные органы иммунной системы
-Лимфатические узлы
-Белая пульпа селезёнки
-Факультативные лимфоидные структуры.
-Миндалины кольца Вальдеера—Пирогова
-Червеобразный отросток слепой кишки
-Пейеровы бляшки
-Солитарные фолликулы.
31. Реакции гиперчувствительности, морфологическая характеристика.
Реакции гиперчувствительности :
-анафилактические
— антителозависимые, цитотоксические
— иммунокомплексные
-клеточно – опосредованные
Реакции 1 типа( немедленный тип , аллергический) :
Местные – атопическая аллергия ( бронхиальная астма, сенная лихорадка , аллергический ринит, пищевая аллергия ) . зависят от места проникновения аллергена и носят характер ограниченного отека кожи ( кожная аллергия, крапивница) , веделений из носа и коньюктивов.
Системная анафилаксия – ответ на внутривенное введение аллергена, к которому организм хозяина предварительно сенсибилизирован ( бронхоспазм, сосудистый шок, анафилактический шок)
Реакции гиперчувствит.1 типа проходят фазы – инициального ответа и позднюю.
— фаза инициального ответа развивается через 30 – 50 минут после контакта с аллергеном и характеризуется расширением сосудов, повышением их проницаемости , а также спазмом гладкой мускулатуры или секреции желез .
— поздняя фаза наблюдается через 2 -8 часов без дополнительных контактов с аллергеном , продолжается несколько дней и характеризуется интенсивной инфильтрацией тканей эозинофилами, нейтрофилами, базофилами, моноцитами , а также повреждением эпителиальных клеток слизистых оболочек.
Развитие гиперчув-и 1 типа обеспечивают IgE– антитела , образующиеся в ответ на аллерген при участии Т хелперов. Система комплимента не активируется.
Реакции 2 типа ( реакция немедленной повышенной чувствительности) – связывание антител на поверхности клеток
— комплиментзависимые ( существует 2 механизма : прямом лизис и опсонизация. В первом случае антитело (IgM,IgG) реагирует с антигеном на поверхности клетки, активируя систему комплимента, которая разрушает плазматич.мембрану этих клеток и вызывает их гибель. Во втором случае клетки мишени , покрытыеIgG(опсонизация) фагоцитируются макрофагами или нейтрофилами. )
— антителозависимые цитотоксические ( не сопровождается фиксацией комплимента , но вызывает кооперацию лейкоцитов , клетки мишени покрытые покрытые (опсонизированные)IgGв низких концентрациях, уничтожаются несенсибилизированными клетками. Лизис этих клеток происходит без фагоцитоза. В этом виде цитотоксичности участвуют моноциты, нейтрофилы, эозинофили, натуральные киллеры клетки. Этот вид цитотоксичности имеет значение при реакции отторжения имплантанта).
— антителоопосредованная дисфункция клеток
— реакции 2 типа обусловленна IgGантителами к экзогенным антигенам , адсорбированным на клетках или внеклеточном матриксе. При таких реакциях в организме появляются антитела направленные против клеток собственных тканей. Антигенные детерминанты могут образовываться в клетках в результате нарушений на генном уровне , приводящих к синтезу атипичных белков. В любом случае, реакция возникает как следствие связывание антител с нормальными или поврежденными структурами клетки или внеклеточного матрикса.
Реакция 3 типа – связанны с отложением иммунных комплексов. Циркулирующие иммуно комплексы ЦИК ( антиген- антитело) вызывают повреждение при попадании в стенку кровенносных сосудов или в фильтрующие структуры ( почки) . Известны 2 типа иммунокомплексных повреждений : 1) формируются при поступлении в организм экзогенного антигена ( вирус, бактерия, чужой белок ) 2) при образовании антител против собственных антигенов.
Заболевания могут быть генерализованными , если комплексы образуются в крови и оседают во многих органах , или же связанными с отдельными органами, например почки ( гламерулонефрит) , суставы (артрит ) , мелкие кровенносные сосуды кожи.
Как только ЦИК оседают в тканях, они инициируют острую воспалительную реакцию. В эту фазу наблядается клинические проявления ( крапивница, лихорадка, увеличение лимфоти.узлов, протеинурия) Потом происходит активация комплимента с образованием его активных комплексов. Иммунные комплексы вызывают агрегацию тромбоцитов и активацию фактора Хагемана, что приводит к усилению воспалит.процесса и образованию микротромбов. В результате развивается гламерулонефрит, васкулит, артрит и др.
— системная иммунокомплексная болезнь (сывороточная болезнь) – возникает в результате пассивной иммунизации , возникающей в результате многократного ввведения больших доз чужеродной сыворотки
— местная иммунокомплексная болезнь ( феномен Артюса) – выражается в локальном некрозе ткани, возникающеи вследствии острого иммунокомплексного васкулита.
— хроническая сывороточная болезнь ( например красная волчанка , связанна с долгим созранением ( персистенцией) аутоантигенов. )
Реакции 4 типа ( замедленного типа)
— контактная гиперчувствительность
— иперувствительность замедленного типа ( туберкулинновый и гранулематозный)
Основными компонентами реакции гиперчувствительности IV типа являются Т-лимфоциты ГЗТ и макрофаги. Примером такой реакции являются контактный дерматит на химические вещества (краску для волос, косметику, стиральные порошки и др.) и реакция на микобактерии туберкулеза. Развитие пролонгированной реакции ГЗТ способно приводить к формированию гранулемы. Гранулематозные поражения кожи наблюдаются при лепре (Mycobacterium leprae). При туберкулезе в легких в результате хронической реакции ГЗТ и экзопродукции макрофагами литических ферментов происходит формирование каверн.
Патанатомия реакции гиперчувствительности :
1)клеточный инфильтрат
2) плазматическое пропитывание и фибриноидной некроз сосудов
3) продуктивные и некротические васкулиты
4) отложениеи иммуноглобулинов
studfiles.net
Сравнительная характеристика некроза и апоптоза — Студопедия.Нет
Некроз и апоптоз являются разновидностями смерти клеток в живом организме.
Отличия апоптоза от некроза связаны с различиями в их распространённости, генетическими, биохимическими, морфологическими и клиническими проявлениями. Существенным отличием апоптоза от некроза является то, что апоптоз распостраняется всегда только на отдельные клетки или их группы, в то время как некроз может захватывать территорию начиная от части клетки до целого органа.
В отличие от некроза разрушение ядра при апоптозе происходит с участием специальных кальций/магний-зависимых эндонуклеаз, расщепляющих молекулы ДНК в участках между нуклеосомами, что приводит к формированию однотипных по размерам фрагментов ДНК, что имеет и своё морфологическое выражение в виде особой структуры хроматина. В цитоплазме клетки, подвергшейся апоптозу, никогда не наблюдается активации гидролитических ферментов, как это бывает при некрозе. Напротив, все органеллы долгое время остаются сохранными и подвергаются конденсации, что связывают с процессами сшивания белковых молекул трансглютаминазами, а также обезвоживания клеток за счёт действия особых селективных ферментных транспортных систем, регулирующих обмен ионов калия, натрия, хлора и воды. Морфологические отличия апоптоза от некроза касаются в основном ультраструктурных перестроек и наиболее достоверно выявляются специальными мофологическими методами.
Нарушения регуляции апоптоза в патологии
и его клиническое значение
Нарушение регуляции апоптоза приводит к возникновению дисбаланса между процессами митоза и гибели клеток в тканях, что отражается на тканевом гомеостазе. Подобные изменения обнаруживают при многих заболеваниях. Выделяют чрезмерный, недостаточный, незавершённый апоптоз.
· Чрезмерный апоптоз. Приводит к чрезмерной клеточной гибели (ВИЧ-инфекция, фульминантные формы гепатитов В и С) или к атрофии (нейродегенеративные заболевания, хроническая ишемия миокарда).
· Недостаточный апоптоз по отношению к уровню пролиферативных процессов. Наблюдается при гиперпластических процессах, опухолевом росте, аутоиммунных болезнях. Снижение уровня апоптоза в тканях способствует выживанию мутированных клеток и может способствовать развитию опухолей, что наблюдается при мутациях p53 и в гормонально-зависимых карциномах молочной железы, предстательной железы и яичника. Недостаточный апоптоз «запрещённых» клонов активированных по каким-либо причинам B-лимфоцитов, продуцирующих аутоантитела, может приводить к развитию аутоиммунных болезней.
· Незавершённый апоптоз в связи с отсутствием фагоцитоза апоптозных телец. Наблюдается при раке лёгкого. Незавершённый характер апоптоза, без последующего фагоцитоза апоптозных телец, можно считать проявлением его патологии при опухолевом росте. Незавершённый апоптоз может являться мощным источником митогенетических факторов, стимулирующих пролиферацию живых опухолевых клеток. Таким образом, можно предположить, что незавершённый апоптоз в раке лёгкого с последующим аутолизом апоптозных телец может ещё в большей степени стимулировать рост опухоли.
Значение апоптоза для клиники велико, поскольку его развитие связано с большинством общепатологических процессов. Особое значение апоптоз имеет для появления атрофии, иммунопатологических процессов, воспаления и опухолевого роста. Примером апоптоза в условиях патологии могут служить процессы атрофии паренхимы органов после обтурации выводных протоков (атрофия поджелудочной и околоушной слюнной желёз) или мочеточников (атрофия почек при гидронефрозе). Апоптоз может развиваться при повреждающем действии вирусов на клетки. Например, при вирусных гепатитах отмечается апоптоз гепатоцитов — тельца Каунсилмена. Апоптоз клеток воспалительного инфильтрата наблюдается в очагах иммунного (лимфоциты) и гнойного (полиморфно-ядерные лейкоциты) воспаления. Гибель B- и T-лимфоцитов, а также смерть клеток-мишеней в ходе реакций клеточного иммунитета и отторжения трансплантата также происходит путём апоптоза. Апоптоз развивается в корковых клетках тимуса при воздействии кортикостероидных гормонов и формировании иммунологической толерантности. Большое значение апоптоз имеет при опухолевом росте и может быть искусственно усилен химиотерапевтическими и лучевыми воздействиями на опухоль.
studopedia.net
Морфологические проявления апоптоза
Апоптоз имеет свои отличительные морфологические признаки как на светооптическом, так и на ультраструктурном уровне. При окраске гематоксилин-эозином апоптоз определяется в единичных клетках или небольших группах клеток. Апоптотические клетки выглядят как округлые или овальные скопления интенсивно эозинофильной цитоплазмы с плотными фрагментами ядерного хроматина. Поскольку сжатие клетки и формирование апоптотических телец происходит быстро и также быстро они фагоцитируются, распадаются или выбрасываются в просвет органа, то на гистологических препаратах он обнаруживается в случаях его значительной выраженности. К тому же апоптоз — в отличие от некроза — никогда не сопровождается воспалительной реакцией, что также затрудняет его гистологическое выявление (см. таблицу 1).
Таблица 1
Сравнительная характеристика некроза и апоптоза
Признак | Апоптоз | Некроз |
Индукция | Активируется физиологическими или патологическими стимулами | Различная в зависимости от повреждающего фактора |
Распространенность | Одиночная клетка | Группа клеток |
Биохимические изменения | Энергозависимая фрагментация ДНК эндогенными эндонуклеазами. Лизосомы интактные. | Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты. |
Распад ДНК | Внутриядерная конденсация с расщеплением на фрагменты | Диффузная локализация в некротизированной клетке |
Целостность клеточной мембраны | Сохранена | Нарушена |
Морфология | Сморщивание клеток и фрагментация с формированием апоптотических телец с уплотненным хроматином | Набухание и лизис клеток. |
Воспалительный ответ | Нет | Обычно есть |
Удаление погибших клеток | Поглощение (фагоцитоз) соседними клетками | Поглощение (фагоцитоз) нейтрофилами и макрофагами. |
Наиболее четко морфологические признаки выявляются при электронной микроскопии. Для клетки, подвергающейся апоптозу характерно:
Сжатие клетки. Клетка уменьшается в размерах; цитоплазма уплотняется; органеллы, которые выглядят относительно нормальными, располагаются более компактно. Предполагается, что нарушение формы и объема клетки происходит в результате активации в апоптотических клетках трансглютаминазы. Этот фермент вызывает прогрессивное образование перекрестных связей в цитоплазматических белках, что приводит к формированию своеобразной оболочки под клеточной мембраной, подобно ороговевающим клеткам эпителия.
Конденсация хроматина. Это наиболее характерное проявление апоптоза. Хроматин конденсируется по периферии, под мембраной ядра, при этом образуются четко очерченные плотные массы различной формы и размеров. Ядро же может разрываться на два и более фрагментов.
Механизм конденсации хроматина изучен достаточно хорошо. Эти изменения связаны с расщеплением ядерной ДНК в местах, связывающих отдельные нуклеосомы, что приводит к развитию большого количества фрагментов, в которых число пар оснований делится на 180-200. Эти фрагменты дают характерную картину лестницы при электрофорезе. Эта картина отличается от таковой при некрозе клеток, где длина фрагментов ДНК варьирует. Фрагментация ДНК в нуклеосомах происходит под действием кальций-чувствительной эндонуклеазы. Эндонуклеаза в некоторых клетках находится постоянно (например, тимоцитах), где она активируется появлением в цитоплазме свободного кальция, а в других клетках она синтезируется перед началом апоптоза. Однако еще не установлено, каким образом после расщепления ДНК эндонуклеазой происходит конденсация хроматина.
Формирование в цитоплазме полостей и апоптотических телец. В апоптотической клетке первоначально формируются глубокие впячивания поверхности с образованием полостей, что приводит к фрагментации клетки с формированием окруженных мембраной апоптотических телец, состоящих из цитоплазмы и плотно расположенных органелл, с или без фрагментов ядра.
Фагоцитоз апоптотических клеток или телец окружающими здоровыми клетками, или паренхиматозными, или макрофагами. Апоптотические тельца быстро разрушаются в лизосомах, а окружающие клетки либо мигрируют, либо делятся, чтобы заполнить освободившееся после гибели клетки пространство.
Фагоцитоз апоптотических телец макрофагами или другими клетками активируется рецепторами на этих клетках, которые захватывают и поглощают апоптотические клетки. Одним из таких рецепторов на макрофагах является рецептор витронектина, который является 3-интегрином и активирует фагоцитоз апоптотических нейтрофилов.
Апоптоз принимает участие в следующих физиологических и патологических процессах:
Запрограммированном разрушении клеток во время эмбриогенеза (включая имплантацию, органогенез) и метаморфоза. Несмотря на то, что при эмбриогенезе апоптоз не всегда является отражением “запрограммированной смерти клетки”, это определение апоптоза широко используется различными исследователями.
Гормон-зависимая инволюция органов у взрослых, например, отторжение эндометрия во время менструального цикла, атрезия фолликулов в яичниках в менопаузе и регрессия молочной железы после прекращения лактации.
Удаление некоторых клеток при пролиферации клеточной популяции
Гибель отдельных клеток в опухолях, в основном при ее регрессии, но также и в активно растущей опухоли.
Гибель клеток иммунной системы, как В-, так и Т-лимфоцитов, после истощения запасов цитокинов, а также гибель аутореактивных Т-клеток при развитии в тимусе.
Патологическая атрофия гормон-зависимых органов, например, атрофия предстательной железы после кастрации и истощение лимфоцитов в тимусе при терапии глюкокортикоидами.
Патологическая атрофия паренхиматозных органов после обтурации выводных протоков, что наблюдается в поджелудочной и слюнных железах, почках.
Гибель клеток, вызванная действием цитотоксических Т-клеток, например, при отторжении трансплантата и болезни “трансплантат против хозяина”.
Повреждение клеток при некоторых вирусных заболеваниях, например, при вирусном гепатите, когда фрагменты апоптотических клеток обнаруживаются в печени как тельца Каунсильмена.
Гибель клеток при действии различных повреждающих факторов, которые способны вызвать некроз, но действующих в небольших дозах, например, при действии высокой температуры, ионизирующего излучения, противоопухолевых препаратов.
studfiles.net
Часть 6 Апоптоз Сравнительная характеристика некроза и
 Часть 6 Апоптоз
Часть 6 Апоптоз
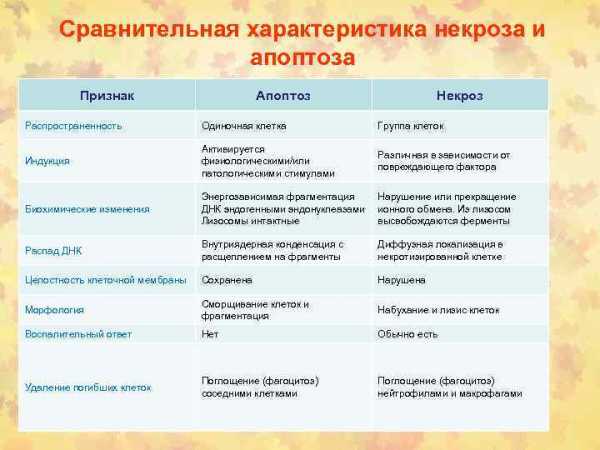 Сравнительная характеристика некроза и апоптоза Признак Апоптоз Некроз Распространенность Одиночная клетка Группа клеток Индукция Активируется физиологическими/или патологическими стимулами Различная в зависимости от повреждающего фактора Биохимические изменения Энергозависимая фрагментация ДНК эндогенными эндонуклеазами Лизосомы интактные Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты Распад ДНК Внутриядерная конденсация с расщеплением на фрагменты Диффузная локализация в некротизированной клетке Целостность клеточной мембраны Сохранена Нарушена Морфология Сморщивание клеток и фрагментация Набухание и лизис клеток Воспалительный ответ Нет Обычно есть Удаление погибших клеток Поглощение (фагоцитоз) соседними клетками Поглощение (фагоцитоз) нейтрофилами и макрофагами
Сравнительная характеристика некроза и апоптоза Признак Апоптоз Некроз Распространенность Одиночная клетка Группа клеток Индукция Активируется физиологическими/или патологическими стимулами Различная в зависимости от повреждающего фактора Биохимические изменения Энергозависимая фрагментация ДНК эндогенными эндонуклеазами Лизосомы интактные Нарушение или прекращение ионного обмена. Из лизосом высвобождаются ферменты Распад ДНК Внутриядерная конденсация с расщеплением на фрагменты Диффузная локализация в некротизированной клетке Целостность клеточной мембраны Сохранена Нарушена Морфология Сморщивание клеток и фрагментация Набухание и лизис клеток Воспалительный ответ Нет Обычно есть Удаление погибших клеток Поглощение (фагоцитоз) соседними клетками Поглощение (фагоцитоз) нейтрофилами и макрофагами
 Изменение ультраструктуры клеток при некрозе и апоптозе
Изменение ультраструктуры клеток при некрозе и апоптозе
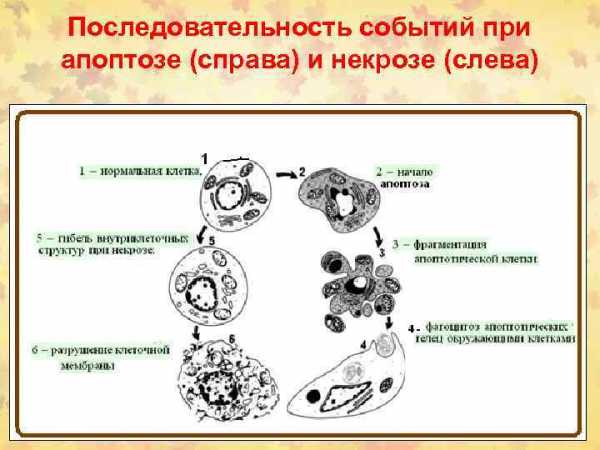 Последовательность событий при апоптозе (справа) и некрозе (слева)
Последовательность событий при апоптозе (справа) и некрозе (слева)
 Стадии реализации программы
Стадии реализации программы
 Функции апоптоза
Функции апоптоза
 Стадии апоптоза • 1. Индукция. Изменения в клеточном окружении, приводящие к активации апоптоза через R и СТ • 2. Исполнение. Клетка решает войти в апоптоз. • 3. Дегенерация. События, связанные с конечным развертыванием клеточных процессов, позволяющих подойти клетке к точке, откуда нет возврата.
Стадии апоптоза • 1. Индукция. Изменения в клеточном окружении, приводящие к активации апоптоза через R и СТ • 2. Исполнение. Клетка решает войти в апоптоз. • 3. Дегенерация. События, связанные с конечным развертыванием клеточных процессов, позволяющих подойти клетке к точке, откуда нет возврата.
 Индукторы и супрессоры апоптоза • Индукторы: дефицит ФР, глюкозы, УФ и гаммаизлучение, перекись, ПОЛ, ГК гормоны, ТХДД, ФНО, экспрессия проапоптотических генов сем. Bcl-2 цитолитические Т-лимфоциты, вирусы, химиотерапевтические лекарства и др. • Супрессоры: экспрессия антиапоптотических генов сем. Bcl-2, MDR, теломеразы, ингибиторы синтеза РНК и белков, мут. р53 и др.
Индукторы и супрессоры апоптоза • Индукторы: дефицит ФР, глюкозы, УФ и гаммаизлучение, перекись, ПОЛ, ГК гормоны, ТХДД, ФНО, экспрессия проапоптотических генов сем. Bcl-2 цитолитические Т-лимфоциты, вирусы, химиотерапевтические лекарства и др. • Супрессоры: экспрессия антиапоптотических генов сем. Bcl-2, MDR, теломеразы, ингибиторы синтеза РНК и белков, мут. р53 и др.
 Инициирующая точка клеточной гибели Стимул 1 Ядро Нестабильность хроматина (антрациклиновые антибиотики). Деградация теломеры 2 Митохондрия Нарушения в мтх. ДНК (мутации в комплексе I), ингибирование дыхания (антимицин). Индукция образования пор РТ (Са++), передислокация гексокиназы (клотримазол) 3 Эндоплазматический ретикулум Мутации в белке презенилин, накопление несобранных белков (туникамицин), деплеция Са++ 4 Цитоплазма Bcl 2 -белки – как мишени 5 Клеточная мембрана Рецепторы смерти (FAS, TNFa)
Инициирующая точка клеточной гибели Стимул 1 Ядро Нестабильность хроматина (антрациклиновые антибиотики). Деградация теломеры 2 Митохондрия Нарушения в мтх. ДНК (мутации в комплексе I), ингибирование дыхания (антимицин). Индукция образования пор РТ (Са++), передислокация гексокиназы (клотримазол) 3 Эндоплазматический ретикулум Мутации в белке презенилин, накопление несобранных белков (туникамицин), деплеция Са++ 4 Цитоплазма Bcl 2 -белки – как мишени 5 Клеточная мембрана Рецепторы смерти (FAS, TNFa)
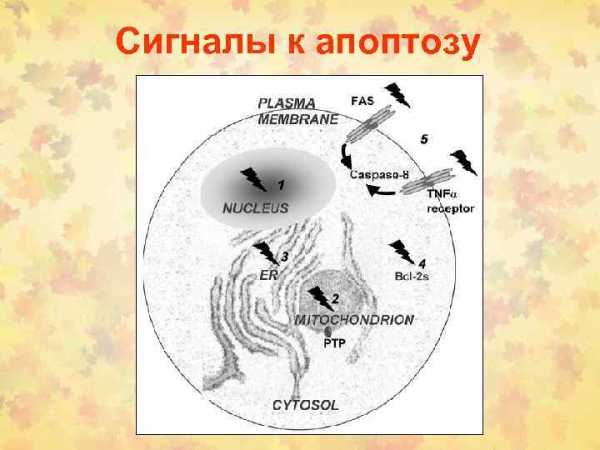 Сигналы к апоптозу
Сигналы к апоптозу
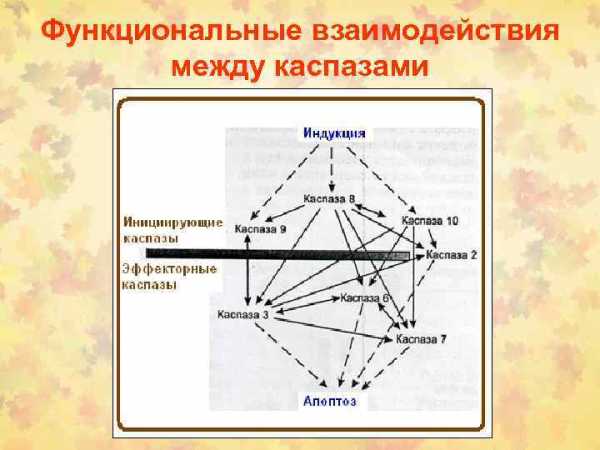 Функциональные взаимодействия между каспазами
Функциональные взаимодействия между каспазами
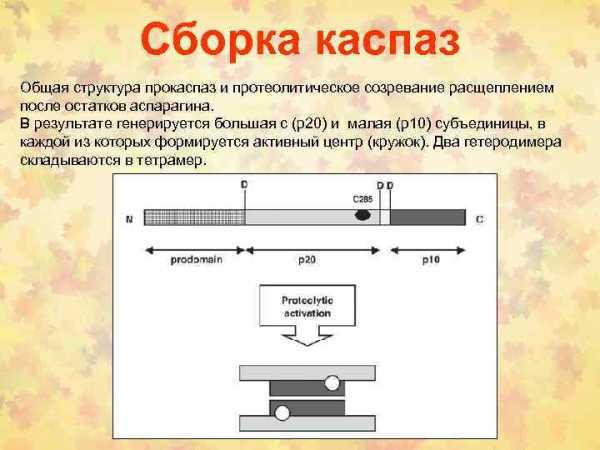 Сборка каспаз Общая структура прокаспаз и протеолитическое созревание расщеплением после остатков аспарагина. В результате генерируется большая с (р20) и малая (р10) субъединицы, в каждой из которых формируется активный центр (кружок). Два гетеродимера складываются в тетрамер.
Сборка каспаз Общая структура прокаспаз и протеолитическое созревание расщеплением после остатков аспарагина. В результате генерируется большая с (р20) и малая (р10) субъединицы, в каждой из которых формируется активный центр (кружок). Два гетеродимера складываются в тетрамер.
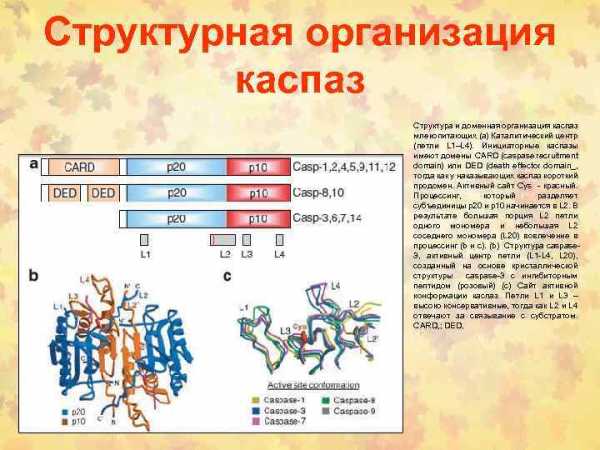 Структурная организация каспаз Структура и доменная организация каспаз млекопитающих (a) Каталитический центр (петли L 1–L 4). Инициаторные каспазы имеют домены CARD (caspase recruitment domain) или DED (death effector domain_, тогда как у наказывающих каспаз короткий продомен. Активный сайт Cys — красный. Процессинг, который разделяет субъединицы p 20 и p 10 начинается в L 2. В результате большая порция L 2 петли одного мономера и небольшая L 2 соседнего мономера (L 20) вовлечение в процессинг (b и c). (b) Структура caspase 3, активный центр петли (L 1 -L 4, L 20), созданный на основе кристаллической структуры caspase-3 с ингибиторным пептидом (розовый) (c) Сайт активной конформации каспаз. Петли L 1 и L 3 – высоко консервативные, тогда как L 2 и L 4 отвечают за связывание с субстратом. CARD, ; DED,
Структурная организация каспаз Структура и доменная организация каспаз млекопитающих (a) Каталитический центр (петли L 1–L 4). Инициаторные каспазы имеют домены CARD (caspase recruitment domain) или DED (death effector domain_, тогда как у наказывающих каспаз короткий продомен. Активный сайт Cys — красный. Процессинг, который разделяет субъединицы p 20 и p 10 начинается в L 2. В результате большая порция L 2 петли одного мономера и небольшая L 2 соседнего мономера (L 20) вовлечение в процессинг (b и c). (b) Структура caspase 3, активный центр петли (L 1 -L 4, L 20), созданный на основе кристаллической структуры caspase-3 с ингибиторным пептидом (розовый) (c) Сайт активной конформации каспаз. Петли L 1 и L 3 – высоко консервативные, тогда как L 2 и L 4 отвечают за связывание с субстратом. CARD, ; DED,
 Лиганды и рецепторы • Лиганды: сем. гомотримерных лигандов TNF — Fas. L, TRAIL (Apo 2 L), TNF α и β, CD 40 L, CD 27 L, OX 40 L. • Рецепторы: FAS и др. рецепторы семейства TNF
Лиганды и рецепторы • Лиганды: сем. гомотримерных лигандов TNF — Fas. L, TRAIL (Apo 2 L), TNF α и β, CD 40 L, CD 27 L, OX 40 L. • Рецепторы: FAS и др. рецепторы семейства TNF
 Взаимодействие лиганда смерти TRAIL с рецептором
Взаимодействие лиганда смерти TRAIL с рецептором
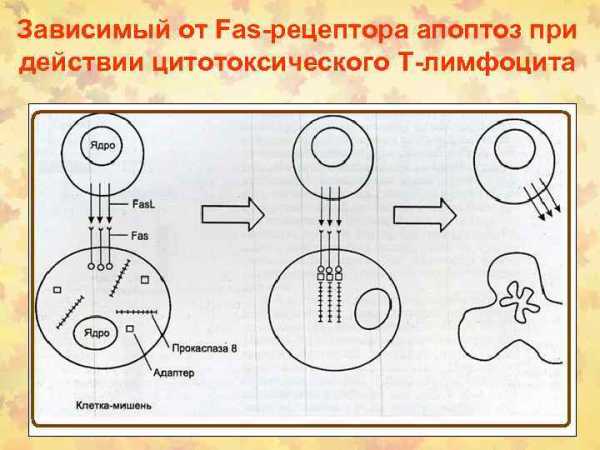 Зависимый от Fas-рецептора апоптоз при действии цитотоксического Т-лимфоцита
Зависимый от Fas-рецептора апоптоз при действии цитотоксического Т-лимфоцита
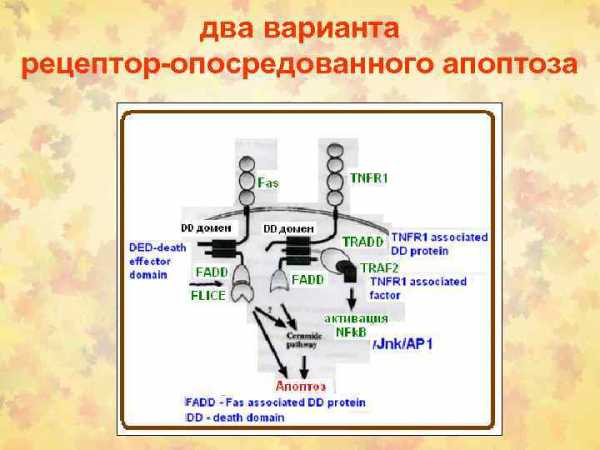 два варианта рецептор-опосредованного апоптоза
два варианта рецептор-опосредованного апоптоза
 Передача КС при апоптозе
Передача КС при апоптозе
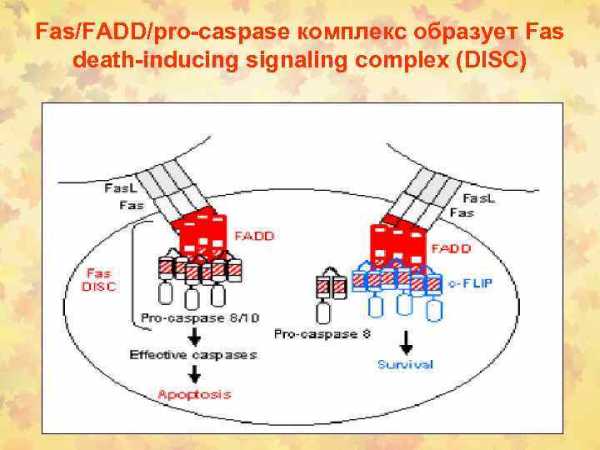 Fas/FADD/pro-caspase комплекс образует Fas death-inducing signaling complex (DISC)
Fas/FADD/pro-caspase комплекс образует Fas death-inducing signaling complex (DISC)
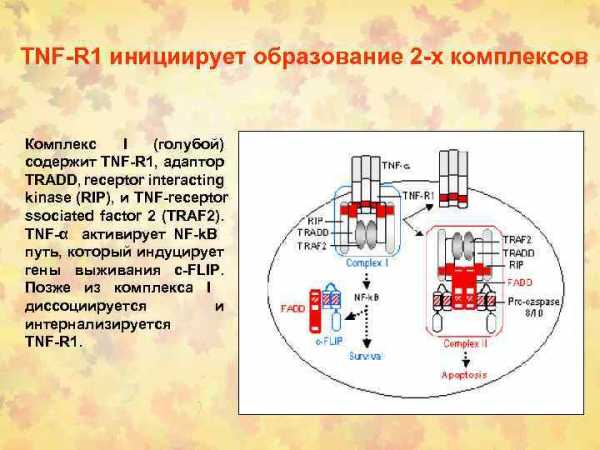 TNF-R 1 инициирует образование 2 -х комплексов Комплекс I (голубой) содержит TNF-R 1, адаптор TRADD, receptor interacting kinase (RIP), и TNF-receptor ssociated factor 2 (TRAF 2). TNF-α активирует NF-k. B путь, который индуцирует гены выживания c-FLIP. Позже из комплекса I диссоциируется и интернализируется TNF-R 1.
TNF-R 1 инициирует образование 2 -х комплексов Комплекс I (голубой) содержит TNF-R 1, адаптор TRADD, receptor interacting kinase (RIP), и TNF-receptor ssociated factor 2 (TRAF 2). TNF-α активирует NF-k. B путь, который индуцирует гены выживания c-FLIP. Позже из комплекса I диссоциируется и интернализируется TNF-R 1.
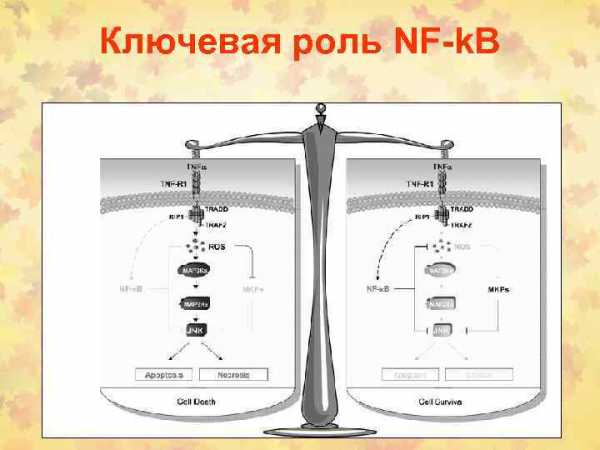 Ключевая роль NF-k. B
Ключевая роль NF-k. B
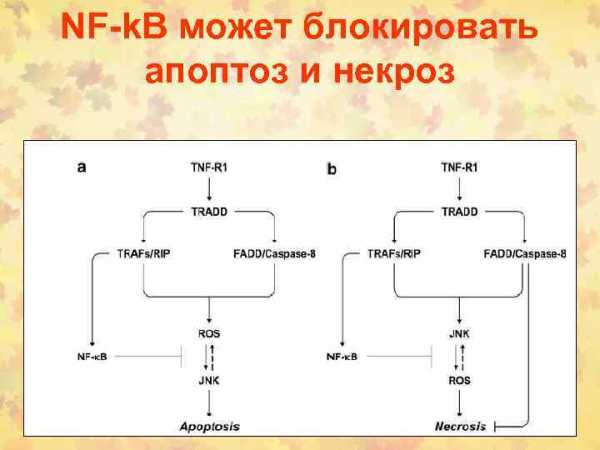 NF-k. B может блокировать апоптоз и некроз
NF-k. B может блокировать апоптоз и некроз
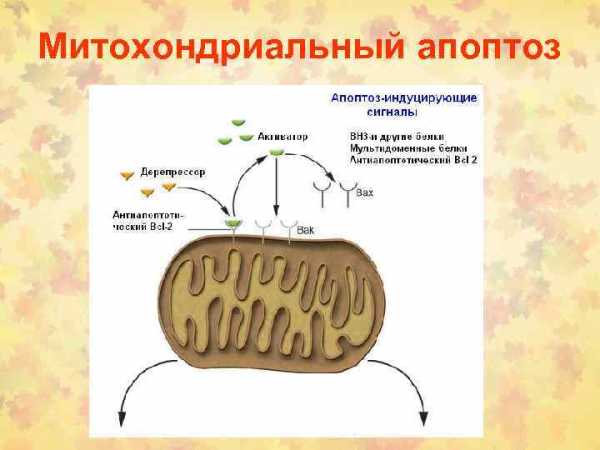 Митохондриальный апоптоз
Митохондриальный апоптоз
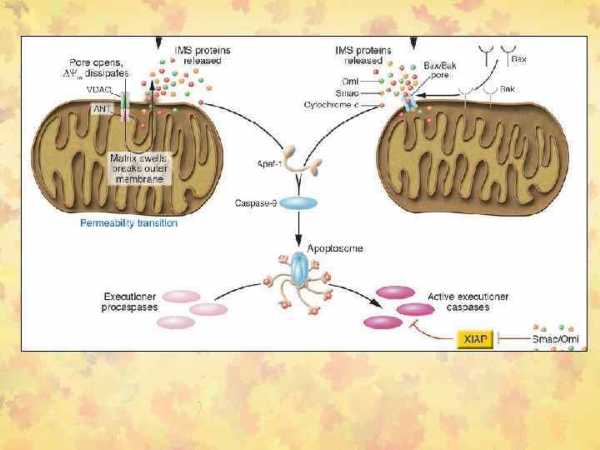
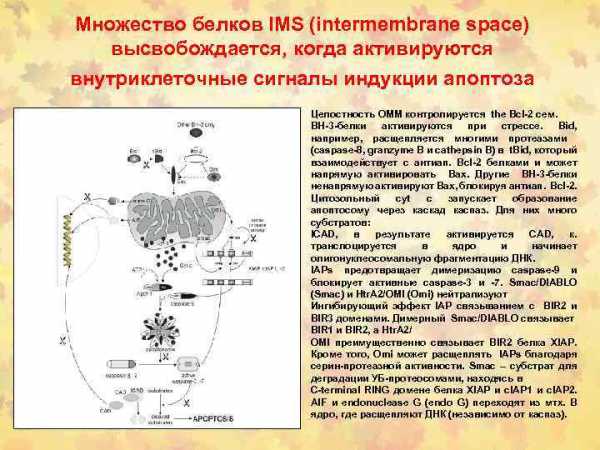 Множество белков IMS (intermembrane space) высвобождается, когда активируются внутриклеточные сигналы индукции апоптоза Целостность OMM контролируется the Bcl-2 сем. BH-3 -белки активируются при стрессе. Bid, например, расщепляется многими протеазами (caspase-8, granzyme B и cathepsin B) в t. Bid, который взаимодействует с антиап. Bcl-2 белками и может напрямую активировать Bax. Другие BH-3 -белки ненапрямую активируют Bax, блокируя антиап. Bcl-2. Цитозольный cyt c запускает образование апоптосому через каскад каспаз. Для них много субстратов: ICAD, в результате активируется CAD, к. транслоцируется в ядро и начинает олигонуклеосомальную фрагментацию ДНК. IAPs предотвращает димеризацию caspase-9 и блокирует активные caspase-3 и -7. Smac/DIABLO (Smac) и Htr. A 2/OMI (Omi) нейтрализуют Ингибирующий эффект IAP связыванием с BIR 2 и BIR 3 доменами. Димерный Smac/DIABLO связывает BIR 1 и BIR 2, а Htr. A 2/ OMI преимущественно связывает BIR 2 белка XIAP. Кроме того, Omi может расщеплять IAPs благодаря серин-протеазной активности. Smac – субстрат для деградации УБ-протеосомами, находясь в C-terminal RING домене белка XIAP и c. IAP 1 и c. IAP 2. AIF и endonuclease G (endo G) переходят из мтх. В ядро, где расщепляют ДНК (независимо от каспаз).
Множество белков IMS (intermembrane space) высвобождается, когда активируются внутриклеточные сигналы индукции апоптоза Целостность OMM контролируется the Bcl-2 сем. BH-3 -белки активируются при стрессе. Bid, например, расщепляется многими протеазами (caspase-8, granzyme B и cathepsin B) в t. Bid, который взаимодействует с антиап. Bcl-2 белками и может напрямую активировать Bax. Другие BH-3 -белки ненапрямую активируют Bax, блокируя антиап. Bcl-2. Цитозольный cyt c запускает образование апоптосому через каскад каспаз. Для них много субстратов: ICAD, в результате активируется CAD, к. транслоцируется в ядро и начинает олигонуклеосомальную фрагментацию ДНК. IAPs предотвращает димеризацию caspase-9 и блокирует активные caspase-3 и -7. Smac/DIABLO (Smac) и Htr. A 2/OMI (Omi) нейтрализуют Ингибирующий эффект IAP связыванием с BIR 2 и BIR 3 доменами. Димерный Smac/DIABLO связывает BIR 1 и BIR 2, а Htr. A 2/ OMI преимущественно связывает BIR 2 белка XIAP. Кроме того, Omi может расщеплять IAPs благодаря серин-протеазной активности. Smac – субстрат для деградации УБ-протеосомами, находясь в C-terminal RING домене белка XIAP и c. IAP 1 и c. IAP 2. AIF и endonuclease G (endo G) переходят из мтх. В ядро, где расщепляют ДНК (независимо от каспаз).
 Модель образования протеосомы
Модель образования протеосомы
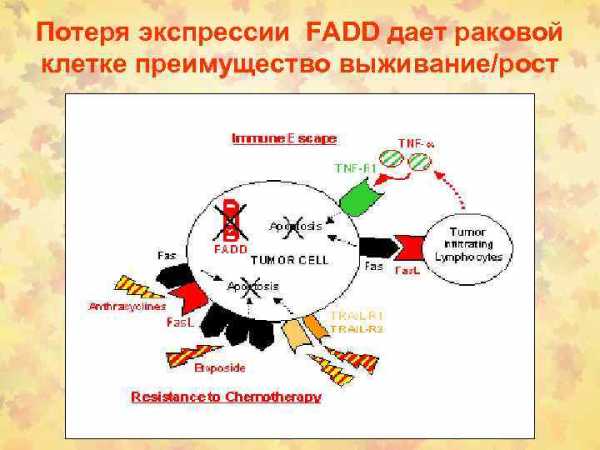 Потеря экспрессии FADD дает раковой клетке преимущество выживание/рост
Потеря экспрессии FADD дает раковой клетке преимущество выживание/рост
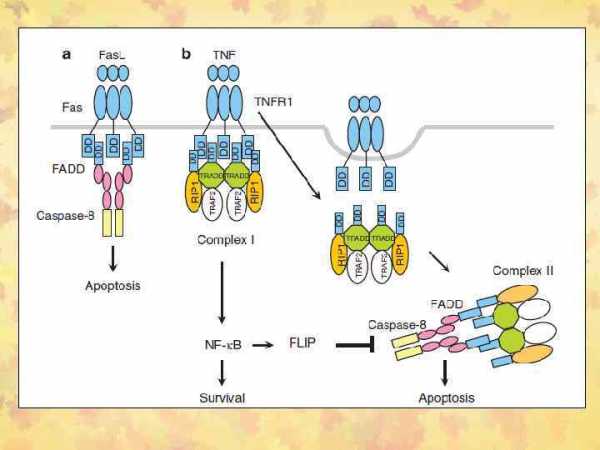
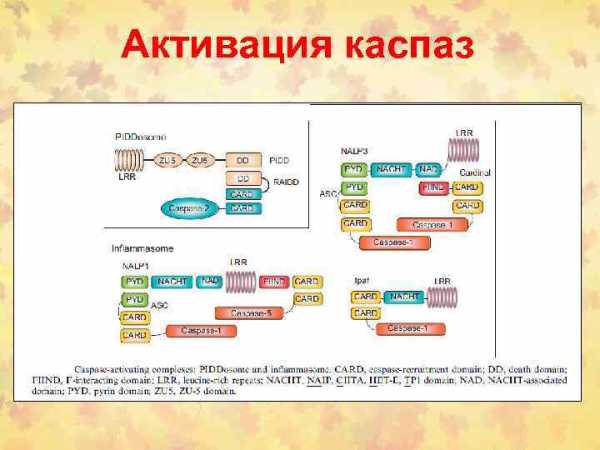 Активация каспаз
Активация каспаз
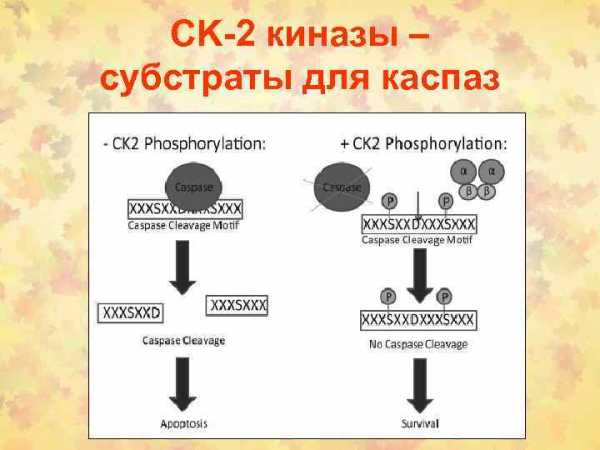 CK-2 киназы – субстраты для каспаз
CK-2 киназы – субстраты для каспаз
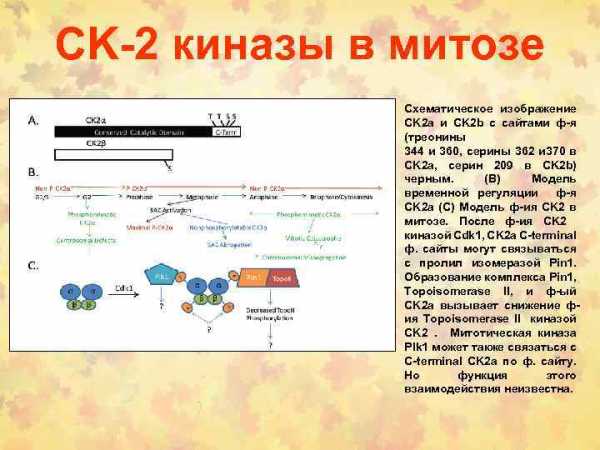 CK-2 киназы в митозе Схематическое изображение CK 2 a и CK 2 b с сайтами ф-я (треонины 344 и 360, серины 362 и 370 в CK 2 a, серин 209 в CK 2 b) черным. (B) Модель временной регуляции ф-я CK 2 a (C) Модель ф-ия CK 2 в митозе. После ф-ия CK 2 киназой Cdk 1, CK 2 a C-terminal ф. сайты могут связываться с пролил изомеразой Pin 1. Образование комплекса Pin 1, Topoisomerase II, и ф-ый CK 2 a вызывает снижение фия Topoisomerase II киназой CK 2. Митотическая киназа Plk 1 может также связаться с C-terminal CK 2 a по ф. сайту. Но функция этого взаимодействия неизвестна.
CK-2 киназы в митозе Схематическое изображение CK 2 a и CK 2 b с сайтами ф-я (треонины 344 и 360, серины 362 и 370 в CK 2 a, серин 209 в CK 2 b) черным. (B) Модель временной регуляции ф-я CK 2 a (C) Модель ф-ия CK 2 в митозе. После ф-ия CK 2 киназой Cdk 1, CK 2 a C-terminal ф. сайты могут связываться с пролил изомеразой Pin 1. Образование комплекса Pin 1, Topoisomerase II, и ф-ый CK 2 a вызывает снижение фия Topoisomerase II киназой CK 2. Митотическая киназа Plk 1 может также связаться с C-terminal CK 2 a по ф. сайту. Но функция этого взаимодействия неизвестна.
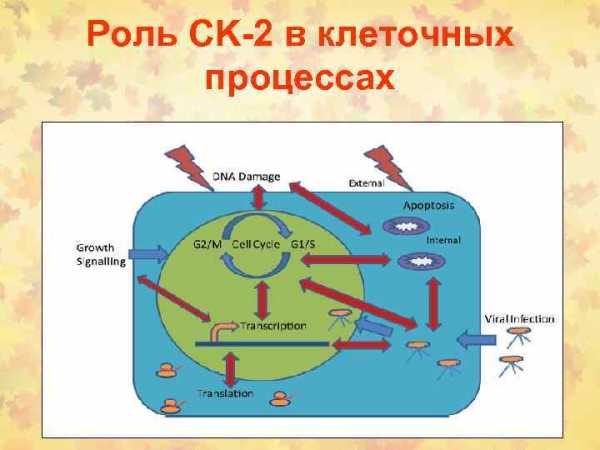 Роль CK-2 в клеточных процессах
Роль CK-2 в клеточных процессах
 Состав семейства Bcl-2 генов
Состав семейства Bcl-2 генов
 Способы взаимодействия между белками Bcl-2
Способы взаимодействия между белками Bcl-2
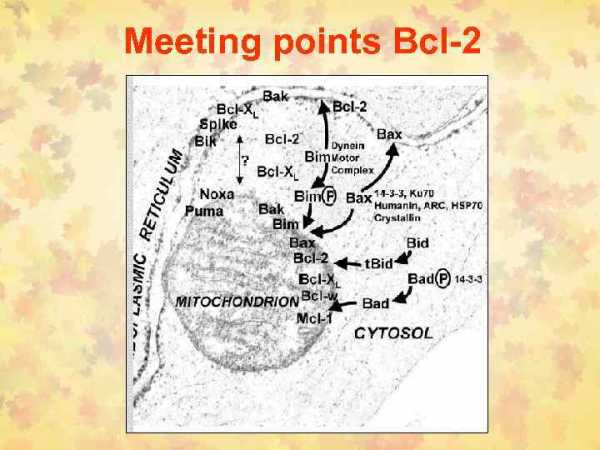 Meeting points Bcl-2
Meeting points Bcl-2
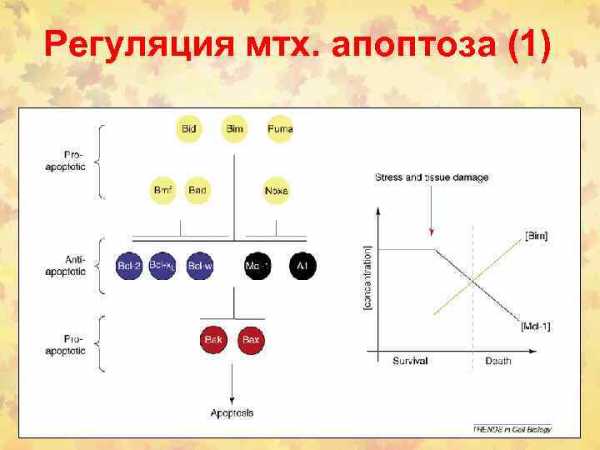 Регуляция мтх. апоптоза (1)
Регуляция мтх. апоптоза (1)
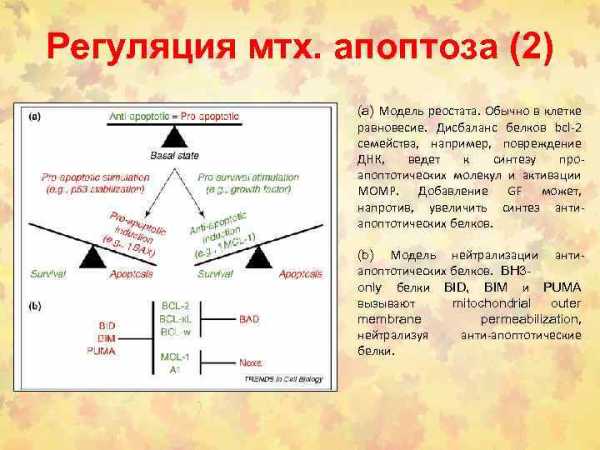 Регуляция мтх. апоптоза (2) (a) Модель реостата. Обычно в клетке равновесие. Дисбаланс белков bcl-2 семейства, например, повреждение ДНК, ведет к синтезу проапоптотических молекул и активации МОМР. Добавление GF может, напротив, увеличить синтез антиапоптотических белков. (b) Модель нейтрализации антиапоптотических белков. BH 3 only белки BID, BIM и PUMA вызывают mitochondrial outer membrane permeabilization, нейтрализуя анти-апоптотические белки.
Регуляция мтх. апоптоза (2) (a) Модель реостата. Обычно в клетке равновесие. Дисбаланс белков bcl-2 семейства, например, повреждение ДНК, ведет к синтезу проапоптотических молекул и активации МОМР. Добавление GF может, напротив, увеличить синтез антиапоптотических белков. (b) Модель нейтрализации антиапоптотических белков. BH 3 only белки BID, BIM и PUMA вызывают mitochondrial outer membrane permeabilization, нейтрализуя анти-апоптотические белки.
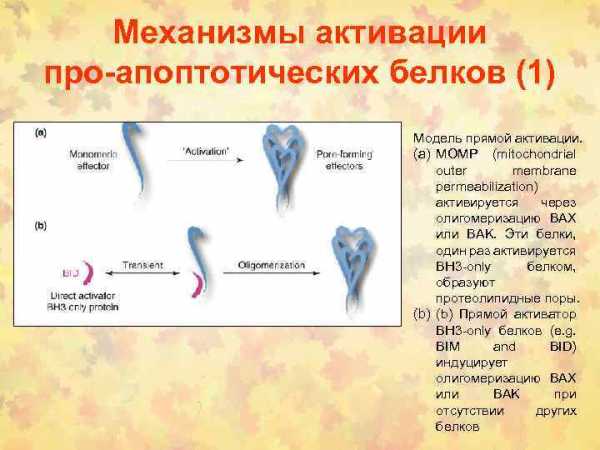 Механизмы активации про-апоптотических белков (1) Модель прямой активации. (a) MOMP (mitochondrial outer membrane permeabilization) активируется через олигомеризацию BAX или BAK. Эти белки, один раз активируется BH 3 -only белком, образуют протеолипидные поры. (b) Прямой активатор BH 3 -only белков (e. g. BIM and BID) индуцирует олигомеризацию BAX или BAK при отсутствии других белков
Механизмы активации про-апоптотических белков (1) Модель прямой активации. (a) MOMP (mitochondrial outer membrane permeabilization) активируется через олигомеризацию BAX или BAK. Эти белки, один раз активируется BH 3 -only белком, образуют протеолипидные поры. (b) Прямой активатор BH 3 -only белков (e. g. BIM and BID) индуцирует олигомеризацию BAX или BAK при отсутствии других белков
 Механизмы активации про-апоптотических белков (2) (c) Подкласс белков BH 3 -only de-repressors/sensitizers, не могут сами активировать BAX или BAK. В этом случае прямой активатор белка BH 3 -only инактивируется анти-апоптотическим белком BCL-2. . Под действием стресса de-repressor/sensitizer BH 3 only белок индуцируется траснкрипционным механизмом или пост-тр. модифиукацией и этот белок связывается с анти-апоптотическим белком, ускоряя инактивацию direct activator BH 3 -only белка. В этом примере BIM секвестируется MCL-1 и индукция Noxa делает возможным взаимодействие BIM и MOMP. (d) MOMP активируются, когда de-repressor/sensitizer BH 3 -only белки конститутивно ингибируют antiapoptotic BCL-2 белки, и любая индукция BID или BIM не остается не вовлеченной в процесс. В этом сценарии лсуществляется ‘sensitized for death’. Белок BCL-x. L ингибируется BAD, в индукция BIM обеспечивает активацию MOMP. Если нет BAD, сигнал MOMP ингибируется BCL-x. L.
Механизмы активации про-апоптотических белков (2) (c) Подкласс белков BH 3 -only de-repressors/sensitizers, не могут сами активировать BAX или BAK. В этом случае прямой активатор белка BH 3 -only инактивируется анти-апоптотическим белком BCL-2. . Под действием стресса de-repressor/sensitizer BH 3 only белок индуцируется траснкрипционным механизмом или пост-тр. модифиукацией и этот белок связывается с анти-апоптотическим белком, ускоряя инактивацию direct activator BH 3 -only белка. В этом примере BIM секвестируется MCL-1 и индукция Noxa делает возможным взаимодействие BIM и MOMP. (d) MOMP активируются, когда de-repressor/sensitizer BH 3 -only белки конститутивно ингибируют antiapoptotic BCL-2 белки, и любая индукция BID или BIM не остается не вовлеченной в процесс. В этом сценарии лсуществляется ‘sensitized for death’. Белок BCL-x. L ингибируется BAD, в индукция BIM обеспечивает активацию MOMP. Если нет BAD, сигнал MOMP ингибируется BCL-x. L.
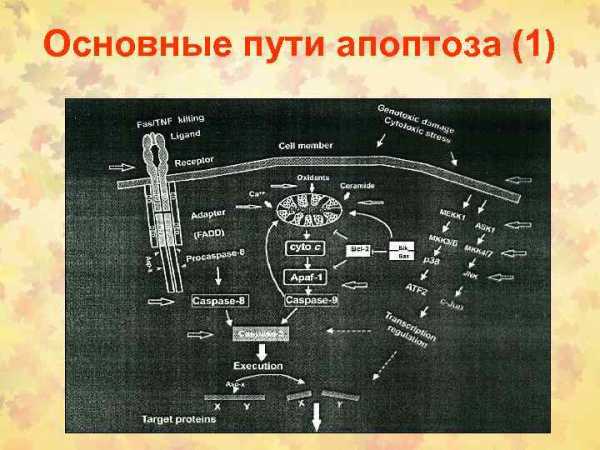 Основные пути апоптоза (1)
Основные пути апоптоза (1)
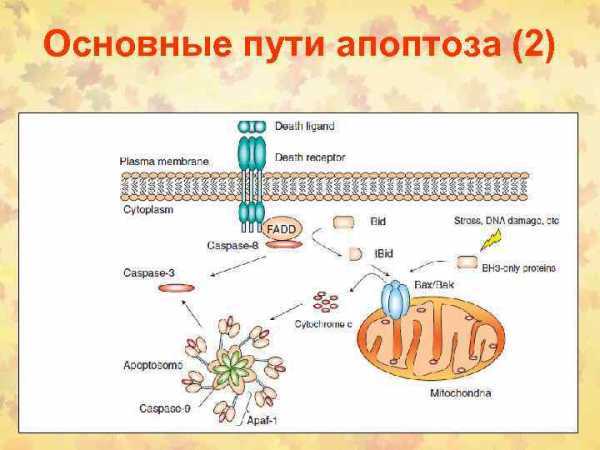 Основные пути апоптоза (2)
Основные пути апоптоза (2)
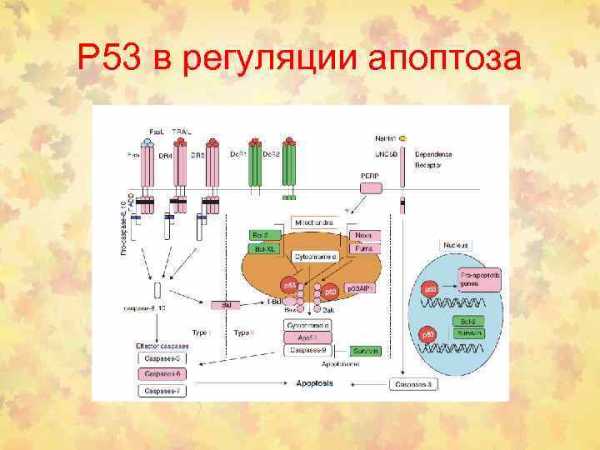 Р 53 в регуляции апоптоза
Р 53 в регуляции апоптоза
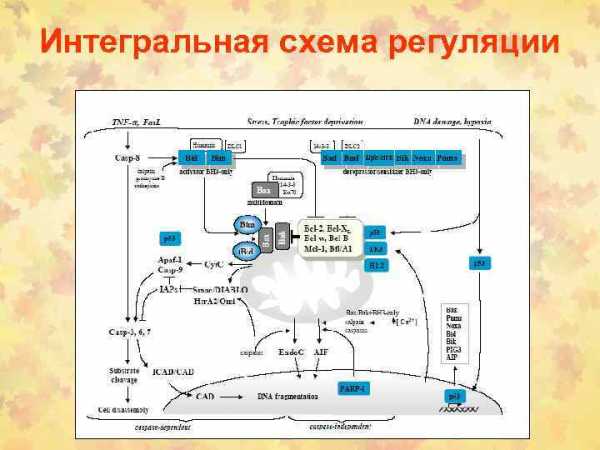 Интегральная схема регуляции
Интегральная схема регуляции
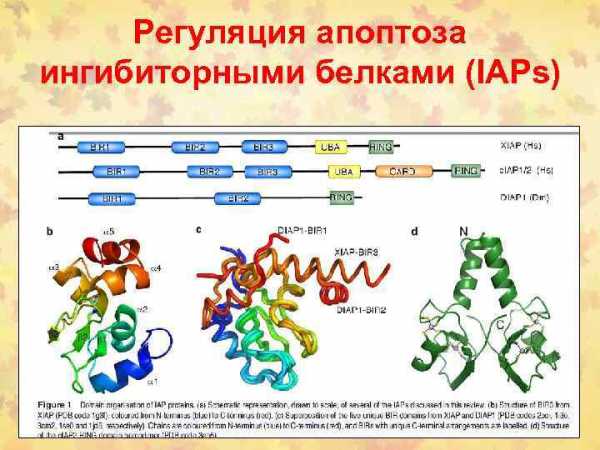 Регуляция апоптоза ингибиторными белками (IAPs)
Регуляция апоптоза ингибиторными белками (IAPs)
 Различная организация BIR
Различная организация BIR
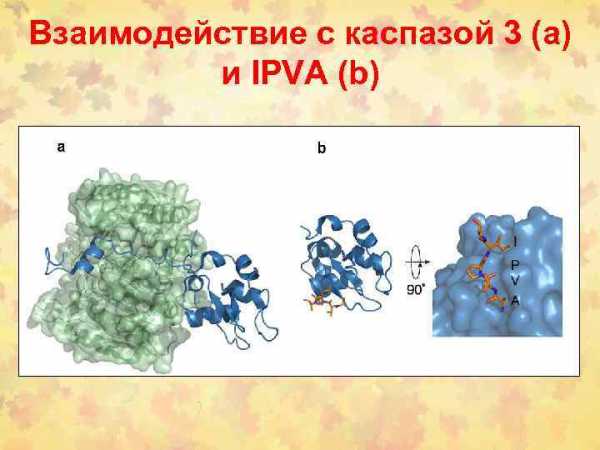 Взаимодействие с каспазой 3 (а) и IPVA (b)
Взаимодействие с каспазой 3 (а) и IPVA (b)
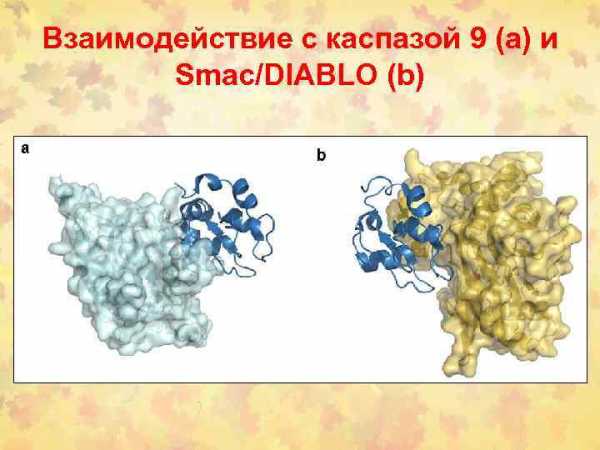 Взаимодействие с каспазой 9 (а) и Smac/DIABLO (b)
Взаимодействие с каспазой 9 (а) и Smac/DIABLO (b)
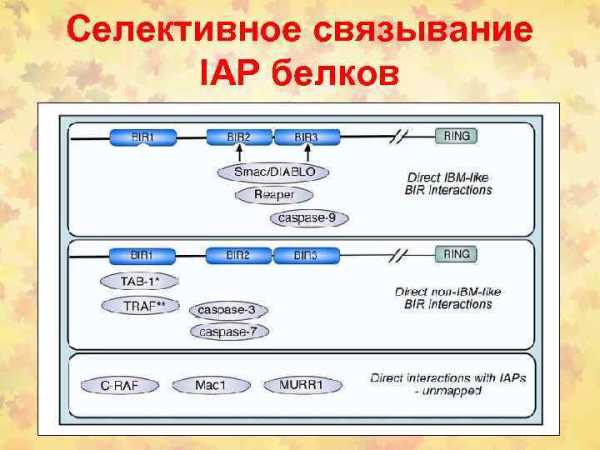 Селективное связывание IAP белков
Селективное связывание IAP белков
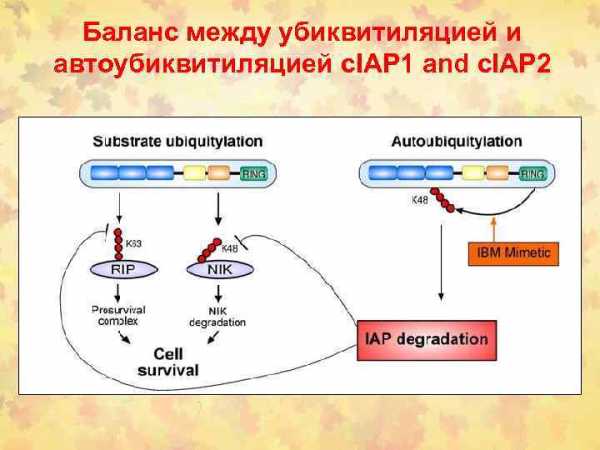 Баланс между убиквитиляцией и автоубиквитиляцией c. IAP 1 and c. IAP 2
Баланс между убиквитиляцией и автоубиквитиляцией c. IAP 1 and c. IAP 2
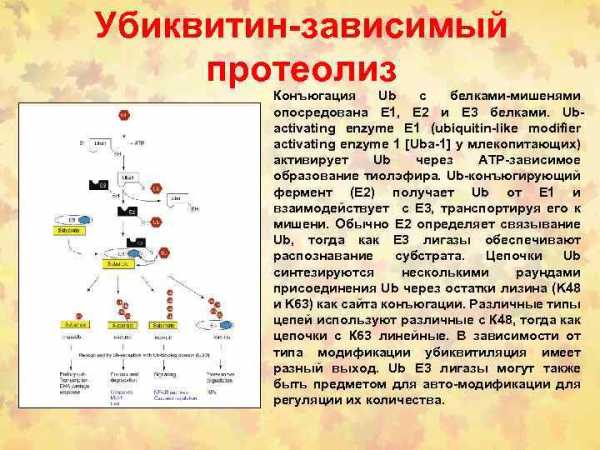 Убиквитин-зависимый протеолиз Конъюгация Ub с белками-мишенями опосредована E 1, E 2 и E 3 белками. Ubactivating enzyme E 1 (ubiquitin-like modifier activating enzyme 1 [Uba-1] у млекопитающих) активирует Ub через ATP-зависимое образование тиолэфира. Ub-конъюгирующий фермент (E 2) получает Ub от E 1 и взаимодействует с E 3, транспортируя его к мишени. Обычно E 2 определяет связывание Ub, тогда как E 3 лигазы обеспечивают распознавание субстрата. Цепочки Ub синтезируются несколькими раундами присоединения Ub через остатки лизина (K 48 и K 63) как сайта конъюгации. Различные типы цепей используют различные с К 48, тогда как цепочки с К 63 линейные. В зависимости от типа модификации убиквитиляция имеет разный выход. Ub E 3 лигазы могут также быть предметом для авто-модификации для регуляции их количества.
Убиквитин-зависимый протеолиз Конъюгация Ub с белками-мишенями опосредована E 1, E 2 и E 3 белками. Ubactivating enzyme E 1 (ubiquitin-like modifier activating enzyme 1 [Uba-1] у млекопитающих) активирует Ub через ATP-зависимое образование тиолэфира. Ub-конъюгирующий фермент (E 2) получает Ub от E 1 и взаимодействует с E 3, транспортируя его к мишени. Обычно E 2 определяет связывание Ub, тогда как E 3 лигазы обеспечивают распознавание субстрата. Цепочки Ub синтезируются несколькими раундами присоединения Ub через остатки лизина (K 48 и K 63) как сайта конъюгации. Различные типы цепей используют различные с К 48, тогда как цепочки с К 63 линейные. В зависимости от типа модификации убиквитиляция имеет разный выход. Ub E 3 лигазы могут также быть предметом для авто-модификации для регуляции их количества.
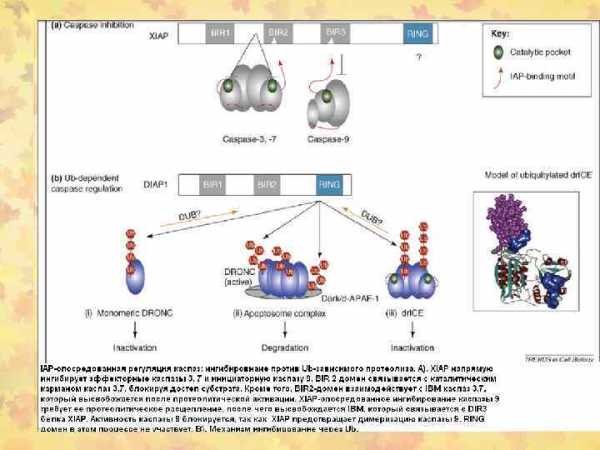
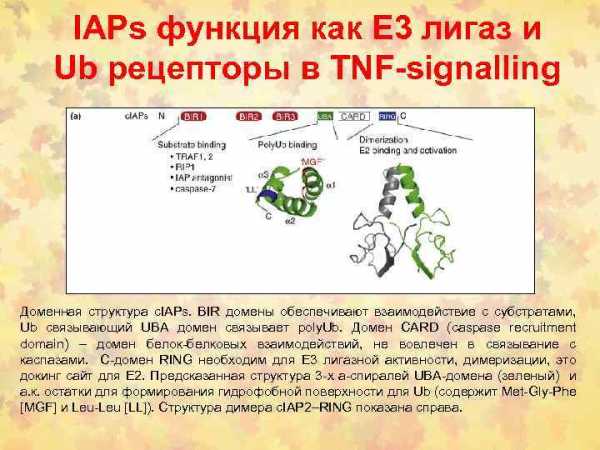 IAPs функция как E 3 лигаз и Ub рецепторы в TNF-signalling Доменная структура c. IAPs. BIR домены обеспечивают взаимодействие с субстратами, Ub связывающий UBA домен связывает poly. Ub. Домен CARD (caspase recruitment domain) – домен белок-белковых взаимодействий, не вовлечен в связывание с каспазами. С-домен RING необходим для E 3 лигазной активности, димеризации, это докинг сайт для E 2. Предсказанная структура 3 -х a-спиралей UBA-домена (зеленый) и а. к. остатки для формирования гидрофобной поверхности для Ub (содержит Met-Gly-Phe [MGF] и Leu-Leu [LL]). Структура димера c. IAP 2–RING показана справа.
IAPs функция как E 3 лигаз и Ub рецепторы в TNF-signalling Доменная структура c. IAPs. BIR домены обеспечивают взаимодействие с субстратами, Ub связывающий UBA домен связывает poly. Ub. Домен CARD (caspase recruitment domain) – домен белок-белковых взаимодействий, не вовлечен в связывание с каспазами. С-домен RING необходим для E 3 лигазной активности, димеризации, это докинг сайт для E 2. Предсказанная структура 3 -х a-спиралей UBA-домена (зеленый) и а. к. остатки для формирования гидрофобной поверхности для Ub (содержит Met-Gly-Phe [MGF] и Leu-Leu [LL]). Структура димера c. IAP 2–RING показана справа.
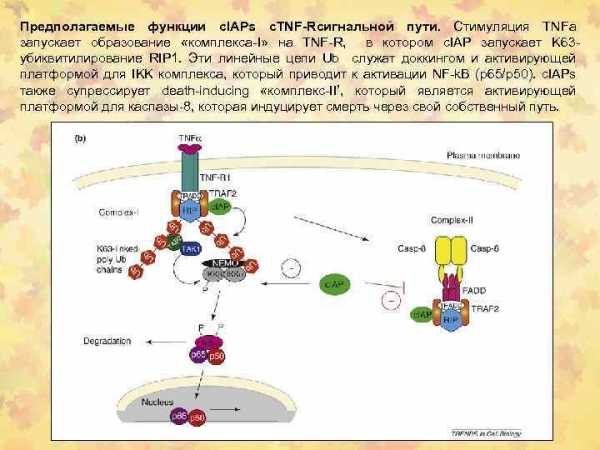 Предполагаемые функции c. IAPs с. TNF-Rсигнальной пути. Стимуляция TNFa запускает образование «комплекса-I» на TNF-R, в котором c. IAP запускает K 63 убиквитилирование RIP 1. Эти линейные цепи Ub служат доккингом и активирующей платформой для IKK комплекса, который приводит к активации NF-k. B (p 65/p 50). c. IAPs также супрессирует death-inducing «комплекс-II’, который является активирующей платформой для каспазы-8, которая индуцирует смерть через свой собственный путь.
Предполагаемые функции c. IAPs с. TNF-Rсигнальной пути. Стимуляция TNFa запускает образование «комплекса-I» на TNF-R, в котором c. IAP запускает K 63 убиквитилирование RIP 1. Эти линейные цепи Ub служат доккингом и активирующей платформой для IKK комплекса, который приводит к активации NF-k. B (p 65/p 50). c. IAPs также супрессирует death-inducing «комплекс-II’, который является активирующей платформой для каспазы-8, которая индуцирует смерть через свой собственный путь.
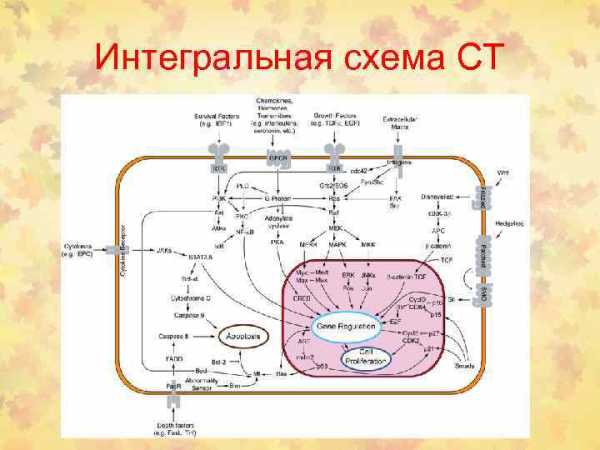 Интегральная схема СТ
Интегральная схема СТ
 Методы определения фрагментации ДНК
Методы определения фрагментации ДНК
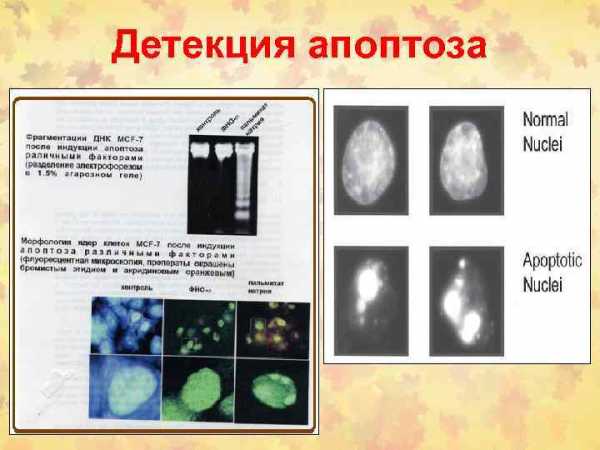 Детекция апоптоза
Детекция апоптоза
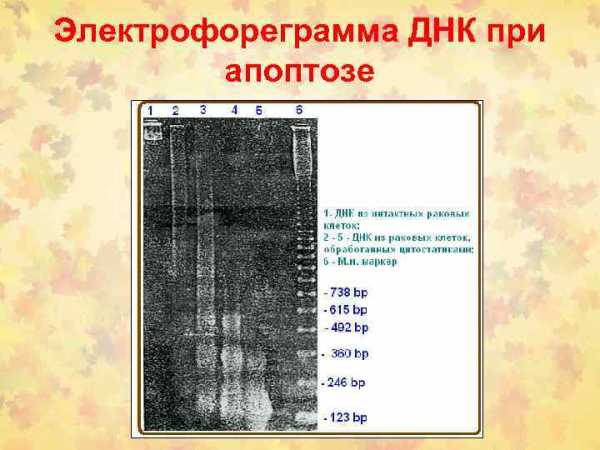 Электрофореграмма ДНК при апоптозе
Электрофореграмма ДНК при апоптозе
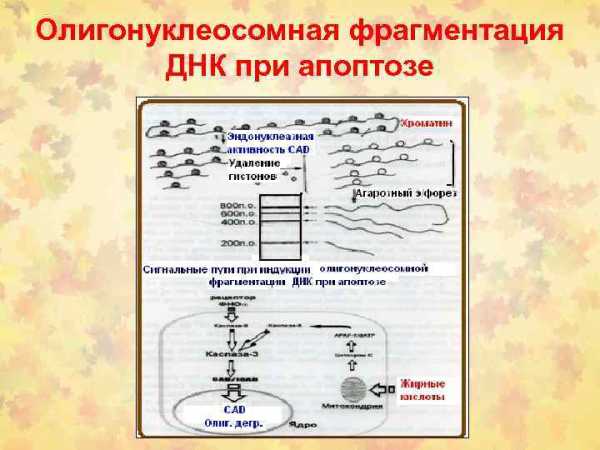 Олигонуклеосомная фрагментация ДНК при апоптозе
Олигонуклеосомная фрагментация ДНК при апоптозе
 Молекулярный имидж клеточной гибели
Молекулярный имидж клеточной гибели
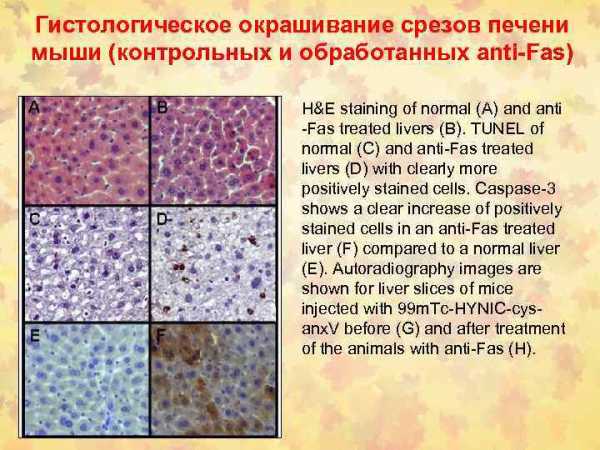 Гистологическое окрашивание срезов печени мыши (контрольных и обработанных anti-Fas) H&E staining of normal (A) and anti -Fas treated livers (B). TUNEL of normal (C) and anti-Fas treated livers (D) with clearly more positively stained cells. Caspase-3 shows a clear increase of positively stained cells in an anti-Fas treated liver (F) compared to a normal liver (E). Autoradiography images are shown for liver slices of mice injected with 99 m. Tc-HYNIC-cysanx. V before (G) and after treatment of the animals with anti-Fas (H).
Гистологическое окрашивание срезов печени мыши (контрольных и обработанных anti-Fas) H&E staining of normal (A) and anti -Fas treated livers (B). TUNEL of normal (C) and anti-Fas treated livers (D) with clearly more positively stained cells. Caspase-3 shows a clear increase of positively stained cells in an anti-Fas treated liver (F) compared to a normal liver (E). Autoradiography images are shown for liver slices of mice injected with 99 m. Tc-HYNIC-cysanx. V before (G) and after treatment of the animals with anti-Fas (H).
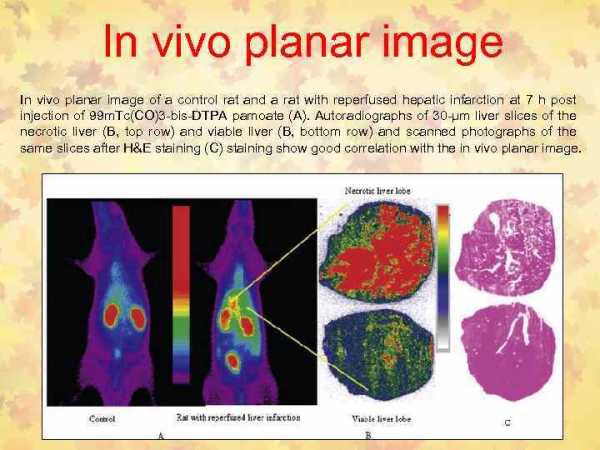 In vivo planar image of a control rat and a rat with reperfused hepatic infarction at 7 h post injection of 99 m. Tc(CO)3 -bis-DTPA pamoate (A). Autoradiographs of 30 -μm liver slices of the necrotic liver (B, top row) and viable liver (B, bottom row) and scanned photographs of the same slices after H&E staining (C) staining show good correlation with the in vivo planar image.
In vivo planar image of a control rat and a rat with reperfused hepatic infarction at 7 h post injection of 99 m. Tc(CO)3 -bis-DTPA pamoate (A). Autoradiographs of 30 -μm liver slices of the necrotic liver (B, top row) and viable liver (B, bottom row) and scanned photographs of the same slices after H&E staining (C) staining show good correlation with the in vivo planar image.
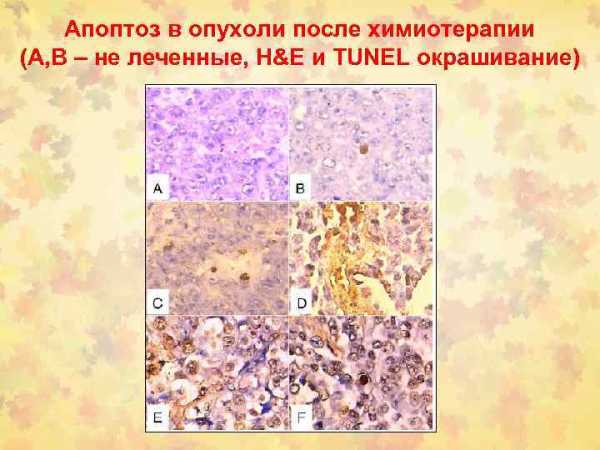 Апоптоз в опухоли после химиотерапии (А, В – не леченные, H&E и TUNEL окрашивание)
Апоптоз в опухоли после химиотерапии (А, В – не леченные, H&E и TUNEL окрашивание)
 Определение активности каспаз
Определение активности каспаз
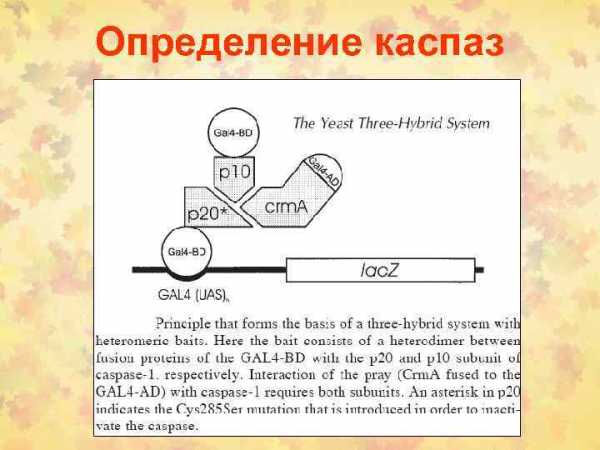 Определение каспаз
Определение каспаз
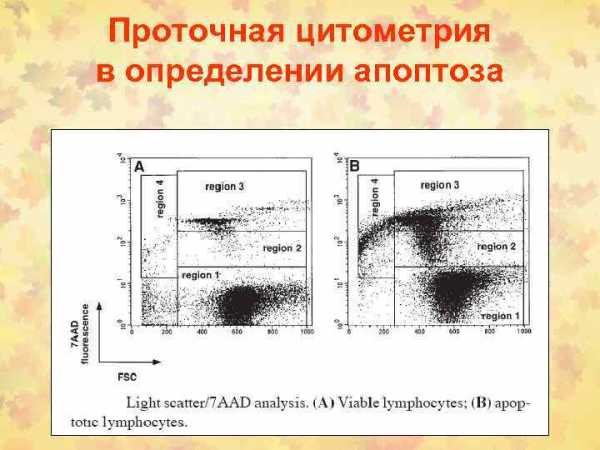 Проточная цитометрия в определении апоптоза
Проточная цитометрия в определении апоптоза
 Определение мит. апоптоза
Определение мит. апоптоза
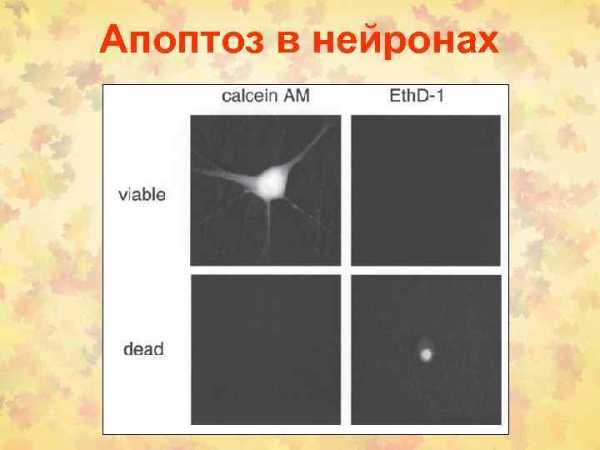 Апоптоз в нейронах
Апоптоз в нейронах
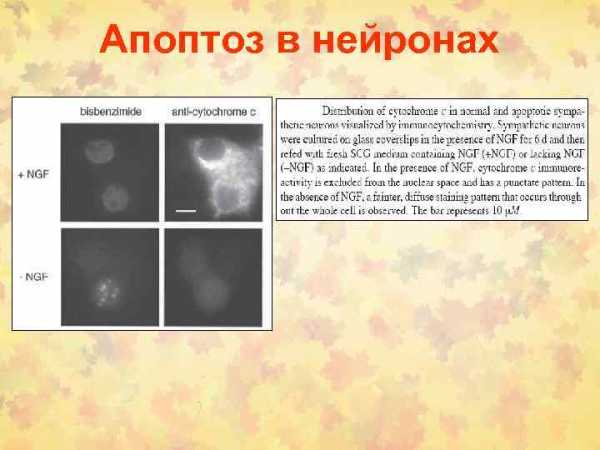 Апоптоз в нейронах
Апоптоз в нейронах
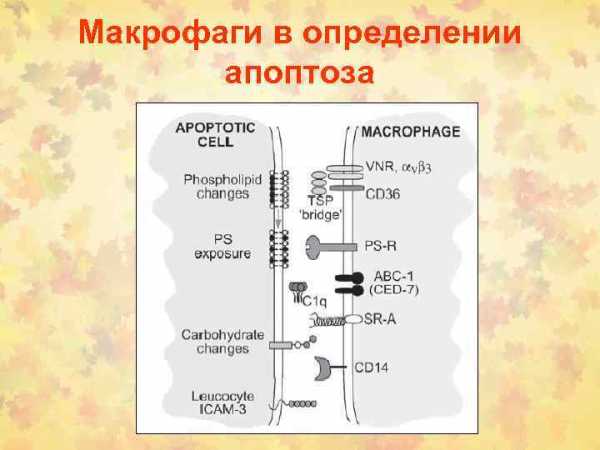 Макрофаги в определении апоптоза
Макрофаги в определении апоптоза
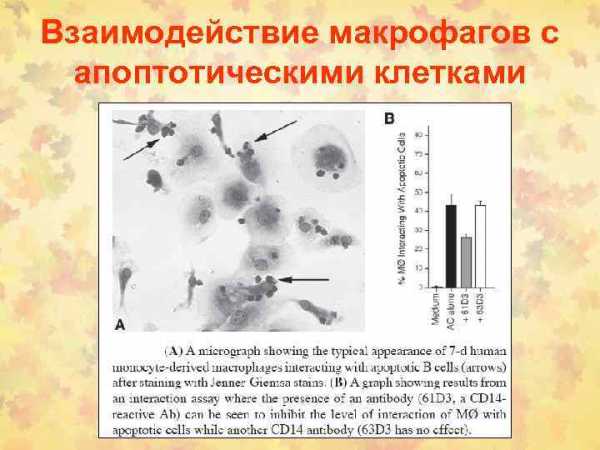 Взаимодействие макрофагов с апоптотическими клетками
Взаимодействие макрофагов с апоптотическими клетками
 Терапевтические мишени для ингибирования апоптоза (доклиническая стадия)
Терапевтические мишени для ингибирования апоптоза (доклиническая стадия)

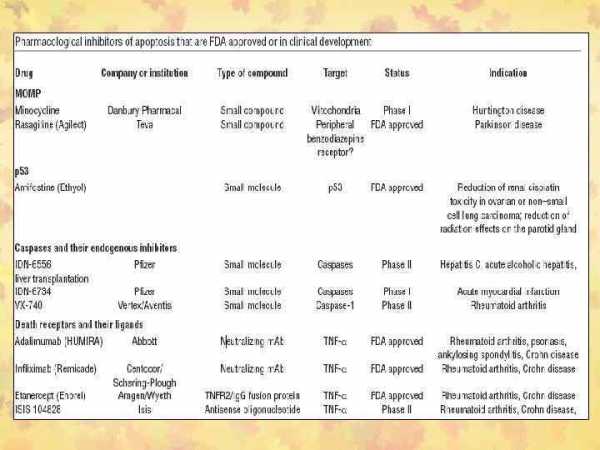
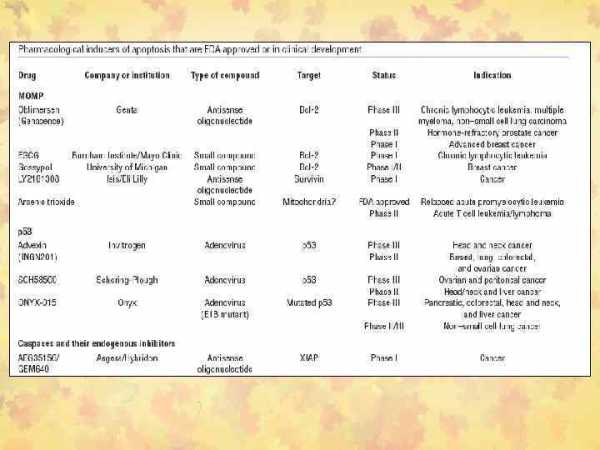
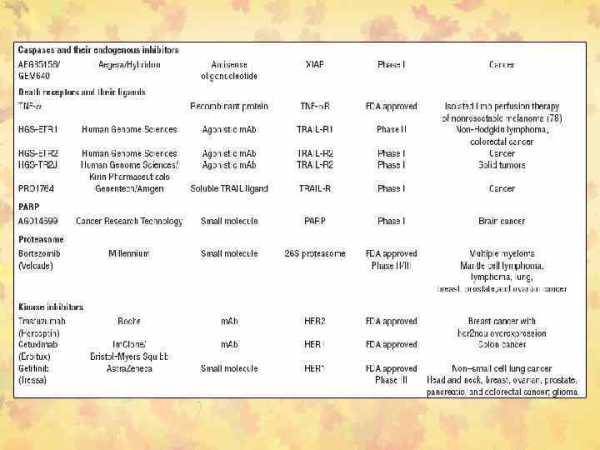


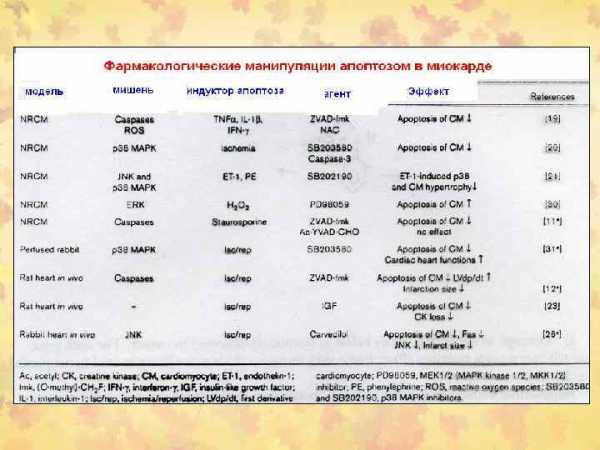
present5.com