Вся правда о метастазах. Даже при IV стадии есть шансы
Слова «рак» и «опухоль» внушают ужас каждому, кто впервые столкнулся с онкологическим диагнозом. Но иногда в ходе борьбы с тяжелой болезнью люди узнают, что есть еще более пугающее слово – «метастазы». Именно эти отсевы злокачественной опухоли являются главным врагом онкологических пациентов. К счастью, с каждым годом результаты лечения пациентов с метастатической стадией рака становятся лучше.
Все самое важное о метастазах рассказывает наш эксперт – заведующий онкологическим отделением №4 ГКОБ №1 ДЗМ, заведующий кафедрой онкологии НГИУВ, доктор медицинских наук, хирург-онколог Владимир Константинович Лядов.
Самый частый и тревожный вопрос для любого онкологического пациента – каков его индивидуальный риск развития отдаленных метастазов (то есть, отсевов клеток первичной опухоли в другие органы). Ведь именно наличие метастазов – отличительный признак последней, наиболее распространенной IVстадии рака.
Клетки, потерявшие контроль
У различных злокачественных опухолей имеются свои особенности. Недаром говорят, что каждый рак уникален. Тем не менее, есть некие универсальные черты и закономерности, которые объединяют практически любые новообразования. Например, все «злокачественные» опухоли обладают свойством метастазировать, то есть распространяться по организму. А доброкачественные опухоли развиваются только в том месте, где впервые возникли.
Любая опухоль – это разрастание клеток какого-либо органа или ткани. Клетки из-за произошедших в них генетических изменений (мутаций) теряют способность ограничивать свой рост и бурно размножаются в организме. На этом этапе опухоль еще может быть доброкачественной. Например, таковы доброкачественные новообразования (полипы) слизистой оболочки толстой кишки. Но если в результате дальнейших мутаций клетки получают возможность не только бесконтрольно делиться, но и распространяться с током лимфы и крови по всему организму, а также приживаться в других органах, давая начало новым очагам рака, то такие опухоли называются злокачественными. В тот момент, когда новые очаги опухоли обнаруживаются с помощью специальных исследований (УЗИ, компьютерная, магнитно-резонансная или позитронно-эмиссионная томография – КТ, МРТ, ПЭТ), врач может диагностировать наличие у пациента распространенной стадии онкологического заболевания. Выделяют регионарные метастазы – очаги рака в ближайших к опухоли лимфатических узлах – это признак местно-распространенного процесса. Если же новые опухоли поражают несколько органов, то это так называемые отдаленные метастазы, которые служат признаком IV, наиболее распространенной стадии рака.
В тот момент, когда новые очаги опухоли обнаруживаются с помощью специальных исследований (УЗИ, компьютерная, магнитно-резонансная или позитронно-эмиссионная томография – КТ, МРТ, ПЭТ), врач может диагностировать наличие у пациента распространенной стадии онкологического заболевания. Выделяют регионарные метастазы – очаги рака в ближайших к опухоли лимфатических узлах – это признак местно-распространенного процесса. Если же новые опухоли поражают несколько органов, то это так называемые отдаленные метастазы, которые служат признаком IV, наиболее распространенной стадии рака.
Отвоевать себе место
Многие пациенты считают, что давать отсевы могут только крупные опухоли. Это не так. Даже крошечные очаги опухолевой ткани, размер которых около одного кубического миллиметра, способны выделять свои клетки в кровоток. В крови каждого онкологического пациента есть такие циркулирующие опухолевые клетки. Но это еще не метастазы. Даже за пределами первичного очага такие клетки находятся под контролем иммунной системы, они еще не способны приживаться и расти в организме. Под влиянием определенных факторов эти клетки укореняются в других органах и могут в последующем дать начало росту метастаза. Почему так происходит – пока не полностью установлено. Например, при некоторых опухолях метастазы могут появиться через 15-20 лет после, казалось бы, успешно проведенного лечения.
Под влиянием определенных факторов эти клетки укореняются в других органах и могут в последующем дать начало росту метастаза. Почему так происходит – пока не полностью установлено. Например, при некоторых опухолях метастазы могут появиться через 15-20 лет после, казалось бы, успешно проведенного лечения.
Чтобы выжить, единичные клетки опухоли, разносимые кровью, находят в организме так называемую преметастатическую нишу, где могут находиться довольно долго. Иногда – годами. Там для них есть условия для сохранения, но пока еще нет новых сосудов, благодаря которым опухоль может питаться. Тем не менее, клетки рака с помощью специальных молекул могут создавать новые сосуды – этот процесс называется неоангиогенез. После того, как очаг опухоли с помощью процесса неоангиогенеза «подключается» к кровеносной системе, метастаз начинает бурно расти.
Метастазы поражают разные органы. Для каждого вида рака есть свои излюбленные места, куда отсев опухоли происходит в первую очередь. Так, рак предстательной железы часто метастазирует в кости. А вот при раке поджелудочной или толстой кишки появление метастазов в костях говорит уже о самой последней стадии, так как в первую очередь эти опухоли поражают печень или легкие. По-разному ведут себя даже опухоли, расположенные в различных участках одного органа. Например, новообразования толстой кишки, которые находятся справа, реагируют на одни препараты, а опухоли, расположенные слева – на другие, что обусловлено различными генетическими изменениями в клетках. Врачи используют эти знания, планируя лечение.
А вот при раке поджелудочной или толстой кишки появление метастазов в костях говорит уже о самой последней стадии, так как в первую очередь эти опухоли поражают печень или легкие. По-разному ведут себя даже опухоли, расположенные в различных участках одного органа. Например, новообразования толстой кишки, которые находятся справа, реагируют на одни препараты, а опухоли, расположенные слева – на другие, что обусловлено различными генетическими изменениями в клетках. Врачи используют эти знания, планируя лечение.
Выявить вовремя
Часто ответственность за свою жизнь и здоровье пациенты перекладывают исключительно на врачей. Но во многом это и собственная ответственность заболевшего человека. Например, некоторые пациенты, пройдя лечение по поводу опухоли и желая забыть этот тяжелый период, отказываются от дальнейшего наблюдения. Однако «прятать голову в песок», имея такое серьезное заболевание, – плохая тактика. Лишь при своевременном, раннем выявлении метастазов шансы на успешное лечение максимальны.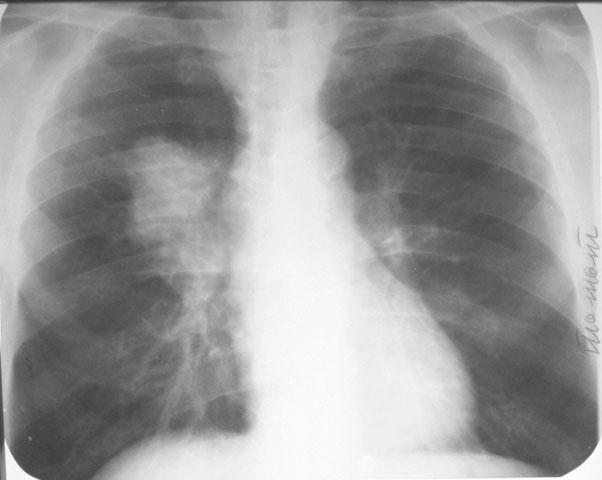
После проведенного лечения каждый пациент должен получить от врача свою схему обследования. Она зависит от вида и стадии рака, а также от тех возможностей, что есть в стране и медицинском учреждении. Наиболее интенсивное наблюдение проводится в первые годы после лечения. По российским рекомендациям в первый год обследования проводятся раз в три месяца, во второй и последующие, до истечения 5 лет – раз в полгода. Считается, что 90% метастазов появляются в течение 5 лет после проведенного лечения, поэтому по достижении пациентом этого срока его либо снимают с учета, либо переводят на наблюдение один раз в год.
У каждого метода обследования – своя точность. Если говорить грубо, то КТ позволяет выявить 90 из 100 пациентов с метастазами, а УЗИ и рентген при большинстве видов рака будут информативны лишь в 70%. Поэтому чаще всего рекомендуются различные виды томографии, позволяющие получить изображения частей тела с разрешением до 1 мм. Для усиления контрастности изображения эти исследования часто проводятся с контрастированием – пациент выпивает или получает внутривенно специальные контрастные препараты, существенно повышающие точность обследования.
Только вперед!
Лечение метастатической болезни гораздо сложнее и пока нередко менее эффективно, чем лечение первичного рака. Но это не повод от него отказываться. С каждым годом лечебных возможностей для таких пациентов становится все больше. Причем шансы у них есть не только на продление жизни, но порой даже на излечение.
Например, в России у 25-30% пациентов, страдающих раком толстой кишки, на момент диагностики сразу выявляются отдаленные метастазы. Еще 20 лет назад онкологи почти ничего не могли предложить таким больным, а сегодня каждый четвертый может претендовать на долгие годы жизни или даже полное излечение. Например, некоторые пациенты при таком диагнозе живут 10 и более лет без проявлений заболеваний.
Метастатический рак лечится теми же методами, что и первичный: с помощью хирургии, облучения и медикаментов. Но лекарственная терапия обычно наиболее эффективна, так как это системный метод лечения, позволяющий воздействовать как на видимые клетки опухоли, так и на те, которые еще нельзя распознать с помощью имеющихся методов обследования.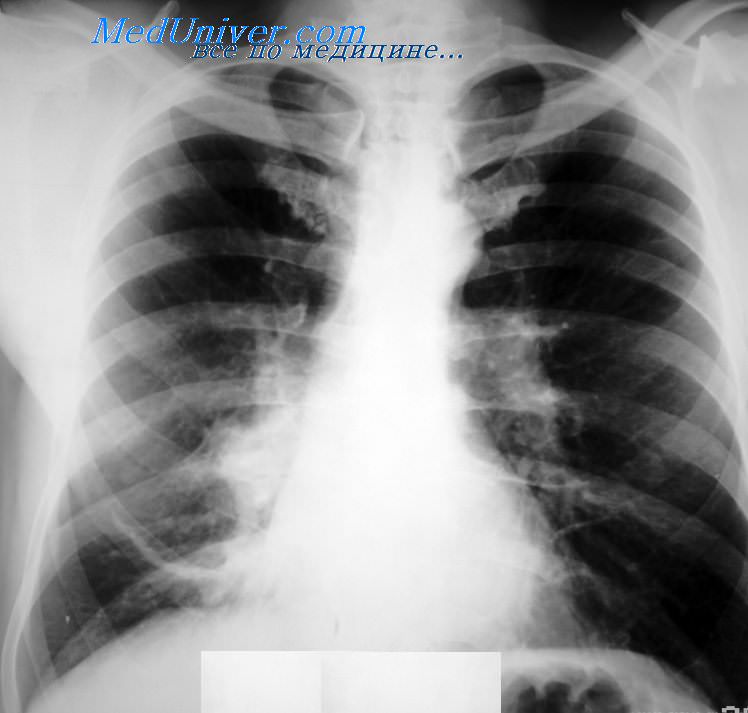
Базовое лекарственное лечение – это традиционная цитотоксическая химиотерапия, подавляющая все быстро делящиеся клетки в организме. Используемые препараты токсичны, поэтому, убивая клетки рака, они негативно влияют и на другие быстро делящиеся клетки. Прежде всего, на клетки слизистой оболочки и волосяные фолликулы. И даже несмотря на широкие возможности сопроводительной терапии, помогающей снизить выраженность побочных эффектов, это довольно агрессивный вид лечения. К счастью, сегодня есть возможность добавить к нему более индивидуальную, прицельную терапию. Это так называемые таргетные препараты, которые действуют строго на определенную молекулярную мишень в опухоли. Когда они только появились, ученые надеялись, что таргетные препараты полностью заменят химиотерапию. Но оказалось, что это пока невозможно. Зато эти два вида лечения отлично дополняют друг друга, позволяя существенно замедлять или даже останавливать рост опухоли. Например, при одном из наиболее агрессивных видов рака молочной железы уже более 15 лет применяются таргетные препараты против молекулы HER-2, которые оказались очень эффективны в отношении этого ранее абсолютно неблагоприятно протекавшего вида рака.
В последние годы были разработаны препараты, позволяющие активировать собственную иммунную систему пациента и «настроить» ее против клеток опухоли. Благодаря иммунотерапии огромная группа ранее считавшихся неизлечимыми пациентов получила надежду на исцеление! Каждый год онкологи получают все новые эффективные методы борьбы с онкологическими заболеваниями, в том числе с метастазами. Поэтому ни в коем случае не стоит отчаиваться, услышав слово «метастазы». Главное – найти команду специалистов, готовую предложить Вам все наиболее современные методики лечения.
Лечение рака 4 стадии | Онкологическая клиника De Vita в СПб
Четвертая стадия рака означает, что онкологическое заболевание прогрессирует, и опухоль дала метастазы, то есть появились вторичные очаги в отдаленных органах (кости, легкие, печень, головной мозг и др.), поэтому необходимо принимать меры и подбирать адекватное лечение. Онкология не стоит на месте, и сейчас в арсенале онкологов есть большое количество новых возможностей для лечения рака 4 стадии, которых не было пять-десять лет назад.
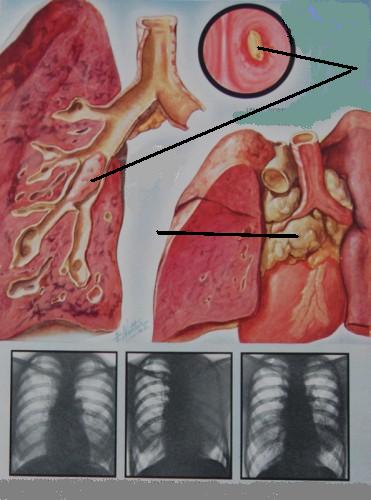 Мы помогаем всем пациентам с онкологическим диагнозом, независимо от стадии заболевания. Наш опыт показывает, что назначение адекватных и современных международных схем лечения даже при 4 стадии рака позволяет существенно продлевать жизнь пациента и улучшать его состояние.
Мы помогаем всем пациентам с онкологическим диагнозом, независимо от стадии заболевания. Наш опыт показывает, что назначение адекватных и современных международных схем лечения даже при 4 стадии рака позволяет существенно продлевать жизнь пациента и улучшать его состояние.Узнайте больше – позвоните по любому из телефонов клиники: +7 (812) 952-83-73, +7 (812) 318-59-90 — и запишитесь на консультацию к онкологу.
Какое лечение возможно при 4 стадии рака?
В настоящее время появилось множество новых противоопухолевых препаратов, которые стабилизируют метастатический процесс и не дают заболеванию прогрессировать, при этом обладают незначительными побочными эффектами.Достижения клинической онкологии сегодня позволяют онкологам активно применять таргетную и иммунотерапию при 4 стадии рака, и существенно улучшать качество жизни пациентов, продлевая ее на максимально возможный срок.
Более того, при правильно подобранной схеме лечения некоторые виды рака на 4 стадии можно перевести в разряд хронических (как сахарный диабет или бронхиальная астма).
При обширном опухолевом поражении и общей интоксикации пациент слабеет, теряет вес, у него ухудшаются показатели крови, нарастает болевой синдром, а также появляются другие тягостные симптомы. Если противоопухолевое лечение (химиотерапия, таргетная, иммунотерапия, лучевая терапия или паллиативная операция) невозможно, то пациента направляют на симптоматическое лечение по месту жительства, под наблюдение районного онколога. Симптоматическая терапия по месту жительства в государственных и муниципальных учреждениях практически не проводится, пациенты предоставлены сами себе. Если такими пациентами никто не занимается, то онкологическое заболевание стремительно прогрессирует, пациенты отправляются в хоспис или погибают дома «под наблюдением онколога по месту жительства».
А задача симптоматической терапии, какой она должна быть на самом деле, — вернуть пациента в курабельное состояние, помочь ему «выйти из ямы», реализовать скрытые резервы организма, чтобы он компенсировался.
Теперь расскажем подробнее о возможностях лечения рака 4 стадии в нашей клинике при конкретных локализациях:
Рак легких — Онкологічна клініка ІННОВАЦІЯ
К основным симптомам заболевания относятся: кашель, одышка, боль в грудной клетке, кровохарканье, потеря массы тела. Выявление большей части этих признаков должно насторожить и заставить срочно обратиться к врачу. Следует отметить, что рак легких, признаки которого являются неспецифическими, т.е. характерными для многих заболеваний органов дыхания. По этой причине, к сожалению, многие пациенты не спешат бить тревогу.
Кроме того, необходимо обращать внимание на такие косвенные признаки, как вялость, апатия, утрата должной активности, небольшое беспричинное повышение температуры тела. Последнее может маскировать рак легкого под вялотекущий бронхит или пневмонию.
Последнее может маскировать рак легкого под вялотекущий бронхит или пневмонию.
В самом начале заболевания рак легкого чаще всего скрывается под «маской» утраты жизненного тонуса, что характеризуется небольшим снижением работоспособности, повышенной утомляемостью, ослаблением интереса и апатией. В последующем у большинства больных рак легких проявляет признаки под «маской» различных респираторных заболеваний: катара дыхательных путей, повторных эпизодов гриппа, бронхита, пневмонии и т. п. Чаще всего, это уже третий период развития болезни, и в это время удается установить явления сопутствующей пневмонии. У больных периодически повышается температура тела, возникает, затем проходит и может вновь повторяться легкое недомогание. Как правило, прием жаропонижающих и противовоспалительных средств, а также так называемые «домашние методы», быстро устраняют (на некоторое время) эти явления. Только повторные приступы недомогания, повторяющиеся на протяжении 1-2 месяцев, наводят больных на мысль о необходимости обратиться за медицинской помощью.
Симптомы рака легкого могут отличаться в зависимости от ряда факторов, главными из которых являются следующие: место, где возникает первичная опухоль – в бронхе (центральный рак) или в ткани легкого (периферический рак), степень сдавливания соседствующих с опухолью органов, наличие метастазов.
Сколько живут с раком легких?
Онкологические заболевания дыхательного аппарата — это наиболее распространенная раковая патология в мире. А конкретно аденокарцинома легкого занимает самый большой сегмент в онкологии по всему земному шару. Именно поэтому вопрос, сколько живут с раком легких, столь актуален и волнует большое количество онкологических больных.
Сразу стоит акцентировать внимание на том факте, что очень точную статистику и конкретные цифры получить представляется затруднительным. Дело в том, что отличаются не только опухоли по виду, но и даже каждый конкретный вид рака у разных людей протекает по-разному, соответственно, прогнозы могут отличаться. И тем не менее, приблизительные цифры по выживаемости есть.
Причины, факторы риска
Рак легких является одной из самых агрессивных форм онкологии, рано метастазирует и никак себя не проявляет на ранних стадиях, сложно поддается терапии. Однако, заболевание имеет высоко верифицированные факторы риска, поэтому в некоторой степени поддается профилактике.
В частности, исследованиями доказано, что в 90% случаев аденокарциномы легкого больные были заядлыми курильщиками табака. Это основная причина, которая повышает риск заболеть в несколько раз. Сотни канцерогенов, содержащихся в табачном дыме, повреждают до 70% всех генов из генома человека и, что важно, только через 5 лет они в большинстве восстанавливаются.
При чем исследованиями доказано, что повреждение ДНК идет уже в первые минуты после вдыхания табачного дыма.
Кроме этого, повышают вероятность заболеть плохая экология, загрязненный воздух, гиподинамия и низкий уровень медицинского обслуживания в стране. Комплекс факторов может привести к тому, что диагностируется рак легких 4 степени. Сколько живут такие пациенты? Рассмотрим детальнее.
Продолжительность жизни при раке легких
В связи с тем, что заболевание протекает очень агрессивно и не имеет специфических начальных признаков, прогноз в основном неблагоприятный. Однако, это в значительной степени коррелирует, в зависимости от индивидуального случая.
Ключевой фактор, от которого зависит выживаемость пациента с раком легких, является стадия, на которой выявлено заболевание и качество оказанного лечения. Так, пятилетняя выживаемость всех видов онкологии на 1й стадии на 80% выше, чем у пациентов с 3 или 4 стадией. Эти же цифры в 2, а иногда и в 3 раза отличаются, если сравнивать лечение рака в странах СНГ и на западе — Европа, Израиль, США.
Не стоит недооценивать инновационные и экспериментальные методы диагностики и лечения. Благодаря многим таким методикам пациенты живут с 4 стадией рака легких, более того, получая симптоматическое лечение, не страдает и качество жизни.
Выживаемость с первой стадией рака легкого
Если заболевание было выявлено на начальной стадии (что бывает достаточно редко), 5-летняя выживаемость пациентов составляет около 60% в странах СНГ и более 85% в Израиле. Как видно, применяются современные методики лечение рака легких в Израиле, в том числе, генная терапия, применение моноклональных антител и молекулярная терапия, могут помочь сохранить пациенту жизнь.
Рак 2 стадии: сколько можно прожить?
На второй стадии аденокарцинома легких выявляется уже намного чаще. Здесь уже присутствуют определенные симптомы и закономерности, проявляются рентгенологические критерии и изменения в анализе крови. Сколько живут при раке легких 2 стадии? Прогноз 5-летней выживаемости в среднем составляет 30-40% в странах бывшего СССР и от 70% в Израиле и США. Цифры, опять же, довольно сильно колеблются.
Очень многое зависит от выбранной тактики лечения, агрессивности конкретной опухоли, наличия метастазов в сторожевых лимфоузлах, которые определяются при диагностике. Стоит отметить, что в Израиле используется позитронно-эмиссионная томография (ПЭТ-КТ), которая позволяет выявить конгломераты в лимфоузлах микро размеров, недоступные другим диагностическим методам.
Продолжительность жизни при раке легких 3 стадии
Третья стадия заболевания уже является довольно запущенной, однако, в отличие от стран СНГ, в Израиле
для онкологов нет нереализуемых задач, и от больных никто не отказывается. Сколько живут при раке легких 3 стадии? В среднем пятилетняя выживаемость в странах третьего мира составляет около 15%, в развитых странах — около 40%.Выживаемость в течение 1 года — в странах СНГ до 30%, в Израиле, Европе и США — около 55%.
Если лечиться в хорошей клинике, используя современные мировые протоколы, высокотехнологичное оборудование, очевидно, что несколько лет можно прожить даже на 3 стадии рака легкого. Кроме этого, качество жизни в случае правильного лечения, будет гораздо выше.
Рак 4 стадии: сколько живут?
В случае обнаружения рака легких на последней, запущенной стадии, прогноз неутешительный. В большинстве ситуаций все, что остается врачу — симптоматическое лечение, облегчение страданий пациента. Сколько живут с раком легких 4 стадии? Здесь статистика разнообразна. В странах СНГ, такие пациенты не доживают до 1 года почти во всех случаях. Это связано с тем, что уже есть метастическое поражение множества ближайших и отдаленных органов, полиорганная недостаточность и системные нарушения.
В странах с развитой медициной, паллиативное лечение и экспериментальная терапия может позволить прожить больным больше года. Продолжительность жизни при раке легких 4 стадии более года — это считается уже огромным достижением врачей и силой воли самого пациента.
Не смотря на пессимистические сценарии, терять надежду на излечение все же не стоит. В Израиле и других развитых странах постоянно идут новые исследования и клинические испытания новых препаратов. Это и таргетные иммунопрепараты и генная модификация клеток и использование моноклональных антител. Бывают ситуации, когда считавшиеся безнадежными больные попадают под программу таких исследований и могут участвовать в такой терапии.
Так, в 2014 году в США было полностью излечено несколько пациентов с 4й стадией рака и массовыми метастазами с помощью экспериментальной методики инъекции модифицированных Т-киллеров (иммунных клеток), которые запрограммировали на борьбу с раковыми клетками.
Основные причины смерти при раке легких
Как умирают при раке легкого? Основные причины три:
- метастазирование опухоли в жизненно важные органы;
- острая дыхательная недостаточность;
- массированное кровотечение из сосудов легких.
Так как аденокарцинома легких метастазирует в плевру, средостение и окружающие ткани — у заболевания может быть масса осложнений, которые также могут повлечь за собой летальных исход, если не будет оказана своевременная помощь.
Сколько осталось жить при метастазах в легкие? Если речь идет не о первичной опухоли в легких, а об метастазах из другого начального очага — здесь прогноз также неутешительный. Независимо от того, где находится первичная опухоль, 1-летняя выживаемость при удаленных метастазах колеблется в районе 30-40%.
Таким образом, выживаемость и прогноз при раке легкого в целом неблагоприятный, однако в значительной степени отличается, в зависимости от ряда факторов. Сколько можно прожить и главное, как, зависит от стадии болезни и от врачей, к которым попал пациент. Поэтому, доверить самое ценное для человека, жизнь, можно лишь грамотным специалистам и клинике с именем.
Лечение рака лёгких — Онкология в Белоруссии: клиники, врачи, методы
Легкие – это орган дыхания, который обеспечивает организм кислородом. Легкие разделено на доли: правое — 3 доли, левое – 2. Доли, в свою очередь, делятся на сегменты.Рак легкого — это бесконтрольный рост и размножение «опухолевых» клеток в ткани легкого.
СИМПТОМЫ РАКА ЛЕГКОГО
Рак легкого часто протекает бессимптомно, т.е. нет каких-либо особых признаков заболевания. Если опухоль уже получила значительное распространение, то к наиболее частым симптомам относятся:
-
1. Длительный кашель.
-
2. Боль в грудной клетке. Особенно усиливающаяся при глубоком вдохе.
-
3. Боли в плече, онемение пальцев рук, опущением века.
-
4. Снижение аппетита и потеря веса.
-
5. Мокрота коричневая, возможно даже с прожилками крови.
-
6. Одышка.
-
7. Лихорадка без явной причины.
-
8. Частые инфекции верхних дыхательных путей, бронхиты, пневмонии и т.д.
-
-
10. Потеря сознания, головные боли, головокружение, нарушение речи и зрения.
Также существует симптомы, которые могут указывать на распространение опухоли за пределы легких:
- Боль в костях
- Увеличение лимфатических узлов.
- Желтое окрашивание кожи и склер.
Записаться на консультацию
Единой причины развития рака легкого нет. Чаще всего это:
-
1. Табакокурение
-
2. Наследственная предрасположенность
-
3. Вредные условия труда
-
4. Хронические заболевания легких
-
5. Ионизирующая радиация
-
6. Возраст старше 50 лет
-
7. Неблагоприятная окружающая среда
-
8. Гормональные изменения
Курение, как активное — так и пассивное, является самым главный факторов развития рака легкого. У курильщиков в 5 раз увеличивает вероятность развития рака!
Разновидности рака легкого
В зависимости от вида клеток опухоли различают мелкоклеточный и не мелкоклеточный рак легкого.
НЕМЕЛКОКЛЕТОЧНЫЙ РАК ЛЕГКОГО наиболее распространен. Это до 80% от всех опухолей легких.В зависимости от строения опухоли не мелкоклеточный рак подразделяется на:
-
Опухоль из ороговевающего эпителия
-
Аденокарцинома
-
Крупноклеточная недифференцированная карцинома
Международная классификация TNM, предложенная в 1997 г. Всемирной организацией здравоохранения (ВОЗ) ввела следующие обозначения:
«N» — обозначает наличие пораженных лимфатических узлов,
«М» — наличие метастазов.
| Неопределяемая карцинома | Tх | N0 | M0 |
|---|---|---|---|
| Стадия 0 | Tis | N0 | M0 |
| Стадия I A | T1 | N0 | M0 |
| Стадия I В | T2 | N0 | M0 |
| Стадия II А | T1 | N1 | M0 |
| Стадия II В | T2 | N1 | M0 |
| Стадия III А | T1-2 | N0 | M0 |
| T3 | N2 | M0 | |
| Стадия III В | любая T | N3 | M0 |
| T4 | любая N | M0 | |
| Стадия IV | любая T | любая N | M1 |
Tis – опухоль, которая не распространяется в соседние ткани,
T1 — опухоль не более 3 см, не распространяющаяся в главный бронх;
T3 — опухоль переходящая на грудную стенку, диафрагму, плевру, перикард (оболочку сердца) или опухоль, не доходящая до области разветвления трахеи менее 2см, или с ателектазом всего легкого или пневмонией всего легкого.
T4 — опухоль, непосредственно переходящая на средостение, сердце, крупные сосуды, трахею, пищевод, тела позвонков, область разветвления трахеи.
Мелкоклеточный рак легкого
Мелкоклеточный рак легкого – это примерно 20% от всех опухолей легких. Данный вариант также известен под названиями «низкодифференцированная нейроэндокринная карцинома» или «мелкоклеточная недифференцированная карцинома».Стадии процесса:
| Неопределяемая карцинома | Tх | N0 | M0 |
|---|---|---|---|
| Стадия 0 | Tis | N0 | M0 |
| Стадия I A | T1 | N0 | M0 |
| Стадия I В | T2 | N0 | M0 |
| Стадия II А | T1 | N1 | M0 |
| Стадия II В | T2 | N1 | M0 |
| Стадия III А | T1-2 | N0 | M0 |
| T3 | N2 | M0 | |
| Стадия III В | любая T | N3 | M0 |
| T4 | любая N | M0 | |
| Стадия IV | любая T | любая N | M1 |
Tis — опухоль не распространяющаяся в соседние ткани,
T1 — опухоль не более 3 см, не распространяющаяся в главный бронх;
T2 — опухоль более 3 см, но не захватывающая все легкое и располагающаяся более 2 см от области разветвления трахеи.
T3 — опухоль переходящая на грудную стенку, диафрагму, плевру, перикард (оболочку сердца) или опухоль, не доходящая до области разветвления трахеи менее 2см, или с ателектазом всего легкого или пневмонией всего легкого.
T4 — опухоль, непосредственно переходящая на средостение, сердце, крупные сосуды, трахею, пищевод, тела позвонков, область разветвления трахеи.
Кроме данной классификации, также широко используется 2х стадийная «VALG» — классификация:
-
1. Локализованный (ограниченный) опухолевый процесс
-
Стадии 0 — III B: заболевание ограниченное одной половиной грудной клетки.
-
2. Распространенная форма опухолевого процесса (стадия IV).
Основным методом лечения рака легкого является хирургический.
Объем операции определяется после обследования и зависит от локализации опухоли в легком и ее распространенности. При периферическом раке чаще выполняется удаление доли легкого (лобэктомия), при центральном – удаление легкого (пневмонэктомия).
В некоторых случаях при центральном раке выполняются бронхопластические операции, при которых удается сохранить долю легкого с наложением межбронхиального анастомоза. При вовлечении в опухоль грудной стенки или анатомических структур средостения выполняются комбинированные операции с резекцией этих структур. Развитие анестезиологии и хирургии сделало возможным в настоящее время выполнение сложных хирургических вмешательств на трахее, а также на легких и сердце с применением искусственного кровообращения.
Использование видеоторакоскопической техники позволяет выполнить резекцию легкого или удаление доли легкого через небольшие разрезы грудной стенки и уменьшить травматичность операции.
После хирургического лечения рака легкого может потребоваться проведение дополнительной химиотерапии или лучевой терапии.
После проведения лечения требуется курс реабилитации и диспансерное наблюдение: первый год каждые 3 месяца осмотр, рентгенография органов грудной клетки в 2-х проекциях, УЗИ органов брюшной полости
Выбор метода лечения — это очень важный этап. Решение специалиста всегда основываться на точных данных диагностики заболевания и индивидуальных особенностей пациента. Общая программа лечения обязательно обсуждается с пациентом и, по его желанию, с его близкими.
Записаться к специалисту
Рак лёгких — диагностика и лечение в центре онкологии ЕМС в Москве
Рак легкого, или бронхогенная карцинома, – злокачественное новообразование, происходящее из ткани бронхов или легочной паренхимы. Рак легких – одно из наиболее распространенных онкологических заболеваний у мужчин и женщин во всем мире.
Виды рака легкого
-
Мелкоклеточный рак легкого (МКРЛ) диагностируется у 10-15% пациентов. Имеет тенденцию к более агрессивному течению, быстрому распространению, рецидивам.
-
Немелкоклеточный рак легкого (НМКРЛ) включает в себя все остальные виды рака легкого и диагностируется у 85-90% пациентов. НМКРЛ имеет подкатегории, наиболее распространенными среди которых являются аденокарцинома и плоскоклеточный рак. Этот вид рака легких нередко является показанием к хирургическому лечению, особенно на ранних стадиях заболевания.
Мелкоклеточный и немелкоклеточный рак лёгкого предполагают разные подходы к хирургическому лечению, лучевой и химиотерапии. До недавнего времени простое гистологическое разделение НМКРЛ и МКРЛ наряду со стадией было адекватным для принятия решения о лечении при впервые установленном диагнозе рака легкого. Сегодня уже доказано, что для определения оптимальной терапии важно отличать аденокарциному, плоскоклеточную карциному и другие гистологические формы опухоли.
Симптомы рака легкого
На ранних стадиях заболевания, при которых лечение будет наиболее эффективным, симптомы незначительны и отсутствуют, что подчеркивает актуальность скрининговых исследований у пациентов, имеющих высокий онкологический риск.
Наиболее частыми клиническими проявлениями рака легкого являются:
-
Кашель – у 50-75 % пациентов
-
Кровохарканье – у 25-50 % пациентов
-
Одышка – у 25 % пациентов
-
Боль в груди – у 20 % пациентов
Появление симптомов, как правило, свидетельствует о далеко зашедшем процессе.
Реже рак легкого может проявляться отклонениями в лабораторных показателях вследствие метастазирования в другие органы (чаще всего в печень, кости, головной мозг) или паранеопластическим синдромом – это комплекс проявлений, не связанных непосредственно с опухолью, но вызванных воздействием раковых клеток на организм.
Паранеопластический синдром включает:
-
гиперкальциемию (повышение концентрации кальция в плазме крови),
-
синдром Кушинга (повышенное выделение гормона кортизола корой надпочечников),
-
гиперкоагуляционные нарушения (усиление свертываемости крови),
-
различные неврологические синдромы (нарушения координации, проблемы с равновесием, трудности при ходьбе, затрудненная речь, глотание и т.д.).
Мелкоклеточный и немелкоклеточный рак легкого могут проявляться одинаковыми симптомами. Но для мелкоклеточного рака характерны:
-
быстрое прогрессирование симптомов,
-
паранеопластический синдром,
-
объемные множественные метастазы в медиастинальные лимфоузлы,
-
синдром верхней полой вены,
-
костные метастазы и метастазы в головной мозг.
Тогда как синдром Панкоста (слабость и боль в руке, вызванная прорастанием опухоли верхней доли легкого в плечевое сплетение) и гиперкальциемия чаще обнаруживаются у пациентов с немелкоклеточным раком легкого.
Диагностика рака легкого
Пациенту с подозрением на рак лёгкого назначается компьютерная топография (КТ) грудной полости и верхних отделов брюшной полости (обычно с контрастированием) для оценки степени распространенности первичной опухоли и возможного распространения в средостение, печень и надпочечники.
Окончательный диагноз рака устанавливается только на основании цитологического исследования (например, плевральной жидкости) или гистологического исследования (биопсии ткани).
Биопсия может быть выполнена одним из следующих способов:
-
Бронхоскопия
-
Эндобронхиальная ультразвуковая бронхоскопия, или EBUS, — техника, которая сочетает в себе применение гибкого бронхоскопа с ультразвуком
-
Тонкоигольная биопсия под контролем КТ
-
Игольная аспирация
-
Торакоцентез
- В том случае, если другие процедуры биопсии не позволили определить диагноз, может потребоваться операция. Наиболее распространенными хирургическими процедурами являются медиастиноскопия, которая используется для биопсии лимфатических узлов в центральной части грудной полости; видео-ассистированная торакоскопическая операция (VATS) — менее инвазивный метод для биопсии легочной ткани; и торакотомия, которая представляет собой полостную операцию по удалению крупных частей легочной ткани или опухолей.
Радиолог, специалист по диагностике онкологических заболеваний Института онкологии EMC профессор Евгений Либсон (Израиль) имеет многолетний опыт проведения тонкоигольных биопсий под контролем КТ, что позволяет многим пациентам избежать открытой операции, выполняемой с диагностической целью.
После биопсии материал отправляется в Гистологическую лабораторию EMC для установки точного диагноза и получения важных характеристик опухоли, которые помогают в дальнейшем выборе лечения.
При необходимости или по желанию пациента проводится верификация диагноза в ведущих клиниках США, Великобритании, Израиля, Германии, Франции, Швейцарии (методом телепатологии). Получение «второго мнения» зарубежного специалиста входит в стандартную стоимость исследования.
Молекулярный анализ опухоли
В Институте онкологии EMC проводится также молекулярный анализ опухоли для определения специфических биомаркеров опухоли или генных мутаций. Это позволяет составить так называемый «молекулярный портрет» опухоли и проводить терапию таргетными препаратами, которая даёт лучший эффект, чем стандартная химиотерапия. Наиболее распространенными биомаркерами рака лёгкого являются мутации EGFR, транслокации ALK и транслокации c-ROS онкогена 1 (онкогена ROS1).
Стадирование
После установления диагноза необходимо провести дообследование для правильного стадирования заболевания. С этой целью могут быть назначены:
-
Ультразвуковые исследования плевральных и брюшной полости, сосудов, лимфатических узлов (для диагностики распространения и вызванных опухолью осложнений)
-
МРТ головного мозга (при наличии неврологической симптоматики)
-
Рентген тазовой области (при боли в области таза)
-
Эхокардиография для оценки злокачественного плеврального выпота (при наличии гипотензии с синусовой тахикардией).
Лабораторные исследования
При подозрении на рак легкого по данным КТ выполняются следующие исследования:
-
Общий анализ крови
-
Электролиты
-
Кальций
-
Щелочная фосфатаза
-
АЛТ, АСТ, билирубин общий
-
Креатинин
-
Общий белок, альбумин и лактатдегидрогеназы (не обязательно)
-
Коагулограмма
Клинический осмотр и лабораторные исследования проводятся для выявления возможных метастазов. Отклонения лабораторных показателей от нормы являются основанием для назначения дополнительных инструментальных исследований.
В EMC применяется современный высокоточный метод стадирования рака легкого — ПЭТ/КТ всего тела. ПЭТ/КТ проводится пациентам с I, II и III стадией заболевания, обязательно проведение исследования перед операцией. ПЭТ/КТ может обнаружить очаги опухоли в лимфатических узлах, не детектируемые с помощью КТ, а также отдаленные метастазы в других органах. Зачастую по результатам ПЭТ/КТ пересматривается первоначальная стадия и тактика лечения.
Стадии немелкоклеточного рака легкого определяются исходя из следующих факторов:
-
размера и расположения опухоли
-
распространения опухоли в лимфатические узлы и ткани внутри грудной полости
-
распространения опухоли за пределы грудной полости (например, рак лёгкого может метастазировать в кости, печень, надпочечники или другие органы).
Стадии немелкоклеточного рака легкого варьируются от I до IV:
-
Стадия I – диаметр опухоли меньше или равен 3 см, опухоль не распространилась ни в какие другие ткани или лимфоузлы.
-
Стадия II – Стадия II означает, что опухоль имеет размер от 3 до 7 см или распространилась в лимфоузлы, или проникла в ткани, окружающие лёгкое, или начала прорастать в просвет бронхов.
-
Стадия IIIA – Стадия IIIA заболевания означает, что опухоль может быть больше 7 см или распространяться в лимфатические узлы в центре грудной полости (средостения), или проросла в ребра, сердце, пищевод или трахею.
-
Стадия IIIB – Стадия IIIB заболевания означает, что опухоль распространилась на лимфатические узлы за пределами средостения или в лимфатические узлы выше или ниже ключицы. К стадии IIIB также относят опухоли, которые распространились на ребра, сердце, пищевод или трахею без вовлечения лимфоузлов средостения.
-
Стадия IV – Стадия IV означает, что рак распространился за пределы грудной полости или на противоположную сторону средостения. На IV стадии рак может привести к скоплению жидкости вокруг легкого или сердца (злокачественный выпот).
Стадии мелкоклеточного рака лёгкого. Техническое разделение мелкоклеточного рака на стадии происходит точно так же, как и для немелкоклеточного рака. Однако варианты лечения обычно определяются по более простой схеме. Обычно мелкоклеточный рак лёгкого характеризуют как «ограниченный» или «распространенный» процесс.
-
ограниченный процесс – это мелкоклеточный рак лёгкого, который ограничен одной стороной грудной полости и поражением регионарных лимфоузлов.
-
распространенный процесс – это мелкоклеточный рак лёгкого, который распространился на противоположную сторону грудной клетки и другие органы за пределами грудной клетки.
Лечение рака легкого
В Институте онкологии EMC реализованы все возможности для оказания помощи пациентам с раком легкого по международным стандартам.
Лечение рака легкого в EMC:
-
Международная команда врачей: специалисты с опытом работы в США, Израиле, Западной Европе.
-
Каждый клинический случай обсуждается на мультидисциплинарном консилиуме. Команда специалистов, включающая в себя онкологов, хирургов, радиологов, морфологов, лучевых терапевтов, определяет тактику лечения индивидуально для каждого пациента.
-
Комплексная диагностика (КТ, МРТ, ПЭТ/КТ)
-
Химиотерапия по современным европейским и американским протоколам, препараты последнего поколения ведущих мировых производителей.
-
Таргетная терапия, основанная на молекулярном анализе опухоли
-
Иммунотерапия
-
Новейшие системы для проведения лучевой терапии и стереотактической лучевой терапии Varian EDGE, Truebeam, США.
-
Психотерапевтическая поддержка пациента и его семьи.
Ранние стадии рака лёгкого обычно поддаются хирургическому лечению с удалением опухоли и окружающей ткани лёгкого. На III стадии рака лёгкого часто показано комбинированное лечение — сочетание химиолучевой терапии и хирургической операции на различных этапах терапии. Если рак распространился за пределы грудной полости (стадия IV), химиотерапия и лучевая терапия применяются для контроля заболевания и его симптомов.
Для пациентов с МКРЛ системная химиотерапия является одним из наиболее важных компонентов лечения, поскольку практически у всех пациентов на момент обращения уже имеет место распространенный МКРЛ. Для пациентов с ограниченной стадией применяется лучевая терапия грудной полости в сочетании с химиотерапией. Часто проводится профилактическая лучевая терапия на головной мозг, чтобы снизить частоту развития метастазов в головном мозге и увеличить выживаемость. Профилактическая лучевая терапия в области головы и грудной клетки также может иметь положительное воздействие у пациентов с полным или частичным ответом на первичную системную химиотерапию.
Хирургическое лечение рака легкого
Хирургическая резекция обеспечивает наилучшую длительную выживаемость и нередко полное излечение у пациентов с немелкоклеточным раком легкого. Однако даже при наличии опухоли, поддающейся удалению, пациент может быть «неоперабельным» ввиду недостаточности функции лёгких или из-за сопутствующих заболеваний, поэтому всестороннее обследование имеет большое значение при подготовке к операции.
Хирургические вмешательства у пациентов с подозрением или установленным диагнозом рака легкого могут быть различными по объему и целям, которые необходимо достичь в результате операции. Прогнозирование объема операции проводится по результатам обследования и совместным решением междисциплинарного консилиума EMC.
При подозрении на рак легкого и невозможности взятия материала для гистологического исследования может понадобиться диагностическая операция:
- Биопсия лимфатических узлов средостения.
Выполняется с использованием современных малоинвазивных технологий – видеомедиастиноскопии или видеоторакоскопии с малыми хирургическими разрезами (1-2 см) и минимальной травмой мышц и других тканей. Операция, как правило, хорошо переносится, длительность госпитализации редко превышает 2-3 дней.
- Биопсия легкого.
Также может быть выполнена видеоторакоскопическим доступом.
Существуют хирургические вмешательства, направленные на удаление плевры или индукцию плевродеза (спаечного процесса в плевральной полости). Проведение таких операций помогает купировать осложнения, связанные с поражением плевры метастазами и развитием рецидивирующего плеврита. Такие осложнения могут не только препятствовать проведению химиотерапии, но и угрожать жизни.
Выбор метода радикального хирургического лечения рака легкого зависит от локализации опухоли, ее размеров, признаков прорастания соседних структур и поражения лимфатических узлов. По объему можно выделить следующие операции:
-
Лобэктомия
-
Пневмонэктомия
-
Билобэктомия и лобэктомия с бронхопластикой или ангиопластикой
-
Сегментэктомия
При выявлении рака легкого на ранней стадии, когда нет прорастания соседних органов и размеры опухоли менее 5-6 см, возможно выполнение операции малоинвазивным доступом – с использованием видеоторакоскопии и малых разрезов.
Лучевая терапия рака легкого в EMC
Стереотаксическая радиохирургия SBRT (Stereotactic Body Radiation Therapy), известная также как SABR (Stereotactic Ablative Body Radiotherapy) является эффективным и безопасным неинвазивным методом лечения немелкоклеточного рака легкого 1 стадии, то есть опухолей размером до 5 см и с интактными лимфатическими узлами). Исследования показали равноценную общую выживаемость и локальный контроль над опухолью при сравнении хирургии (лобэктомии, стандарта лечения на сегодняшний день) и SBRT у пожилых или неоперабельных по сопутствующей патологии пациентов.
Используется от 3 до 5 сеансов (фракций) SBRT.
Центр лучевой терапии EMC под руководством главного радиотерапевта г. Москвы д-ра Нидаля Салима является одним из немногих отделений радиотерапии в мире, где метод стереотаксической радиохирургии используется при лечении первичных и метастатических опухолей легкого, печени, предстательной и поджелудочной железы, головного и спинного мозга и костей. В Центре установлены новейшие системы лучевой терапии EDGE и Truebeam, США, которые позволяют применять самые современные методы лучевого лечения.
Современные технологии в лучевой терапии, такие как IMRT, VMAT/RapidArc, IGRT, позволяют повысить точность облучения и сохранить окружающие опухоль здоровые ткани.
При облучении опухолей легкого, особенно локализующихся в нижних долях, наблюдается высокая подвижность очага на разных фазах дыхания. Применение технологии Gated RapidArc дает возможность облучать опухоль с учетом ее реального отклонения на всех фазах дыхания либо временно останавливать облучение при вдохе/выдохе за пределами заданного интервала.
Опухоль Панкоста лечение
Опухоль Панкоста (опухоль верхней борозды лёгкого) относится к немелкоклеточному раку легкого, который расположен в верхней части легкого. Опухоль затрагивает нервы, вызывая характерные симптомы, такие как:
-
Боль в плече или в руке
-
Мышечная слабость в руке
-
Гиперемия и чрезмерное потоотделение на одной стороне лица
По мере прогрессирования опухоли происходит опущение века (птоз), и полностью прекращается потоотделение на стороне поражения. При отсутствии отделенных метастазов, лечение опухоли Панкоста состоит из химиолучевой терапии и последующей операции.
Лечение рака легких IV стадии
Пациенты с IV стадией заболевания обычно получают лечение системными средствами или симптоматическую паллиативную терапию. У должным образом отобранных пациентов химиотерапия, молекулярная таргетная терапия и/или иммунотерапия могут увеличивать выживаемость без ущерба качеству жизни. Некоторым пациентам целесообразно проведение лучевой терапии и операции в качестве симптоматического паллиативного лечения.
У пациентов с IV стадией заболевания с отдаленными метастазами (например, в головном мозге, надпочечниках), благоприятное влияние может оказать резекция метастазов, а также агрессивное лечение первичной опухоли.
В Институте онкологии EMC созданы все возможности для оказания помощи пациентам с метастатическим раком легкого, в том числе применение новейших препаратов для иммунотерапии (Ниволумаб, Пемброзилумаб), которые продемонстрировали эффективность в повышении выживаемости у пациентов с IV стадией заболевания.
Для улучшения качества жизни пациентов с IV стадией заболевания применяется паллиативная терапия. Мы оказываем всю необходимую помощь тяжелобольным пациентам, включая адекватное обезболивание, проведение паллиативных операций и лучевой терапии, в том числе в экстренном режиме. Одышка в результате полного вовлечения центральных дыхательных путей может поддаваться паллиативному лечению путём удаления опухоли с помощью жёсткого или гибкого бронхоскопа и лазерной коагуляции или криотерапии. Стентирование может потребоваться для поддержания проходимости дыхательных путей, и чтобы создать условия для наружной дистанционной лучевой терапии.
Прогноз при раке легкого
Для пациентов с немелкоклеточным раком легкого фактором, который оказывает наибольшее влияние на прогноз, является стадия по TNM на момент обращения. Выживаемость прогрессивно снижается при более высокой степени заболевания, составляя, в среднем, от 59 месяцев для пациентов с IA стадией заболевания до четырёх месяцев для пациентов с IV стадией.
Клинические признаки на момент установления диагноза также позволяют прогнозировать выживаемость, независимо от стадии болезни. Большинство таких факторов было выявлено в исследованиях, которые преимущественно включали в себя пациентов с прогрессирующими или неоперабельными формами НМКРЛ. Было установлено, что низкая работоспособность и потеря веса связаны со сниженной выживаемостью. Сниженный аппетит, фактор, предшествующий потере веса, также имеет негативное прогностическое значение.
Наиболее важным прогностическим фактором у пациентов с МКРЛ служит степень распространенности заболевания на момент обращения. Для пациентов с ограниченными стадиями болезни средняя продолжительность жизни составляет от 15 до 20 месяцев, пятилетняя выживаемость составляет 10-13%. Для пациентов с прогрессирующими стадиями заболевания средняя продолжительность жизни составляет 8-13 месяцев, а пятилетняя выживаемость — 1-2%. Необходимо учитывать, что это среднестатистические показатели, прогноз в каждом отдельном случае индивидуален.
Факторы риска
Среди всех факторов риска развития рака легкого лидирующая роль принадлежит курению, которое «отвечает» за 90 % случаев развития рака легкого. Риск заболеть раком легкого у человека, выкуривающего пачку сигарет в день на протяжении 40 лет, в 20 раз выше, чем у некурящего. Наличие других канцерогенных факторов, как например, воздействие асбеста, дополнительно увеличивает риск заболевания.
Отказ от курения снижает вероятность развития заболевания, особенно у тех, кто бросил курить в возрасте до 30 лет. Но у бывших курильщиков риск заболеть раком легкого с возрастом выше, чем у тех, кто не курил никогда.
Среди других доказанных факторов риска:
-
Лучевая терапия на область легких. Риск развития рака легких выше у пациентов, которые ранее проходили лучевую терапию по поводу другого онкологического заболевания (в частности, у пациентов, которым проводилась лучевая терапия при раке молочной железы и лимфоме Ходжкина)
-
Экзогенные токсины (асбест, радон, мышьяк, хром, никель, ионизирующее излучение, полициклические ароматические углеводороды, а также пассивное курение).
-
Пневмосклероз (фиброз легких) – по результатам нескольких исследований, риск заболеть раком легких примерно в семь раз выше у пациентов, страдающих легочным фиброзом.
-
ВИЧ-инфекция
-
Генетическая предрасположенность
Роль алкоголя в развитии рака легких требует дальнейшего изучения. Попытки снизить заболеваемость у групп высокого риска с помощью диеты (антиоксидантов, фитоэстрогенов) пока не увенчались успехом. Напротив, в ходе одного из исследований было доказано, что прием курильщиками бета-каротина в составе витаминных препаратов привел к увеличению заболеваемости.
Скрининг рака легкого
Скрининг — исследование, позволяющее выявить заболевания до появления симптомов. До недавнего времени скрининг рака легкого не был широко распространен, так как по результатам нескольких исследований рентгенография грудной клетки и цитологическое исследование мокроты не приводили к снижению смертности от рака легкого.
За последние несколько лет появились более точные методы исследования, такие как низкодозовая компьютерная томография легких. Лучевая нагрузка при проведении данного исследования в 5-10 раз меньше по сравнению со стандартной КТ, что позволяет использовать метод в качестве скрининга.
В результате крупного исследования, проведенного Национальным институтом рака США было установлено, что низкодозовая КТ, проводившаяся курильщикам со стажем, позволила снизить смертность от рака легких на 20% по сравнению с курильщиками, которым в аналогичном режиме выполнялась рентгенография грудной клетки.
На сегодняшний день этот метод рекомендован специальной комиссией США по профилактике заболеваний (United States Preventive Service Task Force — USPSTF) для скрининга рака легкого людям в возрастной группе от 55 до 80 лет и которые при этом имеют 30-летнюю историю курения или бросили курить не более чем 15 назад.
EMC одним из первых центров в России внедрил в практику низкодозовую КТ легких для ранней диагностики рака легкого.
Рак лёгких — лечение за границей
Рак лёгких (бронхиальная карцинома) – это второе по частоте встречаемости онкологическое заболевание у мужчин и третье по частоте встречаемости — у женщин. По сравнению с другими онкозаболеваниями, ежегодно регистрируется больше всего случаев смертности от рака лёгких. Рак лёгких, как правило, развивается из клеток слизистой оболочки бронхиального дерева. В зависимости от внешних характеристик и архитектоники злокачественных клеток, под микроскопом различают мелкоклеточную бронхиальную карциному (рак лёгких) и немелкоклеточную бронхиальную карциному. Немелкоклеточные бронхиальные карциномы составляют ок. 85% от всех онкозаболеваний лёгких.
Курение и пассивное курение – это несомненно самые важные факторы риска возникновения рака лёгких. Другими известными факторами риска является радон, один из радиоактивных благородных газов, который естественным образом выделяется из почвы и вдыхается лёгкими человека, а также загрязнение атмосферного воздуха мелкодисперсной пылью и частицам твердого углерода.
Рак лёгких на ранней стадии в большинстве случаев практически не даёт о себе знать и протекает малосимптомно. По этой причине многие опухоли обнаруживают случайно при рутинном исследовании или уже на поздней стадии. Устойчивые жалобы на проблемы с дыхательными путями (более 4 недель) это тревожный сигнал, требующий обязательного обследования. К этим жалобам относится кашель, мокрота, осиплость (хрипота) и боли в грудной клетке. Следует немедленно обратиться к врачу, если у Вас появился кашель с кровью или есть примесь крови в мокроте (кровохарканье). Чувство усталости, потеря веса и физическая и мышечная слабость – могут быть общими симптомами, указывающими на онкологическое заболевание.
Для диагностики рака лёгких сначала делают рентген лёгких. При наличии подозрительных очагов в лёгких проводят дополнительные исследования, такие, как бронхоскопия и компьютерная томография.
Выбор лечения при раке лёгких зависит от вида рака и стадии заболевания. Если опухоль можно удалить оперативным путём, то хирургическое лечение будет иметь приоритет. Для принятия решения об операбельности опухоли важную роль имеет локализация опухоли и общее состояние пациента. Немелкоклеточная бронхиальная карцинома часто поддается удалению хирургическим путём, в то время как мелкоклеточная карцинома к моменту её обнаружения, к сожалению, в большинстве случаев уже даёт метастазы. Поэтому для этой разновидности опухоли предпочтительна химиотерапия и лучевая терапия (облучение). Хотя препараты новейшего поколения позволяют достичь существенного прогресса в лечении рака лёгких, но на поздних стадиях заболевания часто возможно только паллиативное лечение.
Уход в конце жизни пациентам с далеко зашедшими легкими рак
Реферат
Несмотря на успехи в обнаружении, патологической диагностике и лечении рак легких, у многих пациентов все еще развивается прогрессирующий, неизлечимый и прогрессирующий смертельная болезнь. Как врач, обязанность иногда лечить, часто облегчать и комфорт всегда должен быть постоянным напоминанием нам о потребностях, которые необходимо удовлетворить при уходе за больным раком легких. Четыре ключевые области ухода за пациентами в конце жизни при запущенном раке легких начните с первого распознавания того, «когда пациент приближается к концу жизни ».Врач должен уметь распознать, когда акцент в уходе необходимо сместить с агрессивного подхода к поддержанию жизни на подход, который помогает подготовить и поддержать пациента и членов его семьи через период прогрессивного, неизбежного упадка. Как только потребности будут признаны, Вторая ключевая область — это надлежащее общение, в котором врач должен оказывать помощь. пациенты и члены их семей понимают, в каком состоянии они находятся траектория и чего ожидать. Это включает в себя развитие взаимопонимания, ломку плохого новости, управление ожиданиями и навигация по планам ухода.Впоследствии третий ключевой областью является управление симптомами, которое фокусируется на целях, прежде всего, обеспечить комфорт и достоинство. Симптомы, которые часто встречаются к концу жизни у рак легких включает боль, одышку, делирий и респираторные выделения. Такой симптомы необходимо предвидеть и своевременно устранять соответствующими лекарства и объяснения пациенту и семье. Наконец, для того, чтобы врачей, чтобы обеспечить качественную помощь в конце жизни, необходимо понимать этические принципы, применяемые к вмешательствам по уходу за пациентами в конце жизни.Заблуждения об эвтаназии по сравнению с удержанием или отказом жизнеобеспечивающие методы лечения могут причинить врачу неудобства и неуместные принимать решение.
Ключевые слова: помощь в хосписе, новообразование легких, медицинская этика, паллиативная помощь, отношения между врачом и пациентом, неизлечимая помощь
Введение
Рак легких является наиболее распространенным видом рака, а также наиболее частой причиной рака смерть в современном мире [мир Организация здравоохранения, 2013]. Несмотря на успехи в обнаружении, патологическая диагностика и лечение рака легких, у многих пациентов все еще развивается запущенная, неизлечимая и прогрессирующая со смертельным исходом болезнь.Для большинства пациентов с рак легких, диагноз часто ставится на стадиях III и IV, когда выживаемость все еще очень плохой, с общей 5-летней выживаемостью от 9,5% до 16,8%. Данные из Соединенное Королевство показало, что 67,6% всех пациентов с раком легких имели болезнь III и IV стадии на первоначальный диагноз. В США данные SEER с 2004 по 2010 год зарегистрировали 79% легких. раковые больные на момент постановки диагноза находились на стадии III и IV [Cancer Research UK, 2013; Национальный институт рака SEER программа, 2014]. В Китае проведено популяционное исследование немелкоклеточного легкого. рака в Шанхае, зарегистрировано 76.4% пациентов, которым поставлен диагноз с 2011 по 2013 гг., Находились на стадия III или IV [Fan et al. al. 2015]. Хотя в лечение рака легких, особенно немелкоклеточного рака легких, с прогресс в ингибиторах тирозинкиназы, это привело лишь к незначительным улучшениям в Общая выживаемость. Следовательно, по-прежнему справедливо заявить, что в настоящее время подавляющее большинство пациентов с раком легких в конечном итоге умрут от своей болезни в 5 лет диагностики.
Исследования также показали, что с годами наблюдается тенденция к увеличению среди онкологов продолжать агрессивную онкологическую помощь пациентам, столкнувшимся с последними месяца жизни и с быстрым развитием противораковой терапии, эта тенденция скорее всего, продолжится [Эрл et al. 2004]. Поэтому важно, чтобы любой клиницист, который ведет лечение пациентов с раком легких, должен быть знаком и внимателен к потребности пациентов, которым угрожает конец жизни, поскольку они включают большую часть лечение рака легких.
Когда пациент находится на «конце жизни» и что такое «уход в конце жизни»?
Клиницисты, исследователи и политики в области здравоохранения часто пытаются разделить аккуратные определения с четкими временными рамками, чтобы выявить потребности и определить роли. Однако есть ли временные рамки для определения ухода за пациентами в конце жизни (EOLC)? когда это должно произойти? В настоящее время нет единого мнения относительно определения или времени рамка для «конца жизни». Как правило, многие считают окончание жизни последним. дней до 1–2 недель жизни.В Великобритании руководство Генерального медицинского совета (GMC) относится к пациентам, приближающимся к концу жизни, когда они, вероятно, умрут в следующие 12 месяцев [GMC, 2010; Идзуми et al. 2012]. В США Medicare определяет необходимость для ухода в хосписе в конце жизни как последние 6 месяцев жизни [Национальный хоспис и паллиатив Организация опеки, 2014]. Многие определения, использующие временные рамки, являются исходя из продолжительности жизни пациента; однако выживание — это то, что может никогда не может быть предсказан с большой точностью и действительно является ретроспективным результатом.Следовательно, если бы врач использовал такие определения для выявления пациентов, которым требуется ЭОЛЦ, он понадобится хрустальный шар или ясновидящий, чтобы найти нужного пациента получили соответствующую помощь. Поэтому, когда мы сосредотачиваемся на жестком определении, используя модель дихотомического намерения (), многие пациенты, нуждающиеся в ЭОЛК, будут пропущены, а многие физические, неудовлетворенные психосоциальные и духовные потребности.
Модель дихотомического намерения.
Таким образом, определение EOLC должно основываться на потребностях пациента, а не чем временные рамки.Это можно увидеть в модели комплексного лечебно-паллиативного лечения. намерение (). Следовательно, независимо от временных рамок и активных вмешательств, которые могут проводиться, пациенты с проблемами и потребностями, связанными с этим опасным для жизни состоянием будут рассматриваться соответствующим образом.
Интегрированная лечебно-паллиативная модель.
Качественное исследование показало, что среди приоритетов пациентов и их семей сталкиваются с проблемами серьезных состояний, ограничивающих жизнь, [Steinhauser et al. 2000]:
Лечение боли и симптомов : требуется внимание к физическому дистресс, вызванный болезнью в конце жизни;
Четкое принятие решений : требует хороших коммуникативных навыков и информация для пациента и семьи;
Утверждение личности в целом : требует отношения, поведения сострадание, способствующее развитию достоинства пациентов;
Подготовка к смерти : требует честного общения и служба поддержки;
Завершение : касается выполнения достижимых целей в конце жизнь.
Клиницисты должны знать, что важные потребности пациента в конце жизни не только ограничиваться физическими потребностями, но также включать духовные, экзистенциальные а также психосоциальные потребности.
Следовательно, определение EOLC должно быть описано с точки зрения удовлетворения этих потребностей пациенты и их семьи в конце жизни. В настоящее время нет однозначно принятого определение для EOLC; однако Национальный совет по паллиативной помощи Великобритании разработал рабочее определение в 2006 году, описывая его в зависимости от роли, которую оно играет [Национальный совет по Паллиативная помощь, 2011 г .; Департамент здравоохранения, 2008 г.]:
Уход, который помогает всем людям с запущенными, прогрессирующими и неизлечимыми заболеваниями живите как можно лучше, пока не умрут;
Обеспечивает поддерживающую и паллиативную помощь как пациентам, так и пациентам. семью, которую нужно идентифицировать и встретить на последнем этапе жизни и в тяжелая утрата;
Включает лечение боли и других симптомов, а также психологическая, социальная, духовная и практическая поддержка.
Траектория болезни пациента с запущенным раком описывалась как начальное медленное прогрессирование заболевания, при котором у пациентов будут минимальные симптомы и поддерживать довольно хороший общий статус производительности, пока они постепенно не достигнут точка, где у них начинает развиваться больше симптомов, что затем приводит к более быстрому упадок, который имеет тенденцию к спаду до конца жизни [Murray et al. 2005]. Поэтому, глядя на траекторию болезни у пациентов с запущенным раком легких, период, в котором ЭОЛЦ наиболее необходим, будет в тот период, когда пациент статус производительности быстро снижается, поскольку они приближаются к неизлечимой и быстро прогрессирующая фаза болезни ().
Траектория заболевания распространенным раком легкого.
Шкала эффективности Карновского (КПС).
Обсудив, когда пациенты нуждаются в EOLC, объем EOLC может быть очень большим. В целом, эта статья будет сосредоточена в основном на практических вопросах EOLC у пациентов. приближаются последние дни жизни.
Уход за пациентами в последние дни жизни
Многие врачи не знают, что делать, когда пациенты подходят к ним. эта фаза их болезни, особенно если они не проходили обучение или не подвергались воздействию паллиативная помощь.Однако важно уметь управлять этим периодом жизни. хорошо, потому что в это время может произойти много страданий, не только для терпеливым, но также и для тех, кто любит умирающего человека и заботится о нем. Дама Сисели Сондерс, основательница современного движения хосписов, сказала: «Как люди умирают, живет в воспоминаниях тех, кто продолжает жить ». Следовательно, все врачи должны чувствовать себя обязанными своим пациентам обеспечить, чтобы помимо всех исчерпаны интервенции, всегда будет надежда на мирное и достойная смерть.
В целом, при ведении пациентов, которые приближаются последние дни жизни. Если врачи могут определить эти четыре ключевых области в перспективе в то время, когда пациенты приближаются к своим последним дням, это может помочь в качестве практического руководства по улучшению ухода в конце жизни.
Четыре ключевые области, вызывающие озабоченность, включают:
Распознавание фазы умирания;
Общение с пациентом, семьей и близкими;
Обеспечение лечения симптомов;
Принятие этических решений.
Первый шаг — научиться распознавать, что пациент умирает. основаны на клинических данных, а также на понимании траектории заболевания и прогноз. Как только вы поймете, что пациент находится в фазе смерти, следующий шаг: заключается в том, чтобы сообщить о нашем понимании ситуации семье и близким. Это жизненно важный шаг, и следует помнить, что, хотя мы можем знать пациента очевидно умирает, семья и близкие могут не обращать на это внимания.Говорящий об ожиданиях и постановке целей ухода, уделяя особое внимание комфорту и достоинству. наиболее важно помочь подготовить настройку для последующего EOLC. Так после общение по основным вопросам с семьей и близкими, тогда это необходимо, чтобы врач мог «вести разговор» и действительно управлять и забота о пациенте для оптимизации комфорта и достоинства. Шаг третий, таким образом, заключается в том, чтобы обеспечивать адекватное лечение симптомов, а также заниматься важными психосоциальными и духовные вопросы, которые необходимо решить, чтобы оптимизировать ситуацию и надеюсь способствовать хорошей смерти.Наконец, четвертый шаг — понять этические основы принятия решений и управления в конце жизни. Это из крайне важно, так как врачи должны быть уверены в ведении пациентов в этот критический период жизни. Без четкого понимания этического принципы и политики, которыми руководствуются планы управления в конце жизни, такая забота может привести к конфликтам и дилеммам среди медицинских работников. Мы сейчас посмотрим в каждой области подробно.
Ключевая область первая: распознавание фазы умирания
Распознавание фазы умирания — первый и очень важный шаг в обеспечении хороший EOLC.Хотя это может показаться очень простым и интуитивно понятным навыком, нельзя считать очевидным для всех медицинских работников и во многих случаях, Причина плохого управления в конце жизни — результат неспособности распознать фазу умирания. Когда врачи могут распознать фазу умирания у своих пациентов, это позволяет им начать важные обсуждения с пациентами и семья относительно смерти и умирания. Среди этих обсуждений будет вопросы о выборе в конце жизни и предпочтениях пациента и семьи, чтобы чтобы избежать бесполезных вмешательств.Кроме того, обсуждения, чтобы подготовить членов семьи к предвидеть смерть и понимать процесс умирания важны, чтобы позволить превентивная утрата, чтобы уменьшить шок и бремя смерти. Наконец, следует обсудить с членами медицинской бригады, чтобы изменить приоритеты целей ухода и сместить акцент в уходе на обеспечение комфорта и достоинство, а не продление страданий. Последствия невыполнения признать фазу умирания, как указано Эллершоу, и Уорд будет включать после [Эллершоу и Ward, 2003]:
Пациент теряет доверие к врачу из-за его или ее состояния. ухудшение без признания того, что это происходит;
Семья не знает, что смерть неминуема;
Пациент умирает с неконтролируемыми симптомами, вызывающими тревогу и недостойная смерть;
В случае смерти сердечно-легочная реанимация может быть неуместной. инициирован;
Культурные и духовные потребности не удовлетворяются;
Пациент и семья недовольны.
Существует множество прогностических инструментов, помогающих клиницистам распознать траектория болезни пациентов с хроническими заболеваниями, ограничивающими жизнь, такими как Паллиативная прогностическая оценка, которая использует такие параметры, как статус производительности, клинические симптомы и параметры крови для оценки вероятности болезни пациента выживают более 1 месяца [Glare and Sinclair, 2008]. Такие инструменты полезны, особенно в помощь клиницистам в планировании управления; и может предупредить о важном обсуждение с пациентами прекращения агрессивного лечения.Тем не мение, в последние дни жизни фазу умирания можно распознать по нескольким клинические признаки и симптомы, которые вместе были признаны «Синдром неминуемой смерти» [Ferris et al. 2003; Weissman, 2005]. К ним относятся:
Чрезвычайно вялый: прогрессирующая слабость с уменьшением подвижности до постели. граница;
Снижение познания и сознания: от сонливости и растерянности до бред и, наконец, коматозное состояние;
Плохое пероральное употребление: возрастает трудность переносимости пероральных препаратов и пищу до тех пор, пока вы не сможете пить жидкость глотками с частыми стремление;
Изменения дыхания: в том числе модели Чейна – Стокса. дыхание, частые апноэ и, наконец, нижнечелюстное дыхание;
Конечные выделения: хрип, булькающий звук при дыхании из-за выделения, вибрирующие в дыхательных путях, когда воздух проходит во время дыхания;
Снижение показателей жизненно важных функций: снижение артериального давления, насыщение кислородом, периферический цианоз, слабый пульс и крапчатость.
Морита и его коллеги, которые изучали продолжительность выживания в начале эти признаки неминуемой смерти, сообщили о средней выживаемости пациентов с терминальная секреция — 57 часов, нижнечелюстное дыхание — 7,6 часа, цианозное конечностей — 5,1 часа, а лучевой артерии без пульса — 2,6 часа [Morita et al. 1998].
Ключевая область 2: общение с пациентом и семьей
Исследования показали, что врачи часто чувствуют себя беспомощными и неудобными, когда доведение прогностической информации до пациентов и их семей.Предоставление физическое лечение считается более легким, чем столкновение с отчаянием пациенты и их семьи с обсуждениями в конце жизни [ПОДДЕРЖКА, 1995]. В двух перспективах когортные исследования [Райт et al. 2008; Mack et al. 2012], это было обнаружено, что менее трети онкологов обсуждают вопросы, связанные с окончанием жизни со своими пациентами. Отсутствие обсуждений по окончании срока службы было связано с увеличение использования агрессивной помощи, такой как химиотерапия и отделение интенсивной терапии уход в последний 1 месяц жизни.В конечном итоге это приводит к тому, что пациент становится беднее. удовлетворенность, психологическая заболеваемость и более низкое качество жизни.
И наоборот, когда врачи честно обсуждают вопросы конца жизни со своими пациентам, это приводит к лучшему принятию решений, снижению тревожности и депрессии уровни, а также лучшее качество жизни как для пациентов, так и для семей [Steinhauser et al. al. 2001; Fallowfield et al. 2002; Райт et al. 2008]. Следовательно, общение является жизненно важным часть обеспечения хорошего EOLC.Как только клиницист распознал умирающего фазы у пациента, важно, чтобы это знание было передано относиться к семье должным образом и с состраданием, чтобы они тоже узнали ситуации и будьте готовы.
Общие принципы и шаги в общении с пациентами и семьями, когда обсуждение вопросов, связанных с окончанием срока службы, можно запомнить по аббревиатуре ПОДГОТОВЛЕН, как разработан Клейтоном и его коллегами [Clayton et al. 2007]:
P Подготовьте и усвойте всю обновленную информацию о состояние и состояние пациента
R Сообщение: относится к личности; проявить сочувствие и сострадание
E Ожидания: выявить ожидания пациента и опекуна и предпочтение информации
P Предоставьте информацию простым и понятным языком
A Признавайте эмоции и проблемы
R Реалистичная надежда
E Поощряйте вопросы
D Обсуждение документов в медицинских картах
Из этих шагов наиболее важным было бы наладить хорошее взаимопонимание с семья.Хорошее взаимопонимание можно рассматривать как «паспорт» общения без этого не следует пытаться обсуждать очень серьезный характер. Это просто потому, что, разговаривая с семьей о предвкушении смерть любимого человека — очень серьезное и изменяющее жизнь дело, которое требует, чтобы семья доверяла и верила в то, что слышит. Без установив хорошие отношения до этого, семья может сомневаться в достоверность и точность предоставленной информации [Lim, 2012].
Чтобы наладить хорошее взаимопонимание, клиницистам необходимо уметь относиться к человек, с которым они общаются; во-первых, начав с хорошего введение, а затем объяснение, как они участвуют в уходе за пациент. Затем врач должен дать понять, что он или она осведомлен о деле и в курсе последних проблем. Это где важна подготовка перед обсуждением. Один из самых простых способов терять взаимопонимание с семьей — это демонстрировать незнание рассматриваемого дела упоминание неточной информации.
Следующим важным навыком, помогающим развить семейные отношения, является способность Слушать. Слушание — это навык, который требует не только слышать, что представляет собой человек. говоря, но также внимательно относясь к языку их тела, тону голоса и искренне понимание того, что говорит другой человек. Клиницисты должны слушать чтобы понять, как семья воспринимает состояние пациента. Как только их восприятие будет понято, можно будет общаться таким образом, чтобы удовлетворить их потребности и проявлять сочувствие, которое еще больше укрепить отношения.Пытаясь понять представления семей, следует изучить следующие области:
Insight : Что семья понимает в настоящее время, и что до сих пор объясняли другие врачи?
Обеспокоенность : чего они боятся и какие проблемы требуют разъяснение?
Ожидания : На что они надеются и каковы их цели ухода? Что, по их мнению, будет сделано для пациента?
Можно использовать простую аббревиатуру ICE, чтобы запомнить это.
Ключевая область третья: обеспечение контроля над симптомами в последние дни
Среди симптомов, встречающихся в последние дни жизни пациентов с продвинутой стадией рак легких, наиболее часто встречающиеся приоритетные симптомы включают следующие [Ellershaw et al. al. 2001; Stone и др. . 2001; Квале эт. al. 2007]:
Боль
Одышка
Кашель
Беспокойство и делирий
Терминальные выделения
Клиницисты должны проявлять бдительность, чтобы распознать эти симптомы. знающие и умелые в управлении этими симптомами, которые будут способствовать хороший EOLC.
Таблица 1.
Примеры процесса коммуникации по окончании срока службы.
| Общение с членами семьи | Focus |
|---|---|
| Миссис А: «Доктор, расскажите, пожалуйста, как мой муж?
делаешь? » Доктор:« Да, конечно, я знаю, что вы, должно быть, очень переживает за него ». | Проявление сочувствия имеет большое значение для развития взаимопонимания. |
| Доктор:« За последние несколько дней у кого-нибудь
врачи говорили вам о его состоянии? Что ты
вспомнить, что есть у других врачей
объяснил? » Г-жа А:« Они просто сказали, что он не ну, но никогда ничего не упоминал о своих шансах становиться лучше.’ | Проверка понимания помогает вам использовать ту же длину волны, что и семья |
| Врач: «Глядя на то, каким был ваш муж последние несколько лет
дней, как вы думаете, дела обстоят? » Миссис А:« Он просто кажется становится все слабее и слабее. Он не получает лучше, не так ли? » Доктор:« Боюсь, что это правильно, ему не становится лучше, и рак делает его слабее в день. Я знаю, это должно быть сложно для вас, миссис А., но я боишься, что твой муж умирает ». | Изучение ожиданий поможет вам оценить, насколько глубоко
предмет, который вам нужно пройти Иногда это может просто требовать подтверждения того, что уже подозревается |
| Врач: «Скажите, что вас беспокоит больше всего?» | Изучите проблемы и никогда не предполагайте, что человек хочет знаю |
| Г-жа А: «Неужели вы ничего не можете сделать, чтобы сохранить ему жизнь? Ты должен
сделай что-нибудь, доктор, ПОЖАЛУЙСТА! » Доктор:« Я тебя знаю должна очень сильно его любить, и мысль о его потере должна быть таким болезненным.’ | Решительно реагируйте на эмоциональные высказывания, чтобы показать вам признать выраженные чувства |
| Доктор: «Ваш муж когда-нибудь говорил о том, что он хотел бы или не хотел бы для себя, если бы он сильно заболел как он сейчас? » | Позже, когда будет установлено хорошее взаимопонимание, и понимание, ожидания и опасения изучены, рассмотреть начало обсуждения расширенных планов ухода, таких как реанимация и предпочтительное место смерти и т. д. |
Боль
Боль — частый симптом у пациентов с запущенным раком. Эпидемиологический исследования показывают, что около 70% пациентов с запущенным раком страдают от боль [Teunissen и др. . 2007]. Обезболивание должно: поэтому должны предоставляться на протяжении всего периода болезни больного раком и даже в последние дни. Однако в последние дни у пациента способность говорить и глотать пероральные препараты часто снижается, и это распространенная ошибка среди клиницистов полагать, что на этом этапе пациенты больше не требуются обезболивающие.Функциональная позитронная эмиссия томография головного мозга показала, что даже пациенты с минимальным в сознательном состоянии может воспринимать боль [Boly et al. 2008]. Следовательно, рекомендуется применять все обезболивающие. продолжали в той же дозе, даже когда пациент перешел в менее сознательный конечное состояние.
Такое обезболивающее можно легко продолжить, преобразовав лекарства, такие как пероральный морфин для подкожного морфина или трансдермальный фентанил.Превращение морфина, вводимого подкожно, в морфин для перорального применения достигается с коэффициентом от 2 до 3, а пластырь с фентанилом 25 мкг / ч доставляет дозу, эквивалентную примерно 75 мг перорального морфина в день. Прорывные дозы морфина подкожно (это будет доза между От 1/12 до 1/6 суточной дозы, эквивалентной морфину). доступен в случае дополнительной боли. Это можно определить, наблюдая для невербального поведения, связанного с болью, такого как гримаса и стоны на лице, особенно по движению [Минздрав, 2010].
Одышка
Одышка — очень частый симптом при запущенном раке легких и в конце жизни этот симптом обычно сохраняется и часто усиливается [Kvale et al. al. 2007; Айер и др. . 2014]. Наряду с болью это симптом, который явно способствует плохому качеству жизнь и много горя в последние дни. Помимо паренхимы легких повреждение и обструкция дыхательных путей из-за обширного рака легких, существует множество другие причины одышки у пациентов с распространенным раком легких, включая обструкция верхней полой вены (SVCO), плевральный выпот, наложение грудной клетки инфекция, сопутствующая анемия, сердечная недостаточность, метаболический ацидоз, легочный эмболия и общая мышечная слабость.
В общем, начальный подход к лечению одышки заключается в исправлении что можно исправить, например, обеспечение кислородом, лечение инфекций, дренирование плевральный выпот или использование кортикостероидов у пациентов с SVCO [Twycross et al. al. 2009b]. Однако для пациентов, находящихся в в последние дни жизни, не всегда возможно или возможно исправить эти причины, следовательно, обеспечение адекватного облегчения симптомов является основой управления.
Опиоиды обладают значительным преимуществом при симптоматическом лечении одышки у пациенты с запущенным раком.У пациентов, ранее не принимавших опиоиды, это рекомендуется начинать с низких доз 2-3 мг перорального морфина или 1 мг морфин подкожно 6–8 раз в час и при необходимости. Если пациент переносимость морфина без побочных эффектов, тогда доза может быть постепенно титруют до 4 раз в час, а затем увеличивают по мере необходимости. Для пациентов, которые уже принимают опиоиды от боли, было бы целесообразно увеличить общую дозу опиоида на 20–30% и обеспечить прорывные дозы 1 / 12–1 / 6 от общей суточной дозы при необходимости, если одышка все еще остается серьезной, несмотря на повышенную дозу [Twycross et al. al. 2009b; Абернети и др. 2003; Jennings et al. 2002].
Хотя доказательств у пациентов, находящихся в тяжелом состоянии и беспокойство из-за одышки, добавление бензодиазепина может помочь уменьшить дистресс и беспокойство, которые часто усугубляют восприятие одышки. Если пациенты проявляют сильную тревогу с приступами паники, сублингвально лоразепам 0,5–1 мг могут быть полезны для уменьшения беспокойства. Подкожный мидазолам 2,5–5 мг также можно использовать в качестве альтернативы.Для пациентов, которые постоянно в тяжелом состоянии, непрерывная подкожная инфузия мидазолама 10-20 мг в течение 24 лет. обычно добавляется к опиоидной терапии [Currow et al. 2013; Саймон et al. 2010].
Кашель
Кашель — частый симптом при запущенном раке легких, который проявляется в течение нескольких месяцев и недель. до того, как пациент достигнет терминальной фазы, это может быть источником больших дискомфорт и страдания. Подход к этому симптому обычно зависит от причина кашля и его выделение мокроты или сухость.
При продуктивном кашле, связанном с гнойной мокротой, применяются антибиотики. может быть полезно, если есть инфекционный компонент, вызывающий этот симптом. К способствовать очищению от слизи, простая мера — использовать небулайзерный физиологический раствор. Муколитические агенты, такие как бромгексин, N-ацетилцистеин и гвайфенезин, могут также быть полезным. Если есть сопутствующий бронхоспазм, рассмотрите небулайзированные бронходилататоры. Если наблюдается сильное кровохарканье, могут использоваться антифибринолитические агенты, такие как транексамовая кислота.Паллиативный Лучевая терапия также может быть рассмотрена при сильном кровохарканье.
При сухом кашле, вызывающем беспокойство, и у пациентов, находящихся в последние дни жизни и слишком слаб, чтобы кашлять, опорой для лечения симптомов будет подавить кашель и дать пациенту отдохнуть. Кашель супрессивные средства включают кодеин из линктуса и сильные опиоиды в низких дозах, такие как морфин, гидрокодон, оксикодон или метадон. В тяжелых ситуациях можно рассмотреть распыленный лигнокаин; однако следует соблюдать осторожность, так как это может вызвать бронхоспазм.На этом этапе также можно рассмотреть возможность применения седативных средств. облегчить тяжелое состояние, если другие меры не дали результатов [Molassiotis et al. al. 2010; Twycross et al. 2009b].
Делирий и беспокойство
Делирий и беспокойство — общие симптомы в конце жизни, и они могут быть чрезвычайно хлопотной и изнурительной проблемой как для семьи, так и для персонал больницы. По мере прогрессирования рака и состояния пациента ухудшается, ранним симптомом делирия может быть обращение цикл сна-бодрствования, при котором семья будет жаловаться на то, что пациент не склонен хорошо спит ночью, но спит в основном днем.Как условие ухудшается, у пациента могут развиться гипоактивные или гиперактивные симптомы. Этот может включать симптомы спутанного поведения, бессвязной речи, нецелевого движения и попытки вставать и опускаться с кровати [Breitbart and Alici, 2008].
Столкнувшись с проблемой делирия, сначала следует подумать о простых исследования, чтобы исключить некоторые общие, но обратимые причины делирия такие как запор, гипогликемия, нарушение электролитного баланса, гиперкальциемия, сепсис или побочные эффекты лекарств.При отсутствии других обратимых причина, тогда можно рассмотреть диагноз терминального делирия, который что вызвано терминальным состоянием пациента. Семья может часто находить это пугающе, так как может показаться, что их любимый сходит с ума; это важно объяснить им, что это признак того, что «функция мозга нарушена. постепенно закрывается ».
Лечение делирия можно контролировать с помощью антипсихотических препаратов, таких как галоперидол в качестве первой линии. Это может быть дано перорально или подкожно с типичная доза 1–5 мг на ночь и 1 мг перорально.Помимо галоперидола, Также могут использоваться более новые атипичные нейролептики, такие как оланзапин, кветиапин ® или рисперидон.
Пациенты с гиперактивным делирием могут быть чрезвычайно возбуждены и иногда может потребоваться введение пациенту седативных средств с помощью короткодействующего бензодиазепин, такой как мидазолам. Обычно небольшая доза 2,5–5 мг может быть подкожно, по мере необходимости; однако это также может быть дано как непрерывная подкожная инфузия, постепенно титруемая до дозы между 0.5 и 2 мг в час, если желательна непрерывная седация. Должен быть помните, однако, что бензодиазепины не следует использовать в качестве монотерапии. для возбужденного делирия, так как это может привести к парадоксальному ухудшению возбуждение и должен использоваться в сочетании с антипсихотическими средствами [Twycross et al. al. 2009a].
Конечные выделения
Конечные выделения также известны как термин «предсмертный хрип», и он это знак, который неизбежно возвещает последние несколько часов или короткие дни жизни [Morita et al. al. 1998]. Он имеет звук, напоминающий звук грудная секреция и иногда может быть ошибочно принята за звук острого отек легких. Поэтому для клиницистов важно уметь: распознавать этот симптом и отличать его от других состояний, чтобы избегать бесполезных и ненужных исследований, таких как рентген грудной клетки, внутривенное введение антибиотиков и мониторинг ЭКГ. Ключ к признанию этого симптом в основном заключается в понимании прогноза и болезни пациента. траектория. Следовательно, если это пациент, который, как мы знаем, приближается к в конечной фазе, мы определенно узнаем звук как звук «Предсмертный хрип», а не острый отек легких.
Этот симптом — еще один очень тревожный симптом для членов семьи, поскольку он у них часто создается впечатление, что их любимый «тонет» в их выделения [Wee et al. 2006]. Поэтому важно объясните им, что это связано с выделениями в дыхательных путях, которые вызывают шумные колебания при прохождении воздуха, но не препятствуют вызвать респираторный дистресс у пациента. Также важно объяснить что отсасывание в этом случае бесполезно, так как оно не уменьшит дребезжание, но на самом деле может причинить пациенту больше страданий.Глубокое всасывание на самом деле может привести к стимуляции блуждающего нерва, что может вызвать внезапную брадикардию и асистолия у пациента, который уже находится в терминальной фазе. Несмотря на то что смерть — это ожидаемое событие, для пациента внезапная остановка дыхания во время процедуры отсасывания на самом деле может вызвать большое недовольство среди членов семьи.
Следовательно, лечение этого симптома будет заключаться в применении холинолитиков. лекарства, которые помогут уменьшить количество выделений и, таким образом, уменьшение дребезжащего звука.Обычные лекарства, которые используются в этом случае включают следующие [Twycross et al. 2009a]:
Гиосцина бутилбромид (бускопан) подкожно 20 мг 4–8 раз в час и prn
Подкожный гиосцина гидробромид 400 мкг 4–8 час и prn
Гликопирролат 200 мкг 4–8 час подкожно и prn
Эти лекарства также можно вводить непрерывно в течение 24 часов подкожно. настой.
Ключевая область четыре: принятие этических решений в конце жизни
Принятие клинических решений для пациентов с запущенным раком, которые приближаются конец жизни может быть трудным и временами ставить перед клиническая бригада.Это потому, что как медицинские работники воспринимают долг сохранять и поддерживать святость жизни. В то же время врачи также обязаны действовать в интересах пациента. «Святость доктрины жизни, которая была основным принципом биомедицинской этики до сегодня это принцип, унаследованный от иудео-христианского и гиппократовского традиции вековой давности [Баранцке, 2012]. Что касается ухода за пациентами в конце жизни, около века назад состояние медицинской науки было на уровне, когда часто, было мало сомнений в том, чтобы принять, когда смерть была неизбежна и решения позволить необратимой патологии развиваться естественным путем было легко.Сегодня, однако из-за достижений в области медицинских технологий все больше и больше вмешательства, продлевающие жизнь, открываются и, следовательно, обнаруживаются правильный баланс между количеством и качеством жизни теперь стал основным вызов EOLC. Поэтому клиницисты должны быть знакомы с общими этические принципы, применимые к принятию клинических решений в конце жизни, поскольку это позволяет им практиковать хороший EOLC с ясностью и ясностью совесть. Некоторые проблемы с окончанием жизни, которые могут вызвать сомнения у клиницистов включают:
Прекращение и прекращение поддерживающего жизнь лечения, такого как сердечно-легочная реанимация, искусственная вентиляция легких, искусственная гидратация и питание;
Седативные препараты, применяемые в конце жизни;
Путаница в терминологии эвтаназии.
Часто основной проблемой врача будет: «Предоставляет ли руководство мой пациент в конце жизни ускорит смерть и приблизится ли она к эвтаназии? »Из-за таких опасений клиницисты могут опасаться судебно-медицинских последствия и конфликт внутри себя при принятии решения , как вести пациента в конце жизни, и это может приводят к ухудшению EOLC [Swanson и МакКрари, 1996; Марик и др. 1999; Miccinesi et al. al. 2005].
Отказ от медицинского вмешательства
С этической точки зрения, нет никакой разницы между действиями по отказу от медицинского вмешательства. медицинское вмешательство и отказ от медицинского вмешательства. Следовательно, остановка поддерживающая жизнь терапия ничем не отличается от того, чтобы не начинать ее. Оба действия этически приемлемы при лечении [Ko and Blinderman, 2015; Британский Медицинский Ассоциация, 2009 г .; Ackermann, 2000]:
Futile;
Не в интересах пациента;
Отказано пациентом.
Руководящие принципы в этой ситуации включают автономию и милосердие. Понятно, что пациенты имеют полное право отказаться от лечения. вмешательства, даже если они могут быть полезными. Однако проблема возникает, когда пациент не может выразить эту автономию, и нет четкое предварительное распоряжение. В этой ситуации общение с суррогатом лицо, принимающее решение, чтобы определить предпочтения пациента в отношении ухода, является нормальным упражняться. Иногда это может быть сложно, потому что суррогатное решение производители, которые часто являются близкими родственниками, могут принимать эмоциональные решения, которые представляют свои собственные предпочтения и, возможно, не предпочтения пациента.Следовательно, важно объяснить суррогатному лицу, принимающему решение, что их выбор должен быть таким, который приближается к собственным предпочтениям пациента [Ko and Blinderman, 2015; GMC, 2010].
Клиницисты должны также очень четко помнить, что нет необходимости предлагать все формы поддерживающей жизнь терапии; профессиональное мнение что такие методы лечения не принесут очевидной пользы. Медицинская бесполезность можно определить количественно, имея в виду вмешательство с очень отдаленными шансы получить выгоду; или это может быть определено качественно, то есть вмешательство вряд ли приведет к достижению ориентированных на пациента целей.В клинической на практике, однако, может быть трудно определить бесполезность, поскольку все люди пациент, врач и семья могут иметь разные взгляды на то, что полезны и каковы должны быть цели ухода. Поэтому полезное руководство помочь клиницистам решить, что считать бесполезным, означало бы определить цели лечения в каждом отдельном случае, прежде чем рассматривать вмешательство. Если вмешательство вряд ли приведет к достижению этих целей в каком-либо Кстати, тогда бесполезность следует считать [Schneiderman, 2011].
Одна из самых сложных сфер, связанных с отказом от медицинской помощи. вмешательства — это вопрос искусственного увлажнения и питания. Она имеет Утверждалось, что гидратация и питание считаются основными потребностями заботы, которой никогда не следует лишать ни одного человека. Тем не мение, искусственное увлажнение и питание через зонд для кормления или внутривенное не такие простые, как обычное пероральное кормление и питье. Многие из этические дилеммы отказа от искусственного увлажнения и питания, однако из-за его использования у пациентов со стойкими вегетативными состояниями, где такие вмешательства позволяют пациентам выжить годами, и его абстинентный синдром можно рассматривать как преднамеренный акт по сокращению жизни [Brody et al. al. 2010]. Однако в контексте пациента с запущенный рак, который находится в последних днях жизни, совершенно ясно, что доказательства показали, что искусственная гидратация не приносит пользы для выживаемости. и питание [Хорошо et al. 2008a, 2008b]. Невозможность поддерживать питание пероральным путем на поздних стадиях рака, и убывающая функция, являются маркерами процесса умирания; и обеспечение хороших уход за полостью рта и поддержание чистоты и влажности полости рта — лучшая форма паллиатив.Прекращение искусственного увлажнения и питания в таком случае является недопустимым. поэтому уместно [Сломка, 2003; Twycross et al. 2009а].
Хотя с этической точки зрения клиницисты имеют право отказать или отозвать медицинские вмешательства по причине врачебной бесполезности, следует помнить, что эти решения все же следует обсудить с семьей, чтобы убедиться, что они понять причину и основу таких решений. Если семья, однако, отказываться принимать эти решения и требовать вмешательства, чтобы продолжайте, клиницисты должны передать дело коллеге на секунду мнение и кто может согласиться на продолжение ухода или дальнейшие переговоры управление с семьей [GMC, 2010; Ко, Блиндерман, 2015].
Использование седативных препаратов в конце жизни
Один из распространенных страхов клиницистов по поводу использования седативных препаратов, таких как поскольку морфин или бензодиазепины в конце жизни ускоряют смерть. это распространено мнение, что с помощью таких лекарств и без того хилого и слабого пациенту, эти препараты могут привести к гипотонии, угнетению дыхания и смерть. Из-за этих опасений врачи часто неохотно предоставляют адекватное облегчение боли и седация при беспокойстве в терминале фаза.Однако данные показали, что такие лекарства действительно могут быть назначается пациентам в терминальной фазе, не вызывая каких-либо значительных снижение выживаемости при правильном использовании для облегчения симптомов конец жизни [Мальтони et al. 2012; Морита и др. . 2001, 2005; Сайкс и Thorns, 2003]. Однако, если седативные препараты, такие как морфин или бензодиазепины действительно ускорили смерть, использование таких лекарств может по-прежнему быть оправданным, исходя из принципа «двойного эффекта» и принцип пропорциональности [De Graeff and Dean, 2007; Juth et al. al. 2010; Krakauer et al. 2000].
Принцип «двойного эффекта» гласит, что если действие имеет целью хороший эффект может достичь этого эффекта только с риском произвести вредного воздействия, то это действие этически допустимо при условии, что удовлетворяет следующим условиям:
Акция хороша сама по себе;
Цель состоит исключительно в том, чтобы произвести хороший эффект;
Хороший эффект не достигается плохим эффектом;
Есть достаточная причина для того, чтобы допустить плохой эффект.
Таким образом, этот принцип отличает использование седативных препаратов в конец жизни из-за эвтаназии, так как в этом случае намерение состоит в том, чтобы облегчить боль, одышка или беспокойство, и ни в коем случае не намерен намеренно причинить вред пациенту. Когда используются такие седативные препараты, они вводят в малых дозах и титруют до тех пор, пока не будет получено достаточно достичь желаемого эффекта, что демонстрирует этическая практика, основанная на принцип соразмерности.
Эвтаназия, с другой стороны, не может быть оправдана этими принципами, поскольку в практике эвтаназии используются средства, выходящие за рамки необходимого чтобы просто облегчить симптомы, и цель состоит в том, чтобы вызвать немедленную смерть пациент. Следовательно, даже если врач заявит, что его намерение состоит в том, чтобы облегчить страдания, практика эвтаназии является примером достижения хороший эффект через плохой эффект [Materstvedt et al. 2003].
Запутанная терминология эвтаназии
Терминология, такая как «активная эвтаназия», «пассивная эвтаназия», «добровольная эвтаназия »и« недобровольная эвтаназия », которые широко использовались в литературы, приводят к тому, что врачи чувствуют замешательство и неуверенность в том, что практика фактически представляет собой эвтаназию.Термин «пассивная эвтаназия» часто используется для описания удержания или отказа от бесполезных медицинских вмешательства при «активной эвтаназии» и «добровольной эвтаназии» синонимы описывают активное и преднамеренное администрирование вмешательство, которое приводит к смерти пациента, добровольно просил это. «Недобровольная эвтаназия» описывает акт преднамеренного проведение вмешательства, которое приводит к смерти пациента, у которого добровольно не просил о таком вмешательстве из-за отсутствия возможностей.В чтобы прояснить некоторые из этих часто вводящих в заблуждение терминов, европейские Ассоциация паллиативной помощи опубликовала консенсусное заявление, определяющее эвтаназия как: «Врач умышленно убивает человека прием лекарств по добровольной и компетентной просьбе этого лица ». Далее они пояснили, что эвтаназия всегда должна быть активной, а термин «Пассивная эвтаназия» — это противоречие терминов. Эвтаназия также должна всегда быть добровольным, и «недобровольная» эвтаназия, по сути, является убийством. В поэтому ключевым словом в определении эвтаназии является слово «Преднамеренный».Намерение состоит в том, чтобы убить человека, и успешный результат для наступит немедленная смерть [Matersvedt et al. 2003; Matersvedt, Bosshard, 2015].
Следовательно, врачи должны четко понимать определение эвтаназии, а не путайте это с этически приемлемым менеджментом в конце жизни, например как отказ от бесполезных медицинских вмешательств и паллиативных седация в конце жизни.
Заключение
Несмотря на успехи в лечении рака легких, большинство пациентов все еще умереть от болезни в течение 5 лет после постановки диагноза, и смерть от рака легких может быть связано со многими симптомами и низким качеством жизни.Клиницисты должны поэтому лучше осознавать потребности таких пациентов и изучать основные навыки необходим для ухода за пациентами на этой стадии их болезни.
Хотя в области паллиативной медицины произошли значительные изменения. во всем мире все еще очевидно, что многие пациенты, нуждающиеся в паллиативной помощи, не может получить к нему доступ по разным причинам, например, из-за недостатка знаний и навыков среди медицинских работников отсутствие основных лекарств, особенно опиоиды, и отсутствие систем здравоохранения для оказания такой помощи [Всемирная паллиативная помощь Альянс, 2014].Даже в тех районах, где легко доступны услуги паллиативной помощи. доступны, все еще существуют препятствия, мешающие пациентам получить хороший EOLC уход, например, нежелание клиницистов направлять пациентов к паллиативной помощи услуги, а также нежелание пациентов получать направление из-за негативного восприятия паллиативной помощи и ее значение [Wentlandt et al. 2012].
В мае 2014 года Всемирная организация здравоохранения приняла резолюцию об усилении паллиативной помощи как компонента комплексной помощи на протяжении всей жизни это подчеркнуло необходимость интеграции паллиативной помощи в система здравоохранения для обеспечения доступа для всех нуждающихся [Всемирная организация здравоохранения, 2014].Для этого стремление стать реальностью, все медицинские работники заботятся о пациентах с серьезными заболеваниями, в том числе с раком легких, должны иметь базовые знания и навыки для улучшения ухода к концу жизни в ситуациях, когда лечение больше не Возможность.
Уход в конце жизни пациентам с далеко зашедшими легкими рак
Реферат
Несмотря на успехи в обнаружении, патологической диагностике и лечении рак легких, у многих пациентов все еще развивается прогрессирующий, неизлечимый и прогрессирующий смертельная болезнь.Как врач, обязанность иногда лечить, часто облегчать и комфорт всегда должен быть постоянным напоминанием нам о потребностях, которые необходимо удовлетворить при уходе за больным раком легких. Четыре ключевые области ухода за пациентами в конце жизни при запущенном раке легких начните с первого распознавания того, «когда пациент приближается к концу жизни ». Врач должен уметь распознать, когда акцент в уходе необходимо сместить с агрессивного подхода к поддержанию жизни на подход, который помогает подготовить и поддержать пациента и членов его семьи через период прогрессивного, неизбежного упадка.Как только потребности будут признаны, Вторая ключевая область — это надлежащее общение, в котором врач должен оказывать помощь. пациенты и члены их семей понимают, в каком состоянии они находятся траектория и чего ожидать. Это включает в себя развитие взаимопонимания, ломку плохого новости, управление ожиданиями и навигация по планам ухода. Впоследствии третий ключевой областью является управление симптомами, которое фокусируется на целях, прежде всего, обеспечить комфорт и достоинство. Симптомы, которые часто встречаются к концу жизни у рак легких включает боль, одышку, делирий и респираторные выделения.Такой симптомы необходимо предвидеть и своевременно устранять соответствующими лекарства и объяснения пациенту и семье. Наконец, для того, чтобы врачей, чтобы обеспечить качественную помощь в конце жизни, необходимо понимать этические принципы, применяемые к вмешательствам по уходу за пациентами в конце жизни. Заблуждения об эвтаназии по сравнению с удержанием или отказом жизнеобеспечивающие методы лечения могут причинить врачу неудобства и неуместные принимать решение.
Ключевые слова: помощь в хосписе, новообразование легких, медицинская этика, паллиативная помощь, отношения между врачом и пациентом, неизлечимая помощь
Введение
Рак легких является наиболее распространенным видом рака, а также наиболее частой причиной рака смерть в современном мире [мир Организация здравоохранения, 2013].Несмотря на успехи в обнаружении, патологическая диагностика и лечение рака легких, у многих пациентов все еще развивается запущенная, неизлечимая и прогрессирующая со смертельным исходом болезнь. Для большинства пациентов с рак легких, диагноз часто ставится на стадиях III и IV, когда выживаемость все еще очень плохой, с общей 5-летней выживаемостью от 9,5% до 16,8%. Данные из Соединенное Королевство показало, что 67,6% всех пациентов с раком легких имели болезнь III и IV стадии на первоначальный диагноз. В США данные SEER с 2004 по 2010 год зарегистрировали 79% легких. раковые больные на момент постановки диагноза находились на стадии III и IV [Cancer Research UK, 2013; Национальный институт рака SEER программа, 2014].В Китае проведено популяционное исследование немелкоклеточного легкого. рака в Шанхае, 76,4% пациентов, диагностированных с 2011 по 2013 год, находились в стадия III или IV [Fan et al. al. 2015]. Хотя в лечение рака легких, особенно немелкоклеточного рака легких, с прогресс в ингибиторах тирозинкиназы, это привело лишь к незначительным улучшениям в Общая выживаемость. Следовательно, по-прежнему справедливо заявить, что в настоящее время подавляющее большинство пациентов с раком легких в конечном итоге умрут от своей болезни в 5 лет диагностики.
Исследования также показали, что с годами наблюдается тенденция к увеличению среди онкологов продолжать агрессивную онкологическую помощь пациентам, столкнувшимся с последними месяца жизни и с быстрым развитием противораковой терапии, эта тенденция скорее всего, продолжится [Эрл et al. 2004]. Поэтому важно, чтобы любой клиницист, который ведет лечение пациентов с раком легких, должен быть знаком и внимателен к потребности пациентов, которым угрожает конец жизни, поскольку они включают большую часть лечение рака легких.
Когда пациент находится на «конце жизни» и что такое «уход в конце жизни»?
Клиницисты, исследователи и политики в области здравоохранения часто пытаются разделить аккуратные определения с четкими временными рамками, чтобы выявить потребности и определить роли. Однако есть ли временные рамки для определения ухода за пациентами в конце жизни (EOLC)? когда это должно произойти? В настоящее время нет единого мнения относительно определения или времени рамка для «конца жизни». Как правило, многие считают окончание жизни последним. дней до 1–2 недель жизни.В Великобритании руководство Генерального медицинского совета (GMC) относится к пациентам, приближающимся к концу жизни, когда они, вероятно, умрут в следующие 12 месяцев [GMC, 2010; Идзуми et al. 2012]. В США Medicare определяет необходимость для ухода в хосписе в конце жизни как последние 6 месяцев жизни [Национальный хоспис и паллиатив Организация опеки, 2014]. Многие определения, использующие временные рамки, являются исходя из продолжительности жизни пациента; однако выживание — это то, что может никогда не может быть предсказан с большой точностью и действительно является ретроспективным результатом.Следовательно, если бы врач использовал такие определения для выявления пациентов, которым требуется ЭОЛЦ, он понадобится хрустальный шар или ясновидящий, чтобы найти нужного пациента получили соответствующую помощь. Поэтому, когда мы сосредотачиваемся на жестком определении, используя модель дихотомического намерения (), многие пациенты, нуждающиеся в ЭОЛК, будут пропущены, а многие физические, неудовлетворенные психосоциальные и духовные потребности.
Модель дихотомического намерения.
Таким образом, определение EOLC должно основываться на потребностях пациента, а не чем временные рамки.Это можно увидеть в модели комплексного лечебно-паллиативного лечения. намерение (). Следовательно, независимо от временных рамок и активных вмешательств, которые могут проводиться, пациенты с проблемами и потребностями, связанными с этим опасным для жизни состоянием будут рассматриваться соответствующим образом.
Интегрированная лечебно-паллиативная модель.
Качественное исследование показало, что среди приоритетов пациентов и их семей сталкиваются с проблемами серьезных состояний, ограничивающих жизнь, [Steinhauser et al. 2000]:
Лечение боли и симптомов : требуется внимание к физическому дистресс, вызванный болезнью в конце жизни;
Четкое принятие решений : требует хороших коммуникативных навыков и информация для пациента и семьи;
Утверждение личности в целом : требует отношения, поведения сострадание, способствующее развитию достоинства пациентов;
Подготовка к смерти : требует честного общения и служба поддержки;
Завершение : касается выполнения достижимых целей в конце жизнь.
Клиницисты должны знать, что важные потребности пациента в конце жизни не только ограничиваться физическими потребностями, но также включать духовные, экзистенциальные а также психосоциальные потребности.
Следовательно, определение EOLC должно быть описано с точки зрения удовлетворения этих потребностей пациенты и их семьи в конце жизни. В настоящее время нет однозначно принятого определение для EOLC; однако Национальный совет по паллиативной помощи Великобритании разработал рабочее определение в 2006 году, описывая его в зависимости от роли, которую оно играет [Национальный совет по Паллиативная помощь, 2011 г .; Департамент здравоохранения, 2008 г.]:
Уход, который помогает всем людям с запущенными, прогрессирующими и неизлечимыми заболеваниями живите как можно лучше, пока не умрут;
Обеспечивает поддерживающую и паллиативную помощь как пациентам, так и пациентам. семью, которую нужно идентифицировать и встретить на последнем этапе жизни и в тяжелая утрата;
Включает лечение боли и других симптомов, а также психологическая, социальная, духовная и практическая поддержка.
Траектория болезни пациента с запущенным раком описывалась как начальное медленное прогрессирование заболевания, при котором у пациентов будут минимальные симптомы и поддерживать довольно хороший общий статус производительности, пока они постепенно не достигнут точка, где у них начинает развиваться больше симптомов, что затем приводит к более быстрому упадок, который имеет тенденцию к спаду до конца жизни [Murray et al. 2005]. Поэтому, глядя на траекторию болезни у пациентов с запущенным раком легких, период, в котором ЭОЛЦ наиболее необходим, будет в тот период, когда пациент статус производительности быстро снижается, поскольку они приближаются к неизлечимой и быстро прогрессирующая фаза болезни ().
Траектория заболевания распространенным раком легкого.
Шкала эффективности Карновского (КПС).
Обсудив, когда пациенты нуждаются в EOLC, объем EOLC может быть очень большим. В целом, эта статья будет сосредоточена в основном на практических вопросах EOLC у пациентов. приближаются последние дни жизни.
Уход за пациентами в последние дни жизни
Многие врачи не знают, что делать, когда пациенты подходят к ним. эта фаза их болезни, особенно если они не проходили обучение или не подвергались воздействию паллиативная помощь.Однако важно уметь управлять этим периодом жизни. хорошо, потому что в это время может произойти много страданий, не только для терпеливым, но также и для тех, кто любит умирающего человека и заботится о нем. Дама Сисели Сондерс, основательница современного движения хосписов, сказала: «Как люди умирают, живет в воспоминаниях тех, кто продолжает жить ». Следовательно, все врачи должны чувствовать себя обязанными своим пациентам обеспечить, чтобы помимо всех исчерпаны интервенции, всегда будет надежда на мирное и достойная смерть.
В целом, при ведении пациентов, которые приближаются последние дни жизни. Если врачи могут определить эти четыре ключевых области в перспективе в то время, когда пациенты приближаются к своим последним дням, это может помочь в качестве практического руководства по улучшению ухода в конце жизни.
Четыре ключевые области, вызывающие озабоченность, включают:
Распознавание фазы умирания;
Общение с пациентом, семьей и близкими;
Обеспечение лечения симптомов;
Принятие этических решений.
Первый шаг — научиться распознавать, что пациент умирает. основаны на клинических данных, а также на понимании траектории заболевания и прогноз. Как только вы поймете, что пациент находится в фазе смерти, следующий шаг: заключается в том, чтобы сообщить о нашем понимании ситуации семье и близким. Это жизненно важный шаг, и следует помнить, что, хотя мы можем знать пациента очевидно умирает, семья и близкие могут не обращать на это внимания.Говорящий об ожиданиях и постановке целей ухода, уделяя особое внимание комфорту и достоинству. наиболее важно помочь подготовить настройку для последующего EOLC. Так после общение по основным вопросам с семьей и близкими, тогда это необходимо, чтобы врач мог «вести разговор» и действительно управлять и забота о пациенте для оптимизации комфорта и достоинства. Шаг третий, таким образом, заключается в том, чтобы обеспечивать адекватное лечение симптомов, а также заниматься важными психосоциальными и духовные вопросы, которые необходимо решить, чтобы оптимизировать ситуацию и надеюсь способствовать хорошей смерти.Наконец, четвертый шаг — понять этические основы принятия решений и управления в конце жизни. Это из крайне важно, так как врачи должны быть уверены в ведении пациентов в этот критический период жизни. Без четкого понимания этического принципы и политики, которыми руководствуются планы управления в конце жизни, такая забота может привести к конфликтам и дилеммам среди медицинских работников. Мы сейчас посмотрим в каждой области подробно.
Ключевая область первая: распознавание фазы умирания
Распознавание фазы умирания — первый и очень важный шаг в обеспечении хороший EOLC.Хотя это может показаться очень простым и интуитивно понятным навыком, нельзя считать очевидным для всех медицинских работников и во многих случаях, Причина плохого управления в конце жизни — результат неспособности распознать фазу умирания. Когда врачи могут распознать фазу умирания у своих пациентов, это позволяет им начать важные обсуждения с пациентами и семья относительно смерти и умирания. Среди этих обсуждений будет вопросы о выборе в конце жизни и предпочтениях пациента и семьи, чтобы чтобы избежать бесполезных вмешательств.Кроме того, обсуждения, чтобы подготовить членов семьи к предвидеть смерть и понимать процесс умирания важны, чтобы позволить превентивная утрата, чтобы уменьшить шок и бремя смерти. Наконец, следует обсудить с членами медицинской бригады, чтобы изменить приоритеты целей ухода и сместить акцент в уходе на обеспечение комфорта и достоинство, а не продление страданий. Последствия невыполнения признать фазу умирания, как указано Эллершоу, и Уорд будет включать после [Эллершоу и Ward, 2003]:
Пациент теряет доверие к врачу из-за его или ее состояния. ухудшение без признания того, что это происходит;
Семья не знает, что смерть неминуема;
Пациент умирает с неконтролируемыми симптомами, вызывающими тревогу и недостойная смерть;
В случае смерти сердечно-легочная реанимация может быть неуместной. инициирован;
Культурные и духовные потребности не удовлетворяются;
Пациент и семья недовольны.
Существует множество прогностических инструментов, помогающих клиницистам распознать траектория болезни пациентов с хроническими заболеваниями, ограничивающими жизнь, такими как Паллиативная прогностическая оценка, которая использует такие параметры, как статус производительности, клинические симптомы и параметры крови для оценки вероятности болезни пациента выживают более 1 месяца [Glare and Sinclair, 2008]. Такие инструменты полезны, особенно в помощь клиницистам в планировании управления; и может предупредить о важном обсуждение с пациентами прекращения агрессивного лечения.Тем не мение, в последние дни жизни фазу умирания можно распознать по нескольким клинические признаки и симптомы, которые вместе были признаны «Синдром неминуемой смерти» [Ferris et al. 2003; Weissman, 2005]. К ним относятся:
Чрезвычайно вялый: прогрессирующая слабость с уменьшением подвижности до постели. граница;
Снижение познания и сознания: от сонливости и растерянности до бред и, наконец, коматозное состояние;
Плохое пероральное употребление: возрастает трудность переносимости пероральных препаратов и пищу до тех пор, пока вы не сможете пить жидкость глотками с частыми стремление;
Изменения дыхания: в том числе модели Чейна – Стокса. дыхание, частые апноэ и, наконец, нижнечелюстное дыхание;
Конечные выделения: хрип, булькающий звук при дыхании из-за выделения, вибрирующие в дыхательных путях, когда воздух проходит во время дыхания;
Снижение показателей жизненно важных функций: снижение артериального давления, насыщение кислородом, периферический цианоз, слабый пульс и крапчатость.
Морита и его коллеги, которые изучали продолжительность выживания в начале эти признаки неминуемой смерти, сообщили о средней выживаемости пациентов с терминальная секреция — 57 часов, нижнечелюстное дыхание — 7,6 часа, цианозное конечностей — 5,1 часа, а лучевой артерии без пульса — 2,6 часа [Morita et al. 1998].
Ключевая область 2: общение с пациентом и семьей
Исследования показали, что врачи часто чувствуют себя беспомощными и неудобными, когда доведение прогностической информации до пациентов и их семей.Предоставление физическое лечение считается более легким, чем столкновение с отчаянием пациенты и их семьи с обсуждениями в конце жизни [ПОДДЕРЖКА, 1995]. В двух перспективах когортные исследования [Райт et al. 2008; Mack et al. 2012], это было обнаружено, что менее трети онкологов обсуждают вопросы, связанные с окончанием жизни со своими пациентами. Отсутствие обсуждений по окончании срока службы было связано с увеличение использования агрессивной помощи, такой как химиотерапия и отделение интенсивной терапии уход в последний 1 месяц жизни.В конечном итоге это приводит к тому, что пациент становится беднее. удовлетворенность, психологическая заболеваемость и более низкое качество жизни.
И наоборот, когда врачи честно обсуждают вопросы конца жизни со своими пациентам, это приводит к лучшему принятию решений, снижению тревожности и депрессии уровни, а также лучшее качество жизни как для пациентов, так и для семей [Steinhauser et al. al. 2001; Fallowfield et al. 2002; Райт et al. 2008]. Следовательно, общение является жизненно важным часть обеспечения хорошего EOLC.Как только клиницист распознал умирающего фазы у пациента, важно, чтобы это знание было передано относиться к семье должным образом и с состраданием, чтобы они тоже узнали ситуации и будьте готовы.
Общие принципы и шаги в общении с пациентами и семьями, когда обсуждение вопросов, связанных с окончанием срока службы, можно запомнить по аббревиатуре ПОДГОТОВЛЕН, как разработан Клейтоном и его коллегами [Clayton et al. 2007]:
P Подготовьте и усвойте всю обновленную информацию о состояние и состояние пациента
R Сообщение: относится к личности; проявить сочувствие и сострадание
E Ожидания: выявить ожидания пациента и опекуна и предпочтение информации
P Предоставьте информацию простым и понятным языком
A Признавайте эмоции и проблемы
R Реалистичная надежда
E Поощряйте вопросы
D Обсуждение документов в медицинских картах
Из этих шагов наиболее важным было бы наладить хорошее взаимопонимание с семья.Хорошее взаимопонимание можно рассматривать как «паспорт» общения без этого не следует пытаться обсуждать очень серьезный характер. Это просто потому, что, разговаривая с семьей о предвкушении смерть любимого человека — очень серьезное и изменяющее жизнь дело, которое требует, чтобы семья доверяла и верила в то, что слышит. Без установив хорошие отношения до этого, семья может сомневаться в достоверность и точность предоставленной информации [Lim, 2012].
Чтобы наладить хорошее взаимопонимание, клиницистам необходимо уметь относиться к человек, с которым они общаются; во-первых, начав с хорошего введение, а затем объяснение, как они участвуют в уходе за пациент. Затем врач должен дать понять, что он или она осведомлен о деле и в курсе последних проблем. Это где важна подготовка перед обсуждением. Один из самых простых способов терять взаимопонимание с семьей — это демонстрировать незнание рассматриваемого дела упоминание неточной информации.
Следующим важным навыком, помогающим развить семейные отношения, является способность Слушать. Слушание — это навык, который требует не только слышать, что представляет собой человек. говоря, но также внимательно относясь к языку их тела, тону голоса и искренне понимание того, что говорит другой человек. Клиницисты должны слушать чтобы понять, как семья воспринимает состояние пациента. Как только их восприятие будет понято, можно будет общаться таким образом, чтобы удовлетворить их потребности и проявлять сочувствие, которое еще больше укрепить отношения.Пытаясь понять представления семей, следует изучить следующие области:
Insight : Что семья понимает в настоящее время, и что до сих пор объясняли другие врачи?
Обеспокоенность : чего они боятся и какие проблемы требуют разъяснение?
Ожидания : На что они надеются и каковы их цели ухода? Что, по их мнению, будет сделано для пациента?
Можно использовать простую аббревиатуру ICE, чтобы запомнить это.
Ключевая область третья: обеспечение контроля над симптомами в последние дни
Среди симптомов, встречающихся в последние дни жизни пациентов с продвинутой стадией рак легких, наиболее часто встречающиеся приоритетные симптомы включают следующие [Ellershaw et al. al. 2001; Stone и др. . 2001; Квале эт. al. 2007]:
Боль
Одышка
Кашель
Беспокойство и делирий
Терминальные выделения
Клиницисты должны проявлять бдительность, чтобы распознать эти симптомы. знающие и умелые в управлении этими симптомами, которые будут способствовать хороший EOLC.
Таблица 1.
Примеры процесса коммуникации по окончании срока службы.
| Общение с членами семьи | Focus |
|---|---|
| Миссис А: «Доктор, расскажите, пожалуйста, как мой муж?
делаешь? » Доктор:« Да, конечно, я знаю, что вы, должно быть, очень переживает за него ». | Проявление сочувствия имеет большое значение для развития взаимопонимания. |
| Доктор:« За последние несколько дней у кого-нибудь
врачи говорили вам о его состоянии? Что ты
вспомнить, что есть у других врачей
объяснил? » Г-жа А:« Они просто сказали, что он не ну, но никогда ничего не упоминал о своих шансах становиться лучше.’ | Проверка понимания помогает вам использовать ту же длину волны, что и семья |
| Врач: «Глядя на то, каким был ваш муж последние несколько лет
дней, как вы думаете, дела обстоят? » Миссис А:« Он просто кажется становится все слабее и слабее. Он не получает лучше, не так ли? » Доктор:« Боюсь, что это правильно, ему не становится лучше, и рак делает его слабее в день. Я знаю, это должно быть сложно для вас, миссис А., но я боишься, что твой муж умирает ». | Изучение ожиданий поможет вам оценить, насколько глубоко
предмет, который вам нужно пройти Иногда это может просто требовать подтверждения того, что уже подозревается |
| Врач: «Скажите, что вас беспокоит больше всего?» | Изучите проблемы и никогда не предполагайте, что человек хочет знаю |
| Г-жа А: «Неужели вы ничего не можете сделать, чтобы сохранить ему жизнь? Ты должен
сделай что-нибудь, доктор, ПОЖАЛУЙСТА! » Доктор:« Я тебя знаю должна очень сильно его любить, и мысль о его потере должна быть таким болезненным.’ | Решительно реагируйте на эмоциональные высказывания, чтобы показать вам признать выраженные чувства |
| Доктор: «Ваш муж когда-нибудь говорил о том, что он хотел бы или не хотел бы для себя, если бы он сильно заболел как он сейчас? » | Позже, когда будет установлено хорошее взаимопонимание, и понимание, ожидания и опасения изучены, рассмотреть начало обсуждения расширенных планов ухода, таких как реанимация и предпочтительное место смерти и т. д. |
Боль
Боль — частый симптом у пациентов с запущенным раком. Эпидемиологический исследования показывают, что около 70% пациентов с запущенным раком страдают от боль [Teunissen и др. . 2007]. Обезболивание должно: поэтому должны предоставляться на протяжении всего периода болезни больного раком и даже в последние дни. Однако в последние дни у пациента способность говорить и глотать пероральные препараты часто снижается, и это распространенная ошибка среди клиницистов полагать, что на этом этапе пациенты больше не требуются обезболивающие.Функциональная позитронная эмиссия томография головного мозга показала, что даже пациенты с минимальным в сознательном состоянии может воспринимать боль [Boly et al. 2008]. Следовательно, рекомендуется применять все обезболивающие. продолжали в той же дозе, даже когда пациент перешел в менее сознательный конечное состояние.
Такое обезболивающее можно легко продолжить, преобразовав лекарства, такие как пероральный морфин для подкожного морфина или трансдермальный фентанил.Превращение морфина, вводимого подкожно, в морфин для перорального применения достигается с коэффициентом от 2 до 3, а пластырь с фентанилом 25 мкг / ч доставляет дозу, эквивалентную примерно 75 мг перорального морфина в день. Прорывные дозы морфина подкожно (это будет доза между От 1/12 до 1/6 суточной дозы, эквивалентной морфину). доступен в случае дополнительной боли. Это можно определить, наблюдая для невербального поведения, связанного с болью, такого как гримаса и стоны на лице, особенно по движению [Минздрав, 2010].
Одышка
Одышка — очень частый симптом при запущенном раке легких и в конце жизни этот симптом обычно сохраняется и часто усиливается [Kvale et al. al. 2007; Айер и др. . 2014]. Наряду с болью это симптом, который явно способствует плохому качеству жизнь и много горя в последние дни. Помимо паренхимы легких повреждение и обструкция дыхательных путей из-за обширного рака легких, существует множество другие причины одышки у пациентов с распространенным раком легких, включая обструкция верхней полой вены (SVCO), плевральный выпот, наложение грудной клетки инфекция, сопутствующая анемия, сердечная недостаточность, метаболический ацидоз, легочный эмболия и общая мышечная слабость.
В общем, начальный подход к лечению одышки заключается в исправлении что можно исправить, например, обеспечение кислородом, лечение инфекций, дренирование плевральный выпот или использование кортикостероидов у пациентов с SVCO [Twycross et al. al. 2009b]. Однако для пациентов, находящихся в в последние дни жизни, не всегда возможно или возможно исправить эти причины, следовательно, обеспечение адекватного облегчения симптомов является основой управления.
Опиоиды обладают значительным преимуществом при симптоматическом лечении одышки у пациенты с запущенным раком.У пациентов, ранее не принимавших опиоиды, это рекомендуется начинать с низких доз 2-3 мг перорального морфина или 1 мг морфин подкожно 6–8 раз в час и при необходимости. Если пациент переносимость морфина без побочных эффектов, тогда доза может быть постепенно титруют до 4 раз в час, а затем увеличивают по мере необходимости. Для пациентов, которые уже принимают опиоиды от боли, было бы целесообразно увеличить общую дозу опиоида на 20–30% и обеспечить прорывные дозы 1 / 12–1 / 6 от общей суточной дозы при необходимости, если одышка все еще остается серьезной, несмотря на повышенную дозу [Twycross et al. al. 2009b; Абернети и др. 2003; Jennings et al. 2002].
Хотя доказательств у пациентов, находящихся в тяжелом состоянии и беспокойство из-за одышки, добавление бензодиазепина может помочь уменьшить дистресс и беспокойство, которые часто усугубляют восприятие одышки. Если пациенты проявляют сильную тревогу с приступами паники, сублингвально лоразепам 0,5–1 мг могут быть полезны для уменьшения беспокойства. Подкожный мидазолам 2,5–5 мг также можно использовать в качестве альтернативы.Для пациентов, которые постоянно в тяжелом состоянии, непрерывная подкожная инфузия мидазолама 10-20 мг в течение 24 лет. обычно добавляется к опиоидной терапии [Currow et al. 2013; Саймон et al. 2010].
Кашель
Кашель — частый симптом при запущенном раке легких, который проявляется в течение нескольких месяцев и недель. до того, как пациент достигнет терминальной фазы, это может быть источником больших дискомфорт и страдания. Подход к этому симптому обычно зависит от причина кашля и его выделение мокроты или сухость.
При продуктивном кашле, связанном с гнойной мокротой, применяются антибиотики. может быть полезно, если есть инфекционный компонент, вызывающий этот симптом. К способствовать очищению от слизи, простая мера — использовать небулайзерный физиологический раствор. Муколитические агенты, такие как бромгексин, N-ацетилцистеин и гвайфенезин, могут также быть полезным. Если есть сопутствующий бронхоспазм, рассмотрите небулайзированные бронходилататоры. Если наблюдается сильное кровохарканье, могут использоваться антифибринолитические агенты, такие как транексамовая кислота.Паллиативный Лучевая терапия также может быть рассмотрена при сильном кровохарканье.
При сухом кашле, вызывающем беспокойство, и у пациентов, находящихся в последние дни жизни и слишком слаб, чтобы кашлять, опорой для лечения симптомов будет подавить кашель и дать пациенту отдохнуть. Кашель супрессивные средства включают кодеин из линктуса и сильные опиоиды в низких дозах, такие как морфин, гидрокодон, оксикодон или метадон. В тяжелых ситуациях можно рассмотреть распыленный лигнокаин; однако следует соблюдать осторожность, так как это может вызвать бронхоспазм.На этом этапе также можно рассмотреть возможность применения седативных средств. облегчить тяжелое состояние, если другие меры не дали результатов [Molassiotis et al. al. 2010; Twycross et al. 2009b].
Делирий и беспокойство
Делирий и беспокойство — общие симптомы в конце жизни, и они могут быть чрезвычайно хлопотной и изнурительной проблемой как для семьи, так и для персонал больницы. По мере прогрессирования рака и состояния пациента ухудшается, ранним симптомом делирия может быть обращение цикл сна-бодрствования, при котором семья будет жаловаться на то, что пациент не склонен хорошо спит ночью, но спит в основном днем.Как условие ухудшается, у пациента могут развиться гипоактивные или гиперактивные симптомы. Этот может включать симптомы спутанного поведения, бессвязной речи, нецелевого движения и попытки вставать и опускаться с кровати [Breitbart and Alici, 2008].
Столкнувшись с проблемой делирия, сначала следует подумать о простых исследования, чтобы исключить некоторые общие, но обратимые причины делирия такие как запор, гипогликемия, нарушение электролитного баланса, гиперкальциемия, сепсис или побочные эффекты лекарств.При отсутствии других обратимых причина, тогда можно рассмотреть диагноз терминального делирия, который что вызвано терминальным состоянием пациента. Семья может часто находить это пугающе, так как может показаться, что их любимый сходит с ума; это важно объяснить им, что это признак того, что «функция мозга нарушена. постепенно закрывается ».
Лечение делирия можно контролировать с помощью антипсихотических препаратов, таких как галоперидол в качестве первой линии. Это может быть дано перорально или подкожно с типичная доза 1–5 мг на ночь и 1 мг перорально.Помимо галоперидола, Также могут использоваться более новые атипичные нейролептики, такие как оланзапин, кветиапин ® или рисперидон.
Пациенты с гиперактивным делирием могут быть чрезвычайно возбуждены и иногда может потребоваться введение пациенту седативных средств с помощью короткодействующего бензодиазепин, такой как мидазолам. Обычно небольшая доза 2,5–5 мг может быть подкожно, по мере необходимости; однако это также может быть дано как непрерывная подкожная инфузия, постепенно титруемая до дозы между 0.5 и 2 мг в час, если желательна непрерывная седация. Должен быть помните, однако, что бензодиазепины не следует использовать в качестве монотерапии. для возбужденного делирия, так как это может привести к парадоксальному ухудшению возбуждение и должен использоваться в сочетании с антипсихотическими средствами [Twycross et al. al. 2009a].
Конечные выделения
Конечные выделения также известны как термин «предсмертный хрип», и он это знак, который неизбежно возвещает последние несколько часов или короткие дни жизни [Morita et al. al. 1998]. Он имеет звук, напоминающий звук грудная секреция и иногда может быть ошибочно принята за звук острого отек легких. Поэтому для клиницистов важно уметь: распознавать этот симптом и отличать его от других состояний, чтобы избегать бесполезных и ненужных исследований, таких как рентген грудной клетки, внутривенное введение антибиотиков и мониторинг ЭКГ. Ключ к признанию этого симптом в основном заключается в понимании прогноза и болезни пациента. траектория. Следовательно, если это пациент, который, как мы знаем, приближается к в конечной фазе, мы определенно узнаем звук как звук «Предсмертный хрип», а не острый отек легких.
Этот симптом — еще один очень тревожный симптом для членов семьи, поскольку он у них часто создается впечатление, что их любимый «тонет» в их выделения [Wee et al. 2006]. Поэтому важно объясните им, что это связано с выделениями в дыхательных путях, которые вызывают шумные колебания при прохождении воздуха, но не препятствуют вызвать респираторный дистресс у пациента. Также важно объяснить что отсасывание в этом случае бесполезно, так как оно не уменьшит дребезжание, но на самом деле может причинить пациенту больше страданий.Глубокое всасывание на самом деле может привести к стимуляции блуждающего нерва, что может вызвать внезапную брадикардию и асистолия у пациента, который уже находится в терминальной фазе. Несмотря на то что смерть — это ожидаемое событие, для пациента внезапная остановка дыхания во время процедуры отсасывания на самом деле может вызвать большое недовольство среди членов семьи.
Следовательно, лечение этого симптома будет заключаться в применении холинолитиков. лекарства, которые помогут уменьшить количество выделений и, таким образом, уменьшение дребезжащего звука.Обычные лекарства, которые используются в этом случае включают следующие [Twycross et al. 2009a]:
Гиосцина бутилбромид (бускопан) подкожно 20 мг 4–8 раз в час и prn
Подкожный гиосцина гидробромид 400 мкг 4–8 час и prn
Гликопирролат 200 мкг 4–8 час подкожно и prn
Эти лекарства также можно вводить непрерывно в течение 24 часов подкожно. настой.
Ключевая область четыре: принятие этических решений в конце жизни
Принятие клинических решений для пациентов с запущенным раком, которые приближаются конец жизни может быть трудным и временами ставить перед клиническая бригада.Это потому, что как медицинские работники воспринимают долг сохранять и поддерживать святость жизни. В то же время врачи также обязаны действовать в интересах пациента. «Святость доктрины жизни, которая была основным принципом биомедицинской этики до сегодня это принцип, унаследованный от иудео-христианского и гиппократовского традиции вековой давности [Баранцке, 2012]. Что касается ухода за пациентами в конце жизни, около века назад состояние медицинской науки было на уровне, когда часто, было мало сомнений в том, чтобы принять, когда смерть была неизбежна и решения позволить необратимой патологии развиваться естественным путем было легко.Сегодня, однако из-за достижений в области медицинских технологий все больше и больше вмешательства, продлевающие жизнь, открываются и, следовательно, обнаруживаются правильный баланс между количеством и качеством жизни теперь стал основным вызов EOLC. Поэтому клиницисты должны быть знакомы с общими этические принципы, применимые к принятию клинических решений в конце жизни, поскольку это позволяет им практиковать хороший EOLC с ясностью и ясностью совесть. Некоторые проблемы с окончанием жизни, которые могут вызвать сомнения у клиницистов включают:
Прекращение и прекращение поддерживающего жизнь лечения, такого как сердечно-легочная реанимация, искусственная вентиляция легких, искусственная гидратация и питание;
Седативные препараты, применяемые в конце жизни;
Путаница в терминологии эвтаназии.
Часто основной проблемой врача будет: «Предоставляет ли руководство мой пациент в конце жизни ускорит смерть и приблизится ли она к эвтаназии? »Из-за таких опасений клиницисты могут опасаться судебно-медицинских последствия и конфликт внутри себя при принятии решения , как вести пациента в конце жизни, и это может приводят к ухудшению EOLC [Swanson и МакКрари, 1996; Марик и др. 1999; Miccinesi et al. al. 2005].
Отказ от медицинского вмешательства
С этической точки зрения, нет никакой разницы между действиями по отказу от медицинского вмешательства. медицинское вмешательство и отказ от медицинского вмешательства. Следовательно, остановка поддерживающая жизнь терапия ничем не отличается от того, чтобы не начинать ее. Оба действия этически приемлемы при лечении [Ko and Blinderman, 2015; Британский Медицинский Ассоциация, 2009 г .; Ackermann, 2000]:
Futile;
Не в интересах пациента;
Отказано пациентом.
Руководящие принципы в этой ситуации включают автономию и милосердие. Понятно, что пациенты имеют полное право отказаться от лечения. вмешательства, даже если они могут быть полезными. Однако проблема возникает, когда пациент не может выразить эту автономию, и нет четкое предварительное распоряжение. В этой ситуации общение с суррогатом лицо, принимающее решение, чтобы определить предпочтения пациента в отношении ухода, является нормальным упражняться. Иногда это может быть сложно, потому что суррогатное решение производители, которые часто являются близкими родственниками, могут принимать эмоциональные решения, которые представляют свои собственные предпочтения и, возможно, не предпочтения пациента.Следовательно, важно объяснить суррогатному лицу, принимающему решение, что их выбор должен быть таким, который приближается к собственным предпочтениям пациента [Ko and Blinderman, 2015; GMC, 2010].
Клиницисты должны также очень четко помнить, что нет необходимости предлагать все формы поддерживающей жизнь терапии; профессиональное мнение что такие методы лечения не принесут очевидной пользы. Медицинская бесполезность можно определить количественно, имея в виду вмешательство с очень отдаленными шансы получить выгоду; или это может быть определено качественно, то есть вмешательство вряд ли приведет к достижению ориентированных на пациента целей.В клинической на практике, однако, может быть трудно определить бесполезность, поскольку все люди пациент, врач и семья могут иметь разные взгляды на то, что полезны и каковы должны быть цели ухода. Поэтому полезное руководство помочь клиницистам решить, что считать бесполезным, означало бы определить цели лечения в каждом отдельном случае, прежде чем рассматривать вмешательство. Если вмешательство вряд ли приведет к достижению этих целей в каком-либо Кстати, тогда бесполезность следует считать [Schneiderman, 2011].
Одна из самых сложных сфер, связанных с отказом от медицинской помощи. вмешательства — это вопрос искусственного увлажнения и питания. Она имеет Утверждалось, что гидратация и питание считаются основными потребностями заботы, которой никогда не следует лишать ни одного человека. Тем не мение, искусственное увлажнение и питание через зонд для кормления или внутривенное не такие простые, как обычное пероральное кормление и питье. Многие из этические дилеммы отказа от искусственного увлажнения и питания, однако из-за его использования у пациентов со стойкими вегетативными состояниями, где такие вмешательства позволяют пациентам выжить годами, и его абстинентный синдром можно рассматривать как преднамеренный акт по сокращению жизни [Brody et al. al. 2010]. Однако в контексте пациента с запущенный рак, который находится в последних днях жизни, совершенно ясно, что доказательства показали, что искусственная гидратация не приносит пользы для выживаемости. и питание [Хорошо et al. 2008a, 2008b]. Невозможность поддерживать питание пероральным путем на поздних стадиях рака, и убывающая функция, являются маркерами процесса умирания; и обеспечение хороших уход за полостью рта и поддержание чистоты и влажности полости рта — лучшая форма паллиатив.Прекращение искусственного увлажнения и питания в таком случае является недопустимым. поэтому уместно [Сломка, 2003; Twycross et al. 2009а].
Хотя с этической точки зрения клиницисты имеют право отказать или отозвать медицинские вмешательства по причине врачебной бесполезности, следует помнить, что эти решения все же следует обсудить с семьей, чтобы убедиться, что они понять причину и основу таких решений. Если семья, однако, отказываться принимать эти решения и требовать вмешательства, чтобы продолжайте, клиницисты должны передать дело коллеге на секунду мнение и кто может согласиться на продолжение ухода или дальнейшие переговоры управление с семьей [GMC, 2010; Ко, Блиндерман, 2015].
Использование седативных препаратов в конце жизни
Один из распространенных страхов клиницистов по поводу использования седативных препаратов, таких как поскольку морфин или бензодиазепины в конце жизни ускоряют смерть. это распространено мнение, что с помощью таких лекарств и без того хилого и слабого пациенту, эти препараты могут привести к гипотонии, угнетению дыхания и смерть. Из-за этих опасений врачи часто неохотно предоставляют адекватное облегчение боли и седация при беспокойстве в терминале фаза.Однако данные показали, что такие лекарства действительно могут быть назначается пациентам в терминальной фазе, не вызывая каких-либо значительных снижение выживаемости при правильном использовании для облегчения симптомов конец жизни [Мальтони et al. 2012; Морита и др. . 2001, 2005; Сайкс и Thorns, 2003]. Однако, если седативные препараты, такие как морфин или бензодиазепины действительно ускорили смерть, использование таких лекарств может по-прежнему быть оправданным, исходя из принципа «двойного эффекта» и принцип пропорциональности [De Graeff and Dean, 2007; Juth et al. al. 2010; Krakauer et al. 2000].
Принцип «двойного эффекта» гласит, что если действие имеет целью хороший эффект может достичь этого эффекта только с риском произвести вредного воздействия, то это действие этически допустимо при условии, что удовлетворяет следующим условиям:
Акция хороша сама по себе;
Цель состоит исключительно в том, чтобы произвести хороший эффект;
Хороший эффект не достигается плохим эффектом;
Есть достаточная причина для того, чтобы допустить плохой эффект.
Таким образом, этот принцип отличает использование седативных препаратов в конец жизни из-за эвтаназии, так как в этом случае намерение состоит в том, чтобы облегчить боль, одышка или беспокойство, и ни в коем случае не намерен намеренно причинить вред пациенту. Когда используются такие седативные препараты, они вводят в малых дозах и титруют до тех пор, пока не будет получено достаточно достичь желаемого эффекта, что демонстрирует этическая практика, основанная на принцип соразмерности.
Эвтаназия, с другой стороны, не может быть оправдана этими принципами, поскольку в практике эвтаназии используются средства, выходящие за рамки необходимого чтобы просто облегчить симптомы, и цель состоит в том, чтобы вызвать немедленную смерть пациент. Следовательно, даже если врач заявит, что его намерение состоит в том, чтобы облегчить страдания, практика эвтаназии является примером достижения хороший эффект через плохой эффект [Materstvedt et al. 2003].
Запутанная терминология эвтаназии
Терминология, такая как «активная эвтаназия», «пассивная эвтаназия», «добровольная эвтаназия »и« недобровольная эвтаназия », которые широко использовались в литературы, приводят к тому, что врачи чувствуют замешательство и неуверенность в том, что практика фактически представляет собой эвтаназию.Термин «пассивная эвтаназия» часто используется для описания удержания или отказа от бесполезных медицинских вмешательства при «активной эвтаназии» и «добровольной эвтаназии» синонимы описывают активное и преднамеренное администрирование вмешательство, которое приводит к смерти пациента, добровольно просил это. «Недобровольная эвтаназия» описывает акт преднамеренного проведение вмешательства, которое приводит к смерти пациента, у которого добровольно не просил о таком вмешательстве из-за отсутствия возможностей.В чтобы прояснить некоторые из этих часто вводящих в заблуждение терминов, европейские Ассоциация паллиативной помощи опубликовала консенсусное заявление, определяющее эвтаназия как: «Врач умышленно убивает человека прием лекарств по добровольной и компетентной просьбе этого лица ». Далее они пояснили, что эвтаназия всегда должна быть активной, а термин «Пассивная эвтаназия» — это противоречие терминов. Эвтаназия также должна всегда быть добровольным, и «недобровольная» эвтаназия, по сути, является убийством. В поэтому ключевым словом в определении эвтаназии является слово «Преднамеренный».Намерение состоит в том, чтобы убить человека, и успешный результат для наступит немедленная смерть [Matersvedt et al. 2003; Matersvedt, Bosshard, 2015].
Следовательно, врачи должны четко понимать определение эвтаназии, а не путайте это с этически приемлемым менеджментом в конце жизни, например как отказ от бесполезных медицинских вмешательств и паллиативных седация в конце жизни.
Заключение
Несмотря на успехи в лечении рака легких, большинство пациентов все еще умереть от болезни в течение 5 лет после постановки диагноза, и смерть от рака легких может быть связано со многими симптомами и низким качеством жизни.Клиницисты должны поэтому лучше осознавать потребности таких пациентов и изучать основные навыки необходим для ухода за пациентами на этой стадии их болезни.
Хотя в области паллиативной медицины произошли значительные изменения. во всем мире все еще очевидно, что многие пациенты, нуждающиеся в паллиативной помощи, не может получить к нему доступ по разным причинам, например, из-за недостатка знаний и навыков среди медицинских работников отсутствие основных лекарств, особенно опиоиды, и отсутствие систем здравоохранения для оказания такой помощи [Всемирная паллиативная помощь Альянс, 2014].Даже в тех районах, где легко доступны услуги паллиативной помощи. доступны, все еще существуют препятствия, мешающие пациентам получить хороший EOLC уход, например, нежелание клиницистов направлять пациентов к паллиативной помощи услуги, а также нежелание пациентов получать направление из-за негативного восприятия паллиативной помощи и ее значение [Wentlandt et al. 2012].
В мае 2014 года Всемирная организация здравоохранения приняла резолюцию об усилении паллиативной помощи как компонента комплексной помощи на протяжении всей жизни это подчеркнуло необходимость интеграции паллиативной помощи в система здравоохранения для обеспечения доступа для всех нуждающихся [Всемирная организация здравоохранения, 2014].Для этого стремление стать реальностью, все медицинские работники заботятся о пациентах с серьезными заболеваниями, в том числе с раком легких, должны иметь базовые знания и навыки для улучшения ухода к концу жизни в ситуациях, когда лечение больше не Возможность.
Физические признаки окончания срока службы
Как узнать, что человек с хроническим заболеванием легких вступает в последний этап жизни? На этой странице мы объясняем физические признаки заключительных стадий и способы борьбы с этими симптомами.Мы также объясняем, чего ожидать в последние дни.
На этой странице:
Каковы признаки того, что кто-то приближается к концу жизни?
По мере того, как люди достигают последних стадий хронического заболевания легких, часто происходят типичные физические изменения. Но не всегда легко предсказать, когда жизнь подойдет к концу.
У каждого человека свой жизненный опыт в конце жизни. Наличие этих симптомов не обязательно означает, что кто-то близок к смерти.
Большинство хронических заболеваний легких постепенно ухудшаются в течение нескольких лет.Наиболее частым симптомом является сильная одышка. У некоторых людей дыхание может ухудшиться намного быстрее, в течение недель или месяцев. Это особенно верно в отношении интерстициальных заболеваний легких, таких как IPF.
У тех, кто находится на последней стадии заболевания легких, дыхание заметно ухудшается. После каждого обострения или обострения их функция легких не возвращается на прежний уровень, и дыхание становится труднее.
Ваши легкие становятся менее эффективными из-за долгосрочного заболевания легких.Любое напряжение, даже простая смена позы, разговор или прием пищи, может вызвать у вас одышку. Если вы лежите ровно, вам может стать неудобно дышать, поэтому вы можете попробовать спать в довольно вертикальном положении. Снижение функции легких может привести к снижению уровня кислорода в крови. Это может вызвать задержку жидкости в ногах и животе, что может вызывать дискомфорт. При обострениях обычно еще больше снижается содержание кислорода в крови, что может усугубить эти симптомы.
Другие симптомы могут включать неприятный кашель, плохой аппетит, боль в груди и нарушение режима сна.
Наиболее частые физические симптомы:
- сильная одышка
- снижение функции легких, затрудняющее дыхание
- с частыми обострениями
- испытывают трудности с поддержанием здорового веса тела из-за потери аппетита
- Чувствую себя более тревожно и подавленно.
Вы, ваша семья и лица, осуществляющие уход, можете попросить свою медицинскую бригаду дать дополнительные советы и информацию о том, чего ожидать в ваших конкретных обстоятельствах.
Борьба с симптомами в конце жизни
Боль — частый симптом любого тяжелого физического заболевания и может быть частью нормального процесса умирания. Обычно это хорошо контролируется с помощью правильных лекарств. Эти лекарства могут включать опиоиды (морфиноподобные обезболивающие). Вы можете беспокоиться о приеме опиоидов, если у вас или у вашего близкого есть респираторное заболевание, но они безопасны для людей с заболеваниями легких.
Вам будут давать наркотики таким образом, чтобы вызвать наименьший дискомфорт, боль или стресс.Ваш врач может предложить попробовать низкую дозу жидкого морфина короткого действия. Это нужно для того, чтобы изначально увидеть, насколько вам нужна помощь с вашими симптомами. Если это поможет, ваш врач может посоветовать вам таблетки морфина длительного действия или морфиноподобный пластырь.
Одышку можно улучшить, используя ингаляторы, таблетки и иногда небулайзеры. Если вы чувствуете одышку, может быть полезно использовать ручной вентилятор. Ощущение воздуха на лице может облегчить дыхание.Но если у вас более серьезная одышка и низкий уровень кислорода в крови, длительный прием кислорода может улучшить ваше дыхание и качество жизни.
Долгосрочный домашний кислород необходим, когда легкие больше не могут поддерживать достаточное количество кислорода в крови. Этот кислород обычно доставляется из машины, которая концентрирует кислород из воздуха, называемого концентратором кислорода. Вам необходимо использовать эту машину не менее 15 часов в день. Количество необходимого кислорода тщательно оценивается и контролируется, и со временем может потребоваться его увеличение.Узнать больше о кислородной терапии.
Кислород доступен только по рецепту и предоставляется местным поставщиком кислорода. Как правило, ваша местная команда респираторов оценит вашу потребность в кислороде. Переносной кислород, обычно из небольших баллонов, также доступен и позволяет путешествовать и выезжать на природу.
Ваш терапевт может назначить только паллиативный кислород. Это для людей, которые достигают конечной стадии жизни и имеют низкий уровень кислорода в крови.
Кислородная терапия, используемая для лечения низкого уровня кислорода в крови, не всегда может уменьшить одышку.Если ваша одышка становится очень неприятной, несмотря на использование кислорода, существует ряд лекарств, уменьшающих ощущение одышки. К ним относятся низкие дозы седативных средств, таких как диазепам или лоразепам, а также болеутоляющие средства, называемые опиоидами, такие как морфин.
Беспокойство и депрессия могут быть обычным явлением, если у вас затрудняется дыхание и может ухудшиться самочувствие. Одиночество и изоляция также являются распространенными проблемами, если вы прикованы к дому с хроническим заболеванием легких.
Если вам сложно выйти из дома из-за затрудненного дыхания, обратитесь за помощью к специалисту в области здравоохранения. Беспокойство и депрессия могут стать настолько серьезными, что потребуют отдельного лечения.
Вы также можете найти методы расслабления или дыхания, которые помогают ослабить чувство напряжения и беспокойства. У нас есть больше информации о технике дыхания в Интернете.
Задержка жидкости можно лечить с помощью водных таблеток, называемых диуретиками.Частые походы в туалет могут стать проблемой, если вы чувствуете одышку и вам трудно двигаться. Спросите своего лечащего врача об использовании писсуара или комода. Катетеры — это трубки, по которым моча выходит из мочевого пузыря из организма. Они могут быть полезны в конце жизни, но есть риск осложнений, включая инфекцию и дискомфорт.
Потеря аппетита — обычная проблема и часто является естественной частью процесса болезни. Немного из того, что вам нравится, может помочь увеличить количество еды, доставить вам удовольствие и, в конечном итоге, повысить качество жизни.Если вам трудно глотать, выбирайте более мягкую и влажную пищу.
Иногда небольшие приемы пищи плюс легкие закуски в течение дня работают хорошо. Высококалорийные закуски могут включать пирожные и печенье, сыр и йогурты из цельных сливок. Выбирайте питательные напитки, такие как жирное молоко, горячий шоколад, солодовые напитки, смузи, фруктовые соки и обогащенные супы. Безрецептурные обогащенные супы и молочные коктейли доступны в большинстве супермаркетов и аптек.
Если вы используете кислород, попробуйте использовать носовую канюлю во время еды.Если вы используете маску для лица, не забывайте заменять ее между глотками, чтобы уровень кислорода не падал во время еды.
Если есть действительно трудно, могут помочь пищевые добавки, которые могут назначить врач или медсестра. Вас также могут направить к диетологу. Вы можете купить некоторые пищевые добавки без рецепта, но всегда спрашивайте совета, чтобы подобрать для вас лучшую. Узнайте больше о правильном питании при заболевании легких.
Основные советы по уходу за тем, кому нужна помощь в еде:
- Посмотрите на человека, чтобы он мог видеть вас и свою еду.
- Если человек обычно носит очки или слуховой аппарат, помогите ему надеть их. Это поможет им увидеть, что вы делаете, и услышать, что вы говорите.
- Предлагайте небольшие обеды или порции, которые не подавляют человека.
- Дайте человеку есть медленно. Дайте им достаточно времени, чтобы пережевывать пищу и проглатывать ее. Возможно, им придется переводить дыхание перед каждым глотком.
- Следите за подсказками, которые помогут вам определить, когда они закончили глотать.Если сложно сказать, спросите человека, закончили ли он, или откройте рот, чтобы посмотреть, не осталась ли внутри еда.
- Для напитков используйте широкую чашку или стакан, чтобы пьющему не приходилось запрокидывать голову назад. Вы также можете использовать трубочку для холодных напитков.
- Не торопитесь с едой. Это может увеличить риск попадания пищи в дыхательные пути человека.
- Обратите внимание на признаки усталости. Если человек становится сонным, ему лучше прекратить есть, даже если он еще не закончил прием пищи.Это потому, что люди чаще кашляют или подавляются пищей.
- Если возможно, постарайтесь сделать так, чтобы человек выжидал не менее 15 минут, прежде чем снова лечь в постель или лечь. Это снижает вероятность того, что еда и питье снова попадут в горло и заставят их подавиться.
Кашель может быть проблемой. Сядьте максимально прямо, опираясь на подушки. Существуют лекарства, которые могут помочь остановить мучительный кашель. Их может прописать ваша медицинская бригада.Приступы кашля и сильная одышка также могут вызывать недержание мочи. С этим можно справиться, уменьшив количество напитков, содержащих кофеин, таких как чай и кофе, а также уменьшив потребление алкоголя. Есть также ряд продуктов, которые могут помочь в лечении недержания мочи, в том числе мочевой пузырь и мешок, называемый мочевым катетером. Поговорите со своей медицинской бригадой о том, может ли это помочь.
Икота, несварение желудка и рефлюкс могут быть трудными для лечения, если у вас неизлечимая болезнь. Доступно лечение, чтобы помочь справиться с этими симптомами, и есть вещи, которые вы или ваш опекун можете сделать, чтобы помочь вам чувствовать себя более комфортно.Более подробная информация об этом есть у Марии Кюри на своем веб-сайте.
Усталость (утомляемость) и нарушение сна являются обычным явлением по мере прогрессирования заболевания легких. Усталость может быть вызвана сочетанием беспокойства, депрессии, плохого сна и низкокалорийного потребления. Недостаток сна также может быть вызван такими симптомами, как одышка, боль и кашель, нарушающий сон. Дневной сон также может затруднить сон ночью. Усталость может никогда не исчезнуть полностью, но есть методы, которые помогут вам справиться с ней, а иногда и лекарства, которые могут помочь с некоторыми из причин.Поговорите со своим лечащим врачом о возможных причинах и о том, как с ними бороться.
Обострение болезни может произойти, если вы подхватите инфекцию грудной клетки. Инфекция грудной клетки означает, что у вас будет более сильный кашель с обесцвеченной, желтой или зеленой мокротой, и вы почувствуете одышку. Это следует лечить незамедлительно и обычно улучшается с помощью антибиотиков и короткого курса стероидов.
Если у вас серьезные обострения, вас могут госпитализировать, и вам может потребоваться неинвазивная вентиляция легких, чтобы повысить уровень кислорода, поступающего в легкие.Это осуществляется с помощью маски и портативного устройства, поддерживающего дыхание, путем подачи воздуха или кислорода под небольшим давлением.
Чего мне ожидать в последние несколько дней?
По мере приближения конца жизни вы можете испытать ряд физических и эмоциональных изменений. Они у всех разные. Вы можете заметить изменения в течение недель, дней или даже часов. Некоторые изменения могут быть похожи на признаки обострения, поэтому обсудите их со своим врачом или медсестрой.
Знаков, на которые следует обратить внимание, включают:
- Не хочет есть или пить очень много или совсем.Может затрудниться глотание
- Потеря физической энергии, способность или желание говорить и признаки ухода от семьи и друзей.
- Чувство сонливости или сонливости большую часть времени, очень малоподвижный образ жизни и в конечном итоге теряет сознание. Нет ничего необычного в том, чтобы оставаться в постели или в удобном кресле, а не вставать.
- Изменения частоты или характера дыхания. По мере того, как организм становится менее активным, потребность в кислороде снижается. Между вдохами могут быть длинные паузы, и животик может двигаться вверх и вниз больше, чем грудь.Вдыхание и выдох может вызвать бульканье или хрипы из-за скопления мокроты, которую невозможно откашлять. Помните, что это шумное влажное дыхание может причинить больше беспокойства окружающим, чем пострадавшему. Существуют лекарства, которые могут помочь высушить мокроту.
- Изменение цвета и температуры кожи. Непосредственно перед смертью кожа может стать бледной, влажной и немного прохладной.
- Непроизвольные подергивания. Это нормально и не означает, что кто-то расстроен или неудобен.Если вы заметили это, лучше всего рассказать о них любому специалисту в области здравоохранения, в котором они участвуют в данный момент.
- Требуется кислород, если он еще не используется, и поддержка другого медицинского оборудования. Это не должно мешать физическому контакту. Не бойтесь касаться друг друга и быть рядом.
Использование медицинского оборудования на заключительных этапах
Кислородная терапия может стать обременительной в последние дни и часы жизни. Это связано с тем, что вдувание в дыхательные пути может вызвать болезненность, а по мере того, как человек становится менее осведомленным о своем окружении, это может вызвать расстройство.В этом случае кислородную терапию можно прекратить, даже если уровень кислорода низкий. Это с осознанием того, что это поможет облегчить дискомфорт умирающего, а не способствовать смерти.
В целом, использование медицинского оборудования на заключительных этапах сосредоточено на утешении умирающего и сводится к минимуму, чтобы как можно меньше беспокоить его.
Ваш лечащий врач также может прописать «на всякий случай» лекарства, которые нужно держать дома.Обычно это инъекционные препараты, которые медсестра по месту жительства даст вам при таких симптомах, как боль или одышка, когда пероральные препараты — не лучший выбор. Иногда бывает трудно получить быстрый доступ к лекарствам ночью или в выходные дни. Наличие коробки с лекарствами «на всякий случай» означает, что ваш лечащий врач может быстро контролировать симптомы, если вы испытываете боль или начинаете чувствовать себя плохо.
Читать дальше: Забота о любимом на завершающем этапе
Загрузите нашу информацию об окончании срока службы (PDF, 490 КБ)
Мы стремимся предоставлять бесплатную актуальную экспертную информацию о здоровье легких
Более 6.5 миллионов человек в Великобритании страдают заболеванием легких — дыхание не является чем-то само собой разумеющимся.
Мы хотим дать людям с заболеваниями легких знания, необходимые для хорошей жизни.
Ваша поддержка помогает гарантировать, что мы сможем и дальше предоставлять бесплатные советы и информацию, когда люди в ней больше всего нуждаются.
Если вы найдете наши советы по здоровью полезными, сделайте небольшое пожертвование сегодня.
Пожертвовать сейчас
Этапы 1-4, Limited vs.Extensive
Важно знать стадию рака легких. Он сообщает вам:
- Где опухоль или раковые клетки находятся в ваших легких
- Насколько велика ваша опухоль сейчас
- Если ваш рак в одном месте или распространился
Есть два основных типа рака легких: маленький ячейка и немелкая ячейка. Каждый ставится по-своему.
Знание стадии помогает врачу выбрать для вас подходящее лечение. Это также может помочь им оценить ваши шансы на успех этого лечения.
Одна вещь, которую ваша стадия рака легких не может сказать вам, — это то, как долго вы проживете.
Что такое система TNM?
Для определения стадии рака легкого часто используются буквы T, N и M:
- T обозначает размер опухоли и ее расположение в легких или теле.
- N означает участие узла. Это означает, распространился ли ваш рак на лимфатические узлы рядом с легкими.
- M обозначает метастаз. Это означает, распространился ли ваш рак.Рак легкого может распространиться на другие легкие или печень, кости, мозг, почки, надпочечники или другие части вашего тела.
Ваш врач может определить стадию опухоли с помощью этих букв, а затем уточнить цифры от 0 до 4.
Они измерит размер вашей опухоли в сантиметрах, чтобы дать ей номер. Чем выше число, тем больше опухоль выросла или распространилась.
Они также могут использовать X как число. Это означает, что опухоль невозможно измерить или неясно, насколько далеко она распространилась.
Если ваш врач говорит, что ваш рак легких «неоперабельный», это означает, что хирурги не могут его удалить.
Стадии мелкоклеточного рака легкого
Если у вас этот тип рака, ваш врач может использовать систему TNM. Затем они поместят ваш рак в одну из двух основных стадий:
- Ограниченная стадия. Это всего лишь одно легкое и, возможно, близлежащие лимфатические узлы. Он не распространился ни на легкие, ни через легкие.
- Обширный этап. Ваша опухоль распространилась на другие области ваших легких и груди.Возможно, он распространился на жидкость вокруг ваших легких (так называемая плевра) или других органов, таких как мозг.
Стадии немелкоклеточного рака легкого
Немелкоклеточный рак легкого (НМРЛ) является более распространенным типом рака легких, чем мелкоклеточный.
Один из способов описания НМРЛ — его клиническая или патологическая стадия. Ваш врач может использовать визуализацию, чтобы сфотографировать внутреннюю часть вашего тела, чтобы узнать, на какой клинической стадии находится рак. Чтобы подтвердить диагноз, они могут сделать биопсию, при которой они берут небольшой кусочек ткани опухоли и рассматривают его под микроскопом.
Если вам сделали операцию по удалению рака, ваш врач может осмотреть опухоль и определить патологическую стадию рака. Это говорит вашему врачу, насколько далеко распространился рак.
Наиболее распространенный способ определить стадию опухоли НМРЛ — использовать систему TNM с числами X, 0, 1, 2, 3 или 4 после каждой буквы.
Комбинации цифр и букв описывают:
- Ширина вашей опухоли, измеренная в сантиметрах, или если она слишком мала, чтобы ее вообще можно было измерить
- Где расположена ваша опухоль в легком
- Если в одном легком более одной опухоли
- Если ваши дыхательные пути частично заблокированы или забиты настолько, чтобы вызвать коллапс легких или пневмонию
- Если опухоль распространилась на ваши лимфатические узлы или другие органы
Врачи могут также назначить общие стадии НМРЛ.Вы можете использовать систему TNM и числа для определения стадии рака в каждом из них:
- Оккультная стадия: Раковые клетки могут быть собраны в слизи, которую вы откашливаете. Вашу опухоль нельзя увидеть ни на снимках, ни на биопсии. Его также называют скрытым раком.
- Стадия 0: Ваша опухоль очень маленькая. Раковые клетки не распространились в более глубокие ткани легких или за пределы легких.
- Стадия I («стадия 1»): Рак находится в тканях легких, но не в лимфатических узлах.
- Стадия II («стадия 2»): Заболевание могло распространиться на ваши лимфатические узлы рядом с легкими.
- Стадия III («стадия 3»): Она распространилась дальше в лимфатические узлы и середину груди.
- Стадия IV («стадия 4»): Рак широко распространился по вашему телу. Возможно, он распространился на ваш мозг, кости или печень.
Типы, симптомы, диагностика, лечение и прогноз
Врачи используют стадии, чтобы описать, насколько у вас рак и где он находится в вашем теле.Люди с раком легких III стадии могут быть очень смешанной группой. Их опухоли могут различаться по размеру, месту расположения и расстоянию от места возникновения рака.
Но почти всегда рак III стадии находится только в одном легком. Он также ограничен лимфатическими узлами, органами и другими тканями рядом с этим органом. Более того, рак не распространился и не дал метастазов. Вот почему эту стадию еще называют местнораспространенным или местно-регионарным заболеванием.
Следующая стадия, стадия IV, является последней и самой серьезной стадией рака.
Типы и стадии
Почти 9 из 10 человек с раком легких имеют немелкоклеточный рак легкого (НМРЛ). Более редкий и агрессивный тип называется мелкоклеточным раком легкого. Но пронумерованные стадии используются в основном при более распространенном НМРЛ.
Стадия использует три ключевых критерия, называемых TNM:
Опухоль (T) . Насколько велика и где находится опухоль?
Узлы (N) . Есть ли рак в близлежащих лимфатических узлах?
Метастаз (M) .Насколько далеко рак распространился от своего первоначального места?
Врачи разделяют немелкоклеточный рак легкого III стадии на три основных подтипа. Это помогает им получить более подробную картину вашего рака и выбрать лучшее лечение.
Stage IIIA . У вас одна или несколько опухолей в одном легком. Рак находится в близлежащих лимфатических узлах. Рак может быть в некоторых близлежащих тканях, но он не достиг отдаленных органов.
Стадия IIIB . У вас одна или несколько опухолей в одном легком.Ваш рак мог распространиться на лимфатические узлы выше ключицы и может быть в лимфатических узлах на противоположной стороне груди. Рак может быть в некоторых близлежащих тканях, но не в отдаленных органах.
Этап IIIC. Это наиболее продвинутая стадия III стадии. У вас одна или несколько опухолей в одном легком. Ваш рак распространился на лимфатические узлы над ключицей или на лимфатические узлы на противоположной стороне груди. Рак может быть в грудной стенке, сердце, грудины и других близлежащих тканях, но не распространился на отдаленные органы.
Симптомы
В большинстве случаев немелкоклеточный рак легкого обнаруживается на поздней стадии. Отчасти это связано с тем, что болезнь быстро прогрессирует и часто не имеет признаков на ранних стадиях. Но симптомы могут включать:
Если рак легких III стадии распространился за пределы легких, он может вызвать другие симптомы. Например, у вас может возникнуть боль в костях, если она распространилась на кости.
Диагноз
Вероятно, ваш врач обнаружил рак легких после проверки ваших симптомов.Большинство людей не проходят плановую проверку на наличие болезни, если только они не курят или не подвергаются более высокому риску.
Рентген грудной клетки часто является первым тестом изображения. Если он предполагает, что у вас рак, вам нужно пройти дополнительные тесты, например:
Компьютерная томография (КТ) . Ваш врач может заказать версию этого сканирования с контрастным усилением, которая позволяет получать более подробные изображения.
Ваш врач может провести другие тесты, чтобы проверить степень вашего рака. Они могут включать:
Биопсия. Врач исследует образец вашей ткани под микроскопом, чтобы подтвердить, что это рак.
Лечение
У ваших врачей есть несколько способов лечения в зависимости от размера, местоположения и других характеристик вашего рака:
Хирургия . Если возможно, ваш врач может выбрать операцию по удалению всех опухолей.
Химиотерапия . Вы часто можете получить это после операции, чтобы помочь подавить любой будущий рак.
Радиация .Если хирургическим путем не удалось вылечить весь рак, вы можете пройти лучевую терапию. Или вы можете пройти химиотерапию с последующей лучевой терапией.
Химиолучевой . Если операция невозможна, вы можете пройти курс химиотерапии или лучевой терапии, или и то, и другое одновременно.
Иммунотерапия. Здесь используются лекарства, чтобы сплотить собственную иммунную систему вашего тела для борьбы с раком. Ваш врач может использовать иммунотерапию в качестве первого лечения, если операция не подходит, или использовать ее после химиолучевой терапии.
Перспективы
В США от рака легких умирает больше людей, чем от рака груди, толстой кишки и простаты вместе взятых. Примерно каждый третий человек, у которого диагностирован рак легких IIIA стадии, живет не менее 5 лет после постановки диагноза. Для стадии IIIB средняя 5-летняя выживаемость составляет 26%. Для этапа IIIC это 13%.
Ваш долгосрочный прогноз может быть лучше, если вы:
- Потеряли менее 5% своего веса до начала лечения
- Являетесь ли вы женщиной
- У вас нет легочной инфекции, коллапса легкого или скопления жидкости вокруг легкое
- Имеют тип раковых клеток, которые хорошо поддаются определенному лечению.
Жизнь с раком легких III стадии
Любое серьезное заболевание может принести беспокойство, неуверенность и другие проблемы для вас и ваших близких.Попробуйте:
Управляйте своей болью. Вы можете пострадать не только от рака, но и от лечения. По мере возможности работайте со своими врачами, чтобы контролировать вашу боль. Это также может снизить ваши шансы на депрессию.
Устранение других симптомов. Потеря веса — обычное дело, когда у вас рак. Правильно питайтесь, чтобы поддерживать свои силы и предотвратить инфекции. При постоянном кашле вы можете найти облегчение с помощью:
Легочная реабилитация также может улучшить ваши симптомы и качество жизни . Это может помочь вам легче дышать и оставаться более активным.
Бросить курить. Никогда не поздно остановиться. Люди, которые бросают курить до лечения рака, обычно реагируют лучше. Если вам трудно бросить курить, может помочь программа отказа от курения.
Связаться с другими . Не бывает слишком большой поддержки. Может быть полезно поговорить с медицинским социальным работником, консультантом по психическому здоровью или другими специалистами. Присоединяйтесь к группе поддержки рака лично или онлайн.Узнайте, предлагают ли какие-либо местные группы бесплатные поездки на встречи и другую помощь. У Американского онкологического общества есть каталог программ с возможностью поиска.
Рак легкого — немелкоклеточный: Стадии
НА ЭТОЙ СТРАНИЦЕ: Вы узнаете, как врачи описывают рост или распространение рака. Это называется этапом. Используйте меню для просмотра других страниц.
Стадия — это способ описания того, где находится рак, если или где он распространился, а также влияет ли он на другие части тела.Врачи используют диагностические тесты, чтобы определить стадию рака, поэтому определение стадии может быть неполным, пока не будут завершены все тесты. Знание стадии помогает врачу решить, какой вид лечения лучше всего, и может помочь предсказать прогноз пациента, который является шансом на выздоровление. Существуют разные описания стадий для разных типов рака.
В целом, меньшее количество стадий НМРЛ связано с лучшим исходом. Однако ни один врач не может предсказать, сколько проживет пациент с раком легких, основываясь только на стадии заболевания.Это связано с тем, что рак легких отличается у каждого человека, и лечение каждой опухоли работает по-разному.
Группа стадий рака
Стадия НМРЛ основана на сочетании нескольких факторов, в том числе:
Существует 5 стадий НМРЛ: стадия 0 (нулевая) и стадии с I по IV (с 1 по 4). Один из способов определить стадию НМРЛ — выяснить, может ли хирург полностью удалить рак. Чтобы полностью удалить рак легких, хирург должен удалить опухоль вместе с окружающей здоровой тканью легких и часто близлежащими лимфатическими узлами.Узнайте больше о вариантах лечения НМРЛ.
Этап 0
Это называется заболеванием in situ, что означает, что рак находится «на месте», а не прорастает в близлежащие ткани и не распространился за пределы легкого.
I этап
Рак легких I стадии — это небольшая опухоль, которая не распространилась на лимфатические узлы, что позволяет хирургу полностью удалить ее. Стадия I делится на 2 подэтапа в зависимости от размера опухоли:
- Опухоли стадии IA имеют размер 3 сантиметра (см) или меньше.Опухоли стадии IA могут быть далее разделены на IA1, IA2 или IA3 в зависимости от размера опухоли.
- Опухоли стадии IB имеют размер более 3 см, но не более 4 см.
II этап
Рак легких II стадии делится на 2 подэтапы:
- Рак стадии IIA — это опухоль размером более 4 см, но не более 5 см, которая не распространилась на близлежащие лимфатические узлы.
- Рак легких стадии IIB описывает опухоль размером 5 см или меньше, распространившуюся на лимфатические узлы.Рак стадии IIB также может быть опухолью шириной более 5 см, которая не распространилась на лимфатические узлы.
Иногда опухоли стадии II можно удалить хирургическим путем, а в других случаях требуется дополнительное лечение.
III этап
Рак легких стадии III классифицируется как стадия IIIA, IIIB или IIIC. Этап зависит от размера опухоли и лимфатических узлов, на которые распространился рак. Рак III стадии не распространился на другие отдаленные части тела.
При многих формах рака стадии IIIA и стадии IIIB опухоль может быть трудно, а иногда и невозможно удалить хирургическим путем.Раковые образования стадии IIIC нельзя удалить хирургическим путем. Например, рак легких мог распространиться на лимфатические узлы, расположенные в центре грудной клетки, за пределами легких. Или опухоль могла прорасти в близлежащие структуры в легком. В любом случае вероятность того, что хирург сможет полностью удалить рак, менее высока. Раковые опухоли стадии III, которые не поддаются хирургическому лечению, часто можно успешно лечить с помощью системной терапии и лучевой терапии (см. Типы лечения).
IV этап
Стадия IV означает, что рак легкого распространился более чем на 1 область другого легкого, жидкости, окружающей легкое или сердце, или отдаленных частей тела через кровоток.Как только раковые клетки попадают в кровь, рак может распространиться в любом месте тела. Но более вероятно, что НМРЛ распространится на мозг, кости, печень и надпочечники. IV стадия НМРЛ делится на 2 подэтапы:
- Рак стадии IVA распространился на грудную клетку и / или распространился на 1 область за пределами грудной клетки.
- Стадия IVB распространилась за пределы грудной клетки на более чем 1 место в 1 органе или на более чем 1 орган.
Как правило, хирургическое вмешательство не подходит для лечения рака легких на стадиях IIIB, IIIC или IV.Рак легкого также невозможно удалить, если он распространился на лимфатические узлы над ключицей. Также может быть невозможно удалить, если он превратился в жизненно важные структуры в груди. Эти жизненно важные структуры включают сердце, крупные кровеносные сосуды или основные дыхательные трубки, ведущие к легким. В этих ситуациях врач порекомендует другие варианты лечения.
Рецидивирующий НМРЛ
Рецидивирующий рак — это рак, который вернулся после лечения. Если рак все же вернется, будет проведен еще один раунд тестов, чтобы узнать о степени рецидива.Эти тесты и сканирование часто аналогичны тем, которые проводились во время первоначального диагноза.
Используется с разрешения Американского колледжа хирургов, Чикаго, Иллинойс. Первоначальным и основным источником этой информации является Руководство по стадированию рака AJCC, восьмое издание (2017) , опубликованное Springer International Publishing.
Прогноз
Тип и стадия НМРЛ, а также общее состояние здоровья пациента влияют на прогноз.Хотя НМРЛ поддается лечению на любой стадии, вылечить можно только некоторых людей с определенными стадиями.
Ваш врач может использовать индекс, известный как «статус эффективности», чтобы направлять ваше лечение и определять ваш прогноз. Этот индекс измеряет общую силу и здоровье человека. Люди, которые достаточно сильны, чтобы продолжать повседневную деятельность без посторонней помощи, могут безопасно пройти химиотерапию, лучевую терапию или операцию. Для людей с метастазами в кости или печень от рака легких, чрезмерной потерей веса, продолжающимся употреблением табака или ранее существовавшими заболеваниями, такими как болезнь сердца или эмфизема, лечение может быть не таким эффективным.
Важно отметить, что возраст пациента никогда не позволял предсказать, получит ли он пользу от лечения. Средний возраст людей с раком легких в Соединенных Штатах — 71 год. Возраст пациента никогда не должен использоваться как единственная причина для принятия решения о том, какое лечение лучше, особенно для пожилых пациентов, которые в остальном физически здоровы и не имеют никаких медицинских проблем, кроме рака легких. .
Информация о стадии рака поможет врачу порекомендовать конкретный план лечения. Следующий раздел в этом руководстве — T ypes of Treatment . Используйте меню, чтобы выбрать другой раздел для чтения в этом руководстве.