Препараты для лечения и профилактики коронавирусной инфекции
Принимая во внимание сходство клинической картины легких форм COVID-19 с клинической картиной сезонных ОРВИ, до подтверждения этиологического диагноза в схемы терапии следует включать препараты, рекомендуемые для лечения сезонных ОРВИ, такие как интраназальные формы ИФН-α, препараты индукторов ИФН, а также противовирусные препараты с широким спектром активности, такие как умифеновир.
Умифеновир
Профилактические возможности умифеновира обусловлены интерферониндуцирующей активностью, стимуляцией клеточного и гуморального иммунитета. Среди его показаний — профилактика и лечение гриппа А и В и других ОРВИ у детей с двух лет и взрослых.
Умифеновир имеет довольно богатый опыт клинического применения. Более того: он подлежит безрецептурному отпуску и обычно хорошо переносится, поэтому его можно рекомендовать покупателям.
Это препараты: арбидол, афлюдол, арпефлю, арбидол максимум, умифеновир.
Иммуномодуляторы и иммуностимуляторы
Можно рекомендовать и другие безрецептурные препараты — иммуномодуляторы и иммуностимуляторы.
Например, азоксимера бромид в форме таблеток и суппозиториев, противовирусный препарат, индуцирующий продукцию интерферонов, кагоцел, меглюмина акридонацетат в форме таблеток, тилорон.
Интерфероны
Еще одна группа препаратов, которую можно предлагать для профилактики респираторных инфекций, включая COVID-19, — интерфероны. Активность парентерального интерферона альфа-2а была продемонстрирована еще в отношении MERS-CoV, коронавируса-возбудителя тяжелого ближневосточного респираторного синдрома, вспышка которого была зарегистрирована в 2012 году.
В отечественных временных рекомендациях Минздрава России по COVID-19 описано интраназальное введение раствора рекомбинантного интерферона альфа для профилактики заболевания и у детей, и взрослых, в том числе у беременных женщин, а также лечения легких форм у пациентов младше 60 лет без сопутствующих хронических заболеваний.
В качестве препаратов для повышения иммунного ответа, в том числе и в период пандемии COVID-19, можно рекомендовать назальные капли или назальный дозированный спрей интерферона альфа-2b.
Это препараты: Реаферон-ЕС, Альтевир, Виферон, Лайфферон, Гриппферон, Бинноферон-Альфа и др.
Барьер для «омикрона» и других штаммов: какие средства тормозят вирус
Каким данным об «омикроне» можно верить, а какие – лишь предположения? И есть ли уже сейчас средства, которые выступают как «барьер» для коронавируса? Об этом в программе «О самом главном» рассказали доктор Александр Мясников и профессор, врач-инфекционист Ольга Афанасьева.
Мясников в очередной раз напомнил то, о чем говорил уже не раз: коронавирус пришел навсегда.
«Да, он будет мутировать и надо научиться «сожительствовать» с ним», – говорит врач и ведущий.
По его словам, из-за этого будут меняться и сроки вакцинации – возможно, даже до трех раз в год, надо будет прибегать еще к каким-то мерам защиты.
Врачи отмечают также важность иммунитета, на который негативно воздействует «массовый психоз». По словам инфекциониста, люди сейчас находятся в состоянии стресса: вакцинироваться или нет, заболею или нет?
«Если человек очень боится заболеть, он заболеет», – говорит Афанасьева. «Сто процентов!» – соглашается с ней Мясников.
Они снова напоминают о важности здорового образа жизни, закаливания, физкультуры и профилактики заболеваний.
Врачи отмечают, что есть препараты с профилактическим воздействием даже на коронавирусную инфекцию.
«Когда мы делаем вдох, вирус проходит через носоглотку, и тут важно состояние местного иммунитета. Поэтому сейчас и хотят делать назальные вакцины как «барьер» – чтобы вирус не проникал в нас и не заражал других», – объясняет врач и ведущий.
При этом уже сейчас есть средства, которые как такой своеобразный «барьер» могут притормозить развитие и размножение вируса. Например, интерферон и другие капли в нос или спрей.
«Таким образом мы тормозим размножение вируса», – говорит Афанасьева. «Причем, всех штаммов, включая «омикрон», – добавляет Мясников.
По словам врачей, капли с универсальным противовирусным действием могут снизить риск заболевания пневмонией и бронхитом.
Еще больше интересных новостей – в нашем Instagram и Telegram-канале @smotrim_ru.
Врач-терапевт напомнил о важности начинать лечение «омикрона» с первых же дней недомогания — Газета.Ru
Прослушать новость
Остановить прослушивание
Главный внештатный специалист общей врачебной практики (семейный врач) Виктор Фомин рассказал АГН «Москва» о том, что при заражении «омикрон»-штаммом необходимо не откладывать лечение.
«Если по каким-то причинам вы не пошли в поликлинику и не обратились к врачу, в домашних условиях можно самостоятельно облегчить свое состояние. Первые признаки заболевания — повышение температуры, головная боль, заложенность носа, боль в горле», — отметил терапевт, подчеркнув, что болезнь поначалу напоминает ОРВИ.
Первые признаки заболевания — повышение температуры, головная боль, заложенность носа, боль в горле», — отметил терапевт, подчеркнув, что болезнь поначалу напоминает ОРВИ.
Он отметил, что первым делом в случае заражения нужно остаться дома. Не стоит принимать лекарства для снижения температуры, если она ниже 38 °C. В таком случае лучше прибегнуть к обильному питью до 2 литров жидкостей (стоит обратить внимание на мед, чай с мятой или облепихой), отдыхать, активнее проветривать помещение и прекратить курить.
В случае, если температура превысила 38°C, то тогда, как объяснил Фомин, можно принять жаропонижающие средства, такие как парацетамол или ацетилсалициловая кислота. Но он призвал проявлять осторожность тем людям, которые ранее страдали заболеваниями желудочно-кишечного тракта, порекомендовав им принимать минимальную дозу омепразола или эзомпразола «наряду с жаропонижающими».
Боль в горле, по словам врача, можно облегчить при помощи антисептиков (мирамистин и другие), полоскания (хлоргексидином или другими средствами), специальных леденцов или пастилок, а также спреев. Для борьбы с насморком два-три раза в день необходимо применять назальные капли с сосудосуживающим эффектом или заниматься промыванием носа посредством растворов на базе морской соли. А применение антибиотиков не принесет пользы организму и может ухудшить состояние.
Для борьбы с насморком два-три раза в день необходимо применять назальные капли с сосудосуживающим эффектом или заниматься промыванием носа посредством растворов на базе морской соли. А применение антибиотиков не принесет пользы организму и может ухудшить состояние.
Самостоятельное лечение возможно в течение пяти дней. Если симптомы сохранились и появилась мокрота, то необходимо обратиться к врачу.
Ранее главный инфекционист департамента здравоохранения Москвы Светлана Сметанина заявила, что обильное питье, жаропонижающие и противовирусные препараты помогут в лечении при первых признаках «омикрона».
Перечень лекарств | Медицинский центр «Логус»
Современная Фармация предлагает множество различных лекарственных средств, однако всегда присутствует дефицит лекарств, крайне желательных для обеспечения эффективного лечения тех или иных заболеваний. Это вызвано некоторыми причинами:
- нерентабельностью для производства промышленными масштабами;
- сложностью по составу и технологии производства;
- нестойкостью при хранении и необходимостью индивидуального дозирования;
- необходимостью изготовления лекарств без красителей, консервантов и т.
 п.;
п.;
Восполнить данный дефицит возможно с помощью экстемпорального изготовления лекарственных средств в аптеках, имеющих производственные возможности приготовления лекарств по рецептам врачей и заявкам-требованиям лечебных учреждений.
Осуществляя лечебно-профилактическую деятельность по специальностям «Дерматовенерология», «Акушерство и гинекология», «Онкогинекология» и «Клиническая фармация» медицинский центр «Логус» совместно с Аптекой №431 г. Харькова, имеющей лицензию на производство лекарственных средств, широко используют возможности экстемпоральной рецептуры.
Экстемпоральные лекарственные препараты изготовляемые Аптекой №431 не предназначены для лечения детей до 1-го года и отпускаются пациентам только по назначению врача.
Возможна индивидуальная непереносимость к какому-либо из компонентов лекарственного средства. При появлении нехарактерных реакций следует немедленно обратиться к лечащему врачу.
Перечень лекарственных препаратов, изготовляемых по заказу медицинского центра «ЛОГУС»:
- Бальзам для губ восстанавливающий
- Биотин
- Болтушка от стоматита
- Болтушка противозудная
- Болтушка с клиндамицином
- Болтушка с эритромицином
- Болтушка с левомицетином
- Бура в глицерине
- Вода укропная
- Гель для волос с миноксидилом 2%
- Гель для волос с миноксидилом 5%
- Гель для лечения гипергидроза
- Гель пероксидный
- Гель противогрибковый для обуви
- Гель ретиноевый
- Гель с метронидазолом
- Гель с эстриолом
- Гель сосудосуживающий для лица
- Жидкость Алибура
- Жидкость Бурова
- Жидкость Кастеллани бесцветная
- Жидкость Кричевского
- Жидкость мозольная
- Ихтиол чистый
- Кальция хлорида 10% раствор питьевой
- Комплект для лечения заболеваний, вызванных клещом рода Demodex по методу Демьяновича
- Крем гидратантный
- Крем для лечения розацеа
- Крем с маслом энотеры
- Крем с бетаметазоном комбинированный
- Крем с пантенолом антисептический
- Лак противогрибковый
- Линимент антибактериальный
- Линимент антибактериальный для инстилляций
- Линимент противогрибковый
- Линимент противогрибковый для инстилляций
- Линимент с орнидазолом
- Линимент с орнидазолом для инстилляций
- Лосьон азелаиновый
- Лосьон для укрепления корней волос
- Лосьон квасцовый
- Лосьон противоугревой
- Лосьон с бетаметазоном
- Лосьон таниновый
- Мазь антибактериальная сложная
- Мазь Вилькинсона
- Мазь для век противодемодексная
- Мазь кератолитическая
- Мазь мозольная Длусского
- Мазь назальная по Симановскому
- Мазь от геморроя
- Мазь противогрибковая
- Мазь противозудная
- Мазь ранозаживляющая
- Мазь Рыбакова
- Мазь с бетаметазоном
- Маска противоугревая вяжущая
- Масло салициловое для волос
- Микстура от кашля
- Микстура от мастопатии
- Микстура с цитралем №1, №2
- Микстура Кватера
- Молочко миндальное противоэкземное
- Мыло серное с бурой
- Настойка йодно-салициловая
- Настойка стимулирующая рост волос
- Паста для размягчения ногтевых пластин
- Паста противовоспалительная с ихтиолом
- Паста Розенталя
- Пиоктанин (краситель анилиновый медицинский) водный
- Пиоктанин (краситель анилиновый медицинский) спиртовой
- Повидон-йод 10% раствор
- Полоскание с повидон-йодом
- Полоскание с фурацилином
- Полоскание солевое
- Порошки с пиридоксином
- Присыпка дерматологическая
- Присыпка Житнюка
- Протаргол 1% (2%) капли назальные
- Протирка очищающая для жирной кожи
- Протирание противовоспалительное
- Раствор антибактериальный дренажный
- Раствор антисептический
- Раствор для прижигания кондилом
- Раствор для прижигания эрозий
- Раствор К-2
- Раствор кератолитический
- Раствор тимола
- Раствор фурацилина дренажный
- Сера очищенная
- Сироп от кашля
- Сироп с пантенолом
- Сироп седативный с бромидом натрия
- Спрей для горла с фурацилином
- Спрей для лечения гипергидроза
- Спрей назальный с фурацилином
- Спрей назальный сложный
- Спрей назальный солевой
- Суппозитории антибактериальные
- Суппозитории противовирусные с интерфероном
- Суппозитории противовоспалительные
- Суппозитории противогрибковые
- Суппозитории с клиндамицином
- Суппозитории с лактобактериями
- Суппозитории с орнидазолом
- Суппозитории с пантенолом
- Суппозитории с протеолитическими ферментами
- Суппозитории с хлоргексидином
- Суппозитории с экстрактом прополиса
- Суппозитории с эстриолом
- Суспензия «Циндол»
- Цинка сульфат
- Эмолент
- Эмульсия бензилбензоата
- Эмульсия противодемодексная
- Эмульсия с гидрохиноном
- Эмульсия с димедролом
- Эмульсия серно-ихтиоловая
- Энтеросорбент
Противовирусный назальный спрей от COVID-19 будет запущен в коммерческую эксплуатацию
Birmingham Biotech и Бирмингемский университет, Великобритания, подписали лицензионное соглашение на противовирусный назальный спрей против COVID-19.
Birmingham Biotech и Бирмингемский университет (оба Великобритании) подписали лицензионное соглашение о коммерциализации нового противовирусного назального спрея, защищающего от COVID-19. Лицензионное соглашение распространяется на весь срок действия патентов и дает Birmingham Biotech эксклюзивные права на сбыт и продажу противовирусного назального спрея по всему миру, кроме Индии.Ожидается, что спрей поступит в продажу в Великобритании и Азии в начале 2022 года. Университет.
Состав был разработан профессором Лайамом Гровером из Университета Бирмингема и группой исследователей, участвовавших в его тестировании. Спрей предназначен для инкапсуляции и дезактивации вируса, пока он еще находится в носу, что предотвращает его более широкое поглощение организмом.В его состав входят два соединения, которые уже одобрены регулирующими органами Великобритании, Европы и США и широко используются в медицинских устройствах, лекарствах и пищевых продуктах.
Каждое из этих соединений выполняет определенные функции. Первый представляет собой полисахаридный гель, который может «распыляться», а не «струйно распыляться» при нанесении с помощью обычного аппликатора для назального спрея, и удерживается на эпителии, покрытом слизистой оболочкой в носу, где он покрывает и удерживает вирус, поэтому он не перемещается. дальше по дыхательным путям.Второе соединение представляет собой мощный противовирусный агент под названием каррагинан.
Первый представляет собой полисахаридный гель, который может «распыляться», а не «струйно распыляться» при нанесении с помощью обычного аппликатора для назального спрея, и удерживается на эпителии, покрытом слизистой оболочкой в носу, где он покрывает и удерживает вирус, поэтому он не перемещается. дальше по дыхательным путям.Второе соединение представляет собой мощный противовирусный агент под названием каррагинан.
Исследователи из Бирмингема подтвердили полное ингибирование активности SARS-CoV-2, обеспечиваемое каррагинаном, и способность состава предотвращать сокращение и передачу в клеточной культуре, а также подтвердили, что спрей покрывает площадь поверхности, которая в шесть раз больше, чем при приготовлении. без геля.
«Поскольку ограничения COVID-19 во всем мире постепенно снимаются, существует реальная потребность в эффективных методах защиты от вирусов», — прокомментировал Гровер.«Несмотря на то, что существующие меры, такие как ношение масок и мытье рук, остаются важными, этот назальный спрей обеспечивает дополнительную защитную меру, способную снизить передачу инфекции. Мы очень рады работать с Birmingham Biotech, чтобы предоставить противовирусный назальный спрей людям во всем мире».
Мы очень рады работать с Birmingham Biotech, чтобы предоставить противовирусный назальный спрей людям во всем мире».
В будущем обе стороны планируют совместную разработку других инновационных продуктов и технологий, таких как спреи для горла и назальные спреи от COVID-19, предназначенные для защиты людей от других вирусов.«Мы рады вступить в партнерство с Бирмингемским университетом и иметь возможность работать вместе с его ведущими мировыми академическими исследователями для продвижения медицинских инноваций. У нас есть общее обязательство предоставить наш запатентованный назальный спрей против COVID-19 как можно большему количеству людей по доступной цене, ориентируясь на развивающиеся рынки с наибольшим спросом», — добавил Майкл Хсу, управляющий директор Birmingham Biotech.
Новый назальный спрей от COVID-19 Института Гладстона направлен на «снижение вирусной нагрузки в легких в 100 раз» вниз варианты.
Это новое оружие, которое можно добавить в арсенал против COVID-19. В отличие от многих других, эта терапия доказывает свою эффективность с одной дозы.
В отличие от многих других, эта терапия доказывает свою эффективность с одной дозы.
«При однократном введении, однократной дозе в нос с этими терапевтическими мешающими частицами, которые и мРНК терапевтичны, очень похожи на вакцины», — сказал Леор Вайнбергер, доктор философии, старший исследователь Института Гладстона.
СВЯЗАННЫЙ: Таблетка Pfizer от COVID-19 снижает риск госпитализации или смерти на 89%, сообщает компания.
«Эта концепция была впервые идентифицирована в 1950-х годах и с тех пор стала настоящим святым Граалем в вирусологии. Именно так ее назвали мои коллеги. Нам так и не удалось заставить ее работать», — сказал доктор , Вайнбергер.
В течение последних двух десятилетий доктор Вайнбергер исследовал этот метод лечения таких вирусов, как ВИЧ.
В прошлом году правительство США попросило доктора Вайнбергера и его команду перепрофилировать технологию для борьбы с COVID-19. По их последним данным, он работает против коронавируса.
СВЯЗАННО: Администрация Байдена инвестирует 3,2 миллиарда долларов в противовирусные таблетки от COVID-19
«Это снижает вирусную нагрузку как минимум в 100 раз», — сказал доктор Вайнбергер, добавив: как минимум тысячи копий вируса SARS-CoV-2, и эта клетка умирает или уничтожается вирусом.Когда терапевтическое средство присутствует вместо того, чтобы производить тысячи копий вируса, клетка становится фабрикой по производству тысяч копий вируса. терапевтическое и снижает количество вируса.
Их данные получены в результате тестирования на хомяках под руководством исследователя Института Гладстона доктора Сонали Чатурведи. — сказал д-р Чатурведи. вакцина одновременно.Не откладывайте, врачи говорят
«Эта терапия отслеживает мутации вируса и не отстает от них. можно наблюдать эффективность этой терапии у хомяков в течение пяти дней. Через пять дней хомяк избавился от вируса».
Луз Пенья: «Как вы думаете, когда эта терапия станет общедоступной?»
Д-р Вайнбергер: «Я думаю, что, учитывая наше партнерство с отраслью, особенно с VxBiosciences, и мы надеемся, что, учитывая клинические испытания, которые начнутся в начале следующего года, мы надеемся, что сможем ускорить это так же, как вакцины против COVID были ускорены и представьте это общественности в начале 2023 года. »
»
Copyright © 2022 КГО-ТВ. Все права защищены.
Противовирусный назальный спрей VIRALEZE™ — Starpharma
Противовирусный назальный спрей VIRALEZE™
VIRALEZE™ был разработан Starpharma, мировым лидером в разработке новых медицинских продуктов на основе собственной технологии дендримеров, в качестве противовирусного назального спрея, предназначенного для создания увлажняющего и защитного барьера в носу. VIRALEZE™ также содержит SPL7013, который, как показали лабораторные исследования, инактивирует широкий спектр респираторных/простудных вирусов.
Было показано, что полость носа является основным местом, где респираторные вирусы, включая вирусы простуды и SARS-CoV-2 (вирус, вызывающий COVID-19), закрепляются перед распространением в организме (Hou et al., 2021). ).
SPL7013 изначально был разработан Starpharma из-за его противовирусной активности, и было показано, что он блокирует широкий спектр вирусов в доклинических исследованиях in vitro и in vivo (Bernstein et al, 2003; Jiang et al, 2005; Gong et al. al, 2005; Lackman-Smith et al, 2008; Tyssen et al, 2010; Telwatte et al, 2011; Romanowski et al, 2021).
al, 2005; Lackman-Smith et al, 2008; Tyssen et al, 2010; Telwatte et al, 2011; Romanowski et al, 2021).
Starpharma впоследствии сгенерировала и опубликовала лабораторные данные, показывающие, что SPL7013 также инактивирует >99,9% коронавируса SARS-CoV-2 (Paull et al., 2021a).
Starpharma также опубликовала данные, демонстрирующие защитную эффективность противовирусного назального спрея VIRALEZE™ против заражения SARS-CoV-2 in vivo на гуманизированной мышиной модели коронавирусной инфекции. Результаты исследования показали, что ВИРАЛЕЗ™ при интраназальном введении снижал вирусную нагрузку на >99,9% (по сравнению с контролем с физиологическим раствором) в легких и трахее животных, инфицированных SARS-CoV-2.Защитные эффекты VIRALEZE™ против SARS-CoV-2 у животных согласуются с ранее зарегистрированной вирулицидной активностью in vitro SPL7013, которая снижает инфекционный SARS-CoV-2, включая вариант Delta, на >99,9% в течение 30 секунд. воздействия. Результаты исследования in vivo (проведенного в Исследовательском институте Скриппса) были опубликованы в рецензируемом журнале Viruses в специальном выпуске под названием «Медицинские вмешательства для лечения и профилактики инфекций SARS-CoV-2». (Пол и др., 2021б).
(Пол и др., 2021б).
SPL7013 инактивирует несколько «вызывающих озабоченность вариантов» SARS-CoV-2, включая альфа-, бета-, гамма- и дельта-варианты, при этом запланировано тестирование других вариантов по мере их появления и становятся доступными.
Кроме того, Starpharma объявила, что в лабораторных исследованиях было показано, что SPL7013 блокирует респираторно-синцитиальный вирус человека (HRSV) и блокирует заражение другими пандемическими коронавирусами (SARS-CoV, MERS-CoV) и вирусами гриппа.
SPL7013 – это запатентованная, точно разработанная большая отрицательно заряженная молекула, которая, как было показано, не попадает в кровоток после местного нанесения на эпителиальные поверхности слизистых оболочек. В VIRALEZE™ SPL7013 предназначен для локального формирования барьера в месте нанесения в полости носа, чтобы физически улавливать и тем самым инактивировать респираторные вирусы.
«Старфарма» получила финансирование на разработку и коммерциализацию VIRALEZE™ в рамках программы «Мост биомедицинских переводов» Фонда будущих медицинских исследований правительства Австралии.
VIRALEZE™ зарегистрирован для продажи в Европе, Индии, Вьетнаме, Новой Зеландии и Саудовской Аравии. VIRALEZE™ запущен в Великобритании через LloydsPharmacy, как было объявлено 25 марта 2021 г., а затем в Европе через онлайн-магазин Starpharma, как было объявлено 6 мая 2021 г. VIRALEZE™ также запущен во Вьетнаме, как было объявлено 3 декабря 2021 г. для ряда рынков, включая Австралию, с намерением распространить его на другие рынки. VIRALEZE™ не одобрен для продажи или поставки в Австралию.
SPL7013 также входит в состав продуктов, зарегистрированных более чем в 45 странах и доступных для продажи в Великобритании, Европе, Японии, Юго-Восточной Азии, Австралии и Новой Зеландии.
Механизм действия VIRALEZE™
ВИРАЛЕЗ™ наносится на носовую полость, где впервые прикрепляются и начинают размножаться респираторные вирусы, вызывающие простуду, грипп и более тяжелые респираторные заболевания.
VIRALEZE™ обеспечивает увлажняющий и защитный барьер в носу и содержит SPL7013, который физически захватывает и инактивирует вирусы.Лабораторные исследования показали, что SPL7013 инактивирует вирусы (Paull et al., 2021a).
SPL7013 действует путем улавливания вирусов и блокирования взаимодействия между белками прикрепления вируса или «шипами» и клетками человека, которые вирусы стремятся заразить.
Белки«спайков» на поверхности вирусов, которые вступают в контакт с VIRALEZE™, физически захватываются SPL7013. Это взаимодействие является необратимым («вирулицидным»), и заблокированные вирусы больше не могут заражать клетки.
Затем «заблокированные» вирусы выводятся естественным путем через носовую слизь.
На механизм действия SPL7013, по-видимому, не влияют мутации в шиповидных белках SARS-CoV-2, которые делают вирус более заразным, как это произошло со штаммом Delta. Вместо этого мутации, которые заставляют вирус более легко взаимодействовать с клетками и, следовательно, более заразными, могут сделать его более восприимчивым к захвату и блокированию с помощью SPL7013.
ВИРАЛЕЗ™ хорошо переносится в клиническом исследовании многократных доз
Starpharma завершила рандомизированное двойное слепое плацебо-контролируемое исследование безопасности, переносимости и всасывания VIRALEZE™ у 40 здоровых добровольцев, которые использовали продукт четыре раза в день в течение 14 дней (объявлено 17 августа 2021 г.).Продукт хорошо переносился, о заметных или серьезных побочных эффектах не сообщалось, и ни один из участников не прекратил использование продукта. Исследование также подтвердило, что SPL7013 не всасывается в кровоток после многократного назального применения. Этот вывод согласуется с предыдущими обширными доклиническими и клиническими данными, свидетельствующими об отсутствии системной абсорбции SPL7013 после местного нанесения на слизистые оболочки.
Хоу, Ю. Дж. и др. Обратная генетика SARS-CoV-2 выявляет переменный градиент инфекции в дыхательных путях. Cell, 2020, 182(2), 429-446.e14.
Полл, Дж. Р.А. и другие. Вирулицидная и противовирусная активность астодримера натрия в отношении SARS-CoV-2 in vitro. Antivirus Research, 2021(a), 191, 105089.
Р.А. и другие. Вирулицидная и противовирусная активность астодримера натрия в отношении SARS-CoV-2 in vitro. Antivirus Research, 2021(a), 191, 105089.
Paull, J.R.A. и другие. Защитные эффекты 1% назального спрея астодримера натрия против назального заражения SARS-CoV-2 у мышей K18-hACE2. Вирусы, 2021(b), 13, 1656.
9354505000159
Для получения дополнительной информации:
Загрузить объявление ASX: продажи и распространение VIRALEZE™ в Саудовской Аравии и странах Персидского залива (PDF, 274 КБ) — 3 февраля 2022 г.
Загрузить Объявление ASX: противовирусный назальный спрей VIRALEZE™ зарегистрирован в Саудовской Аравии (PDF, 239 КБ) — 14 декабря 2021 г.
Загрузить объявление ASX: VIRALEZE™ успешно запущен во Вьетнаме (PDF, 215 КБ) — 13 декабря 2021 г.
Загрузить Объявление ASX: Соглашение о распространении и запуск VIRALEZE™ во Вьетнаме (PDF, 224 КБ) — 3 декабря 2021 г.
Загрузить объявление ASX: VIRALEZE™ зарегистрирована во Вьетнаме с запуском на этой неделе (PDF, 214 КБ) — 1 декабря 2021 г.
Загрузить объявление ASX: распространение и поставка VIRALEZE™ во Вьетнам (PDF, 224 КБ) — 26 октября 2021 г.
Загрузить объявление ASX: соглашение VIRALEZE ADMENTA — дополнительная информация (PDF, 204 КБ) — 12 октября 2021 г.
Загрузить Объявление ASX: запуск VIRALEZE™ в аптеках ADMENTA Italia Group в Италии (PDF, 435 КБ) — 8 октября 2021 г.
Загрузить Объявление ASX: VIRALEZE защищает от SARS-CoV-2 в модели вызова (PDF, 347 КБ) — 23 августа 2021 г.
Загрузить объявление ASX: VIRALEZE™ хорошо переносится в клиническом исследовании с многократными дозами (PDF, 219 КБ) — 17 августа 2021 г.
Загрузить объявление ASX: VIRALEZE SPL7013 вирулицидный (>99.99%) по сравнению с вариантом Delta (PDF, 520 КБ) — 27 июля 2021 г.
Загрузить уведомление ASX: обновление VIRALEZE UK (PDF, 320 КБ) — 21 июня 2021 г.
Загрузить объявление ASX: VIRALEZE SPL7013 обладает вирулицидным действием против нескольких вариантов COVID (PDF, 520 КБ) — 18 июня 2021 г.
Загрузить объявление ASX: противовирусный назальный спрей VIRALEZE зарегистрирован для продажи в Индии (PDF, 520 КБ) — 11 июня 2021 г.
Загрузить объявление ASX: VIRALEZE SPL7013 высокоактивен в отношении британского варианта коронавируса (PDF, 520 КБ) — 1 июня 2021 г.
Загрузить Объявление ASX: VIRALEZE™ запускается в Европе (PDF, 218 КБ) – 6 мая 2021 г.
Загрузить объявление ASX: компания LloydsPharmacy выпустила VIRALEZE™ в Великобритании (PDF, 224 КБ) — 30 марта 2021 г.
Загрузить объявление ASX: запуск VIRALEZE™ совместно с LloydsPharmacy в Великобритании (PDF, 241 КБ) — 25 марта 2021 г.
Загрузить объявление ASX: SPL7013 активен против других пандемических коронавирусов (PDF, 418 КБ) – 3 марта 2021 г.
Загрузить Объявление ASX: противовирусный назальный спрей VIRALEZE™ зарегистрирован в Европе (PDF, 226 КБ) — 23 февраля 2021 г.
Загрузить полное объявление: исследование назального спрея VIRALEZE COVID-19 начнется в январе (PDF, 71 КБ) — 22 декабря 2020 г.
Загрузить полное объявление: Назальный спрей VIRALEZE™ COVID-19 будет готов к продаже в первом квартале 2021 года (PDF, 113 КБ) — 10 декабря 2020 г.
Загрузить полное объявление: SPL7013 демонстрирует мощную противовирусную активность в отношении РСВ, что расширяет возможности использования назального спрея (PDF, 95 КБ) — 19 ноября 2020 г.
Загрузить полное объявление: SPL7013 Назальный спрей COVID-19, вирулицидный против SARS-CoV-2 (PDF, 183 КБ) – 14 сентября 2020 г.
Загрузить полное объявление: назальный спрей SPL7013 от COVID-19 — обновленная информация о разработке (PDF, 267 КБ) — 25 августа 2020 г.
Загрузить объявление ASX: SPL7013 демонстрирует значительную активность против SARS-CoV-2 (коронавирус) (файл в формате pdf, 69 КБ) – 15 апреля 2020 г.
Ингибирование SARS-CoV-2 с помощью мукоадгезивного амфифильного хитозана, который может использоваться в качестве противовирусного назального спрея В исследовании использовали A549
ACE2+ ) 32 . Для всех культур MEM Дульбекко (ThermoFisher Scientific, Польша) с добавлением 3% фетальной бычьей сыворотки (инактивированной нагреванием; ThermoFisher Scientific, Польша) и антибиотиков: пенициллин (100 ЕД/мл), стрептомицин (100 мкг/мл) и ципрофлоксацин ( 5 мкг/мл). Для анализа ex vivo использовали коммерчески доступные культуры MucilAir HAE (Epithelix Sarl, Швейцария). Все культуры выращивали при 37 °C в атмосфере 5% CO 2 .
Для всех культур MEM Дульбекко (ThermoFisher Scientific, Польша) с добавлением 3% фетальной бычьей сыворотки (инактивированной нагреванием; ThermoFisher Scientific, Польша) и антибиотиков: пенициллин (100 ЕД/мл), стрептомицин (100 мкг/мл) и ципрофлоксацин ( 5 мкг/мл). Для анализа ex vivo использовали коммерчески доступные культуры MucilAir HAE (Epithelix Sarl, Швейцария). Все культуры выращивали при 37 °C в атмосфере 5% CO 2 .Изолят SARS-CoV2 026 V-03883 (Charité — Universitätsmedizin Berlin, Германия, Европейский архив вирусов — Global — EVAG, https://www.european-virus-archive.com) для работы in vitro. SARS-CoV-2 был изолирован Munchen-1.2 2020/984 35 для работы in vivo. Все эксперименты с инфекционными агентами проводились в установке ABSL3 + , разрешенной для работы с переносимыми по воздуху возбудителями BSL3, включая вирус SARS-CoV-2.
Для определения жизнеспособности клеток использовали набор XTT (Biological Industries, Израиль). Также использовались следующие реагенты: набор для выделения вирусной ДНК/РНК (A&A Biotechnology, Польша), набор для обратной транскрипции кДНК высокой емкости (Thermo Fisher Scientific, Польша), набор для количественной ПЦР в реальном времени (зонд RT-HS-PCR mix, A&A Biotechnology, Польша) и олигонуклеотиды кПЦР в реальном времени перечислены в таблице 1.
Соединения GPCQ перечислены в таблице 2. Соединения суспендировали в 1 × PBS до конечной концентрации 5 мг/мл. Все запасы хранили при 4 °C до использования.
Методы
Культура ткани
Цитотоксичность соединений оценивали путем инкубации конфлюэнтных монослоев клеток Vero E6 и A549 ACE2+ с диапазоном концентраций соединения GCPQ. Анализ XTT был проведен через 48 часов в соответствии с протоколом производителя с использованием 200 000 клеток на лунку и DMEM с добавлением фетальной бычьей сыворотки, пенициллина и стрептомицина (см. выше в материалах).
Способность каждого соединения ингибировать репликацию вируса определяли путем инфицирования конфлюэнтных монослоев Vero E6 и A549 ACE2+ вирусом SARS-CoV-2 при 400 TCID 50 /мл в присутствии тестируемых соединений или фосфатного буфера физиологический раствор — PBS (TCID 50 = 50% инфекционной дозы тканевой культуры). Были включены имитационные контроли (клеточный лизат без вируса) и средние (дополненные DMEM — см. выше) контроли. Каждое соединение присутствовало во время и после заражения.Затем клетки инкубировали в течение 2 часов при 37 °C и 5% CO 2 . После этого клетки трижды промывали PBS и повторно наносили каждое соединение на монослой клеток. 100 мкл супернатантов клеточной культуры впоследствии собирали из каждой обозначенной лунки через два дня культивирования. Опыты проводились в трехкратной повторности.
Были включены имитационные контроли (клеточный лизат без вируса) и средние (дополненные DMEM — см. выше) контроли. Каждое соединение присутствовало во время и после заражения.Затем клетки инкубировали в течение 2 часов при 37 °C и 5% CO 2 . После этого клетки трижды промывали PBS и повторно наносили каждое соединение на монослой клеток. 100 мкл супернатантов клеточной культуры впоследствии собирали из каждой обозначенной лунки через два дня культивирования. Опыты проводились в трехкратной повторности.
Ингибирование репликации вируса при НАО оценивали путем заражения MucilAir™ (Epithelics Sarl, Швейцария) вирусом SARS-CoV-2 при 5000 TCID 50 /мл в присутствии GCPQa или PBS.GCPQa, разведенный в PBS, добавляли к апикальной стороне вставки (200 мкг/мл или 500 мкг/мл) и инкубировали при 37 °C в течение 30 минут до инфицирования. После завершения предварительной инкубации соединение удаляли, добавляли свежие разведения соединения с вирусом и инкубировали в течение 2 ч при 37 °C.-snimaetzalozhennostnosa-bodhiaroma-1000x1000.jpg) Затем апикальную сторону HAE трижды промывали PBS, повторно наносили каждое соединение и снова инкубировали в течение 30 минут при 37 °C. После последней инкубации с GCPQ образцы (50 мкл) собирали, а культуры НАЭ оставляли в воздушно-жидкостной интерфазе.Каждые 24 часа апикальную поверхность НАО инкубировали в течение 30 минут с GCPQ или PBS, и образцы собирали для оценки выхода вируса. Вирусную РНК выделяли из апикальных смывов или супернатанта клеточной культуры, выделяли РНК (Viral DNA/RNA; A&A Biotechnology, Польша), обратно транскрибировали в кДНК (High Capacity cDNA Reverse Transcription Kit; ThermoScientific, Польша) и подвергали КПЦР-анализ. Вкратце, кДНК амплифицировали в реакционной смеси, содержащей 1 × мастер-микс для ПЦР (A&A Biotechnology, Польша), в присутствии зонда (100 нМ) и праймеров (450 нМ каждый), последовательности представлены в таблице 1.
Затем апикальную сторону HAE трижды промывали PBS, повторно наносили каждое соединение и снова инкубировали в течение 30 минут при 37 °C. После последней инкубации с GCPQ образцы (50 мкл) собирали, а культуры НАЭ оставляли в воздушно-жидкостной интерфазе.Каждые 24 часа апикальную поверхность НАО инкубировали в течение 30 минут с GCPQ или PBS, и образцы собирали для оценки выхода вируса. Вирусную РНК выделяли из апикальных смывов или супернатанта клеточной культуры, выделяли РНК (Viral DNA/RNA; A&A Biotechnology, Польша), обратно транскрибировали в кДНК (High Capacity cDNA Reverse Transcription Kit; ThermoScientific, Польша) и подвергали КПЦР-анализ. Вкратце, кДНК амплифицировали в реакционной смеси, содержащей 1 × мастер-микс для ПЦР (A&A Biotechnology, Польша), в присутствии зонда (100 нМ) и праймеров (450 нМ каждый), последовательности представлены в таблице 1.
Реакцию проводили на установке Fast Real-Time PCR 7500 (Life Technologies, Польша) по схеме: 2 мин при 50°С и 10 мин при 92°С, затем 40 циклов по 15 с при 92°С. °C и 1 мин при 60 °C. Для оценки количества копий гена N готовили стандарты ДНК, как описано ранее 36 . Полученные данные представлены в виде выхода вируса и в виде логарифмического значения удаления (LRV), показывая относительное уменьшение количества вируса в культуральной среде клеток по сравнению с контролем.
°C и 1 мин при 60 °C. Для оценки количества копий гена N готовили стандарты ДНК, как описано ранее 36 . Полученные данные представлены в виде выхода вируса и в виде логарифмического значения удаления (LRV), показывая относительное уменьшение количества вируса в культуральной среде клеток по сравнению с контролем.
Интраназальная доставка на модели здорового животного
GCPQ (молекулярная масса = 10 кДа, молярный % пальмитоильных групп = 16 и молярный % групп четвертичного аммония = 13) радиоактивно метили с использованием двухстадийной стратегии: сначала применяли ацилирующий реагент [N-сукцинимидил -3[4-гидроксифенил]пропионат — реагент Болтона и Хантера (BH)] сначала ковалентно связывали с GCPQ, а затем комплекс GCPQ-BH йодировали с помощью 125 I. Вкратце, GCPQ (90 мг) растворяли в ДМСО. (3 мл). К этому раствору добавляли 200 мкл триэтиламина и 0.05 молярных эквивалентов (10 мг) реагента BH, и реакции давали возможность протекать в течение ночи при комнатной температуре при перемешивании. На следующий день конъюгат GCPQ-BH осаждали, используя смесь ацетон:диэтиловый эфир (1:2, об./об.), и осадок промывали 3 раза той же смесью ацетон:диэтиловый эфир. Промытый осадок растворяли в метаноле (2 мл) и подвергали диализу против воды в течение ночи. Затем подвергнутый диализу GCPQ-BH сушили вымораживанием и собирали. Мечение GCPQ-BH с помощью 125 I проводили с использованием йодирующих гранул ® (Thermo Scientific Pierce, Великобритания).Вкратце, GCPQ-BH (20 мг) и 100 мг GCPQ растворяли в метаноле при перемешивании, затем метанол удаляли в вакууме и к сухой пленке добавляли трис-HCL-буфер (25 мМ, pH 4,8, 1,8 мл) для получения конечная концентрация 66,7 мг/мл. Затем этот раствор добавляли в пробирку, содержащую I 125 (1 мКи, 17 Ки/мг, 0,392 нмоль, Perkin-Elmer, США) и четыре гранулы для йодирования® (Thermo Scientific Pierce, Великобритания). Реакцию инкубировали в течение 1,5 ч при комнатной температуре, после чего реакцию останавливали, отделяя раствор от гранул.
На следующий день конъюгат GCPQ-BH осаждали, используя смесь ацетон:диэтиловый эфир (1:2, об./об.), и осадок промывали 3 раза той же смесью ацетон:диэтиловый эфир. Промытый осадок растворяли в метаноле (2 мл) и подвергали диализу против воды в течение ночи. Затем подвергнутый диализу GCPQ-BH сушили вымораживанием и собирали. Мечение GCPQ-BH с помощью 125 I проводили с использованием йодирующих гранул ® (Thermo Scientific Pierce, Великобритания).Вкратце, GCPQ-BH (20 мг) и 100 мг GCPQ растворяли в метаноле при перемешивании, затем метанол удаляли в вакууме и к сухой пленке добавляли трис-HCL-буфер (25 мМ, pH 4,8, 1,8 мл) для получения конечная концентрация 66,7 мг/мл. Затем этот раствор добавляли в пробирку, содержащую I 125 (1 мКи, 17 Ки/мг, 0,392 нмоль, Perkin-Elmer, США) и четыре гранулы для йодирования® (Thermo Scientific Pierce, Великобритания). Реакцию инкубировали в течение 1,5 ч при комнатной температуре, после чего реакцию останавливали, отделяя раствор от гранул. Для удаления свободного йода (при свободный йод удаляют добавлением 50 мкл реакционной смеси на колонку и центрифугированием при 2800 об/мин в течение 2 мин). Элюент помещали в ультрацентрифужные фильтры Amicon (3 кДа, Millipore, США) с 200 мкл H 2 O и подвергали повторным промывкам (посредством центрифугирования при 10 000 об/мин в течение 10 мин) до получения незначительного количества вымытой воды. считает.
Для удаления свободного йода (при свободный йод удаляют добавлением 50 мкл реакционной смеси на колонку и центрифугированием при 2800 об/мин в течение 2 мин). Элюент помещали в ультрацентрифужные фильтры Amicon (3 кДа, Millipore, США) с 200 мкл H 2 O и подвергали повторным промывкам (посредством центрифугирования при 10 000 об/мин в течение 10 мин) до получения незначительного количества вымытой воды. считает.
Все эксперименты на животных проводились в соответствии с лицензией Министерства внутренних дел Великобритании (PPL 70/8224) и были одобрены местным комитетом по этике — Органом по защите животных и этике UCL. Эксперименты на животных проводились в соответствии с рекомендациями, содержащимися в лицензии, и соблюдались рекомендации ARRIVE, однако ослепление или рандомизация не проводились. В предварительном исследовании на самцах мышей Balb/C весом 25 г (Чарльз-Ривер, Великобритания), которым был обеспечен свободный доступ к стандартной пище для грызунов и воде, интраназально вводили меченый радиоактивным изотопом GCPQ-BH (10 мг/кг, 1. 2 МБк), с помощью пипетки поместив 5 мкл материала с радиоактивной меткой в ноздри мыши и позволив мышам понюхать дозу. В различные моменты времени после введения GCPQ-BH, меченого радиоактивным изотопом, животных анестезировали изофлураном (1–2% об./об. в кислороде), поддерживали при 37 ºC и подвергали анализу NanoSPECT/CT (Mediso, США).
2 МБк), с помощью пипетки поместив 5 мкл материала с радиоактивной меткой в ноздри мыши и позволив мышам понюхать дозу. В различные моменты времени после введения GCPQ-BH, меченого радиоактивным изотопом, животных анестезировали изофлураном (1–2% об./об. в кислороде), поддерживали при 37 ºC и подвергали анализу NanoSPECT/CT (Mediso, США).
ОФЭКТ/КТ-визуализация и анализ in vivo
ОФЭКТ/КТ-сканы головы мыши через 30 мин, 2 ч 30 мин и 24 ч после назального введения были получены с использованием сканера NanoSPECT/CT (Mediso, Венгрия).Мышей анестезировали изофлураном (1-2% об./об. в кислороде) и поддерживали при 37°С. Изображения ОФЭКТ были получены в течение 30 минут с использованием 4-головочного сканера с девятью отверстиями диаметром 1,4 мм в режиме спирального сканирования со временем на просмотр 60 с. Впоследствии КТ-изображения были получены с использованием источника рентгеновского излучения с пиковым напряжением 45 кВ (кВп), временем экспозиции 500 мс в 180 проекциях, шагом 0,5 и временем получения 4:30 мин. Температуру тела поддерживали с помощью обдува теплым воздухом, а дыхание и внутреннюю температуру тела контролировали на всем протяжении.КТ-изображения были реконструированы с использованием программного обеспечения Bioscan InVivoScope (Bioscan, США) с размером вокселя 124 × 124 × 124 мкм, тогда как изображения ОФЭКТ были реконструированы с использованием HiSPECT (ScivisGmbH, Bioscan) в матрице 256 × 256. Изображения объединяли и анализировали с использованием программного обеспечения VivoQuant (Invicro, A Konica Minolta Company). Трехмерные области интереса (ROI) были созданы для поглощения в ноздрях для каждой временной точки, а активность рассчитывалась как процент введенной дозы. Репрезентативные изображения масштабируются одинаково (одинаковые минимальные и максимальные значения).После окончательного сканирования мышь умерщвляли и всю голову мыши анализировали с использованием куриметра (Capintech, Mirion Technologies, Великобритания) для подтверждения ex vivo концентрации 125 I.
Температуру тела поддерживали с помощью обдува теплым воздухом, а дыхание и внутреннюю температуру тела контролировали на всем протяжении.КТ-изображения были реконструированы с использованием программного обеспечения Bioscan InVivoScope (Bioscan, США) с размером вокселя 124 × 124 × 124 мкм, тогда как изображения ОФЭКТ были реконструированы с использованием HiSPECT (ScivisGmbH, Bioscan) в матрице 256 × 256. Изображения объединяли и анализировали с использованием программного обеспечения VivoQuant (Invicro, A Konica Minolta Company). Трехмерные области интереса (ROI) были созданы для поглощения в ноздрях для каждой временной точки, а активность рассчитывалась как процент введенной дозы. Репрезентативные изображения масштабируются одинаково (одинаковые минимальные и максимальные значения).После окончательного сканирования мышь умерщвляли и всю голову мыши анализировали с использованием куриметра (Capintech, Mirion Technologies, Великобритания) для подтверждения ex vivo концентрации 125 I.
Ингибирование вирусов in vivo у трансгенных мышей, экспрессирующих рецептор ACE2
Все эксперименты на животных были одобрены местным комитетом по этике. Трансгенных мышей, экспрессирующих белок ACE2 человека под промотором человеческого цитокератина 18, приобретали в лаборатории Джексона, США.Мышей помещали на карантин не менее чем за 7 дней до эксперимента. Каждая экспериментальная группа состояла из 10 животных (14 животных в контрольной группе). GPCQa вводили один раз в день интраназально (20 мг/кг в день). Контрольная группа лечения получала ремдесивир внутримышечно (25 мг/кг в сутки). Мыши имели свободный постоянный доступ к воде во время эксперимента (от - 1 до 6 дня после заражения).
Мыши получали GPCQ или ремдесивир каждые 24 часа с - 1 дня до 6 дня после заражения.Никаких побочных эффектов в ходе эксперимента не наблюдалось. В 0-й день животных заражали интраназально вирусом SARS-CoV-2 (Munchen-1.2 2020/984; по 5 мкл в каждую ноздрю) в дозе 426 000 TCID 50 /мл, что соответствовало ~ 3 × 10 5 БОЕ. . Вирус размножали и титровали на клетках Vero до инфицирования. Зараженных мышей осматривали и взвешивали ежедневно. На 6-й день после заражения животных убивали передозировкой анестетика. Были взяты мазки из носа и собран мозг.Ткани гомогенизировали с использованием гомогенизатора шариков (TissueLyser II, Qiagen, Польша). Вирусную РНК выделяли с помощью набора для выделения микроРНК mirVana™ (ThermoFisher Scientific, Польша) в соответствии с инструкциями производителя. Вирусную инфекцию количественно определяли с использованием метода RT-qPCR, описанного выше.
. Вирус размножали и титровали на клетках Vero до инфицирования. Зараженных мышей осматривали и взвешивали ежедневно. На 6-й день после заражения животных убивали передозировкой анестетика. Были взяты мазки из носа и собран мозг.Ткани гомогенизировали с использованием гомогенизатора шариков (TissueLyser II, Qiagen, Польша). Вирусную РНК выделяли с помощью набора для выделения микроРНК mirVana™ (ThermoFisher Scientific, Польша) в соответствии с инструкциями производителя. Вирусную инфекцию количественно определяли с использованием метода RT-qPCR, описанного выше.
Статистический анализ
Статистический анализ проводился с использованием однофакторного дисперсионного анализа плюс посттесты Тьюки. Статистическая значимость была установлена на уровне p < 0,05.
Антисептический назальный спрей назодин проявляет потенциальную противовирусную активность против SARS-CoV-2
Группа международных ученых недавно исследовала эффективность PVP-1, комплекса поливинилпирролидона и йода, в профилактике тяжелого острого респираторного синдрома, вызванного коронавирусом 2 (SARS-CoV-2). Используя культур клеток in vitro , ученые отмечают, что состав PVP-1, используемый в коммерчески доступном назальном спрее (Nasodine), легко инактивирует SARS-CoV-2 в течение короткого периода времени. Исследование в настоящее время доступно на сервере препринтов bioRxiv *.
Используя культур клеток in vitro , ученые отмечают, что состав PVP-1, используемый в коммерчески доступном назальном спрее (Nasodine), легко инактивирует SARS-CoV-2 в течение короткого периода времени. Исследование в настоящее время доступно на сервере препринтов bioRxiv *.
Фон
Тяжелый острый респираторный синдром коронавирус 2 (SARS-CoV-2), возбудитель коронавирусной болезни 2019 (COVID-19), в основном передается от человека к человеку через крупные респираторные капли.Однако есть данные, свидетельствующие о возможности передачи вируса воздушно-капельным путем. Известно, что вирус более эффективно размножается в верхних дыхательных путях, чем в нижних дыхательных путях. Два белка клетки-хозяина, а именно ангиотензинпревращающий фермент-2 (ACE2) и трансмембранная протеаза серин 2 (TMPRSS2), которые необходимы для слияния вирусной оболочки с мембраной клетки-хозяина и проникновения вируса, высоко экспрессируются в назальных и альвеолярных эпителиальных клетках. , подтверждая факт преимущественной репликации вируса в верхних дыхательных путях.
, подтверждая факт преимущественной репликации вируса в верхних дыхательных путях.
Поскольку выделение вируса из носовой полости и верхних дыхательных путей является основным путем передачи инфекции, ранняя терапевтическая элиминация SARS-CoV-2 в носовой полости может значительно снизить риск передачи от человека к человеку, а также распространения инфекции. инфекции нижних дыхательных путей и других органов.
В текущем исследовании ученые изучили эффективность PVP-1 в устранении инфекции SARS-CoV-2, проведя серию из экспериментов in vitro .Известно, что ПВП-1 обладает широким спектром антимикробного действия и обычно используется в качестве дезинфицирующего средства для кожи и слизистых оболочек. В этом исследовании ученые специально оценили эффективность имеющегося в продаже антисептического назального спрея Nasodine, который содержит клинически одобренный состав 0,5% PVP-1.
Дизайн исследования
Из двух изолятов SARS-CoV-2, использованных в исследовании, один инкубировали с назодином в течение 1 минуты. Другой инкубировали либо с назодином, либо с 0.5% PVP-1 в физиологическом растворе в течение 15 секунд, 5 минут или 15 минут. Для измерения остаточных титров вируса и определения эффективности состава PVP-1 использовали как методы, основанные на ПЦР, так и на основе клеточных культур.
Другой инкубировали либо с назодином, либо с 0.5% PVP-1 в физиологическом растворе в течение 15 секунд, 5 минут или 15 минут. Для измерения остаточных титров вируса и определения эффективности состава PVP-1 использовали как методы, основанные на ПЦР, так и на основе клеточных культур.
Важные замечания
Проведя анализ на основе клеточных культур, ученые обнаружили, что назодин может полностью ингибировать репликацию SARS-CoV-2. Напротив, для SARS-CoV-2, обработанного контрольной средой (без назодина), наблюдалась устойчивая репликация.
Для дальнейшего подтверждения ученые использовали анализ на основе цитопатического эффекта (CEP), чтобы определить влияние назодина на другой штамм SARS-CoV-2.Они сочли две временные точки (15 секунд и 5 минут) клинически значимыми для назального применения, поскольку активность назального препарата на основе PVP-1 постепенно снижается со временем из-за инактивации йода назальными белками.
Результаты анализа показали, что назодин значительно снижает репликацию SARS-CoV-2 в течение 15 секунд после воздействия. Более того, после 15 минут обработки не было обнаружено жизнеспособного вируса. Важно отметить, что состав назодина показал сравнительно лучшую эффективность, чем препарат PVP-1 в физиологическом растворе, с точки зрения снижения титров вируса.Эффективность состава назодина была выше в обе клинически значимые временные точки (15 секунд и 5 минут).
Более того, после 15 минут обработки не было обнаружено жизнеспособного вируса. Важно отметить, что состав назодина показал сравнительно лучшую эффективность, чем препарат PVP-1 в физиологическом растворе, с точки зрения снижения титров вируса.Эффективность состава назодина была выше в обе клинически значимые временные точки (15 секунд и 5 минут).
Титр назодина и контрольного образца SARS-CoV-2 с помощью анализа TCID50 и обнаружения РНК с помощью TaqMan RT-PCR в реальном времени. SARS-CoV-2 подвергали воздействию указанных тестовых растворов в течение 1 минуты перед серийным разведением (1:3) и инкубацией на клетках Vero либо в течение 0 (ноль), либо в течение 96 часов. Значения выражены как среднее пороговое значение цикла (Ct) + SEM (n=3) в зависимости от коэффициента разбавления. (A) Нулевой момент времени (0 ч) титрование инокулята, используемое для определения исходных значений Ct обработанных образцов до репликации в клетках Vero.(B) Титры, связанные с культурами, собранными через 96 ч после инокуляции клеток Vero.
Значение исследования
Исследование показывает, что назодин, клинически одобренный назальный спрей с 0,5% ПВП-1, обладает значительной противовирусной активностью в отношении SARS-CoV-2 и потенциально может использоваться для ранней эрадикации SARS-CoV-2 в полости носа. . Чтобы лучше справляться с пандемией COVID-19, назодин потенциально можно использовать вместе с другими мерами контроля для предотвращения передачи вируса.
В настоящее время ученые проводят клинические испытания, чтобы проверить, одинаково ли важны эти эффекты in vitro для пациентов с COVID-19. Они считают, что назодин может быть эффективным дополнительным вмешательством для недавно диагностированных пациентов с COVID-19 с точки зрения замедления прогрессирования заболевания и выделения вируса.
*Важное примечание
bioRxiv публикует предварительные научные отчеты, которые не прошли рецензирование и, следовательно, не должны рассматриваться как окончательные, направляющие клиническую практику/поведение, связанное со здоровьем, или рассматриваться как установленная информация.
В Израиле начинается производство «спасательного» спрея для носа, убивающего 99,9% вирусов
Назальный спрей, который будет позиционироваться как способный убивать 99,9% вирусных частиц, начал сходить с производственных линий на израильском заводе.
Этот спрей мог бы предотвратить большую часть случаев заражения COVID-19 в мире, сказал The Times of Israel его изобретатель, доктор Гилли Регев.
«Мы надеемся, что наш назальный спрей теперь спасет жизни многих людей в странах, которые ждут вакцины», — сказал Регев, биохимик, выросший в Израиле, который стал соучредителем компании SaNOtize и разработал спрей в Канаде.«Это будет доступно по цене и может быть использовано для профилактики, для защиты от любой респираторной вирусной инфекции».
Она сказала, что в лаборатории было показано, что он эффективен против широкого спектра вирусов, и сказала, что новые варианты коронавируса не повлияют на его эффективность, подчеркнув: «Он содержит противовирусный препарат широкого спектра действия, который убивает все вирусы. и все варианты».
и все варианты».
Медицинский 3D-анимационный кадр, показывающий структуру коронавируса (https://www.ScientificAnimations.com/coronavirus-symptoms-and-prevention-explained-through-medical-animation/)
Регев назвал Enovid «эквивалентом дезинфицирующего средства для рук для носа» и сказал, что он создает физический барьер в носовых проходах, чтобы остановить вирусы, наряду с «химическим барьером» из оксида азота, который известен своими антимикробными свойствами. «Окись азота означает, что это специальный спрей, который не просто блокирует вирусы, но фактически убивает их», — сказала она.
Подпишитесь на Tech Israel Daily и никогда не пропустите главные новости Израиля о технологиях
Регистрируясь, вы соглашаетесь с условиями Израиль станет первой страной, где будет продаваться спрей.Министерство здравоохранения дало временное разрешение на его продажу в качестве медицинского устройства, подходящего для людей в возрасте 12 лет и старше — это означает, что его могут использовать многие, у кого еще нет одобрения для вакцин против коронавируса — с указанием на упаковке: «Научно протестировано, чтобы убить 99,9%». вирусов в течение 2 минут».
вирусов в течение 2 минут».
Флакон Enovid, нового противовирусного спрея для носа, который производится в Израиле (любезно предоставлено SaNOtize)
Он также был одобрен для продажи в Новой Зеландии, и запрашивается одобрение в других странах, включая Великобританию.
Регев сказал, что завод в Нес-Ционе недалеко от Тель-Авива работает над тем, чтобы к маю произвести от 200 000 до 500 000 бутылок. «После этого мы надеемся выйти на мощность в миллион бутылок в месяц», — сказал выпускник Еврейского университета, добавив: «Я надеюсь, что этот продукт принесет Израилю гордость и рабочие места».
Заявление на упаковке основано на тестировании в лаборатории, в ходе которого спрей подвергался воздействию ряда живых вирусов, включая грипп и SARS-CoV-2.Она признала, что эксперименты проводились вне человеческого тела, в пробирках, и не дают окончательных доказательств того, насколько эффективен спрей в носовых проходах, хотя она сказала, что они очень обнадеживают.
Отдельное исследование, не упомянутое на упаковке, показало, что спрей может уменьшить воздействие COVID-19 на инфицированных.
На прошлой неделе фонды SaNOtize и Ashford and St Peter’s Hospitals NHS Foundation Trust в Суррее, Великобритания, объявили о результатах клинических испытаний, свидетельствующих о том, что спрей может предотвратить передачу COVID-19, сократить его течение и уменьшить тяжесть симптомов и повреждения в те, кто уже заразился.Исследование было представлено в ведущий медицинский журнал для обзора и публикации.
Члены семьи в защитном снаряжении навещают родственника в отделении коронавируса больницы Шааре Цедек в Иерусалиме, 3 февраля 2021 г. (Йонатан Синдел/Flash90)
Спрей был полностью разработан к моменту начала пандемии, так как был изобретен в основном для борьбы с гриппом. Его нововведением является процедура дозирования оксида азота. «Обычно он поставляется в газовых баллонах и обычно доставляется в больницы, но мы хотели найти практичный способ доставки его в виде жидкого противомикробного препарата и потратили на его разработку последние 12 лет», — сказал Регев.
Ингредиенты спрея смешиваются при введении с образованием оксида азота, сказала она, отметив: «Все компоненты широко используются в пищевой промышленности и имеют очень высокий профиль безопасности». Каждая бутылка содержит месячный запас для одного человека для распыления два раза в день для защиты от вирусов.
Она сказала: «Теоретически мы могли бы распространить его еще год назад, но нам нужно было получить одобрение регулирующих органов. Это самое большое разочарование, что мы пытались 24/7 в течение года вывести его на рынок, и это могло бы спасти много жизней.Я считаю, это предотвратило бы заражение и, следовательно, уменьшило бы смертность».
Вы цените The Times of Israel?
Если да, то у нас есть запрос.
Каждый день наши журналисты стремятся держать вас в курсе самых важных событий, заслуживающих вашего внимания. Миллионы людей полагаются на ToI для быстрого, честного и бесплатного освещения Израиля и еврейского мира.
Мы заботимся об Израиле, и мы знаем, что вы тоже. Итак, сегодня у нас есть просьба: выразите свою признательность за нашу работу, присоединившись к Сообществу The Times of Israel, эксклюзивной группе для таких читателей, как вы, которые ценят и поддерживают нашу работу финансово.
Итак, сегодня у нас есть просьба: выразите свою признательность за нашу работу, присоединившись к Сообществу The Times of Israel, эксклюзивной группе для таких читателей, как вы, которые ценят и поддерживают нашу работу финансово.
Вы преданный читатель
Мы очень рады, что за последний месяц вы прочитали статей X Times of Israel .
Вот почему десять лет назад мы запустили Times of Israel, чтобы предоставить таким проницательным читателям, как вы, обязательные к прочтению статьи об Израиле и еврейском мире.
Теперь у нас есть запрос. В отличие от других новостных агентств, мы не установили платный доступ. Но поскольку журналистика, которой мы занимаемся, обходится дорого, мы приглашаем читателей, для которых The Times of Israel стала важной, поддержать нашу работу, присоединившись к сообществу The Times of Israel.
Всего за 6 долларов в месяц вы можете поддержать нашу качественную журналистику, наслаждаясь The Times of Israel БЕЗ РЕКЛАМЫ , а также получая доступ к эксклюзивному контенту , доступному только членам сообщества Times of Israel.
Спасибо,
Дэвид Горовиц, главный редактор The Times of Israel
Эффективность и безопасность противовирусного назального спрея йота-каррагинан: рандомизированное двойное слепое плацебо-контролируемое предварительное исследование на добровольцах с ранними симптомами простуды | Респираторные исследования
Субъекты
Для исследования были набраны здоровые добровольцы старше 18 лет, которые были заранее проинструктированы и подписали заявление о согласии до любых процедур, связанных с исследованием.Анонимность была гарантирована, так как данные исследования и информация о субъектах хранились в безопасности для предотвращения передачи третьим лицам. Субъекты могли выйти из исследования в любое время без ущерба для дальнейшего лечения.
Субъекты могли выйти из исследования в любое время без ущерба для дальнейшего лечения.
Следующие симптомы оценивались при включении в исследование и в каждый день исследования: местные симптомы включали боль в горле, заложенность носа, насморк, кашель, чихание, а системные симптомы определялись как головная боль, боль в мышцах и озноб. Симптомы оценивались по 4-балльной шкале: 0 = отсутствие (симптом не проявлялся в течение предыдущих 24 часов), 1 = легкая (чувствительная, но не беспокоящая или раздражающая), 2 = умеренная (симптомы иногда беспокоят/раздражают), 3 = тяжелая ( симптомы беспокоят/раздражают большую часть времени).Эта система оценки была разработана Джексоном в 1958 г. и широко используется в клинических исследованиях простуды [14]. Чтобы набрать субъектов с ранним началом простуды, при включении в исследование субъекты имели баллы симптомов 1 или выше для боли в горле, насморка или заложенности носа и общий балл симптомов 9 или менее для суммы баллов тяжести, включая головную боль, мышечная боль, озноб, боль в горле, насморк, заложенный нос, кашель и чихание. Участники исследования согласились воздерживаться от приема любых других лекарств, предназначенных для предотвращения, купирования или лечения симптомов кашля/простуды/гриппа, начиная с момента включения в исследование и до 7-го дня.
Участники исследования согласились воздерживаться от приема любых других лекарств, предназначенных для предотвращения, купирования или лечения симптомов кашля/простуды/гриппа, начиная с момента включения в исследование и до 7-го дня.
Участники были исключены из исследования по следующим заранее определенным причинам: нежелание подписывать форму согласия, известная гиперчувствительность или аллергия на любой компонент исследуемого препарата, клинически значимое сердечно-сосудистое, эндокринное, неврологическое, респираторное или желудочно-кишечное заболевание или история , или любое другое текущее заболевание, которое рассматривалось исследователем в качестве критерия исключения, например текущий аллергический ринит, хроническая обструктивная болезнь легких (ХОБЛ). Хотя в протоколе исследования это прямо не упоминалось, астма была таким критерием исключения, и пациенты с астмой не были набраны.Кроме того, субъекты также исключались исследователем, если имелось серьезное искривление носовой перегородки или другое состояние, которое могло вызвать заложенность носа, например, носовые полипы или операции на носу/придаточных пазухах в прошлом, и влияющие на оценку симптомов. Кроме того, участники с историей злоупотребления алкоголем / психоактивными веществами или принимающие рецептурные лекарства / сопутствующую терапию, кроме контрацепции, например. системные стероиды, интраназальные препараты, антибиотики также были исключены исследователем.Другими причинами исключения были случаи простуды или гриппоподобных симптомов в течение более 48 часов, курение в настоящее время, отношения с любым исследовательским персоналом и введение любого исследуемого препарата или участие в любом другом клиническом испытании в течение 4 недель после включения в наше исследование. Все сопутствующие заболевания или состояния следует лечить в соответствии с преобладающей медицинской практикой.
Кроме того, участники с историей злоупотребления алкоголем / психоактивными веществами или принимающие рецептурные лекарства / сопутствующую терапию, кроме контрацепции, например. системные стероиды, интраназальные препараты, антибиотики также были исключены исследователем.Другими причинами исключения были случаи простуды или гриппоподобных симптомов в течение более 48 часов, курение в настоящее время, отношения с любым исследовательским персоналом и введение любого исследуемого препарата или участие в любом другом клиническом испытании в течение 4 недель после включения в наше исследование. Все сопутствующие заболевания или состояния следует лечить в соответствии с преобладающей медицинской практикой.
Дизайн и цель исследования
Настоящее исследование было разработано как одноцентровое, рандомизированное, двойное слепое, плацебо-контролируемое сравнительное исследование с параллельными группами у субъектов с ранними симптомами простуды для оценки эффективности 0.Назальный спрей 12% Йота-Каррагинан для раннего лечения простудных заболеваний. Выбранный дизайн исследования, контрольные группы и оцениваемые переменные являются стандартными для этой области исследований, как и используемые порядковые шкалы. Блок-схема исследования показана на рисунке 1.
Выбранный дизайн исследования, контрольные группы и оцениваемые переменные являются стандартными для этой области исследований, как и используемые порядковые шкалы. Блок-схема исследования показана на рисунке 1.
Блок-схема для участников исследования, включая демографические данные.
Рандомизация субъектов проводилась после проверки критериев включения/исключения. Ни исследователи, ни испытуемые не знали назначенного лечения.Рандомизация проводилась путем предоставления каждому испытуемому назальному спрею уникального кодового номера. Рандомизированным субъектам назначали назальный спрей при посещении 1 (день лечения 1). Субъекты заполняли ежедневный дневник оценки симптомов простуды в течение 7 дней и подвергались промыванию носа в 1-й день перед первым лечением и в 3-й или 4-й дни. Назальное дозирование исследуемого препарата составляло 3 раза в день в течение 4 дней.
Исследование проводилось в период с февраля по май 2008 г. в Центре исследований простуды и заболеваний носа Кардиффской школы биологических наук Кардиффского университета, Великобритания.Симптомы и применение лечения документировались в дневнике пациента. Кодирование было выполнено компанией CRO Bioconsult GmbH (Перхтольдсдорф, Австрия), а декодирование — после просмотра проб и блокировки базы данных.
в Центре исследований простуды и заболеваний носа Кардиффской школы биологических наук Кардиффского университета, Великобритания.Симптомы и применение лечения документировались в дневнике пациента. Кодирование было выполнено компанией CRO Bioconsult GmbH (Перхтольдсдорф, Австрия), а декодирование — после просмотра проб и блокировки базы данных.
Это исследование проводилось в соответствии с Руководством ICH E6 по надлежащей клинической практике (CPMP/ICH/135/95)5, а также принципами Хельсинкской декларации, местного законодательства о наркотиках и стандартных операционных процедур исследователя, спонсор и CRO участвуют. Протокол исследования и прилагаемая документация (форма согласия, информация о субъекте, ИРК и т.) были одобрены ответственным Комитетом по этике местных исследований Юго-Восточного Уэльса[15]. Подписанный протокол исследования был доступен редактору журнала в процессе рецензирования. Это исследование было зарегистрировано в Европейском реестре клинических испытаний под номером Eudract 2007-007577-23.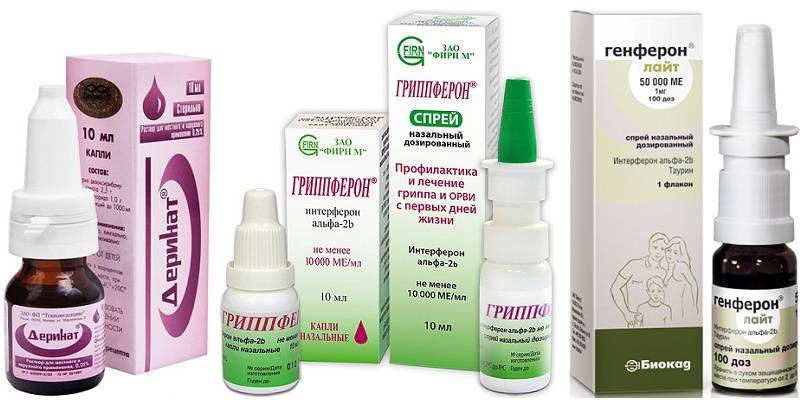
Конечные точки исследования
Первичная мера эффективности определялась проспективно как средняя общая оценка симптомов (TSS) для 2-4 дней исследования, при этом TSS представляла собой сумму 8 индивидуальных баллов симптомов, как описано выше.Максимальный балл TSS составлял 24 для каждой записанной временной точки. Для статистического анализа TSS 2-4 дней исследования суммировали для каждого субъекта и рассчитывали индивидуальные средние значения.
Вторичная мера эффективности определялась проспективно как TSS в отдельные дни исследования 1/2/3/4/5, как средняя общая оценка системных симптомов (TSSS) (головная боль, мышечная боль, озноб) для дней исследования 2-4, и TSSS в отдельные учебные дни 1/2/3/4/5. Другими вторичными переменными эффективности были оценка местных симптомов (LSS) (боль в горле, заложенность носа, насморк, кашель, чихание) в среднем на 2-4 дни исследования и в отдельные дни исследования 1/2/3/4/5 и индивидуальные оценка симптомов (ISS) (головная боль, мышечная боль, зябкость, боль в горле, заложенность носа, насморк, кашель, чихание) в отдельные дни исследования 1/2/3/4/5.
Исследовательские переменные эффективности включали обнаружение вируса/общую вирусную нагрузку, экспрессию цитокинов, обнаруженную в назальном смыве, и приемлемость испытуемых назальных спреев с использованием визуальной аналоговой шкалы (ВАШ, 1-10). Кроме того, были собраны данные о готовности испытуемых использовать продукт в будущем по порядковой шкале (полностью согласен, согласен, не согласен, категорически не согласен).
Исследуемый препарат и дозировка
Назальный спрей Йота-Каррагинан (Verum; немаркированный Coldamaris профилактический ® ) 1,2 г/л, NaCl 5 г/л, вода для инъекций [WFI] ad 20 мл 20.4 г) и плацебо (NaCl 9 г/л, WFI ad 20 мл 20,4 г) были произведены MoNo chem-pharm Produkte GmbH (Вена, Австрия). Растворы для опрыскивания были прозрачными, бесцветными, без запаха и без частиц. Назальные спреи Verum и плацебо были идентичны по форме, размеру и цвету, что позволяло провести двойной слепой дизайн, и были рандомизированы в CRO. Перед введением спрей нужно было встряхнуть и заправить до образования мелкодисперсного тумана. Одно распыление по 140 мкл вводили в каждую ноздрю 3 раза в день в течение 4 дней.В 1-й день первое нанесение спрея было проведено при включении в исследование (с 9:00 до 17:00), следующие два применения спрея проводились через равные промежутки времени в оставшиеся часы бодрствования в 1-й день. равномерно распределены в часы бодрствования. Чтобы контролировать соблюдение протокола исследования, возвращенные флаконы со спреем взвешивали и сравнивали с массой при выдаче, тем самым оценивая массу лекарства, принятого за период исследования. Субъект № 10 (плацебо) пропустил первую дозу в 1-й и 4-й дни, третью дозу во 2-й день и, следовательно, принял только 75% запланированных доз.Все остальные испытуемые имели 100% соответствие согласно дневниковой документации. В целом в этом исследовании было достигнуто 99,3% соответствия. В зависимости от момента включения в исследование ожидаемый диапазон разницы в весе составлял от 2,80 г до 3,36 г. Средняя разница в группе активного препарата составила 3,12 г (± 0,84 г), а в группе плацебо — 3,84 г (± 1,85 г), что свидетельствует о том, что было введено больше доз плацебо, чем настоящего препарата.
Одно распыление по 140 мкл вводили в каждую ноздрю 3 раза в день в течение 4 дней.В 1-й день первое нанесение спрея было проведено при включении в исследование (с 9:00 до 17:00), следующие два применения спрея проводились через равные промежутки времени в оставшиеся часы бодрствования в 1-й день. равномерно распределены в часы бодрствования. Чтобы контролировать соблюдение протокола исследования, возвращенные флаконы со спреем взвешивали и сравнивали с массой при выдаче, тем самым оценивая массу лекарства, принятого за период исследования. Субъект № 10 (плацебо) пропустил первую дозу в 1-й и 4-й дни, третью дозу во 2-й день и, следовательно, принял только 75% запланированных доз.Все остальные испытуемые имели 100% соответствие согласно дневниковой документации. В целом в этом исследовании было достигнуто 99,3% соответствия. В зависимости от момента включения в исследование ожидаемый диапазон разницы в весе составлял от 2,80 г до 3,36 г. Средняя разница в группе активного препарата составила 3,12 г (± 0,84 г), а в группе плацебо — 3,84 г (± 1,85 г), что свидетельствует о том, что было введено больше доз плацебо, чем настоящего препарата.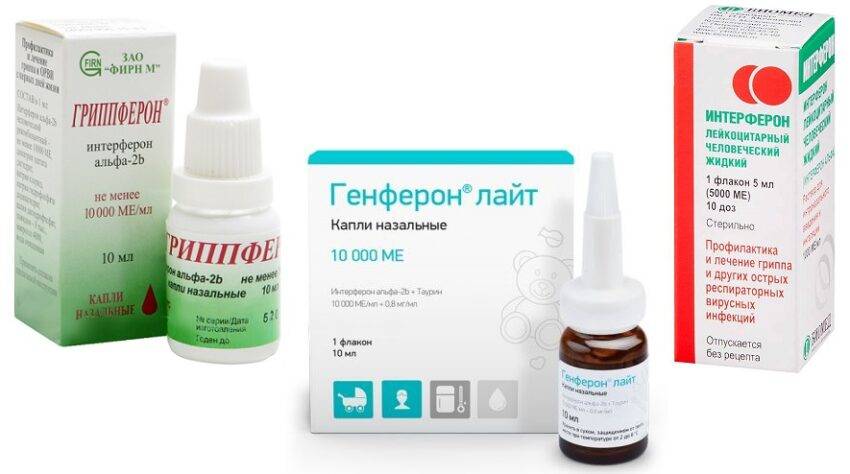 Этот результат подтверждает хорошее согласие, о котором сообщили субъекты в дневнике.
Этот результат подтверждает хорошее согласие, о котором сообщили субъекты в дневнике.
Начало симптомов простуды (дни до визита 1) отображается в дополнительном файле 1: Таблица S1.
Анализ назального смыва
Назальный лаваж проводили в 1-й день (включение в исследование) и в 3-й или 4-й дни. образцы объединены (на субъекта) перед обработкой при 4°C в течение 3 часов. 8 частей лаважа смешивали с 1 частью 5% бычьего альбумина (Sigma Aldrich, Вена, Австрия) и 1 частью 10-кратного коктейля ингибиторов протеазы (Roche, Германия), делили на 5 образцов и хранили при -80°C до дальнейшего анализа.
Для определения респираторной вирусной нагрузки и идентификации вируса в промывных водах носа проводили ПЦР-анализ в реальном времени на вирус гриппа типа А+В, респираторно-синцитиальный вирус типа А+В, вирус парагриппа типов 1/2/3/4, коронавирус типы OC43 и 229E, риновирусы (вирусы большой/малой группы), метапневмовирус человека. Анализы проводили с использованием наборов QiAamp Viral RNA Mini и Qiagen QuantiFast Probe PCR Kit (QIAGEN GmbH, Hilden, Germany), RealAccurate Respiratory RT PCR Kit (Pathofinder, Maastricht, Netherlands) и Real Time PCR 7900 HT Sequence Detection (Applied Biosystems, Foster City). , США) в соответствии с инструкциями производителя.Эта установка позволяет обнаруживать 12 РНК-вирусов, на долю которых приходится примерно 90% инфекций дыхательных путей. Вкратце, образцы объемом 140 мкл оттаивали на льду, переносили в 560 мкл буфера AVL с РНК-носителем, добавляли 10 мкл внутреннего контроля, а элюированную РНК хранили при -20°C в течение максимум 4 часов до переноса в -80°C. С. Реакцию ОТ-ПЦР проводили в конечном объеме 20 мкл. Использовали следующие условия циклера в реальном времени: обратная транскрипция 30 мин при 50°С, 15 мин активация ДНК-полимеразы Taq и инактивация обратных транскриптаз при 95°С, 15 с денатурация при 94°С, 60 с отжиг и удлинение при 55°С, 42 цикла.Значения ct всех положительных образцов были антилогарифмированы на основе 2. Результирующие значения вирус-положительных образцов из первого визита были приняты за 100%. Относительное количество положительных на вирус образцов при втором посещении рассчитывали в процентах от значения первого посещения.
, США) в соответствии с инструкциями производителя.Эта установка позволяет обнаруживать 12 РНК-вирусов, на долю которых приходится примерно 90% инфекций дыхательных путей. Вкратце, образцы объемом 140 мкл оттаивали на льду, переносили в 560 мкл буфера AVL с РНК-носителем, добавляли 10 мкл внутреннего контроля, а элюированную РНК хранили при -20°C в течение максимум 4 часов до переноса в -80°C. С. Реакцию ОТ-ПЦР проводили в конечном объеме 20 мкл. Использовали следующие условия циклера в реальном времени: обратная транскрипция 30 мин при 50°С, 15 мин активация ДНК-полимеразы Taq и инактивация обратных транскриптаз при 95°С, 15 с денатурация при 94°С, 60 с отжиг и удлинение при 55°С, 42 цикла.Значения ct всех положительных образцов были антилогарифмированы на основе 2. Результирующие значения вирус-положительных образцов из первого визита были приняты за 100%. Относительное количество положительных на вирус образцов при втором посещении рассчитывали в процентах от значения первого посещения.
Образцы лаважа анализировали в двух повторностях для измерения относительного количества цитокинов. Концентрацию цитокинов определяли с помощью набора Milliplex MAP Human Cytokine/Chemokine Kit в 96-луночном планшете (Millipore Corp., Сент-Чарльз, США) согласно инструкции производителя. 0,9% NaCl использовали в качестве матрицы, соответствующей лаважной среде, и измеряли следующие цитокины: IL-1 α, IL-1 β, IL-2, IL-3, IL-4, IL-5, IL-6, IL-7. , ИЛ-8, ИЛ-9, ИЛ-10, ИЛ-12 р40, ИЛ-12 р70, ИЛ-13, ИЛ-15, ИЛ-17, ЭФР, эотаксин, фракталкин, Г-КСФ, ГМ-КСФ, ИФН -γ, IP-10, MCP-1, MIP-1 α, MIP-1 β, TNF-α, FGF-2, GRO (включает GRO альфа, бета и гамма), IFN-α2, IL-1ra, MCP- 3, MDC, sCD40L, VEGF. Флуоресценцию определяли в ридере Luminex 100, а данные анализировали с помощью программного обеспечения Luminex (Riverside CA, USA) с использованием метода подбора логистической кривой с 4 параметрами.Нижний предел количественного определения составлял 3,2 пг/мл, значения ниже были установлены как «ноль».