Заражение Helicobacter pylori: симптомы, последствия, лечение
Helicobacter pylori (хеликобактер пилори) – бактерия, заселяющая различные отделы желудка и двенадцатиперстной кишки. Микроорганизм, зачастую называемый просто «хеликобактер», провоцирует развитие множества заболеваний гастродуоденальной зоны: гастрита, дуоденита, язвы желудка и двенадцатиперстной кишки.
Что представляет собой бактерия Helicobacter pylori?
Впервые бактерия была открыта более 100 лет назад (в далеком 1875 году), однако её роль в развитии рецидивирующих заболеваний пищеварительной системы была доказана и признана лишь в 1994 году.
Бактерия распространяется контактно-бытовым путем: через предметы обихода и личной гигиены, при поцелуях, и пр. Инфицирование может вызывать развитие симптомов или же человек может быть бессимптомным носителем бактерии – всё зависит от штамма инфекции и состояния иммунитета больного. Бессимптомное носительство наблюдается в большинстве случаев.
Helicobacter pylori — чем она опасна для нас?
Отличительной чертой всего рода Helicobacter, в который входит хеликобактер пилори, является способность выживать и размножаться в кислотной среде, которая характерна для содержимого желудка. Спиралевидная форма и жгутики позволяют бактерии проникать сквозь густой слой слизи, который защищает слизистую оболочку желудка и двенадцатиперстной кишки от воздействия кислоты.
Бактерия закрепляется и начинает размножаться в слизистой желудка. В процессе жизнедеятельности Helicobacter pylori синтезирует ряд токсинов, под воздействием которых клетки слизистой оболочки желудка повреждаются и погибают, а защитный слой слизи — растворяется. В результате кислотная среда начинает воздействовать непосредственно на незащищенные клетки слизистой оболочки, вызывая воспаления и язвы.
Важно понимать, что Helicobacter pylori – не единственная причина гастрита и язвы, хоть и важный фактор, способствующий развитию заболеваний пищеварительной системы.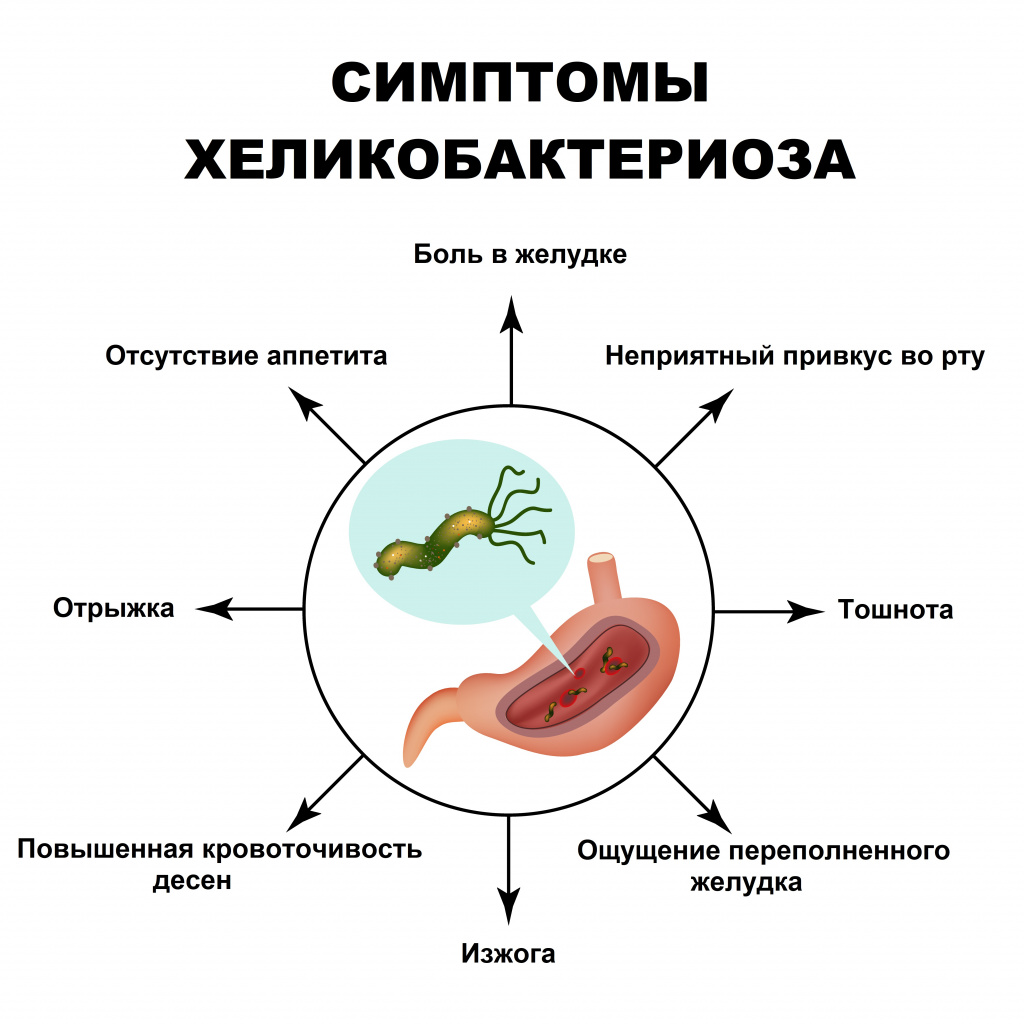
Симптомы заболеваний органов желудочно-кишечного тракта
Для гастрита, заболевания, которое наиболее часто ассоциируется с Helicobacter pylori, характерны следующие симптомы:
- регулярные боли в желудке;
- отрыжка и изжога;
- тошнота;
- неприятный привкус во рту;
- расстройства пищеварения;
- возможно повышение температуры.
Язва желудка проявляется длительными болями в верхней части живота, ослабевающими после приема пищи. Если симптомы игнорировать – появляются резкие и сильные боли (часто ночные), запоры, возможно желудочное кровотечение.
Назначение врачом анализа на хеликобактер и подготовка к нему
Появление вышеперечисленных симптомов – серьезный повод для обращения к гастроэнтерологу, который, среди прочих обследований, назначит и тест на хеликобактер. Такое обследование обязательно также, если болезни пищеварительного тракта есть у других членов семьи или возникают у пациента повторно.
Существует несколько методов диагностики Helicobacter pylori: дыхательный тест, анализ кала и анализ крови. Анализ крови на хеликобактер, как и анализ кала не требует от пациента подготовки при сдаче биоматериала в лабораторию. При анализе кала определяется наличие самой бактерии, а при анализе крови – антител, вырабатываемых организмом против неё. Потому у людей с ослабленным иммунным ответом (пожилые люди, пациенты с иммуносупрессией), тест на антитела к хеликобактеру может дать ложноотрицательный результат.
Наиболее надежный способ выявить хеликобактер пилори – лабораторное исследование биоптата, полученного во время гастроскопии. В данном случае пациент должен быть подготовлен к проведению гастроскопии (главное требование – прийти на обследование натощак). В лаборатории «Медлаб» быстро и качественно проводят все необходимые исследования на предмет хеликобактера.
Лечение Helicobacter pylori
Эрадикация (уничтожение бактерии) проводится при помощи антибиотиков. Если патоген диагностируется не только у пациентов с хеликобактером, но и у членов их семей, то лечение может проводиться всей семье, чтобы избежать повторного инфицирования. В данный момент врачи зачастую сходятся на мнении, что лечить хеликобактер нет необходимости, если у пациента не наблюдается никаких симптомов заболеваний желудочно-кишечного тракта.
Если патоген диагностируется не только у пациентов с хеликобактером, но и у членов их семей, то лечение может проводиться всей семье, чтобы избежать повторного инфицирования. В данный момент врачи зачастую сходятся на мнении, что лечить хеликобактер нет необходимости, если у пациента не наблюдается никаких симптомов заболеваний желудочно-кишечного тракта.
Важно понимать, что самолечение хеликобактера антибиотиками недопустимо, ведь только врач может определить необходимость антибиотикотерапии (оценить потенциальный вред и пользу от приема препаратов), назначить эффективную дозировку и курс, достаточный для полного уничтожения бактерии.
Желудочная бактерия и старение кожи: есть ли связь?
Что такое желудочная бактерия
Хеликобактер также может вызывать воспаление и раздражение слизистой оболочки желудка (гастрит). А в редких случаях невылеченная инфекция может привести к раку желудка.
Helicobacter pylori — это разновидность микробов, обитающих в желудке. Эти бактерии, открытые сравнительно недавно, в 1983 году, присутствуют в организме примерно половины людей, и большинство из них даже не испытывают никакого дискомфорта.
Эти бактерии, открытые сравнительно недавно, в 1983 году, присутствуют в организме примерно половины людей, и большинство из них даже не испытывают никакого дискомфорта.
H. pylori размножается в слизистой оболочке желудка и двенадцатиперстной кишки. Бактерии выделяют фермент, называемый уреазой, который превращает мочевину в аммиак. Этот аммиак защищает бактерии от желудочного сока. По мере размножения хеликобактер разъедает ткани желудка, что приводит к гастриту и / или язвенной болезни.
Причины появления хеликобактер пилори
Бактерии хеликобактер пилори присутствуют примерно у 50–75% населения Земли и чаще всего встречается у детей. Инфекция наиболее распространена в развивающихся странах.
Люди с Helicobacter pylori почти всегда заражаются ей в детстве, вероятно, от других детей. Она обнаруживается в слюне, зубном налете и в фекалиях. Инфекция может передаваться через поцелуи и через перенос бактерий с рук тех, кто не вымыл их после дефекации.
Ученые считают, что желудочная бактерия также может передаваться через воду и пищу, зараженную ей.
Обычно хеликобактер остается в желудке на протяжении всей жизни, если ее не лечить с помощью, например, антибиотиков.
И до сих пор неясно, почему только у некоторых людей с этой инфекцией развивается язва желудка.
Симптомы и диагностика
У большинства людей, инфицированных Helicobacter pylori, симптомы отсутствуют.
Обычно признаки присутствия бактерии в организме можно заметить при развитии гастрита или язвенной болезни. Они включают:
-
Тупая или жгучая боль в желудке (чаще через несколько часов после еды и ночью). Боль длится от нескольких минут до нескольких часов.
-
Необъяснимая потеря веса.
-
Вздутие живота.

-
Тошнота и рвота.
-
Несварение желудка (диспепсия).
-
Отрыжка.
-
Потеря аппетита.
-
Темный стул (из-за крови в нем).
При подозрении на наличие хеликобактер пилори ваш лечащий врач может назначить один или несколько из следующих тестов:
-
Дыхательный тест. Суть в том, что пациент выдыхает в мешок до и после того, как выпьете специальный раствор. Тест измеряет количество выделяемого углекислого газа. Более высокий его уровень после употребления раствора говорит о присутствии желудочной бактерии.
-
Исследование эндоскопического материала. через глотку в желудок вводится гибкая трубка. Небольшой образец ткани из слизистой оболочки желудка или кишечника берется для проверки на наличие Helicobacter pylori.

-
Анализ кала. Наиболее традиционный метод выявления бактерий.
Влияние Helicobacter Pylori на процессы старения клеток
H. pylori вызывают множество заболеваний, не связанных с желудочно-кишечным трактом. В частности, бактерия провоцирует немало проблем с кожей:
-
Хроническая крапивница. Несколько исследований обнаружили связь между инфекцией H. pylori и хронической крапивницей. Считается, что хеликобактер увеличивает проницаемость слизистой оболочки желудка и, таким образом, усиливает воздействие аллергенов в желудочно-кишечном тракте. Кроме того, иммунный ответ на H. pylori вырабатывает антитела, которые могут способствовать высвобождению гистамина в коже.
-
Розацеа. Желудочная бактерия также может повышать уровень закиси азота в крови или тканях, что способствует покраснению при розацеа.

-
Псориаз. H. pylori может быть одним из организмов, способных вызывать воспалительную реакцию при псориазе.
-
Синдром Шегрена. Хеликобактер пилори может вызывать аутоиммунную реакцию кожи и желез, вызывая синдром Шегрена.
Также желудочную бактерию связывают и с другими недугами:
-
Очаговая алопеция;
-
Атопический дерматит;
-
Болезнь Бехчета;
-
Генерализованный зуд;
-
Идиопатическая тромбоцитопеническая пурпура;
-
Красный плоский лишай и т.д.
Несколько небольших исследований показали, что искоренение H. pylori положительно влияет на такие кожные заболевания, как крапивница, болезнь Бехчета, красный плоский лишай, атопический дерматит, болезнь Свита и системный склероз.
Кроме того, выяснилось, что хеликобактер пилори производят большое количество белков, обладающих выраженным иммунногенным действием, которые “в ответе” за развитие воспалительных реакций.
Также они выделяют цитотоксины (онкобелки), тормозящие пролиферацию и подвижность эпителиальных клеток. Так, в 2010 г. уже было показано, что секреция цитотоксина CagA H. Pylori индуцирует клеточное старение эпителиальных клеток желудка человека и в итоге приводит к возникновению желудочно-кишечных расстройств и системному воспалению.
В исследовании, опубликованном в журнале Biogerontology, польские генетики попытались объяснить прямое повреждающее действие H. Pylori на кожу. По их мнению, оно происходит за счет стимуляции стресс-индуцированного преждевременного старения клеток кожи, в частности, фибробластов и кератиноцитов. Исследователи считают, что такое действие H. Pylori будет обусловлено еще и увеличением выработки активных форм кислорода и азота, воспалением, эпигенетическими изменениями и повреждением ДНК. Все это также является биомаркерами клеточного старения.
Все это также является биомаркерами клеточного старения.
Отметим, что стареющие клетки способны синтезировать провоспалительные соединения (интерлейкины, факторы роста), которые могут оказывать неблагоприятное воздействие на окружающие клетки и ткани.
Краткие выводы
-
Helicobacter pylori — это разновидность микробов, обитающих в желудке. По мере размножения хеликобактер разъедает ткани желудка, что приводит к гастриту и / или язвенной болезни.
-
У большинства людей, инфицированных Helicobacter pylori, симптомы отсутствуют.
-
Бактерия провоцирует некоторые дерматологические заболевания.
-
Некоторые исследования говорят о связи хеликобактер с преждевременным старением кожи.
Список использованной литературы
-
Маев И.
 В., Самсонов А.А., Андреев Н.Г., Кочетов С.А. Эволюция представлений о диагностике и лечении инфекции Helicobacter pylori (по материалам консенсуса Маастрихт IV, Флоренция 2010) // Вестник практического врача. — 2012. Спецвыпуск 1 — С. 6-30.
В., Самсонов А.А., Андреев Н.Г., Кочетов С.А. Эволюция представлений о диагностике и лечении инфекции Helicobacter pylori (по материалам консенсуса Маастрихт IV, Флоренция 2010) // Вестник практического врача. — 2012. Спецвыпуск 1 — С. 6-30.
-
Успенский Ю.П., Суворов А.Н., Барышникова Н.В. Инфекция Helicobacter pylori в клинической практике. СПб.: ИнформМед, 2011. — 587 с.
Хеликобактер пилори — Медичний центр «Ліко-Мед»
Дата публикации 3 октября 2018
Helicobacter Pylori
Helicobacter (H. pylori) представляют собой распространенный тип бактерий, живущих в желудке и верхней части кишечника. H. Pylori является основной причиной появления большинства пептических язв, поражений слизистой оболочки желудка или верхнего отдела кишечника. Данная бактерия ослабляет слизистую оболочку желудка, что способствует разъеданию футеровок желудочным соком, вызывая жжение в животе и боль.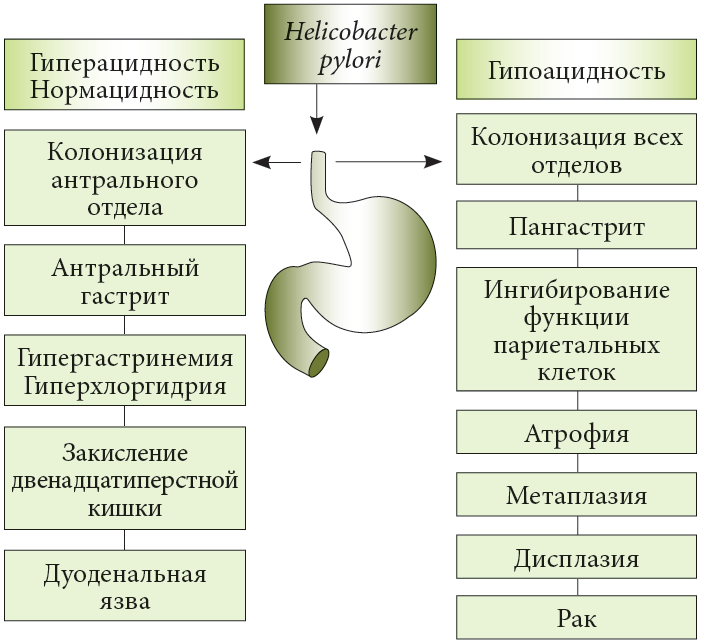
Чего ожидать?
У некоторых людей, у которых имеются H. Pylori, не наблюдается никаких симптомов. У других же после заражения спустя несколько месяцев или недель проявляются различные заболевания, вызванные деятельностью инфекционных бактерий. Лечить появившиеся язвы следует сразу, так как в скором времени состояние больного может ухудшиться, а болезни приобрести хроническую форму.
Хроническая язвенная болезнь может спровоцировать рак кишечника, а тяжелые формы данной патологии стать причиной внутренних кровотечений или блокады желудка. Перфорированные язвы, которые характеризуются наличием отверстий в слизистой желудка, требуют срочной медпомощи.
Распространенность
Хеликобактерная инфекция диагностируется примерно у 1 человека из 50, независимо от места проживания и образа жизни.
Лечение
- Антибиотики;
- Лекарственные средства, подавляющие кислотность;
- Антациды;
- Диета.
Что можно предпринять самому?
Для предотвращения осложнений следует избегать острой пищи, кофеина, алкоголя и табакокурения. Для обезболивания не следует принимать нестероидные препараты, так как они оказывают негативное раздражающее воздействие на слизистую желудка.
Для обезболивания не следует принимать нестероидные препараты, так как они оказывают негативное раздражающее воздействие на слизистую желудка.
Отрегулируйте свой рацион питания и избегайте стрессовых ситуаций. Препараты, подавляющие кислотность могут ослабить признаки язвы, но подобные средства не рекомендуется принимать длительное время. Лучше всего посетить своего доктора, который выяснит причины возникновения язвы и при необходимости назначит эффективные антибиотики.
Чем усугубляется?
НПВП, кофеин, сигареты, алкоголь и длительное голодание
Когда обращаться к врачу?
При появлении внезапной сильной боли в области живота, рвоты с кровью, черного или дегтеобразного стула с примесью крови.
О чем спросить врача?
- Мне нужно принимать антацидные препараты?
- Я нуждаюсь в приеме антибиотиков?
- Через какое время возникнут осложнения?
- Мне следует волноваться при кишечных кровотечениях?
- Может ли у меня быть что-то более серьезное, чем язва?
Постановка диагноза
Медицинский анамнез и проведение физикального исследования дает возможность диагностировать заболевание. Врач может назначить анализ крови, провести дыхательный тест на наличие хеликобактерных бактерий, а также рентген желудка или эндоскопию. При проведении эндоскопии больной находится под наркозом, а специалист через горло, при помощи специального прибора осматривает желудок, чтобы подтвердить наличие язвы или других поражений.
Врач может назначить анализ крови, провести дыхательный тест на наличие хеликобактерных бактерий, а также рентген желудка или эндоскопию. При проведении эндоскопии больной находится под наркозом, а специалист через горло, при помощи специального прибора осматривает желудок, чтобы подтвердить наличие язвы или других поражений.
Диагностика причин гастрита и язвы
Основной причиной гастрита и язвы (заболеваний желудка и двенадцатиперстной кишки) является наличие в организме человека Helicobacter pylori (Хеликобактер пилори) — самой распространенной инфекции органов пищеварения. Чаще всего попадание бактерии происходит в детстве, поскольку защитные механизмы в это время недостаточно сильны. Инфекция может распространяться через соприкосновение человека с зараженными предметами в местах общественного пользования. В семье, где есть больные хеликобактериозом, вероятность заражения наиболее велика, так как инфекция «прячется» в предметах гигиены, посуде, дверных ручках.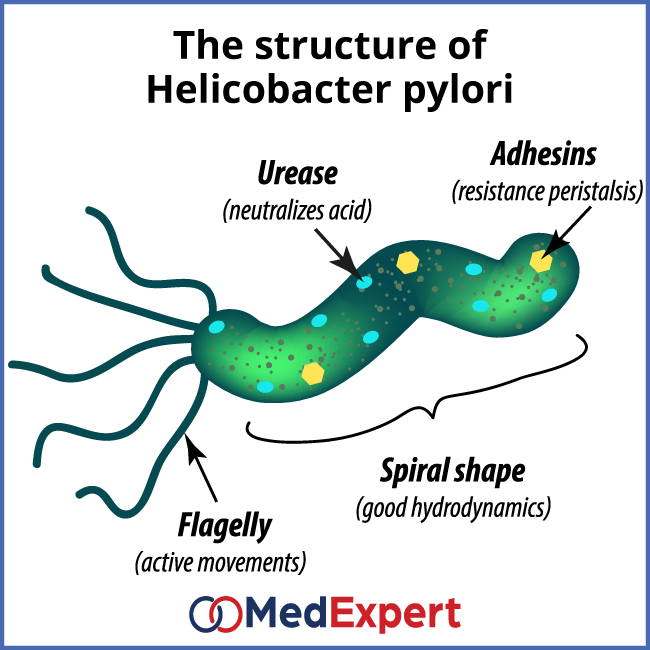
При размножении бактерия разрушительно действует на наш желудок. При этом выделяются токсины, которые вызывают воспаление слизистой оболочки желудка, а впоследствии способствуют возникновению гастрита. Ослабление слизистой желудка или двенадцатиперстной кишки приводит к их истончению и появлению язв. Первые признаки заболевания — постоянная ноющая или острая боль верхней части живота, сопровождающаяся кислой отрыжкой, изжогой и тошнотой, нарушением стула, запахом изо рта. Симптомы заболевания могут проявиться не сразу, ведь Хеликобактер активизируется в момент ослабления организма. Одним из основных пусковых механизмов является хронический стресс и психоэмоциональные перегрузки. Несбалансированное питание, слишком сухая, горячая, острая и соленая пища способствуют обострению болезни. Усугубляет процесс развития болезней злоупотребление алкоголем и отравление организма никотином.
Где сдать анализы при гастрите и язве?
В случае, когда имеются подозрения на заболевания желудка, необходимо сдать анализы на гастрит и язву. И тому есть веские причины:
- она устойчива к кислой среде желудка, может обитать в организме на протяжении многих лет и стать причиной развития рака желудка;
- своевременное обследование позволит назначить правильное лечение и предотвратить возникновение серьезных осложнений.
Рекомендуем Вам пройти полное обследование на Хеликобактер пилори в медицинской лаборатории «Синэво».
Сдать анализ на гастрит и язву можно в Минске, Гомеле, Бресте, Гродно, Витебске, Могилеве, Бобруйске, Барановичах, Солигорске, Слуцке, Полоцке, Новополоцке, Орше, Жлобине, Светлогорске, Молодечно, Пинске, Борисове, Мозыре, Речице, Сморгони.
Причины возникновения метеоризма: факты и мифы
Метеоризм – один из самых частых симптомов расстройства пищеварения.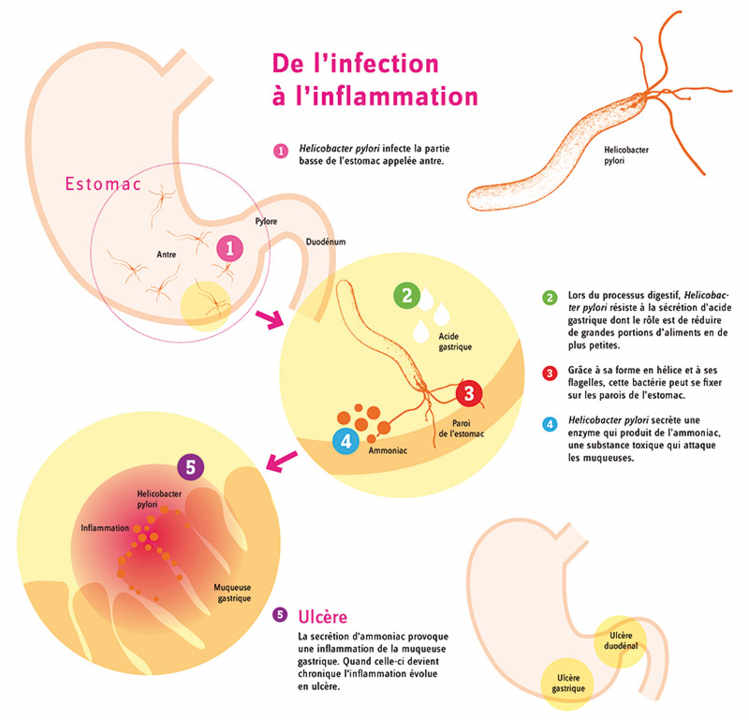 В эфире канала «Россия 1» ведущие программы «О самом главном» Михаил Полицеймако и Сергей Агапкин вместе с врачом-гастроэнтерологом Сергеем Вяловым разобрали несколько популярных фактов о метеоризме и решили, какие из них действительно заслуживают доверия, а какие нет.
В эфире канала «Россия 1» ведущие программы «О самом главном» Михаил Полицеймако и Сергей Агапкин вместе с врачом-гастроэнтерологом Сергеем Вяловым разобрали несколько популярных фактов о метеоризме и решили, какие из них действительно заслуживают доверия, а какие нет.
В норме человек выпускает газы около 14 раз в день. «Если метеоризм, например, каждый час, тогда это, конечно, перебор. Если метеоризм настолько надувает живот, что он увеличивается в размере, это тоже тревожный звонок. Еще если метеоризм сопровождается не только ощущением надутости, но и распиранием изнутри наружу, как будто живот хочет взорваться, это тоже тревожный симптом», – объяснил врач-гастроэнтеролог, гепатолог Сергей Сергеевич Вялов.
Причины метеоризма
Неправильное питание. Большинство газообразных веществ находится в кишечнике. Нехватка в рационе овощей, фруктов и богатой клетчаткой растительной пищи приводит к нарушению стула. Старайтесь съедать в сутки минимум 500 г фруктов!
Попадание избыточного количества воздуха в ЖКТ при употреблении еды. Стресс и тревожность ускоряют перистальтику кишечника! Пережевывайте пищу тщательно, пейте медленно, старайтесь не говорить во время еды! При склонности к повышенному газообразованию пейте воду минимум за полчаса до еды!
Стресс и тревожность ускоряют перистальтику кишечника! Пережевывайте пищу тщательно, пейте медленно, старайтесь не говорить во время еды! При склонности к повышенному газообразованию пейте воду минимум за полчаса до еды!
Воспалительные заболевания кишечника. Язвенный колит или болезнь Крона – серьезные заболевания кишечника. Если при употреблении в пищу большего количества клетчатки газообразование усиливается, значит, можно говорить о наличии слабого воспаления или раздражения в кишечнике.
Хеликобактер пилори. Продукты жизнедеятельности этой бактерии вызывают воспаление и повреждение слизистой оболочки желудка. Нарушается слизистый барьер и выработка соляной кислоты, что ведет к нарушению работы кислотопроизводящих клеток. Бактерии в тонком кишечнике начинают активно размножаться, возникает газообразование, что ведет к постоянному вздутию. Сдайте анализ на наличие хеликобактер пилори!
Факты и мифы
Сырые овощи и отруби приводят к метеоризму. Сырые овощи чуть больше способствуют газообразованию и вздутию, чем термически обработанные.
Прием антибиотиков или других лекарственных препаратов. Некоторые антибиотики убивают микробов и в кишечнике, что приводит к вздутию и газообразованию. Однако, например, препарат амоксициллин в сочетании с клавулановой кислотой вызывает астматическую диарею, но на микрофлору не влияет.
Метеоризм и дисбактериоз – это синонимы. Дисбактериоз в подавляющем большинстве случаев сопровождается метеоризмом. Дисбаланс в составе микрофлоры кишечника может стать причиной язвенного колита.
Язва желудка
Язва желудка является одним из самых опасных заболеваний желудочно-кишечного тракта (ЖКТ). Она представляет собой появление трофических нарушений на слизистой желудка, которые не заживают. Язвенная болезнь является хронической патологией.
Язвенная болезнь желудка часто является следствием гастрита, протекающего без должно лечения.
Симптомы язвы желудка
К основным признакам наличия язвы желудка принято относить:
- Ярко выраженные болевые ощущения в верхней части живота;
- Тяжесть внизу живота;
- Отрыжка, усиленное газообразование и изжога;
- Снижение аппетита и тошнота;
- Запоры;
- Повышенная потливость.

Помните: язва возникает в разных частях желудка, поэтому и болевой синдром может проявляться в различных областях живота. Даже при появлении слабовыраженной боли – незамедлительно обратитесь к врачу, чтобы не дать болезни прогрессировать.
Так, например, при язве большой кривизны желудка боль выражается очень слабо, переносится легко. По этой причине зачастую ее диагностируют уже на этапе активного развития патологии.
Встречаются и такие случаи язвенной болезни, когда она протекает без симптомов, отсутствуют боли. Именно поэтому рекомендуется регулярно наблюдаться у врача-гастроэнтеролога.
Причины возникновения язвенной болезни
Возбудителем язвенной болезни является спиралевидная бактерия под
названием Хеликобактер пилори.
Не последнюю роль в нарушении
работы органов ЖКТ играет изобилие в нашем рационе вредных
продуктов, а также пристрастие к пагубным привычкам. Среди причин
появления язвы желудка также стоит отметить:
Среди причин
появления язвы желудка также стоит отметить:
- Хронический гастрит;
- Частый прием лекарственных препаратов;
- Плохая наследственность;
- Постоянные стрессы.
Лечение язвы желудка
Поскольку язва желудка означает деформацию слизистой оболочки желудка (эрозия и трофические нарушения), она требует особого комплексного лечения и регулярного наблюдения у специалиста.
Конкретные методы лечения зависят от того, чем именно было вызвано появление патологии, поэтому должны назначаться врачом-гастроэнтерологом. Опытный специалист может назначить:
- Специальные препараты от язвенной болезни – лекарственная терапия подразумевает прием антибактериальных препаратов и может состоять из двух этапов;
- Диетотерапия;
- Лечебная физкультура;
- Оперативное вмешательство (назначается редко – в крайнем
случае).

Важно понимать, что при появлении желудочной язвы заниматься самолечением и откладывать поход к врачу категорически нельзя.
Несвоевременное обращение к специалисту может привести к перфорации язвы – появлении сквозного отверстия в стенке желудка и двенадцатиперстной кишки. При этом все содержимое желудка попадает в брюшную полость, что приводит к воспалению брюшины.
Не затягивайте с визитом к врачу – берегите свое здоровье!
Запишитесь на прием к специалисту, заполнив форму
на сайте. Или позвоните нам по телефону +7 (812) 303-07-03 доб.1
+7 (921) 963-85-00.
HUBT-20P — Intermed Innovation
HUBT – 20P – это устройство, которое используется в медицинских учреждениях для обнаружения инфекции хеликобактера пилори в желудке человека. Детектор используется для проведение дыхательного теста с 14С-мочевиной, которое позволяет диагностировать инфекцию Хеликобактер пилори с помощью анализа выдыхаемого газа.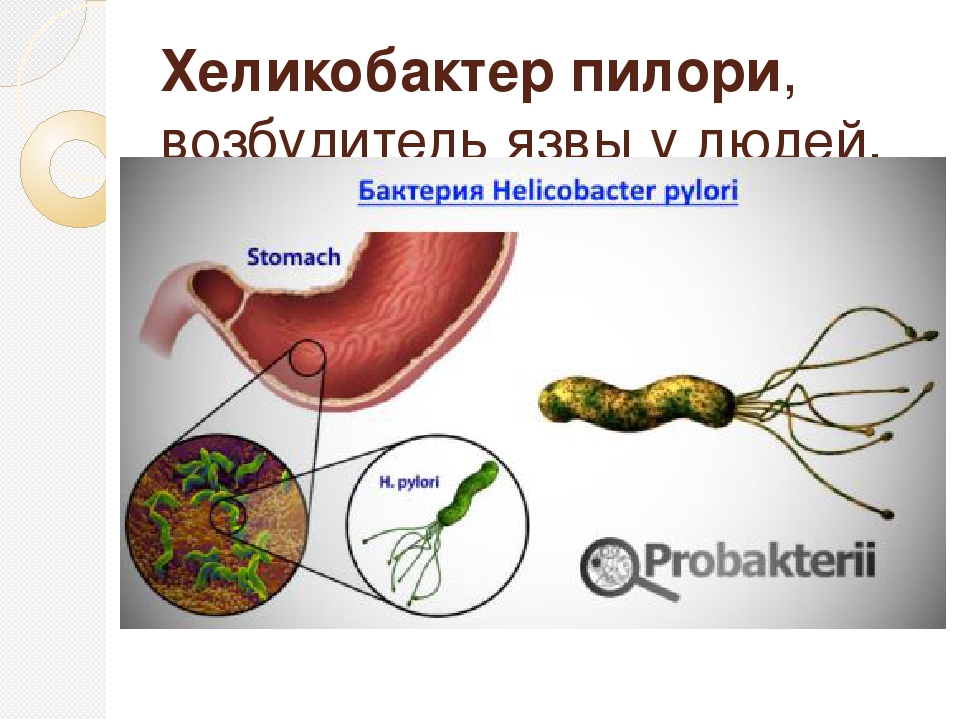
Бактерия Хеликобактер пилори (H. pylori) – является основной причиной развития гастрита и пептической язвы, а также считается причиной возникновения рака желудка у некоторых пациентов. Доказано, что эта бактерия инфицирует более 50% населения Земли, а в развивающихся странах этот показатель достигает 80%.
В 2005 году Нобелевская премия по физиологии или медицине была присуждена Барри Маршалу и Робину Уорену «За работы по открытию и изучению влияния бактерии Хеликобактер пилори на возникновение гастрита и пептической язвы».
Главные особенности HUBT-20P дыхательного теста с 14С-мочевиной:
Компактное внешнее устройство и его портативность с улучшенной конструкции.
Высокотехнологичные компоненты, обеспечивающее его высокую эффективность и надежность работы.
Интуитивно понятный и удобный пользовательский интерфейс на английском языке.
Простота в эксплуатации и автоматический анализ проб, для запуска которого не требуется нажатие кнопок.
Полностью автоматическая диагностика неисправностей, автоматическое вычитывание фона детектора и автоматическая калибровка.
Выпускает С-величину и автоматическое определение положительного или отрицательного результата.
Встроенный термопринтер с функцией автоматической печати данных.
Адаптирован к внешним ПК, с возможностью передачи информации по локальной сети с печатью графиков по настраиваемым шаблонам для соответствия требованиям различных медицинских учреждениях.
Что такое дыхательный тест с 14С-мочевиной?
Дыхательный тест – эта неинвазивная диагностика с применением дыхательных тестов (используется мочевина, меченная 13С и 14С) базируется на высокой уреазной активности H. pylori (Хеликобактер пилори). Под действием уреазы в желудке мочевина, меченная изотопом углерода, расщепляется до аммиака и углекислого газа, содержащего метку. Углекислый газ попадает в кровь и выводится из организма через легкие, при этом в выдыхаемом воздухе увеличивается содержание углерода.
В большинстве стран мира широко применяются радиоактивный 14С, для регистрации которого необходим сцинтилляционный счетчик (детектор Хеликобактер пилори), а также нерадиоактивный 13С изотоп, для определение которого масс-спектрометры (анализатор для определения концентрации). Оба варианта являются высокоспецифичными и высокочувствительными тестами.
Инфицирование Хеликобактер пилори помимо уреазного дыхательного теста выявляются также другими существующими неинвазивными методами: серологических исследований, анализа кала на антиген. До тех пор применяются также инфицирование бактерии инвазивным методом: исследование микробной культуры, гистологическое исследование и быстрый уреазный тест с использованием биопсийной пробы.
Преимущества дыхательного теста с 14С-мочевиной:
Дыхательный тест с 14С-мочевиной имеет следующие преимущества:
Точность: Чувствительность составляет — 95%, специфичность – 95% — 100%.
Комфорт: Неинвазивная процедура, которая не требует введения эндоскопа и хорошо переносится пациентами.
Удобство: Проведение анализа на месте взятия пробы сводит неудобства для пациентов к минимуму.
Безопасность: Метод предполагает воздействие пренебрежимо малых доз радиации, в связи с чем он был освобожден от нормативных ограничений по использованию радиоактивных материалов в США и в Китае.
Простота: Простая операция, не требующий особого обращения.
Скорость: На полное проведение теста необходимо 30 минут, а результаты доступны на месте взятия пробы.
Применение дыхательного теста с 14С-мочевиной:
Для первичной диагностики диспепсии и мониторинга инфекции Хеликобактер пилори после лечения.
При лечении инфекции Хеликобактер пилори у пациентов с язвой желудка и (или) двенадцатиперстной кишки, хроническим активным гастритом, антральным гастритом или злокачественной MALT-лимфомой желудка.
В качестве меры предупреждения возникновения рака желудка или для диагностики лиц с раком желудка в семейном анамнезе.
В случае отказа от гастроскопии.
Для диагностики пациентов, принимающих НПВП (нестероидные противовоспалительные препараты) на протяжении долгого времени.
При железодефицитной анемии неясного генеза.
При идиопатической тромбоцитопенической пурпуре (ИТП).
В ходе фекального обследование.
Комплект для дыхательного тестирование с 14С-мочевиной:
Комплект для дыхательного тестирование с 14С-мочевиной используется для выявления уреазы в желудке как вспомогательный метод при диагностике инфекции Хеликобактер пилори (H. pylori). В комплект дыхательного тестирование входит:
Капсулы с 14С-мочевиной: 27,8 кБк (0, 75 мкКи) в одной капсуле; по 40 капсул в упаковке.
Картриджи для сбора проб: 40 штук в упаковке.
Листок-вкладыш.
Схема проведение дыхательного теста с 14С-мочевиной:
Перед проведением дыхательного теста пациент не должен употреблять пищу и пить напитки в течение 2-х часов.
За 15 минут до проведение дыхательного теста пациент должен принять капсулу с 14С-мочевиной и запить водой, далее принять спокойное положение сидя.
После 15-ти минут, пациент должен взять картридж для сбора пробы и подуть в него через специальное отверстие непрерывно в течение 3-х минут, пока в картридже на индикаторе не изменится с оранжевого цвета на желтый цвет.
После, вставить картридж с желтым цветом на индикаторе в устройство для анализа. По окончании анализа результат отобразится на экране детектора.
Результат анализа обозначает следующие данные, в случае: Если пациент здоров, указывается отрицательное значение Hp (-) C (СРМ) ≤ 40; Если пациент болен, то указывается положительное значение Hp (+) C (СРМ) ≥ 40.
При запросе на получение данных анализа и статических вычислений, полученную информацию можно передать по локальной сети или распечатать через встроенный термопринтер.
Спецификация дыхательного теста с 14С-мочевиной:
Эффективность обнаружения 14С-мочевины из контрольного источника: с 15%.
Фон детектора 14С: ≤ 50 имп/мин (СРМ).
Допустимое относительное отклонение эффективности обнаружения 14С: ≤ 30% после проведения анализа.
Технические характеристики:
Принцип работы детектора: Регистрация ионизирующего излучения.
Питание: 220V переменного тока ± 22V, 47-51 Гц.
Тип защиты: Класс защиты от поражения электрическим током I и II.
Условия эксплуатации: При температуре 5-40 °C, влажности ≤ 75% и атмосферном давлении 75-106 Кпа.
Энергопотребление: ˂ 30В · А.
Время прогрева: ≥ 30 мин.
Среднее время нормальной работы: ≥ 1000 ч.
Фиксированное время измерения: 250с (допустимый диапазон ± 1%).
Размер: 32 х 30 х 28 см (Д х В х Ш).
Вес: 13,5 кг.
Helicobacter pylori (для родителей) — Nemours Kidshealth
Что такое
Helicobacter pylori ? Helicobacter pylori (H. pylori) — это тип бактерий. Эти микробы являются частой причиной заболеваний пищеварительной системы, в том числе:
Эти микробы являются частой причиной заболеваний пищеварительной системы, в том числе:
- Гастрит: раздражение и воспаление слизистой оболочки желудка
- Пептические язвы (часто называемые язвами желудка): язвы на слизистой оболочке желудка, тонкой кишки или пищевода
- в более позднем возрасте, рак желудка
Дети могут болеть в животе по разным причинам, включая несварение желудка, вирусы, стресс и беспокойство, а также аппендицит.Большинство болей в животе не вызываются бактериями Helicobacter pylori (HEL-ih-ko-bak-tur pie-LOR-eye).
Каковы признаки и симптомы инфекции
H. pylori ?Многие люди, зараженные инфекцией H. pylori , не осознают этого. Часто эти инфекции не вызывают симптомов.
Когда бактерии действительно вызывают симптомы, обычно это либо симптомы гастрита, либо язвенной болезни.
У детей симптомы гастрита (ga-STRYE-tis) могут включать:
У детей старшего возраста и взрослых наиболее частым симптомом язвенной болезни является длительная или жгучая боль в животе, обычно в области ниже ребер и выше пупка. Эта боль часто усиливается натощак и проходит, как только человек ест, пьет молоко или принимает антацидные лекарства.
Эта боль часто усиливается натощак и проходит, как только человек ест, пьет молоко или принимает антацидные лекарства.
Пептические язвы, которые могут вызвать кровотечение:
- кровавая рвота (hee-muh-TEM-uh-sis): кровавая рвота или рвота, похожая на кофейную гущу
- мелена (muh-LEE-nuh): стул (какашки) черный, кровавый или похожий на смолу
Как люди заражаются инфекцией
H. pylori ?Люди могут проглотить H.pylori из зараженной пищи, воды или столовой посуды. Инфекции чаще всего встречаются в местах скопления людей, а также в местах, где отсутствует чистая вода или хорошая канализация. Люди также могут передавать бактерии через слюну (слюну) и другие жидкости организма.
Как диагностируется инфекция
H. pylori ? Проблемы, вызываемые инфекциями H. pylori , могут возникать при многих заболеваниях. Чтобы выяснить, есть ли у кого-либо инфекция H. pylori , врачи могут провести различные виды анализов.
Врачи могут:
- Посмотрите на слизистую оболочку желудка. Перед этой процедурой пациенту вводят успокаивающее средство. Затем врач вводит эндоскоп — небольшую гибкую трубку с крошечной камерой на конце — вниз по горлу в желудок и двенадцатиперстную кишку (первая часть тонкой кишки). Врач может взять образцы слизистой оболочки (биопсия), чтобы проверить наличие признаков инфекции и бактерий H. pylori .
- Сделайте анализы крови, чтобы найти H.pylori . Антитела — это белки, которые иммунная система вырабатывает для избавления от микробов. Обычно они остаются в нашем организме на тот случай, если нам снова придется бороться с тем же микробом. Положительный тест может свидетельствовать о прошлом контакте с H. pylori , но не об активной инфекции.
- Проведите дыхательный тест , который может определить углерод, расщепленный H. pylori после того, как пациент выпьет раствор.
 На дыхательные тесты требуется время, они не показывают, насколько серьезна инфекция, и их трудно сделать у маленьких детей.
На дыхательные тесты требуется время, они не показывают, насколько серьезна инфекция, и их трудно сделать у маленьких детей. - Сделайте анализ стула , который может обнаружить белков H. pylori в стуле (фекалиях). Как и в случае с тестом на дыхание, тесты стула не могут показать, насколько серьезна инфекция.
Как лечится инфекция
H. pylori ?Врачи используют антибиотики для лечения инфекций H. pylori . Один антибиотик может не убить бактерии, поэтому врачи часто назначают комбинацию антибиотиков. Чтобы облегчить проблемы с кислотами желудка, врачи обычно также назначают антациды или препараты, подавляющие кислотность.
Лечение антибиотиками излечивает многие случаи гастрита и язвенной болезни, вызванной H. pylori , особенно язвы двенадцатиперстной кишки.
Ребенок с симптомами кровотечения из желудка или тонкой кишки будет лечиться в больнице.
Чем могут помочь родители?
Инфекцию H.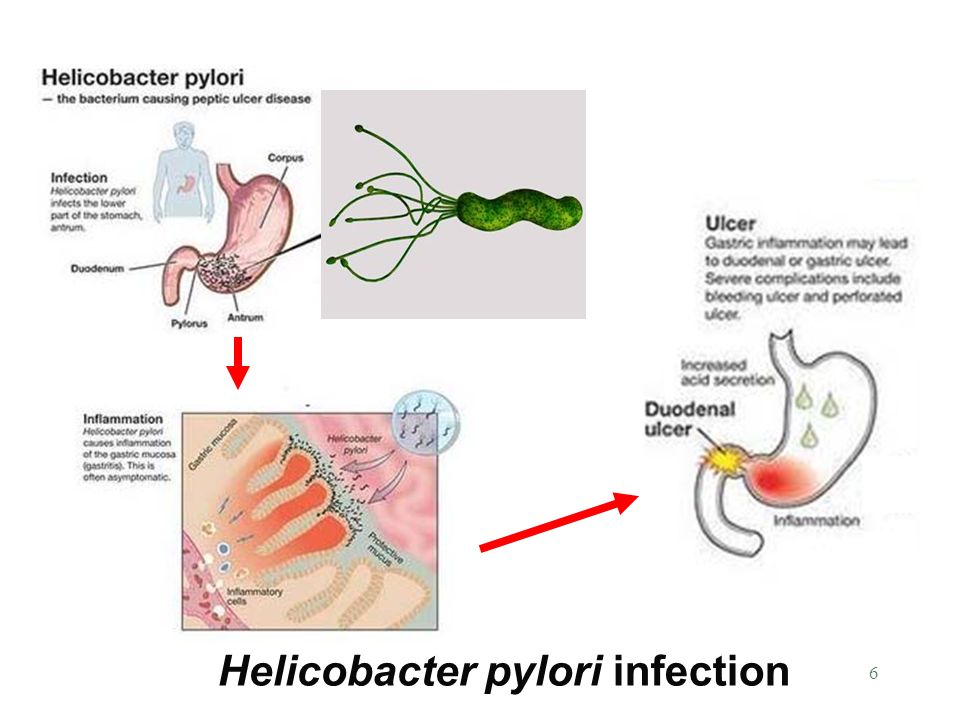 pylori можно вылечить с помощью антибиотиков. Поэтому самое важное, что могут сделать родители, — это давать своему ребенку антибиотик в соответствии с указаниями в течение всего срока, назначенного врачом.
pylori можно вылечить с помощью антибиотиков. Поэтому самое важное, что могут сделать родители, — это давать своему ребенку антибиотик в соответствии с указаниями в течение всего срока, назначенного врачом.
Чтобы облегчить боль в животе, придерживайтесь регулярного графика приема пищи. Планируйте приемы пищи так, чтобы желудок вашего ребенка не оставался пустым в течение длительного времени. Лучше всего есть 5 или 6 небольших приемов пищи каждый день, и вашему ребенку следует отдыхать после каждого приема пищи.
Не давайте ребенку аспирин, аспиринсодержащие препараты, ибупрофен или противовоспалительные препараты. Они могут вызвать раздражение желудка или вызвать желудочное кровотечение.
Можно ли предотвратить инфекцию
H. pylori ?Вакцины против H.pylori . Но эти шаги могут защитить вашу семью от многих болезней и помочь снизить риск заражения H. pylori :
- Мыть руки хорошо и часто, особенно после посещения туалета, а также перед приготовлением или приемом пищи.

- Избегайте еды, если не уверены, что она была приготовлена безопасно.
- Пейте воду из безопасного источника.
Когда мне звонить врачу?
Немедленно позвоните своему врачу, если у вашего ребенка есть какие-либо из этих симптомов:
- Сильная боль в животе
- рвота с кровью или похожая на кофейную гущу
- Кровавые, черные или похожие на смолу какашки
- Продолжительная грызущая или жгучая боль в области под ребрами, которая проходит после еды, питья молока или приема антацидов
Что такое H.Пилори? Симптомы, причины, диагностика, лечение и профилактика
Рекомендуется посещать врача каждый раз, когда у вас возникают необычные боли в желудке или жалобы, особенно если они постоянные или повторяющиеся.
Немедленно обратитесь к врачу, если у вас возникнут следующие симптомы:
- Сильная боль в животе или другая боль в животе
- Не проходит боль в животе или животе
- Затруднения при глотании
- Кровавый, черный или дегтеобразный стул
- Кровавая или похожая на кофейную гущу рвота
 pylori .
pylori .Сначала ваш врач, вероятно, проведет медицинский осмотр и спросит о вашей истории болезни. Затем они могут порекомендовать один или несколько из этих тестов для выявления бактерий.
Анализ крови Может быть проведен анализ крови для выявления антител H. pylori в вашем организме. Хотя анализы крови выполнить легко, они часто не так точны, как другие диагностические подходы. Дыхательный тест Дыхательный тест заключается в проглатывании таблетки, жидкости или пудинга, содержащих углерод.Если у вас инфекция H. pylori , ваш врач сможет обнаружить молекулы углерода, когда вы выдыхаете в мешок.У маленьких детей часто бывает сложно провести дыхательные тесты, и вы не можете принимать определенные лекарства, такие как ингибиторы протонной помпы, антибиотики или пепто-бисмол (субсалицилат висмута), в течение недели или двух до сдачи теста. .
Анализ кала Образец кала может помочь врачам обнаружить белки, которые связаны с H. pylori .Перед прохождением этого теста вам необходимо прекратить прием таких лекарств, как ингибиторы протонной помпы, антибиотики или субсалицилат висмута. Верхняя эндоскопия
pylori .Перед прохождением этого теста вам необходимо прекратить прием таких лекарств, как ингибиторы протонной помпы, антибиотики или субсалицилат висмута. Верхняя эндоскопия Во время верхней эндоскопии ваш врач сначала даст вам легкое успокаивающее средство, а затем продет длинную трубку с крошечной камерой на конце через горло, мимо пищевода и в желудок. Это позволит вашему врачу заглянуть внутрь вашего пищеварительного тракта и при необходимости удалить небольшие кусочки ткани (известные как образцы биопсии).
Если образцы ткани взяты, их можно проанализировать на инфекцию H. pylori . Эндоскопия считается более инвазивной, чем другие методы, такие как анализ кала или дыхательный тест. Следует ли вам проходить обследование на H. pylori? В местах, где высок риск заражения H. pylori , врачи проверяют здоровых людей на наличие бактерий, даже если у них нет признаков или симптомов, что называется медицинским обследованием.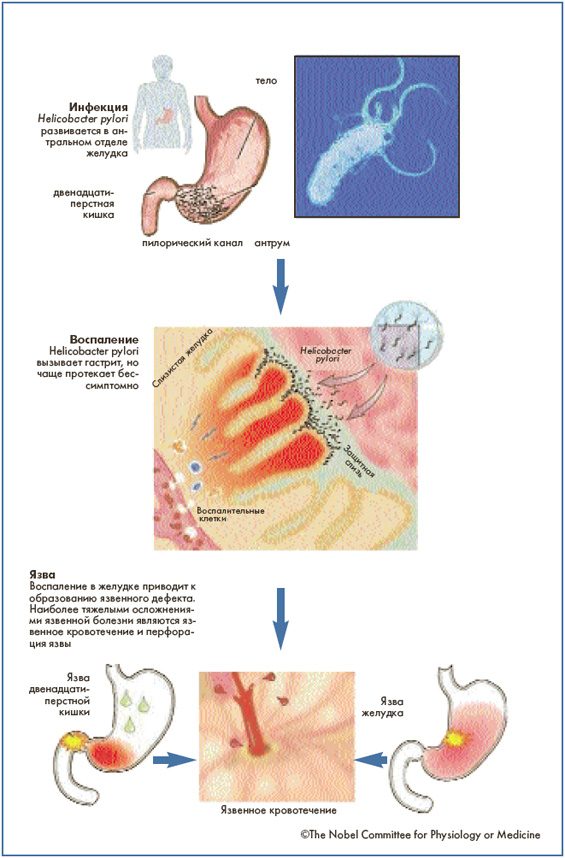 Но в медицинском сообществе ведутся споры о том, полезна ли такая степень скрининга.
Но в медицинском сообществе ведутся споры о том, полезна ли такая степень скрининга.
Многие люди с H. pylori не испытывают никаких симптомов болезни и даже не подозревают, что у них инфекция.
Если у вас действительно есть симптомы или развиваются осложнения, лечение обычно бывает успешным. Инфекцию H. pylori часто можно вылечить с помощью лечения, состоящего из антибиотиков и препаратов, снижающих кислотность.
Хеликобактер пилори | Пациент
Что такое инфекция Helicobacter pylori и кто ею подвержен?
Helicobacter pylori (обычно называемый H. pylori ) — это микроб (бактерия). Он может инфицировать слизистую оболочку желудка и двенадцатиперстной кишки (первый отдел кишечника). Он есть у более половины населения мира. Это чаще встречается в развивающихся странах.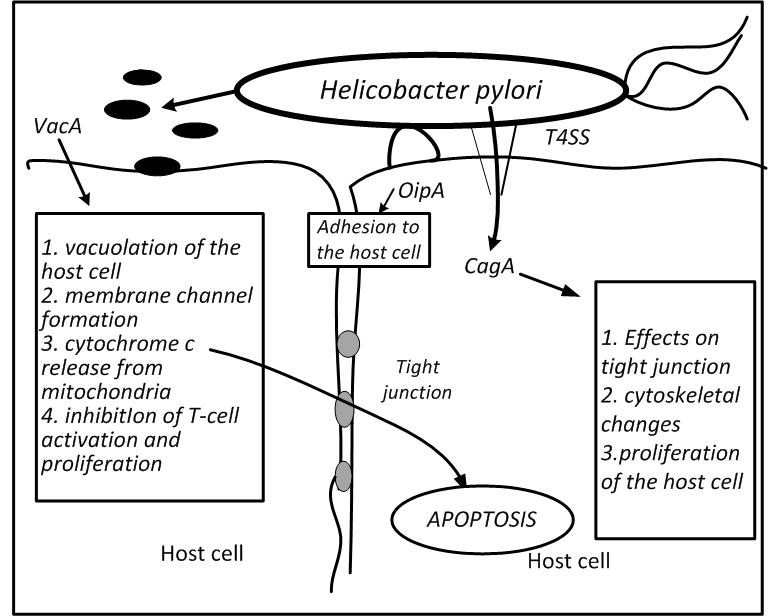 Почему и когда люди заражаются, неизвестно. Иногда он присутствует у детей, и некоторые ученые считают, что мы приобретаем его в очень раннем возрасте.Примерно 15 из 100 человек инфицированы в Великобритании, и со временем это становится все реже. После заражения, если не лечить, инфекция обычно сохраняется на всю оставшуюся жизнь.
Почему и когда люди заражаются, неизвестно. Иногда он присутствует у детей, и некоторые ученые считают, что мы приобретаем его в очень раннем возрасте.Примерно 15 из 100 человек инфицированы в Великобритании, и со временем это становится все реже. После заражения, если не лечить, инфекция обычно сохраняется на всю оставшуюся жизнь.
Кого следует обследовать на Helicobacter pylori и лечить, если он обнаружен?
Если у вас повторяющиеся симптомы несварения желудка (повторяющаяся диспепсия)
Если у вас повторяющаяся диспепсия (диспепсия, которая проходит, а затем возвращается снова), обычно перед выполнением любых других тестов проводят тест на H. pylori .При обнаружении H. pylori часто назначается эрадикационная терапия. Точный диагноз может быть неизвестен. Например, может быть неясно, вызвана ли диспепсия язвой двенадцатиперстной кишки, желудка или неязвенной диспепсией. Это можно подтвердить, только заглянув в кишечник с помощью теста, называемого гастроскопией (эндоскопией). Однако, если симптомы исчезнут после лечения H. pylori , это конец. Вам не нужны дополнительные анализы, такие как гастроскопия. Вы не будете точно знать, что вызвало симптомы, но это не имеет значения, если симптомы исчезли.
Однако, если симптомы исчезнут после лечения H. pylori , это конец. Вам не нужны дополнительные анализы, такие как гастроскопия. Вы не будете точно знать, что вызвало симптомы, но это не имеет значения, если симптомы исчезли.
Другие причины для тестирования
Если вы относитесь к одной из следующих групп, вам могут предложить тест на H. pylori и предложить лечение с помощью эрадикационной терапии, если она будет обнаружена. Если вы:
- У вас язва двенадцатиперстной кишки или желудка. Эрадикационная терапия обычно излечивает язву.
- Есть неязвенная диспепсия. Эрадикационная терапия может помочь и устранить симптомы, но в большинстве случаев это не так.
- Иметь родственника первой степени родства (мать, отец, брат, сестра или ребенок), у которого был диагностирован рак желудка.Рекомендуется лечение, даже если у вас нет никаких симптомов. Цель состоит в том, чтобы снизить риск рака желудка в будущем.
- Принимаете или собираетесь принимать долгосрочные противовоспалительные препараты, такие как ибупрофен, диклофенак, аспирин и т.
 Д. Комбинация этих лекарств и H. pylori увеличивает риск развития язвы желудка.
Д. Комбинация этих лекарств и H. pylori увеличивает риск развития язвы желудка. - Есть МАЛТОМА.
- Воспаление слизистой оболочки желудка (атрофический гастрит).
- Перенесли операцию по удалению рака желудка.
- У вас необъяснимая железодефицитная анемия.
- Есть состояние, называемое хронической идиопатической тромбоцитопенической пурпурой. Это необычное заболевание крови, при котором количество тромбоцитов в крови становится очень низким. Некоторые исследования предполагают возможную связь между инфекцией H. pylori и этим заболеванием.
Какие проблемы вызывает Helicobacter pylori?
Обычно проблем нет
Большинство людей инфицированы H.pylori не имеют симптомов или проблем, вызванных инфекцией. Эти люди не знают, что они инфицированы. Некоторые из микробов (бактерий) H. pylori могут просто безвредно жить в слизистой оболочке желудка и двенадцатиперстной кишки.
Язвы желудка и двенадцатиперстной кишки
H.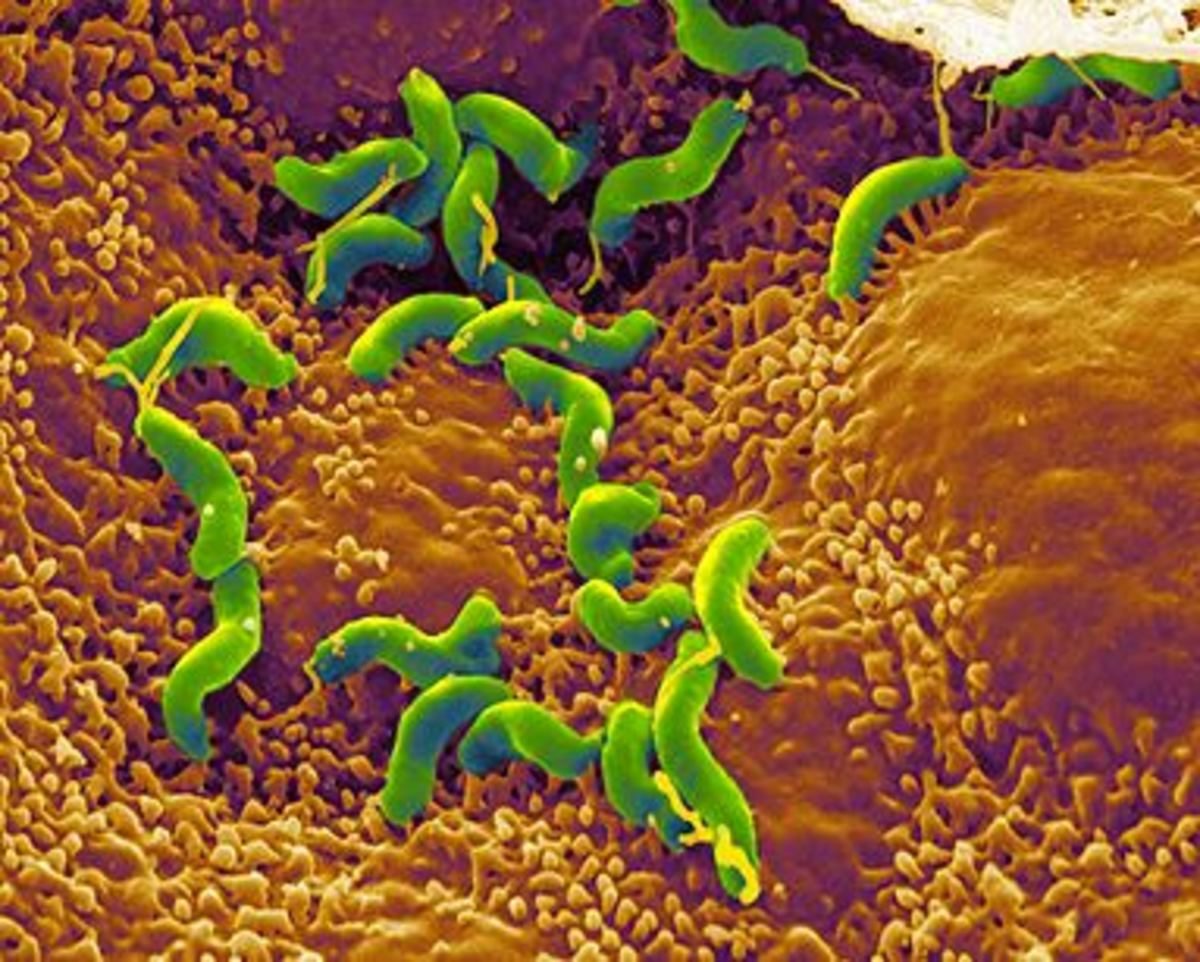 pylori является наиболее частой причиной язв двенадцатиперстной кишки и желудка (язвы желудка). Примерно у 3 из 20 человек, инфицированных H. pylori , развивается язва. Язва возникает, когда слизистая оболочка желудка или двенадцатиперстной кишки повреждается кислотой, вырабатываемой в желудке, и обнажается подлежащая ткань.
pylori является наиболее частой причиной язв двенадцатиперстной кишки и желудка (язвы желудка). Примерно у 3 из 20 человек, инфицированных H. pylori , развивается язва. Язва возникает, когда слизистая оболочка желудка или двенадцатиперстной кишки повреждается кислотой, вырабатываемой в желудке, и обнажается подлежащая ткань.
У некоторых людей H. pylori вызывает воспаление слизистой оболочки желудка или двенадцатиперстной кишки. Это называется гастритом и может привести к другим состояниям, таким как дефицит витамина B12. При гастрите слизистый защитный барьер каким-то образом нарушается (а в некоторых случаях увеличивается количество кислоты). Похоже, это позволяет кислоте вызывать воспаление и язвы.
Неязвенная диспепсия
Это состояние, при котором у вас периодически возникают приступы несварения желудка (диспепсия), которые не вызваны язвой или воспалением.Иногда это называют функциональной диспепсией. H. pylori иногда встречается у людей с неязвенной диспепсией.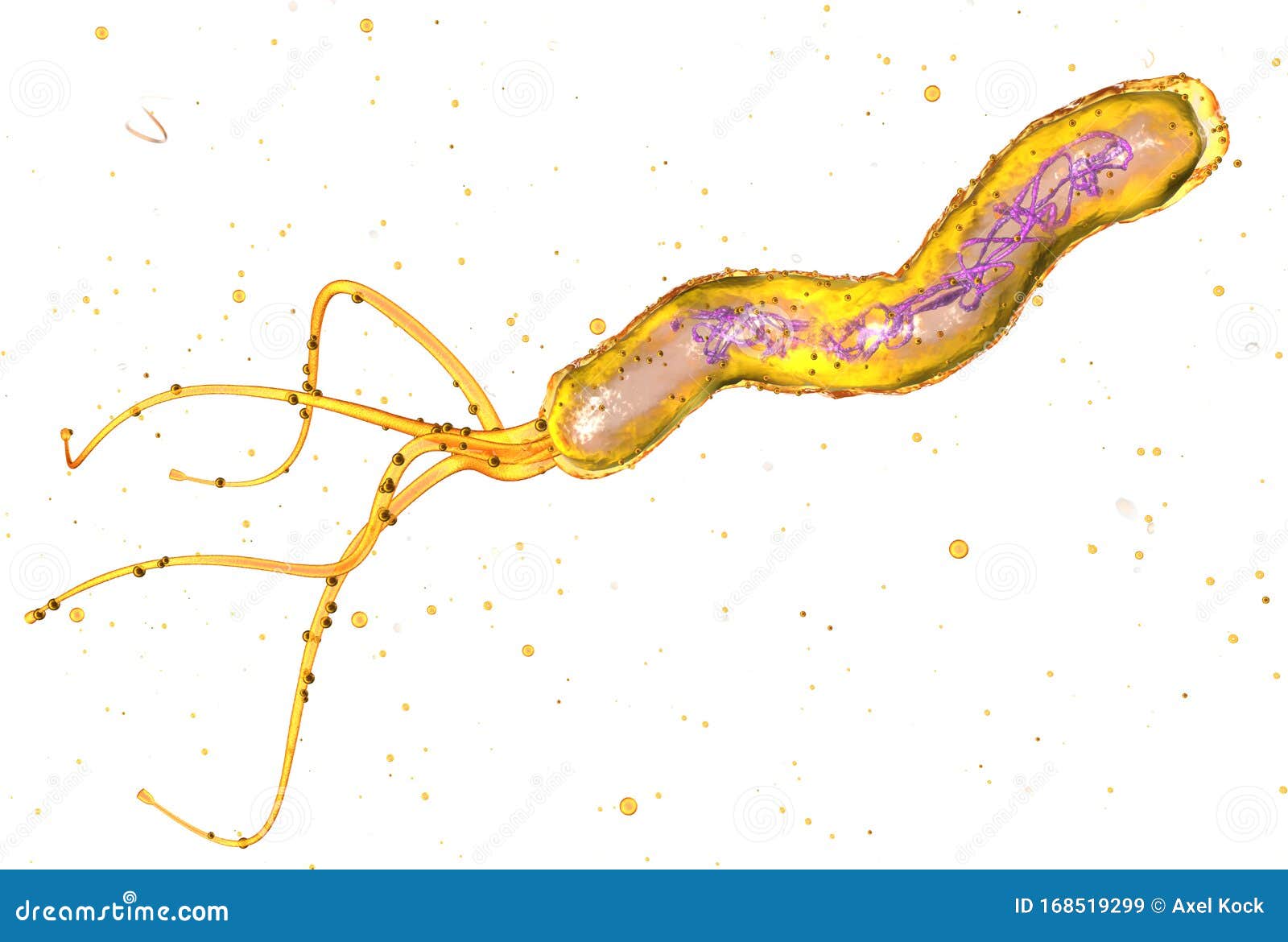 Избавление от H. pylori излечивает некоторые случаи, но в большинстве случаев ничего не меняет. Причина большинства случаев неязвенной диспепсии неизвестна.
Избавление от H. pylori излечивает некоторые случаи, но в большинстве случаев ничего не меняет. Причина большинства случаев неязвенной диспепсии неизвестна.
Рак желудка
Считается, что риск развития рака желудка повышается при длительном инфицировании H. pylori . Однако следует подчеркнуть, что подавляющее большинство людей с H.pylori не болеют раком желудка. Повышенный риск невелик. Ваш риск может быть выше, если у вас есть H. pylori в дополнение к тому, что у вас есть родственник первой степени (мать, отец, брат, сестра или ребенок), у которого был диагностирован рак желудка.
Лимфома лимфоидной ткани, ассоциированная со слизистой оболочкой желудка — a MALToma
Это редкий и необычный тип рака желудка. Считается, что инфекция H. pylori играет определенную роль в развитии этого состояния.
Как диагностируется Helicobacter pylori?
Различные тесты могут обнаружить H.pylori :
- Дыхательный тест может подтвердить, что у вас инфекция H.
 pylori . Образец вашего дыхания анализируется после того, как вы выпьете особый напиток. Примечание : перед этим тестом вы не должны были принимать какие-либо антибиотики в течение как минимум четырех недель. Кроме того, вам не следует принимать ингибитор протонной помпы (ИПП) или антагонист рецепторов H 2 в течение как минимум двух недель. (Это препараты, подавляющие кислотность.) Кроме того, вы не должны ничего есть в течение шести часов до теста.Причина этих правил в том, что лекарства и еда могут повлиять на результат теста.
pylori . Образец вашего дыхания анализируется после того, как вы выпьете особый напиток. Примечание : перед этим тестом вы не должны были принимать какие-либо антибиотики в течение как минимум четырех недель. Кроме того, вам не следует принимать ингибитор протонной помпы (ИПП) или антагонист рецепторов H 2 в течение как минимум двух недель. (Это препараты, подавляющие кислотность.) Кроме того, вы не должны ничего есть в течение шести часов до теста.Причина этих правил в том, что лекарства и еда могут повлиять на результат теста. - Альтернативным тестом является анализ стула на антиген. В этом тесте вы даете образец стула (фекалий) размером с горошину, который проверяется на H. pylori . Примечание : перед этим тестом вы не должны были принимать какие-либо антибиотики в течение как минимум четырех недель. Кроме того, вам не следует принимать лекарство, подавляющее кислоту антагониста рецепторов PPI или H 2 , в течение как минимум двух недель.

- В анализе крови можно обнаружить антитела к H.pylori . Иногда это используется для подтверждения того, что вы инфицированы или были инфицированы H. pylori . Однако может пройти год, прежде чем этот тест станет отрицательным после того, как инфекция исчезнет. Таким образом, бесполезно подтверждать, устранило ли лечение инфекцию (если это необходимо знать). При необходимости, дыхательный тест или тест на антиген в стуле обычно используются, чтобы проверить, исчезла ли инфекция после лечения.
- Иногда берут небольшой образец (биопсию) слизистой оболочки желудка, если у вас гастроскопия (эндоскопия).Образец можно протестировать на H. pylori .
Как Helicobacter pylori выводится из желудка и двенадцатиперстной кишки?
H. pylori убивается некоторыми антибиотиками. Однако для полного избавления от него требуется комбинация лекарств. Это называется комбинированной терапией, хотя, поскольку она избавляет (уничтожает) микробы, ее также называют эрадикационной терапией. Вам нужно принимать два антибиотика одновременно. Кроме того, нужно принимать лекарство, снижающее кислотность желудка.Это позволяет антибиотикам хорошо работать в желудке. Вам нужно принимать эрадикационную терапию в течение недели. Важно принимать все лекарства точно так, как указано, и пройти полный курс.
Вам нужно принимать два антибиотика одновременно. Кроме того, нужно принимать лекарство, снижающее кислотность желудка.Это позволяет антибиотикам хорошо работать в желудке. Вам нужно принимать эрадикационную терапию в течение недели. Важно принимать все лекарства точно так, как указано, и пройти полный курс.
Эрадикационная терапия устраняет H. pylori в 9 из 10 случаев при правильном проведении полного курса . Если вы не пройдете полный курс, вероятность излечения инфекции снижается. Второй курс эрадикационной терапии с использованием других антибиотиков обычно эффективен, если первый курс не избавляет от инфекции.
Эрадикационную терапию иногда называют тройной терапией, поскольку она включает три лекарства — два антибиотика и лекарство, подавляющее кислотность.
Последующее наблюдение
Если у вас расстройство желудка (диспепсия), обычно необходимо только проверить, исчез ли H. pylori , если симптомы вернутся после лечения.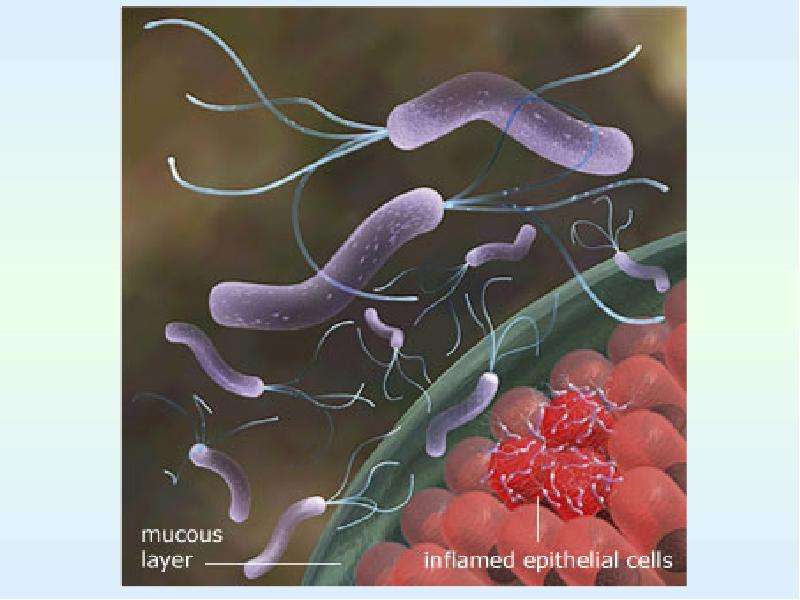 Если у вас язва желудка или двенадцатиперстной кишки, тестирование обычно проводится через 6-8 недель после лечения.
Если у вас язва желудка или двенадцатиперстной кишки, тестирование обычно проводится через 6-8 недель после лечения.
Есть ли побочные эффекты у эрадикационной терапии?
Примерно у 3 из 10 человек развиваются побочные эффекты при эрадикационной терапии.К ним относятся расстройство желудка (диспепсия), плохое самочувствие (тошнота), диарея и головные боли. Однако стоит продолжить полный курс, если побочные эффекты не так уж и велики. Может быть рекомендован переход на другой набор лекарств, если первая комбинация не устраняет H. pylori , или если она вызвала серьезные побочные эффекты, и вам пришлось прекратить ее прием.
Helicobacter Pylori — Здоровье детей округа Ориндж
Что вызывает инфекцию H. pylori?
Исследователи не знают, что заставляет людей развивать H.pylori . Считается, что H. pylori передается перорально от человека к человеку при тесном или фекально-оральном контакте. Большинство людей впервые сталкиваются с ним в детстве.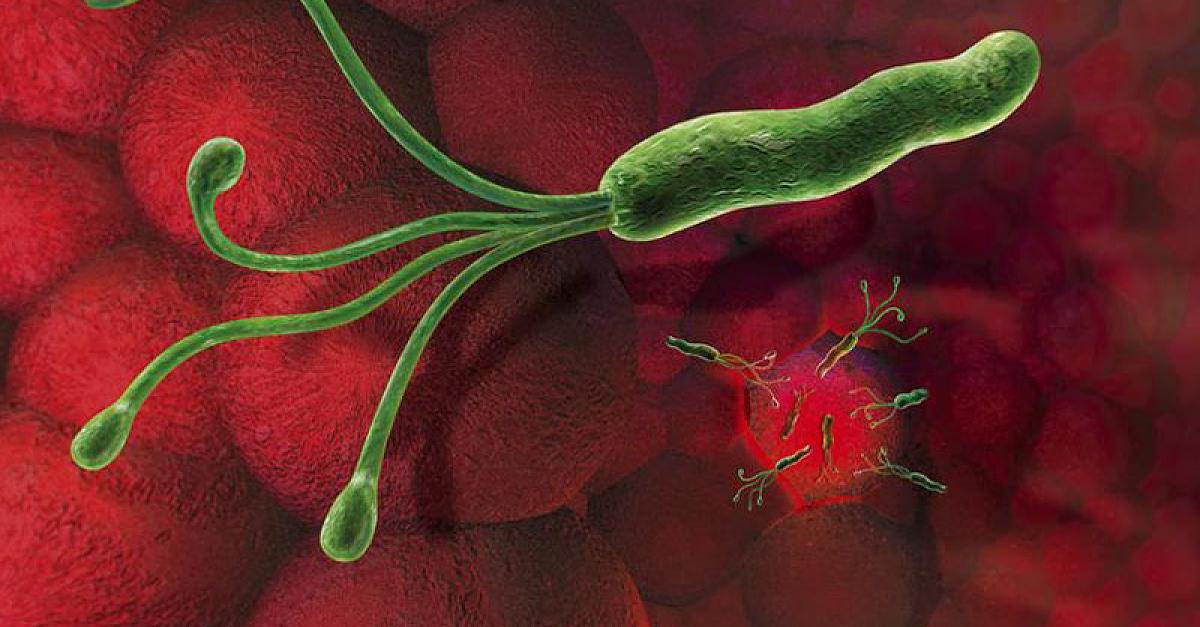
Каковы симптомы H. pylori?
После заражения H. pylori может развиться гастрит (воспаление слизистой оболочки желудка). Однако у большинства людей никогда не будет симптомов или проблем, связанных с инфекцией. При наличии симптомов они могут включать следующее:
- Дискомфорт в животе, который:
— вызывает тупую, грызущую боль
— возникает через два-три часа после еды
— приходит и уходит в течение нескольких дней или недель
— возникает посреди ночи при пустом желудке
— Есть облегчение от еды или приема антацидов. - Тошнота
- Рвота
- отрыжка
- Вздутие живота
- Потеря аппетита
- Похудание.
Симптомы H. pylori могут выглядеть как другие заболевания или проблемы со здоровьем. Если ваш ребенок испытывает эти симптомы, важно записаться на прием к детскому гастроэнтерологу.
Как диагностируется
H. pylori ?В дополнение к полной истории болезни и физическому осмотру врач ребенка может запросить другие анализы, в том числе:
- Анализы крови.
 Эти тесты выявляют антитела, указывающие на присутствие бактерии. Узнайте больше о анализах крови в CHOC.
Эти тесты выявляют антитела, указывающие на присутствие бактерии. Узнайте больше о анализах крови в CHOC. - Тест стула. Этот тест выявляет признаки бактерии в стуле и является более чувствительным и специфичным, чем анализ крови. Узнайте больше о тестах стула.
- Дыхательные пробы. Этот тест определяет, присутствует ли углерод после питья раствора, содержащего мочевину. Присутствие углерода указывает на высвобождение уреазы H.пилори.
- Тканевые тесты. Ткань удалена во время эндоскопии. Эндоскопия или EGD — это процедура, которая позволяет врачу исследовать пищевод, желудок и двенадцатиперстную кишку изнутри. Тонкая гибкая трубка с подсветкой, называемая эндоскопом, вводится в рот и горло, затем в пищевод, желудок и двенадцатиперстную кишку. Эндоскоп позволяет врачу осматривать эту область тела изнутри, а также вводить инструменты через прицел для взятия образца ткани для биопсии (при необходимости).
 Эта ткань используется для:
Эта ткань используется для:
— определения присутствия фермента уреазы
— исследования присутствующих бактерий под микроскопом
— запуска теста на культуру для выращивания большего количества бактерий для исследования.
Подробнее об эндоскопии.
Как лечить
H. pylori ?В CHOC наша команда гастроэнтерологов встречается с каждым пациентом, его или ее семьей и другими членами медицинской бригады ребенка, включая направляющих врачей и специалистов, для создания плана лечения, учитывающего медицинское, физическое, социальное и эмоциональное благополучие пациента. -существование.Специальное лечение обычно основано на:
- Возраст ребенка, общее состояние здоровья и история болезни
- Степень заболевания
- Переносимость ребенком определенных лекарств, процедур или методов лечения
- Ожидания от течения болезни.
Лечение может включать:
- Лекарства, подавляющие выработку кислоты, в том числе:
— h3-адреноблокаторы. Они уменьшают количество кислоты, которую производит желудок, блокируя гистамин, мощный стимулятор секреции кислоты.
Они уменьшают количество кислоты, которую производит желудок, блокируя гистамин, мощный стимулятор секреции кислоты.
— Ингибиторы протонной помпы. Они более полно блокируют выработку кислоты в желудке, останавливая кислотный насос желудка, который является последним этапом секреции кислоты.
— Протекторы слизистой оболочки желудка. Защищают слизистую оболочку желудка от кислоты и помогают убить бактерии. - Антибиотики для уничтожения бактерий.
Инфекция Helicobacter pylori и кожные заболевания
Автор: д-р Юджин Тан, регистратор дерматологии, больница Вайкато, Гамильтон, Новая Зеландия, 2009 г.
Что такое хеликобактер пилори?
Helicobacter pylori ( H. pylori ) — это бактерии, обнаруженные в желудке, которые вызывают большинство случаев язвенной болезни. Около половины населения мира имеют бактерии, что делает их наиболее распространенной бактериальной инфекцией у людей [1].
Инфекция H. pylori чаще встречается в развивающихся странах. Риск заражения H. pylori связан с социально-экономическим статусом и плохими условиями жизни, такими как перенаселенность, отсутствие чистой проточной воды и большее количество братьев и сестер.В результате большинство детей в развивающихся странах инфицированы в возрасте до 10 лет.
В Новой Зеландии распространенность инфекции выше среди маори и полинезийцев. Исследования показывают, что около 5% европейских детей заражаются H. pylori в возрасте 20 лет, в отличие от 50% полинезийских детей [2].
Точный путь заражения остается неизвестным, но наиболее вероятной причиной является передача от человека к человеку через оральное / оральное или фекальное / оральное воздействие. Такие действия, как совместное использование еды, столовых приборов или несоблюдение гигиены туалета, могут привести к передаче H.pylori другому человеку.
Какие заболевания связаны с инфекцией
H. pylori ?
pylori ?H. pylori вызывает прямое заболевание желудка. Другие состояния, вероятно, связаны с иммунным ответом организма на бактерии.
- Хронический гастрит (воспаление слизистой оболочки желудка)
- Язвенная болезнь
- Рак желудка
- Некоторые виды лимфом (рак лимфоидной ткани)
Каковы симптомы H.pylori?
У большинства людей с инфекцией H. pylori симптомы отсутствуют. Симптомы возникают, если инфицирование H. pylori вызывает язвенную болезнь желудка или гастрит. Эти симптомы могут быть неспецифическими и включать:
- Боль в животе (обычно в верхней части живота)
- Тошнота
- Рвота
- Вздутие живота
- Стул красного или смолистого цвета (указывает на кишечное кровотечение)
- Низкий показатель крови (анемия).
Как H. pylori повреждает желудок?
Повреждение слизистой оболочки желудка происходит из-за сложного взаимодействия бактерий и иммунного ответа хозяина.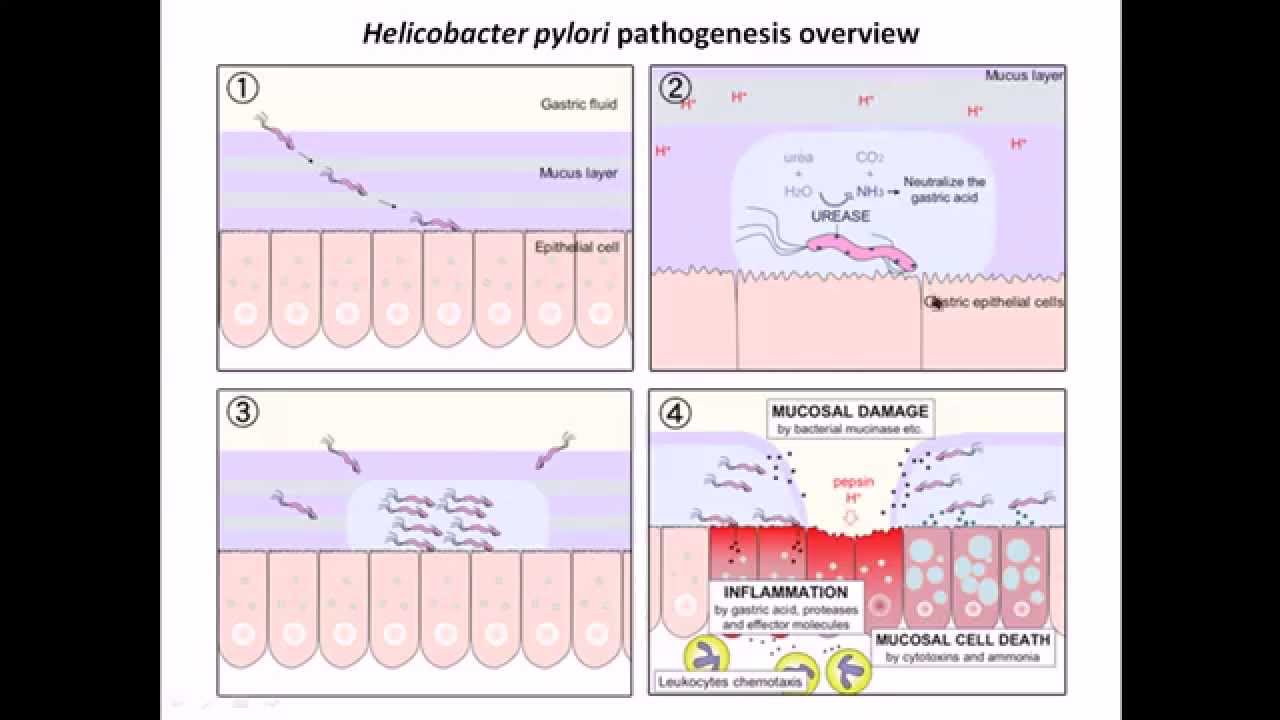 H. pylori выделяет несколько ферментов и микробных продуктов, которые непосредственно повреждают слизистую оболочку желудка. Иммунная система реагирует, вызывая бурную воспалительную реакцию в попытке уничтожить бактерии. В результате этой воспалительной реакции происходит непреднамеренное повреждение слизистой оболочки желудка.
H. pylori выделяет несколько ферментов и микробных продуктов, которые непосредственно повреждают слизистую оболочку желудка. Иммунная система реагирует, вызывая бурную воспалительную реакцию в попытке уничтожить бактерии. В результате этой воспалительной реакции происходит непреднамеренное повреждение слизистой оболочки желудка.
Какие исследования проводятся на H. pylori?
Существует несколько тестов для обнаружения присутствия H. pylori в желудке:
- Анализ крови — выявляет специфические антитела против бактерии H. pylori .
- Дыхательный тест — включает в себя питье раствора карбамида, меченного углеродом. Этот раствор расщепляется на H. pylori, , и продукты его распада можно обнаружить в дыхании.
- Тест стула — обнаруживает H.pylori в фекалиях.
- Эндоскопическое исследование — включает использование оптических инструментов для визуального осмотра внутренних частей тела. Гибкая трубка вводится через рот в желудок и верхние отделы тонкой кишки.
 Небольшие образцы ткани могут быть взяты из стенки желудка, которые затем проверены на H. pylori .
Небольшие образцы ткани могут быть взяты из стенки желудка, которые затем проверены на H. pylori .
Анализ крови и дыхательный тест часто являются первым подходом к тестированию на H. pylori .Эндоскопическая биопсия — относительно инвазивная процедура, которую часто проводят пациенты, которым требуется эндоскопия по другой причине.
Кого следует тестировать?
Американский колледж гастроэнтерологии рекомендует тестирование в следующих ситуациях [3]:
- Пациенты с активной язвенной болезнью
- История документально подтвержденной язвенной болезни
- Лимфома желудочного солода (лимфоидной ткани, связанной со слизистой оболочкой)
- Пациенты, перенесшие резекцию рака желудка на ранней стадии.
Тестирование не рекомендуется людям с бессимптомным течением (без симптомов) или без язвенной болезни в анамнезе. Однако определенные группы населения, которые подвержены риску развития язвы или рака желудка, могут быть рассмотрены для бессимптомного тестирования.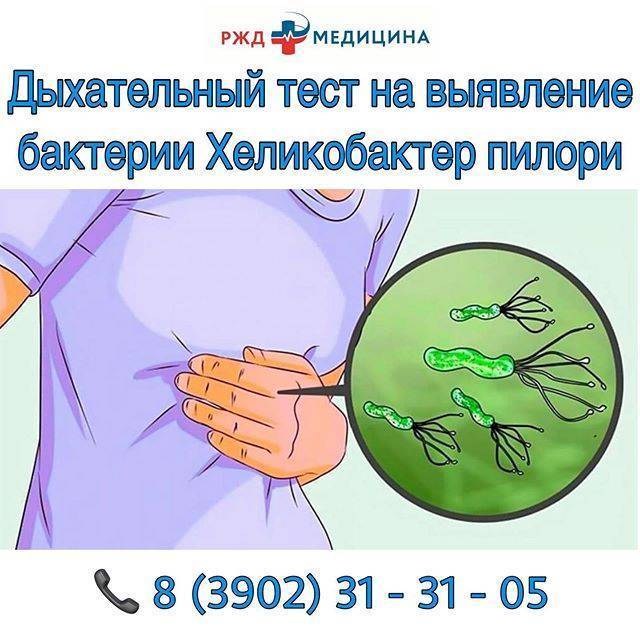
Что такое лечение?
Лечение инфекции H. pylori включает прием нескольких лекарств в течение 7–14 дней («тройная терапия»), например, ингибитора протонной помпы (ингибитор секреции желудочной кислоты), такого как омепразол 40 мг один раз в день, амоксициллин 1 г два раза в день и кларитромицин 500 мг два раза в день.
Лечение излечивает до 90% людей.
Какая связь между H. pylori и кожными заболеваниями?
H. pylori были причастны к множеству заболеваний, не связанных с желудочно-кишечным трактом. Кожа является примером, и несколько исследований предположили связь со следующими состояниями [4,5]:
Влияет ли лечение H. pylori на кожные заболевания?
Несколько небольших исследований показали, что искоренение H.pylori имеет положительный результат при некоторых кожных заболеваниях, таких как крапивница, болезнь Бехчета, красный плоский лишай, атопический дерматит, болезнь Свита и системный склероз. Условия, которые могут не принести пользу, — это псориаз и розацеа.
Условия, которые могут не принести пользу, — это псориаз и розацеа.
Эти исследования не являются рандомизированными и включают небольшое количество пациентов, поэтому в настоящее время нельзя сделать окончательного вывода об эрадикации H. pylori при кожных заболеваниях.
Каталожные номера
- Обложка TL, Blaser MJ.Helicobacter pylori в здоровье и болезни. Гастроэнтерология 2009; 136: 1863-73. Медлайн.
- Fraser A. Helicobacter pylori: историческая перспектива 1983–2003 гг. N Z Med J 2004; 117: 1194. U896. Полный текст.
- Chey WD, Вонг, Британская Колумбия. Руководство Американского колледжа гастроэнтерологии по лечению инфекции Helicobacter pylori. Am J Gastroenterol 2007; 102: 1808-25. Медлайн.
- Hernando-Harder AC, Booken N, Goerdt S. et al. Инфекция Helicobacter pylori и дерматологические заболевания.Eur J Dermatol 2009. Medline.
- Wedi B, Kapp A. Инфекция Helicobacter pylori при кожных заболеваниях: критическая оценка.
 Am J Clin Dermatol 2002; 3: 273-82. Медлайн.
Am J Clin Dermatol 2002; 3: 273-82. Медлайн.
В DermNet NZ
Другие веб-сайты
Книги о кожных заболеваниях
См. Книжный магазин DermNet NZ.
Обновленная информация о Helicobacter pylori как причине рака желудка — FullText — Опухоли желудочно-кишечного тракта 2014, Vol. 1, № 3
Абстрактные
Справочная информация: Рак желудка является второй по частоте причиной смерти от рака во всем мире.Подавляющее большинство рака желудка — это рак, связанный с воспалением, вызванный инфицированием Helicobacter pylori . Окислительный стресс, индуцированный H. pylori , повреждает ДНК, что приводит к генетической нестабильности. Кроме того, сам по себе H. pylori может вызывать повреждение ДНК и эпигенетические изменения, которые вызывают генетическую нестабильность и неопластическую трансформацию. Резюме: Штамм-специфичные компоненты H. pylori действуют в сочетании с факторами хозяина и факторами окружающей среды и питания, значительно усиливая воспалительную реакцию и, следовательно, риск рака.Вариации нескольких ключевых факторов, таких как остров патогенности cag и белок VacA, могут вызывать более выраженный воспалительный ответ в клетках-хозяевах. Генетический полиморфизм в организме хозяина, такой как ген IL-1β, и хромосомы 9p21.3 и 10q23 также играют важную роль. Наконец, диета является основным внешним фактором, регулирующим риск рака желудка. Ключевое сообщение: Большинство видов рака желудка связаны с воспалением, вызванным инфекцией H.pylori . Ликвидация H. pylori важна для профилактики и лечения рака желудка. Практическое значение: Эрадикация H. pylori приводит к излечению гастрита и предотвращению дальнейшего генетического повреждения, вызванного H. pylori . Искоренение H. pylori до развития атрофического гастрита может предотвратить развитие рака желудка.
pylori действуют в сочетании с факторами хозяина и факторами окружающей среды и питания, значительно усиливая воспалительную реакцию и, следовательно, риск рака.Вариации нескольких ключевых факторов, таких как остров патогенности cag и белок VacA, могут вызывать более выраженный воспалительный ответ в клетках-хозяевах. Генетический полиморфизм в организме хозяина, такой как ген IL-1β, и хромосомы 9p21.3 и 10q23 также играют важную роль. Наконец, диета является основным внешним фактором, регулирующим риск рака желудка. Ключевое сообщение: Большинство видов рака желудка связаны с воспалением, вызванным инфекцией H.pylori . Ликвидация H. pylori важна для профилактики и лечения рака желудка. Практическое значение: Эрадикация H. pylori приводит к излечению гастрита и предотвращению дальнейшего генетического повреждения, вызванного H. pylori . Искоренение H. pylori до развития атрофического гастрита может предотвратить развитие рака желудка. Япония предприняла общенациональную программу по выявлению и ликвидации H.pylori , а также наблюдение за теми, кто подвергся эрадикации H. pylori слишком поздно, чтобы исключить риск рака. Уничтожение H. pylori в масштабах всего населения приведет к тому, что рак желудка станет исчезающе редким заболеванием.
Япония предприняла общенациональную программу по выявлению и ликвидации H.pylori , а также наблюдение за теми, кто подвергся эрадикации H. pylori слишком поздно, чтобы исключить риск рака. Уничтожение H. pylori в масштабах всего населения приведет к тому, что рак желудка станет исчезающе редким заболеванием.
© 2014 S. Karger AG, Базель
Введение
Helicobacter pylori — это микроаэрофильный грамотрицательный спиральный бактериальный патоген, который поражает более 50% мирового населения [1].Инфекция H. pylori обычно передается в детстве и сохраняется на всю жизнь [2]. Как и при многих хронических инфекциях, у большинства людей симптомы отсутствуют, и лишь у небольшой части пациентов развивается клиническое заболевание. H. pylori считается патогеном, поскольку он повсеместно вызывает прогрессирующее воспаление и повреждение слизистой оболочки желудка. Первичные клинические проявления инфекции со стороны желудочно-кишечного тракта — язвенная болезнь и рак желудка [3,4]. На протяжении более 100 лет было признано, что атрофический гастрит тесно связан с раком желудка.Открытие H. pylori в начале 1980-х позволило идентифицировать причину хронического воспаления слизистой оболочки желудка и, таким образом, основную причину рака желудка [5,6]. В 1994 г. H. pylori был объявлен канцерогеном класса I (определенный) для человека [7], и эта классификация была подтверждена в 2012 г. [8]. В настоящее время рак желудка сгруппирован среди опухолей, связанных с воспалением, с H. pylori как необходимой, но недостаточной причиной.
Первичные клинические проявления инфекции со стороны желудочно-кишечного тракта — язвенная болезнь и рак желудка [3,4]. На протяжении более 100 лет было признано, что атрофический гастрит тесно связан с раком желудка.Открытие H. pylori в начале 1980-х позволило идентифицировать причину хронического воспаления слизистой оболочки желудка и, таким образом, основную причину рака желудка [5,6]. В 1994 г. H. pylori был объявлен канцерогеном класса I (определенный) для человека [7], и эта классификация была подтверждена в 2012 г. [8]. В настоящее время рак желудка сгруппирован среди опухолей, связанных с воспалением, с H. pylori как необходимой, но недостаточной причиной.
Рак желудка
На рак желудка приходится примерно 10% всех онкологических заболеваний во всем мире.Это четвертый по распространенности рак и вторая по значимости причина смерти от рака. Во всем мире наблюдается неуклонное снижение как заболеваемости, так и смертности от рака желудка [9]. Частично это снижение связано с падением распространенности H. pylori , связанным с улучшением санитарии и уровня жизни, что в совокупности снизило скорость заражения инфекцией. Также наблюдалось снижение заболеваемости раком желудка среди инфицированных людей, связанное с изменениями окружающей среды, особенно с улучшением питания (т.е., охлаждение вместо соления и копчения для сохранения продуктов питания и улучшенная транспортировка, в результате чего свежие продукты доступны в течение всего года).
Частично это снижение связано с падением распространенности H. pylori , связанным с улучшением санитарии и уровня жизни, что в совокупности снизило скорость заражения инфекцией. Также наблюдалось снижение заболеваемости раком желудка среди инфицированных людей, связанное с изменениями окружающей среды, особенно с улучшением питания (т.е., охлаждение вместо соления и копчения для сохранения продуктов питания и улучшенная транспортировка, в результате чего свежие продукты доступны в течение всего года).
Рак в основном является результатом генетической нестабильности. Небольшая часть рака желудка является наследственной и связана с наследственными генетическими аномалиями, которые включают изменения в генах-супрессорах опухолей, протоонкогенах, генах-привратниках, ферментах, факторах роста и мембранных или ядерных рецепторах [10].Многие виды рака, включая рак желудка, возникают в результате хронического воспаления [11]. Хроническая инфекция H. pylori вызывает пожизненное острое и хроническое воспаление желудка, которое может привести к повреждению ДНК и генетической нестабильности [12]. Недавно было обнаружено, что организм H. pylori может также вызывать генетическую нестабильность, включая разрывы двухцепочечной ДНК, и может вызывать активацию генов и подавление активности посредством эпигенетических путей [13]. Патогенез генетической нестабильности, связанной с H. pylori , сложен и еще не полностью изучен, при этом важную роль играют как активные формы кислорода, вызванные воспалением, так и активные формы азота [14] (рис.1).
Хроническая инфекция H. pylori вызывает пожизненное острое и хроническое воспаление желудка, которое может привести к повреждению ДНК и генетической нестабильности [12]. Недавно было обнаружено, что организм H. pylori может также вызывать генетическую нестабильность, включая разрывы двухцепочечной ДНК, и может вызывать активацию генов и подавление активности посредством эпигенетических путей [13]. Патогенез генетической нестабильности, связанной с H. pylori , сложен и еще не полностью изучен, при этом важную роль играют как активные формы кислорода, вызванные воспалением, так и активные формы азота [14] (рис.1).
Рис. 1
Схема развития рака желудка кишечного типа. Из ссылки [13], с разрешения. ROS = активные формы кислорода.
Хотя H. pylori вызывает пожизненное воспаление слизистой оболочки желудка, рак желудка не является предопределенным исходом. Клинические проявления инфекции варьируются в зависимости от региона: важный хозяин, штамм H.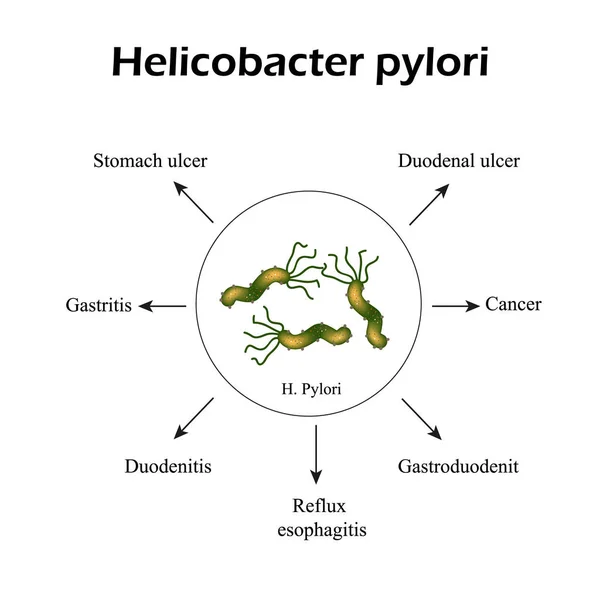 pylori и факторы окружающей среды взаимодействуют, чтобы определить исход для конкретного пациента и региона.Поскольку H. pylori является необходимой причиной рака желудка, высокая частота рака желудка требует высокой распространенности H. pylori . Однако даже среди обществ с высоким уровнем распространенности H. pylori , таких как Китай, существуют сильные географические различия в заболеваемости раком желудка. Наиболее важным фактором, который в настоящее время признан важным в H. pylori — взаимодействиях с окружающей средой, приводящих к раку желудка, является диета (т. Е. Риск рака наиболее высок в регионах с сезонным питанием, где свежие фрукты и овощи отсутствуют в течение длительного времени и где соль и курение являются основными методами консервирования пищевых продуктов) [15].
pylori и факторы окружающей среды взаимодействуют, чтобы определить исход для конкретного пациента и региона.Поскольку H. pylori является необходимой причиной рака желудка, высокая частота рака желудка требует высокой распространенности H. pylori . Однако даже среди обществ с высоким уровнем распространенности H. pylori , таких как Китай, существуют сильные географические различия в заболеваемости раком желудка. Наиболее важным фактором, который в настоящее время признан важным в H. pylori — взаимодействиях с окружающей средой, приводящих к раку желудка, является диета (т. Е. Риск рака наиболее высок в регионах с сезонным питанием, где свежие фрукты и овощи отсутствуют в течение длительного времени и где соль и курение являются основными методами консервирования пищевых продуктов) [15].
Как и следовало ожидать, горячие точки рака желудка часто присутствуют в горных регионах и регионах с заметными сезонными колебаниями, где широко распространены сезонные диеты, часто трудно достать свежие фрукты и овощи, а соль является основным методом консервирования продуктов питания. Регионы с низким риском рака — это, как правило, районы, где свежие фрукты и овощи доступны в течение всего года [15]. Важность факторов окружающей среды лучше всего иллюстрируется тем фактом, что даже высокий уровень H.pylori — высокая заболеваемость раком желудка В странах может наблюдаться быстрое снижение заболеваемости раком желудка, несмотря на незначительные изменения или отсутствие изменений в распространенности H. pylori или штамме H. pylori . В настоящее время это лучше всего иллюстрируется в Японии, еще одной стране с высоким уровнем заболеваемости раком желудка. В Японии произошло быстрое снижение заболеваемости раком желудка, что совпало с переходом на западные диеты и заменой соли на охлаждение в качестве основного метода хранения продуктов (рис.2). Это заметное изменение произошло во всех возрастных группах, несмотря на отсутствие изменений в генетике хозяина и в наиболее распространенном штамме H. pylori . Кроме того, иммигранты из стран с высокой заболеваемостью раком желудка в регионы с низкой заболеваемостью раком, например из Японии на Гавайи, сохраняют свой исходный риск рака, тогда как их дети, рожденные в новой среде, обычно имеют гораздо меньшую заболеваемость раком желудка [17].
Регионы с низким риском рака — это, как правило, районы, где свежие фрукты и овощи доступны в течение всего года [15]. Важность факторов окружающей среды лучше всего иллюстрируется тем фактом, что даже высокий уровень H.pylori — высокая заболеваемость раком желудка В странах может наблюдаться быстрое снижение заболеваемости раком желудка, несмотря на незначительные изменения или отсутствие изменений в распространенности H. pylori или штамме H. pylori . В настоящее время это лучше всего иллюстрируется в Японии, еще одной стране с высоким уровнем заболеваемости раком желудка. В Японии произошло быстрое снижение заболеваемости раком желудка, что совпало с переходом на западные диеты и заменой соли на охлаждение в качестве основного метода хранения продуктов (рис.2). Это заметное изменение произошло во всех возрастных группах, несмотря на отсутствие изменений в генетике хозяина и в наиболее распространенном штамме H. pylori . Кроме того, иммигранты из стран с высокой заболеваемостью раком желудка в регионы с низкой заболеваемостью раком, например из Японии на Гавайи, сохраняют свой исходный риск рака, тогда как их дети, рожденные в новой среде, обычно имеют гораздо меньшую заболеваемость раком желудка [17].
Рис.2
Изменения в заболеваемости раком желудка, несмотря на незначительные изменения в H.pylori среди японских мужчин в возрасте 65–69 лет во второй половине ХХ века. Адаптировано из [16], с разрешения.
Бактериальные факторы
Признание того, что H. pylori была причиной рака желудка, вызвало большой интерес к вопросу о том, могут ли быть бактериальные факторы, которые были особенно важны для определения исхода отдельной инфекции. Бактерии обладают множеством факторов, необходимых для колонизации и длительного проживания в желудке, особенно когда желудок изменяется в ответ на инфекцию.Таким образом, геном H. pylori кодирует продукты, которые повышают его способность выживать и размножаться в кислой среде и избегать выброса из желудка вместе с регулярным опорожнением питательных веществ и другого содержимого просвета. Как и ожидалось, организмы подвижны и способны перемещаться из негостеприимных районов в районы с более благоприятными условиями и наличием питательных веществ. H. pylori выражают различные спайки, позволяющие организмам прилипать к поверхности желудка, чтобы их не смыло [18].Прикрепление организма к клеткам также влияет на их поведение, в том числе делает дефицитные питательные вещества доступными непосредственно из клеток-хозяев [19]. H. pylori может также проникать и выживать в поверхностных клетках слизистой оболочки желудка, которые обеспечивают другую нишу, позволяющую избежать агрессивной среды желудка, а также иммунного ответа хозяина, направленного на устранение инфекции [20].
H. pylori выражают различные спайки, позволяющие организмам прилипать к поверхности желудка, чтобы их не смыло [18].Прикрепление организма к клеткам также влияет на их поведение, в том числе делает дефицитные питательные вещества доступными непосредственно из клеток-хозяев [19]. H. pylori может также проникать и выживать в поверхностных клетках слизистой оболочки желудка, которые обеспечивают другую нишу, позволяющую избежать агрессивной среды желудка, а также иммунного ответа хозяина, направленного на устранение инфекции [20].
Гистологическим признаком инфекции H. pylori является сочетание острого и хронического воспаления, называемого воспалением «острое-хроническое».Считается, что воспаление слизистой оболочки особенно важно для улучшения доставки питательных веществ в организм. Интересно, что слизистая оболочка желудка пациентов с ВИЧ / СПИДом обычно лишена видимых H. pylori , что согласуется с воспалением, играющим критическую роль в захвате желудка H. pylori [21]. H. pylori также может частично подорвать иммунный ответ. Например, H. pylori , действуя через дендритные клетки, может преимущественно индуцировать ответ Т-регуляторных клеток по сравнению с ответами Th2 / Th27 [22,23].Однако субпопуляции Th2 и Th27 Т-клеток в первую очередь опосредуют хронический гастрит [24]. В дополнение к сильному полиморфноядерному и мононуклеарному ответу клеток, существует также приток Т-регуляторных клеток в слизистую оболочку, которые имеют тенденцию подавлять иммунный ответ. Более того, ИЛ-10, продуцируемый Т-регуляторными клетками, приводит к снижению выработки ИЛ-8, что способствует устойчивости бактерий в организме хозяина и способствует иммунной толерантности [25]. В целом H. pylori , как и другой хронический патоген человека, Mycobacterium tuberculosis , прекрасно адаптирован к жизни у людей, что отчасти является причиной сложности создания эффективной вакцины для предотвращения инфекции.
pylori [21]. H. pylori также может частично подорвать иммунный ответ. Например, H. pylori , действуя через дендритные клетки, может преимущественно индуцировать ответ Т-регуляторных клеток по сравнению с ответами Th2 / Th27 [22,23].Однако субпопуляции Th2 и Th27 Т-клеток в первую очередь опосредуют хронический гастрит [24]. В дополнение к сильному полиморфноядерному и мононуклеарному ответу клеток, существует также приток Т-регуляторных клеток в слизистую оболочку, которые имеют тенденцию подавлять иммунный ответ. Более того, ИЛ-10, продуцируемый Т-регуляторными клетками, приводит к снижению выработки ИЛ-8, что способствует устойчивости бактерий в организме хозяина и способствует иммунной толерантности [25]. В целом H. pylori , как и другой хронический патоген человека, Mycobacterium tuberculosis , прекрасно адаптирован к жизни у людей, что отчасти является причиной сложности создания эффективной вакцины для предотвращения инфекции.
С момента своего открытия ученые изучали, как H. pylori вызывает воспаление, а также связь между предполагаемыми факторами бактериальной вирулентности и типом и тяжестью воспалительной реакции. Усилия, как правило, сосредоточены на изолированных предполагаемых факторах вирулентности, и только сейчас мы начинаем видеть исследования, направленные на понимание сложных взаимодействий, которые могут иметь место. Особый интерес вызвали белков внешней мембраны H. pylori , такие как BabA, SabA, OipA, AlpA / B, homB [26,27,28], остров патогенности cag ( cag PAI) и вакуолизирующий цитотоксин VacA [29,30,31].Важно помнить, что не было обнаружено непатогенных H. pylori (т.е. все H. pylori вызывают воспаление слизистой оболочки желудка и были связаны с развитием язвенной болезни и раком желудка). Тем не менее, патогенность H. pylori , оцениваемая с точки зрения риска развития клинического исхода, лучше всего связана со способностью штамма вызывать воспаление [32,33,34]. Например, штаммы, считающиеся наиболее патогенными (то есть те, которые обладают cag PAI), связаны примерно с удвоением риска рака желудка по сравнению со штаммами, не имеющими cag PAI.Трудно переоценить тот факт, что все H. pylori являются патогенами и что различия между штаммами заключаются только в степени риска, и, как правило, факторы хозяина и окружающей среды, связанные с повышенной воспалительной реакцией на инфекцию, также увеличивают риск желудочного атрофия и рак желудка.
pylori вызывает воспаление, а также связь между предполагаемыми факторами бактериальной вирулентности и типом и тяжестью воспалительной реакции. Усилия, как правило, сосредоточены на изолированных предполагаемых факторах вирулентности, и только сейчас мы начинаем видеть исследования, направленные на понимание сложных взаимодействий, которые могут иметь место. Особый интерес вызвали белков внешней мембраны H. pylori , такие как BabA, SabA, OipA, AlpA / B, homB [26,27,28], остров патогенности cag ( cag PAI) и вакуолизирующий цитотоксин VacA [29,30,31].Важно помнить, что не было обнаружено непатогенных H. pylori (т.е. все H. pylori вызывают воспаление слизистой оболочки желудка и были связаны с развитием язвенной болезни и раком желудка). Тем не менее, патогенность H. pylori , оцениваемая с точки зрения риска развития клинического исхода, лучше всего связана со способностью штамма вызывать воспаление [32,33,34]. Например, штаммы, считающиеся наиболее патогенными (то есть те, которые обладают cag PAI), связаны примерно с удвоением риска рака желудка по сравнению со штаммами, не имеющими cag PAI.Трудно переоценить тот факт, что все H. pylori являются патогенами и что различия между штаммами заключаются только в степени риска, и, как правило, факторы хозяина и окружающей среды, связанные с повышенной воспалительной реакцией на инфекцию, также увеличивают риск желудочного атрофия и рак желудка.
Вирулентный потенциал бактерий
Остров патогенности cag
PAI cag представляет собой геномный остров размером примерно 40 т.п.н., состоящий примерно из 30 генов [31,35].CagA — очень иммуногенный белок, кодируемый геном cagA , и присутствие антитела CagA часто используется в качестве маркера присутствия интактного PAI cag [36]. Связь CagA-положительных штаммов с увеличением риска рака желудка [30,37,38] привела к тому, что CagA стал одним из наиболее широко изученных белков H. pylori . Однако большинство исследований с CagA было проведено in vitro с ограниченными корреляциями in vitro-in vivo. cag PAI кодирует систему секреции типа IV (T4SS), через которую CagA вводится в клетки-хозяева [36,39], где он подвергается фосфорилированию тирозина (CagA PY ) в Glu-Pro-Ile-Tyr-Ala (EPIYA ) мотивы [40].Недавние исследования показали, что штаммы с cagA с большим количеством сегментов EPIYA-C связаны с более высоким риском рака желудка, чем штаммы с cagA с одним сегментом C-типа [41,42]. Это открытие также согласуется с паттерном сегментов EPIYA, касающихся способности индуцировать IL-8. Однако есть данные о том, что штаммы с большим количеством повторов EPIYA имеют пониженную способность выживать в кислой среде, предполагая, что множественные повторы являются эпифеноменом, который возникает после развития атрофии.Получение долгосрочных проспективных данных от людей относительно изменения количества повторов EPIYA нецелесообразно и, вероятно, было бы неэтичным, поскольку потребовало бы отсрочки терапии у пациента, инфицированного доказанным канцерогеном. Исследования количества повторов EPIYA у детей исследовали эту гипотезу косвенно и согласуются с гипотезой о том, что множественные сегменты являются приобретенным феноменом [43].
Другая проблема с экстраполяцией результатов экспериментов с CagA связана с механизмом проникновения белка в клетку.Обычно CagA вводится через плазматическую мембрану. Однако в ряде критических экспериментов использовалась трансфекция, которая, вероятно, не отражает нормальные процессы. Другие исследовали трансгенных животных и предположили, что CagA может обладать онкогенными свойствами [44]. Связь этого наблюдения с тем, что происходит при естественной инфекции, остается неясной. Однако после инъекции в клетку и фосфорилирования CagA PY может связываться и аберрантно активировать тирозинфосфатазу SHP2, которая затем может нарушать регуляцию пролиферации и подвижности клеток [41,45,46], а также связываться с дефектным по разделению 1 (PAR1) / Киназа, регулирующая сродство к микротрубочкам (MARK) через последовательность мультимеризации CagA, не зависит от фосфорилирования тирозина [47].Связывание CagA ингибирует киназную активность PAR1b, что может привести к нарушению полярности эпителиальных клеток [47]. Недавно также сообщалось, что CagA способен индуцировать переход от поляризованных эпителиальных клеток (демонстрирующих клеточную адгезию) к более инвазивному фенотипу [48]. Другие предполагаемые детерминанты вирулентности, расположенные на cag PAI, такие как cagE , cagG , cagH , kcagI , cagL и cagM , необходимы для индукции cag PAI. cagT и cagY необходимы для образования игольчатой структуры, которая служит для инъекции cagA в клетку-хозяин [36,49]. Роль этих других факторов в патогенезе исходов заболевания, связанного с H. pylori , остается менее ясной, чем с CagA. Также сообщалось, что в некоторых штаммах H. pylori PAI cag разделен на две отдельные области из-за интеграции последовательности вставки IS 605 [36].Предполагаемые транспозазы IS 605 ( tnpA и tnpB ) могут опосредовать разрушение PAI cag [36] и также могут влиять на вирулентность H. pylori [50]. В целом точная биологическая роль и клиническая значимость этих двух детерминант остаются плохо изученными.
Хотя результаты CagA интригуют, важно помнить, что присутствие CagA также связано с язвой двенадцатиперстной кишки, которая связана с фенотипом неатрофического гастрита и низким риском рака желудка.В целом представляется вероятным, что наиболее важной функцией CagA является его способность взаимодействовать с мембранными белками и запускать каскад сигнальных трансдукций, ведущих к индукции усиленного воспалительного ответа (например, посредством продукции IL-8). В надлежащих условиях усиленное воспаление будет способствовать неопластической трансформации [36,45,51], что еще раз подчеркивает фундаментальную роль воспаления в канцерогенезе желудка. На сегодняшний день лишь немногие из наблюдений in vitro подтверждены in vivo.Например, желудочный эпителий пациентов с язвой двенадцатиперстной кишки сохраняет свои характеристики как «плотный» эпителий без признаков значительного нарушения полярности клеток или каких-либо других признаков, описанных in vitro.
VacA
VacA, вакуолизирующий цитотоксин H. pylori , обладает способностью индуцировать вакуоли in vitro в инфицированных клетках культуры ткани [52]. Практически все штаммы H. pylori обладают геном vacA , однако между изолятами существует значительная вариация последовательностей.Наибольшее разнообразие локализовано в четырех регионах: сигнальная последовательность (s, типы аллелей s1a, s1b, s1c, s2), промежуточная (i, типы аллелей i1, i2), средняя (m, типы аллелей m1, m2) и область автотранспортера. [29,53]. Эти вариации вносят вклад в различия в вакуолизирующей активности in vitro различных штаммов H. pylori [29], причем штаммы s1 / m1 являются наиболее цитотоксичными. Заражение штаммами, содержащими формы s1, i1 и m1 vacA , было связано с более высоким риском рака желудка по сравнению со штаммами s2 / m2 [30,54].Однако важно отметить, что присутствие этих так называемых более вирулентных генотипов VacA также связано с совместным присутствием CagA. Большинство исследований были сосредоточены на одном изолированном факторе, а не на группах или комбинациях факторов, которые тесно связаны между собой, и такая направленность значительно увеличила вероятность ложных наблюдений.
VacA, как было показано, играет важную роль в способности H. pylori выживать в клетках-хозяевах, и это может быть его наиболее важной активностью [55].Например, возможно, что общий воспалительный ответ может быть меньше у штаммов s2 или m2, если они менее способны повышать выживаемость H. pylori в эпителиальных клетках.
Было проведено множество исследований VacA in vitro. Например, VacA взаимодействует с многочисленными молекулами рецепторов на поверхности хозяина in vitro и может запускать различные реакции, включая внедрение пор в клеточную мембрану, модификацию эндолизосомных функций, вакуолизацию клеток, апоптоз и иммунное ингибирование [56,57,58].VacA также может нацеливаться на митохондрии, вызывая гибель клеток-хозяев [59,60]. Domanska et al. [60] показали, что VacA может образовывать анионный канал к внутренней митохондриальной мембране p34-зависимым образом, тогда как Yamasaki et al. [61] сообщили, что VacA косвенно приводит к высвобождению цитохрома c путем активации проапоптотических белков Bax и Bak. NH 4 Cl был способен усиливать как вакуолизацию, вызванную VacA, так и активацию Bax. Опять же, корреляции in vitro-in vivo, как правило, отсутствуют, поэтому результаты исследований in vitro остаются спекулятивными.
Генетическая нестабильность
Геномная нестабильность лежит в основе рака и может привести к изменениям в экспрессии генов; геномная нестабильность считается одним из необходимых шагов в канцерогенезе. Хроническое воспаление и окислительный стресс, вызванное H. pylori , создают среду, способствующую повреждению ДНК и повреждению тканей [13,62,63]. Повреждение ДНК приводит к генетической нестабильности и, в конечном итоге, к неопластической трансформации. Трансгенная мышь Big Blue — полезная система для исследования повреждений ДНК в различных тканях, включая желудок.Использование модели трансгенных мышей Big Blue подтвердило, что инфекция H. pylori была связана с высокими уровнями повреждения ДНК (т. Е. Трансверсии AT в GC и GC в TA были увеличены в четыре раза после 6 месяцев инфекции по сравнению с клетками, выделенными из неинфицированного контроля. мыши) [64,65]. В дополнение к трансверсиям пар оснований было идентифицировано по крайней мере пять различных генетических механизмов, включая двухцепочечных разрывов ДНК, связанных с инфекцией H. pylori, , нарушение репарации несоответствия ДНК, экспрессия цитидиндезаминазы, вызванная аберрантной активацией (которая вызывает вовлеченные нуклеотидные изменения). при мутациях ДНК), аберрантное метилирование промоторов генов в слизистой оболочке желудка и аберрантная экспрессия микроРНК [65] (рис.3).
Рис. 3
Механизмы геномных нестабильностей, связанных с инфекцией H. pylori . Адаптировано из [63], с разрешения. AID = цитидиндезаминаза, индуцированная активацией.
Факторы хозяина
Существует обширная литература о полиморфизмах генов во взаимодействии с хозяином, которые регулируют воспалительный ответ (то есть усиление или снижение иммунного ответа) и его влиянии на различные заболевания, от пародонта до ревматоидного артрита.Гены-хозяева взаимодействуют с факторами вирулентности на протяжении всего патогенеза инфекции и заболевания [66]. Идентификация и различение полиморфизмов генов-хозяев, влияющих на восприимчивость в популяциях с высокой заболеваемостью раком желудка, было серьезной проблемой. Генетические полиморфизмы в разных генах, контролирующих воспалительный ответ, были связаны с разными способностями реагировать на воспалительные стимулы, что приводило к разной степени ответа. Таким образом, полиморфизмы гена IL-1β, в частности IL-1, β-31 и IL-1, β-511, приводят к увеличению продукции IL-1β, воспалению, гипохлоргидрии, атрофии желудка и аденокарциноме желудка [67,68].Более того, недавние крупномасштабные исследования ассоциации генов в масштабе всего генома были сосредоточены на генах, участвующих в пролиферации, дифференцировке и выживании клеток, а также путях репарации ДНК [69]. Области хромосомы 9p21.3 и 10q23 были идентифицированы как локусы генетической предрасположенности к множественным фенотипам заболеваний, включая рак желудка [70,71]. Также присутствуют полиморфизмы в некоторых генах, связанных с инфекцией H. pylori . Присутствие антигенов Льюиса, которые включают группу фукозилированных олигосахаридов, может опосредовать прикрепление H.pylori на слизистую оболочку желудка человека [54]. Одно исследование показало, что пациенты с раком желудка имели более высокую распространенность фенотипа Le a + b- и более низкую частоту фенотипа Le a-b + (p <0,05) по сравнению с контрольной группой, не страдающей раком [72]. Локусы TLR-1 и FCGR2A были связаны с серопревалентностью H. pylori и вероятностью инфицирования людей H. pylori [73].
Диета, питание и другие факторы
Многие клинические эпидемиологические исследования показали важность диеты в канцерогенезе желудка [74,75,76].Факторы риска включают чрезмерное потребление соли, низкое потребление ненасыщенных жиров, свежих овощей и фруктов. Проспективное исследование, проведенное среди населения Японии, предполагает, что высокое потребление соли с пищей (> 10 г в день) является значительным фактором риска рака желудка, и эта связь оказалась более сильной при наличии инфекции H. pylori с атрофическим гастритом. [77]. Витамин С может быть защитным фактором против дисплазии и рака желудка, как предполагало проспективное исследование с участием 3433 человек в 1989–1990 годах, проведенное в Линьцю, Китай, регионе с очень высокими показателями рака желудка [78].Однако после 11 лет наблюдения не было выявлено значительной связи между употреблением поливитаминов и риском рака желудка [79]. Высокое потребление соленых и осушенных продуктов в настоящее время часто является результатом более низкого экономического статуса и отсутствия охлаждения. В последнее время наблюдается рост возможностей перевозки фруктов и овощей и, следовательно, сокращение их доступности только в определенные сезоны. Кроме того, использование холодильного оборудования для хранения также было связано со снижением заболеваемости раком желудка в развитых странах.В развивающихся странах плохая обработка и приготовление пищи по-прежнему является серьезной проблемой и связана с более высокой заболеваемостью раком желудка [80,81].
Выводы
В настоящее время признано, что H. pylori вызывает не менее 95% всех случаев рака желудка [63]. Риск рака желудка на протяжении всей жизни варьируется в зависимости от населения, при этом высокая распространенность рака желудка колеблется от 1 до примерно 20%. Рак желудка — это рак, связанный с воспалением, и, помимо воспаления, H.pylori может напрямую вызывать генетическую нестабильность. Риск рака желудка увеличивается пропорционально степени и тяжести атрофического гастрита [65]. Лечение H. pylori до развития атрофического гастрита по существу предотвратит развитие рака желудка. Эрадикация H. pylori по истечении этого времени снижает заболеваемость раком, но не предотвращает его полностью [63]. H. pylori -индуцированное повреждение желудка прогрессирует и его скорость непредсказуема, так что H.pylori — единственный метод предотвращения рака или снижения риска рака желудка. Япония осуществила общенациональную программу по обнаружению и ликвидации H. pylori наряду с эпиднадзором за теми, у кого был атрофический гастрит на момент ликвидации H. pylori , чтобы снизить смертность от рака среди тех, у кого H. pylori искоренение было проведено слишком поздно, чтобы исключить риск [82]. Уничтожение H. pylori в масштабах всего населения приведет к тому, что рак желудка станет исчезающе редким заболеванием.Когда больше стран последуют примеру Японии и приступят к программе ликвидации H. pylori , рак желудка станет редким заболеванием.
Выражение признательности
Доктор Грэм получает частичную поддержку со стороны Управления исследований и разработок Службы медицинских исследований по делам ветеранов, гранты Службы здравоохранения R01 DK062813 и DK56338, которые финансируют Центр болезней органов пищеварения Техасского медицинского центра. Авторы несут исключительную ответственность за содержание и не обязательно отражают официальную точку зрения VA или NIH.
Заявление о раскрытии информации
Доктор Грэм является неоплачиваемым консультантом компании Novartis по вопросам разработки вакцины для лечения или профилактики инфекции H. pylori . Он является оплачиваемым консультантом RedHill Biopharma по новым методам лечения H. pylori и получил поддержку исследований для культивирования H. pylori . Он является консультантом компании Otsuka Pharmaceuticals по вопросам диагностики дыхания. Он получил лицензионные отчисления от патентов Медицинского колледжа Бейлора, покрывающих материалы, относящиеся к дыхательному тесту на содержание C-мочевины 13 .
Список литературы
- Член парламента Уильямса, Pounder RE: Helicobacter pylori : от доброкачественного к злокачественному. Am J Gastroenterol 1999; 94 (11 доп.): S11-S16.
- Kusters JG, van Vliet AH, Kuipers EJ: Патогенез инфекции Helicobacter pylori .Clin Microbiol Rev 2006; 19: 449-490.
- Peek RM Jr, Blaser MJ: Helicobacter pylori и аденокарциномы желудочно-кишечного тракта. Нат Рев Рак 2002; 2: 28-37.
- Салама Н.Р., Хартунг М.Л., Мюллер А: Жизнь в желудке человека: стратегии сохранения бактериального патогена Helicobacter pylori .Nat Rev Microbiol 2013; 11: 385-399.
- Уэмура Н., Окамото С., Ямамото С., Мацумура Н., Ямагути С. и др.: Инфекция Helicobacter pylori и развитие рака желудка. N Engl J Med 2001; 345: 784-789.
- Форман Д., Ньюэлл Д. Г., Фуллертон Ф., Ярнелл Дж. В., Стейси А. Р. и др.: Связь между инфекцией Helicobacter pylori и риском рака желудка: данные проспективного исследования.BMJ 1991; 302: 1302-1305.
- Всемирная организация здравоохранения / Международное агентство по изучению рака: Монографии МАИР по оценке канцерогенных рисков для людей. Том 61: Шистосомы, печеночные двуустки и Helicobacter pylori . Лион, Международное агентство по изучению рака, 1994.
- Хеликобактер пилори . Биологические агенты: Обзор канцерогенов человека, том 100B. Лион, Международное агентство по изучению рака, 2012 г., стр. 385-435.
- Паркин Д.М., Брей Ф., Ферли Дж., Пизани П.: Глобальная статистика рака, 2002.CA Cancer J Clin 2005; 55: 74-108.
- Линч HT, Грэди В., Суриано Дж., Хантсман Д. Рак желудка: новые генетические разработки. J Surg Oncol 2005; 90: 114-133; Обсуждение 133.
- Coussens LM, Werb Z: Воспаление и рак.Природа 2002; 420: 860-867.
- Ernst PB, Gold BD: спектр заболеваний Helicobacter pylori : иммунопатогенез гастродуоденальной язвы и рака желудка. Анну Рев Микробиол 2000; 54: 615-640.
- Hanada K, Graham DY: Helicobacter pylori и молекулярный патогенез рака желудка кишечного типа.Expert Rev Anticancer Ther 2014, Epub опережает печать.
- Купер Х., Адами Х.О., Трихопулос Д: Инфекции как основная предотвратимая причина рака человека. J Intern Med 2000; 248: 171-183.
- Грэм Д.Ю.: Инфекция Helicobacter pylori в патогенезе язвы двенадцатиперстной кишки и рака желудка: модель.Гастроэнтерология 1997; 113: 1983-1991.
- Грэм Д.Ю., Лу Х., Ямаока Ю.: загадка Африки, Азии или Индии, Восточная Азия Helicobacter pylori : факты или медицинские мифы. Журнал Dig Dis 2009; 10: 77-84.
- Маскаринек Дж., Но Дж. Дж.: Влияние миграции на заболеваемость раком среди японцев на Гавайях.Этн Дис 2004; 14: 431-439.
- Evans DJ Jr, Evans DG: Helicobacter pylori adhesins: обзор и перспективы. Helicobacter 2000; 5: 183-195.
- Боянова Л. Роль факторов вирулентности Helicobacter pylori в приобретении железа из эпителиальных клеток желудка хозяина и влияние на колонизацию бактерий.Future Microbiol 2011; 6: 843-846.
- Дин Н.С., Хуанг С.Дж., Гонг Л., Квок Т., Девениш Р.Дж .: Влияние аутофагических процессов на внутриклеточную судьбу Helicobacter pylori : больше уловок от загадочного патогена? Аутофагия 2013; 9: 639-652.
- Невин Д.Т., Морган С.Дж., Грэм Д.Й., Гента Р.М.: Helicobacter pylori гастрит у ВИЧ-инфицированных пациентов: обзор.Helicobacter 2014, Epub опережает печать.
- Kao JY, Zhang M, Miller MJ, Mills JC, Wang B, et al: Helicobacter pylori Ускользание от иммунитета опосредуется индуцированным дендритными клетками перекосом Treg и подавлением Th27 у мышей. Гастроэнтерология 2010; 138: 1046-1054.
- Wang YH, Gorvel JP, Chu YT, Wu JJ, Lei HY: Helicobacter pylori ухудшает ответы дендритных клеток мыши на инфекцию.PLoS One 2010; 5: e10844.
- Итон К.А., Меффорд М., Тевенот Т.: Роль субпопуляций Т-клеток и цитокинов в патогенезе гастрита Helicobacter pylori у мышей. J. Immunol. 2001; 166: 7456-7461.
- Робинсон К., Кенефек Р., Пиджон Е.Л., Шакиб С., Патель С. и др.: Язвенная болезнь, вызванная Helicobacter pylori , связана с неадекватными ответами регуляторных Т-клеток.Кишечник 2008; 57: 1375-1385.
- Jung SW, Sugimoto M, Graham DY, Yamaoka Y: статус homB Helicobacter pylori в качестве нового маркера, позволяющего отличить рак желудка от язвы двенадцатиперстной кишки. J Clin Microbiol 2009; 47: 3241-3245.
- Махдави Дж., Сонден Б., Хуртиг М., Олфат Ф.О., Форсберг Л. и др.: Helicobacter pylori, , адгезин SabA при хронической инфекции и хроническом воспалении.Наука 2002; 297: 573-578.
- Odenbreit S, Swoboda K, Barwig I, Ruhl S, Boren T и др.: Профиль экспрессии белка внешней мембраны в клинических изолятах Helicobacter pylori . Инфекция Иммун 2009; 77: 3782-3790.
- Atherton JC, Cao P, Peek RM Jr, Tummuru MK и др.: Мозаицизм в вакуолизирующих аллелях цитотоксина Helicobacter pylori .Связь определенных типов vacA с выработкой цитотоксина и пептической язвой. J. Biol Chem. 1995; 270: 17771-17777.
- Basso D, Zambon CF, Letley DP, Stranges A, Marchet A, et al: Клиническая значимость Helicobacter pylori полиморфизмов генов cagA и vacA. Гастроэнтерология 2008; 135: 91-99.
- Censini S, Lange C, Xiang Z, Crabtree JE, Ghiara P, et al: cag, остров патогенности Helicobacter pylori , кодирует факторы вирулентности, специфичные для типа I и связанные с заболеванием. Proc Natl Acad Sci U S. A 1996; 93: 14648-14653.
- Палли Д., Масала Г., Дель Джудис Г., Плебани М., Бассо Д. и др.: Инфекция CagA + Helicobacter pylori и риск рака желудка в исследовании EPIC-EURGAST.Int J Cancer 2007; 120: 859-867.
- Пламмер М., ван Дорн Л.Дж., Франчески С., Клетер Б., Канциан Ф. и др.: Helicobacter pylori, , генотип, связанный с цитотоксином, и предраковые поражения желудка. J Natl Cancer Inst 2007; 99: 1328-1334.
- Queiroz DM, Mendes EN, Rocha GA, Oliveira AM, Oliveira CA и др.: CagA-позитивный Helicobacter pylori и риск развития рака желудка в Бразилии.Int J Cancer 1998; 78: 135-139.
- Акопянц Н.С., Клифтон С.В., Керсулите Д., Крэбтри Дж. Э., Юри Б. Е. и др.: Анализ острова патогенности cag Helicobacter pylori . Мол Microbiol 1998; 28: 37-53.
- Hatakeyama M: Helicobacter pylori CagA — бактериальный нарушитель, вызывающий канцерогенез желудка.Int J Cancer 2006; 119: 1217-1223.
- Blaser MJ, Perez-Perez GI, Kleanthous H, Cover TL, Peek RM и др.: Заражение штаммами Helicobacter pylori , обладающими cagA, связано с повышенным риском развития аденокарциномы желудка. Cancer Res 1995; 55: 2111-2115.
- Enroth H, Kraaz W, Engstrand L, Nyren O, Rohan T: Helicobacter pylori типы штаммов и риск рака желудка: исследование случай-контроль. Эпидемиологические биомаркеры рака до 2000 г .; 9: 981-985.
- Фишер В. Сборка и молекулярный механизм действия аппарата секреции Helicobacter pylori Cag типа IV.FEBS J 2011; 278: 1203-1212.
- Backert S, Selbach M: Тирозин-фосфорилированные бактериальные эффекторные белки: враги внутри. Тенденции Microbiol 2005; 13: 476-484.
- Хатакеяма М: Онкогенные механизмы белка Helicobacter pylori CagA.Нат Рев Рак 2004; 4: 688-694.
- Yamaoka Y, Kodama T, Kashima K, Graham DY, Sepulveda AR: Варианты 3′-области гена cagA в изолятах Helicobacter pylori от пациентов с различными заболеваниями, ассоциированными с H. pylori . J. Clin Microbiol 1998; 36: 2258-2263.
- Ямаока Й., Редди Р., Грэм Д.Ю.: Helicobacter pylori Генотипы фактора вирулентности у детей в Соединенных Штатах: ключи к генотипу и взаимосвязям результатов. J Clin Microbiol 2010; 48: 2550-2551.
- Ohnishi N, Yuasa H, Tanaka S, Sawa H, Miura M и др.: Трансгенная экспрессия Helicobacter pylori CagA индуцирует желудочно-кишечные и гематопоэтические новообразования у мышей.Proc Natl Acad Sci U S A 2008; 105: 1003-1008.
- Хигаши Х., Цуцуми Р., Муто С., Сугияма Т., Азума Т. и др.: Тирозинфосфатаза SHP-2 как внутриклеточная мишень для белка CagA Helicobacter pylori . Наука 2002; 295: 683-686.
- Хигаши Х., Накая А., Цуцуми Р., Йокояма К., Фуджи Ю. и др.: Helicobacter pylori CagA индуцирует Ras-независимый морфогенетический ответ посредством рекрутирования и активации SHP-2.J Biol Chem 2004; 279: 17205-17216.
- Саадат I, Хигаши Х., Обузе С., Умеда М., Мурата-Камия Н. и др.: Helicobacter pylori CagA нацелена на киназу PAR1 / MARK для нарушения полярности эпителиальных клеток. Природа 2007; 447: 330-333.
- Bagnoli F, Buti L, Tompkins L, Covacci A, Amieva MR: Helicobacter pylori CagA индуцирует переход от поляризованных к инвазивным фенотипам в клетках MDCK.Proc Natl Acad Sci U S A 2005; 102: 16339-16344.
- Pachathundikandi SK, Tegtmeyer N, Backert S: Передача сигнала Helicobacter pylori во время взаимодействия с рецепторами белка клетки-хозяина эпителиальных и иммунных клеток. Кишечные микробы 2013; 4: 454-474.
- Маттар Р., Маркес С.Б., Монтейро Мдо С., Дос Сантос А.Ф., Ирия К. и др.: Helicobacter pylori гены острова патогенности cag: клиническое значение для развития язвенной болезни в Бразилии.J Med Microbiol 2007; 56 (Pt 1): 9-14.
- Stein M, Bagnoli F, Halenbeck R, Rappuoli R, Fantl WJ, et al: c-Src / Lyn киназы активируют Helicobacter pylori CagA посредством фосфорилирования тирозина мотивов EPIYA. Мол микробиол 2002; 43: 971-980.
- Leunk RD, Johnson PT, David BC, Kraft WG, Morgan DR: Цитотоксическая активность в фильтратах бульонных культур Cam pylobacter pylori .J Med Microbiol 1988; 26: 93-99.
- Rhead JL, Letley DP, Mohammadi M, Hussein N, Mohagheghi MA и др.: Новая вакуолизирующая детерминанта цитотоксина Helicobacter pylori , промежуточная область, связана с раком желудка. Гастроэнтерология 2007; 133: 926-936.
- Фигейредо C, Machado JC, Pharoah P, Seruca R, Sousa S, et al: Helicobacter pylori и генотипирование интерлейкина 1: возможность идентифицировать людей с высоким риском карциномы желудка.J Natl Cancer Inst 2002; 94: 1680-1687.
- Гринфилд Л.К., Джонс Н.Л.: Модуляция аутофагии с помощью Helicobacter pylori и его роль в канцерогенезе желудка. Тенденции Microbiol 2013; 21: 602-612.
- Peek RM Jr, Crabtree JE: Инфекция Helicobacter и неоплазия желудка.Дж. Патол 2006; 208: 233-248.
- Амиева М.Р., Эль-Омар Е.М.: Взаимодействие бактерий и хозяев при инфекции Helicobacter pylori . Гастроэнтерология 2008; 134: 306-323.
- Ву Х, Накано Т., Мацузаки Ю., Оои Ю., Коно Т. и др.: Новый тип системы внутрибактериальной нанотранспортации для VacA в Helicobacter pylori .Med Mol Morphol 2014, Epub впереди печати.
- Jain P, Luo ZQ, Blanke SR: Helicobacter pylori вакуолизирующий цитотоксин A (VacA) задействует механизм деления митохондрий, чтобы вызвать гибель клеток-хозяев. Proc Natl Acad Sci U S A 2011; 108: 16032-16037.
- Domanska G, Motz C, Meinecke M, Harsman A, Papatheodorou P, et al: Helicobacter pylori Токсин VacA / субъединица p34: нацеливание анионного канала на внутреннюю митохондриальную мембрану.PLoS Pathog 2010; 6: e1000878.
- Yamasaki E, Wada A, Kumatori A, Nakagawa I, Funao J, et al: Helicobacter pylori вакуолизирующий цитотоксин индуцирует активацию проапоптотических белков Bax и Bak, что приводит к высвобождению цитохрома с и гибели клеток, независимо от вакуолизации.J. Biol Chem. 2006; 281: 11250-11259.
- Uehara T, Ma D, Yao Y, Lynch JP, Morales K, et al: Инфекция H. pylori связана с повреждением ДНК Lgr5-положительных эпителиальных стволовых клеток в желудке пациентов с раком желудка. Dig Dis Sci 2013; 58: 140-149.
- Шиотани А., Сен П., Грэм Д. Я .: Ликвидация рака желудка теперь возможна и практична.Semin Cancer Biol 2013; 23: 492-501.
- Дженкс П.Дж., Джереми А.Х., Робинсон П.А., Уокер М.М., Крэбтри Дж. Э.: Длительное инфицирование Helicobacter felis и инактивация гена супрессора опухолей р53 кумулятивно увеличивают частоту мутаций желудка у трансгенных мышей Big Blue.Дж. Патол 2003; 201: 596-602.
- Touati E, Michel V, Thiberge JM, Ave P, Huerre M и др.: Дефицит OGG1 защищает от воспаления и мутагенных эффектов, связанных с инфекцией H. pylori у мышей. Helicobacter 2006; 11: 494-505.
- He C, Chen M, Liu J, Yuan Y: Генетические факторы хозяина реагируют на патогенные ступенчатые факторы вирулентности Helicobacter pylori при канцерогенезе желудка.Mutat Res Rev. Mutat Res 2014; 759: 14-26.
- Sheu BS, Sheu SM, Yang HB, Huang AH, Wu JJ: Экспрессия Льюиса в желудке хозяина определяет бактериальную плотность Helicobacter pylori при генопозитивной инфекции babA2. Кишечник 2003; 52: 927-932.
- Sheu MJ, Yang HB, Sheu BS, Cheng HC, Lin CY и др.: Фенотип хозяина эритроцитов Льюиса (A + B-) является фактором с семейной кластеризацией для повышенного риска несердечного рака желудка, связанного с Helicobacter pylori, .J Gastroenterol Hepatol 2006; 21: 1054-1058.
- Кьюрилло М.А.: Роль полиморфизмов генов в раке желудка и его предшественниках: современные знания и перспективы в странах Латинской Америки. Всемирный журнал J Gastroenterol 2014; 20: 4503-4515.
- Абнет СС, Фридман Н.Д., Ху Н., Ван З., Ю К. и др.: Общий локус восприимчивости в PLCE1 в 10q23 для аденокарциномы желудка и плоскоклеточного рака пищевода.Нат Генет 2010; 42: 764-767.
- Гу Ф., Пфайфер Р.М., Бхаттачарджи С., Хан С.С., Тейлор П.Р. и др.: Общие генетические варианты в области 9p21 и их ассоциации с множественными опухолями. Br J Cancer 2013; 108: 1378-1386.
- Эль-Омар Е.М., Кэррингтон М., Чоу WH, Макколл К.Э., Лещ Дж. Х. и др.: Полиморфизмы интерлейкина-1, связанные с повышенным риском рака желудка.Природа 2000; 404: 398-402.
- Mayerle J, den Hoed CM, Schurmann C, Stolk L, Homuth G, et al: Идентификация генетических локусов, связанных с серологическим статусом Helicobacter pylori . JAMA 2013; 309: 1912-1920.
- Nemati A, Mahdavi R, Naghizadeh Baghi A: Исследование схемы питания и других факторов риска рака желудка методом случай-контроль.Перспектива укрепления здоровья, 2012 г .; 2: 20-27.
- Биничи Д.Н., Коджа Т., Дурсун Х. Диетические привычки, демографические и социально-экономические факторы риска вновь диагностированного рака желудка в регионе Восточной Анатолии в Турции: эндемический регион рака верхних отделов желудочно-кишечного тракта. Dig Dis Sci 2009; 54: 2629-2633.
- Lazarevic K, Nagorni A, Rancic N, Milutinovic S, Stosic L, et al: Диетические факторы и риск рака желудка: исследование случай-контроль в больнице. ЖУРНАЛ 2010; 15: 89-93.
- Shikata K, Kiyohara Y, Kubo M, Yonemoto K, Ninomiya T. и др.: Проспективное исследование потребления соли с пищей и заболеваемости раком желудка в определенной популяции Японии: исследование Hisayama.Int J Cancer 2006; 119: 196-201.
- You WC, Zhang L, Gail MH, Chang YS, Liu WD и др.: Дисплазия желудка и рак желудка: Helicobacter pylori , витамин C в сыворотке и другие факторы риска. J Natl Cancer Inst 2000; 92: 1607-1612.
- Dawsey SP, Hollenbeck A, Schatzkin A, Abnet CC: проспективное исследование использования витаминов и минеральных добавок и риска рака верхних отделов желудочно-кишечного тракта.PLoS One 2014; 9: e88774.
- La Vecchia C, Negri E, D’Avanzo B, Franceschi S: Использование электрического холодильника и риск рака желудка. Br J Cancer 1990; 62: 136-137.
- Цай Л., Чжэн З.Л., Чжан З.Ф .: Факторы риска рака кардии желудка: исследование случай-контроль в провинции Фуцзянь.Всемирный журнал J Gastroenterol 2003; 9: 214-218.
- Асака М., Като М., Сакамото Н.: Дорожная карта по ликвидации рака желудка с ликвидацией Helicobacter pylori и последовательным эпиднадзором в Японии. Журнал Гастроэнтерол 2014; 49: 1-8.
Автор Контакты
Дэвид Ю.Graham, MD
Департамент медицины
Michael E. DeBakey VAMC и Медицинский колледж Бейлора, RM 3A-320 (111D)
2002 Holcombe Boulevard, Houston, TX 77030 (США)
E-Mail dgraham @ bcm. edu
Подробности статьи / публикации
Предварительный просмотр первой страницы
Опубликовано онлайн: 18 июля 2014 г.
Дата выпуска: август 2014 г.
Количество страниц для печати: 11
Количество рисунков: 3
Количество столов: 0
ISSN: 2296-3774 (печатный)
eISSN: 2296-3766 (онлайн)
Для дополнительной информации: https: // www.karger.com/GAT
Авторские права / Дозировка препарата / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или с помощью какой-либо системы хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарств: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарств, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новый и / или редко применяемый препарат.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
Helicobacter Pylori — обзор
Пятьдесят или более процентов иммигрантов из эндемичных, слаборазвитых стран могут иметь желудочный H.pylori .
Инфекция H. pylori связана с язвой желудка и двенадцатиперстной кишки, гастритом и раком желудка. Это не было связано с кислотным рефлюксом, эзофагитом или раком пищевода.
Тем не менее, у большинства инфицированных людей не наблюдается никаких последствий заражения.
Инфекция H. pylori диагностируется (в порядке от наименее к наиболее дорогостоящему) по серологическому анализу, антигену кала, дыхательному тесту мочевины или эндоскопической биопсии.
Пациенты с задокументированными язвами, лимфомой MALT или с риском рака желудка должны пройти обследование и пройти лечение в случае положительного результата. Универсальное тестирование для бессимптомных людей в настоящее время не рекомендуется.
Стандартное лечение обычно состоит из двух эффективных антибиотиков и одного неантибиотика (висмут или ингибитор протонной помпы).
Тестирование следует проводить только в том случае, если предполагается получение положительного результата теста.Лечение следует проводить только в том случае, если можно обоснованно ожидать соблюдения режима лечения.
Лица с серьезными инфекциями (подтвержденная язва, MALT-лимфома или высокий риск рака желудка) должны пройти тестирование на успешную ликвидацию через 6–12 недель после лечения. Методы тестирования на эрадикацию включают антиген в кале, дыхательные тесты на мочевину или эндоскопическую биопсию. (Серология бесполезна для тестирования на эрадикацию.)
Нобелевская премия по медицине в 2005 г. была присуждена Робину Уоррену и Барри Маршаллу за их выделение, идентификацию и признание патофизиологических последствий бактерии, способной хронически инфицировать слизистую желудка. .Начиная с 1983 года, эти исследователи сообщили о неожиданном наблюдении, что бактерия Helicobacter pylori является основной причиной язв желудка и двенадцатиперстной кишки. 1 Впоследствии инфекция желудка H. pylori также убедительно была признана фактором риска острого и хронического гастрита, диспепсии, карциномы желудка и формы лимфомы желудка, известной как «лимфоидная ткань, связанная со слизистой оболочкой» (MALT). В-клеточная лимфома. После колонизации и / или заражения H.pylori особенно распространены среди иммигрантов, поэтому важно, чтобы врачи, оказывающие помощь пациентам-иммигрантам, знали об этом организме.


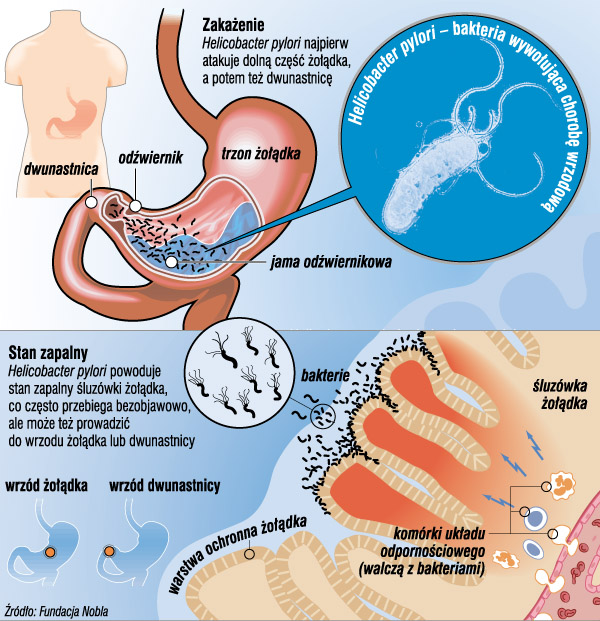
 В., Самсонов А.А., Андреев Н.Г., Кочетов С.А. Эволюция представлений о диагностике и лечении инфекции Helicobacter pylori (по материалам консенсуса Маастрихт IV, Флоренция 2010) // Вестник практического врача. — 2012. Спецвыпуск 1 — С. 6-30.
В., Самсонов А.А., Андреев Н.Г., Кочетов С.А. Эволюция представлений о диагностике и лечении инфекции Helicobacter pylori (по материалам консенсуса Маастрихт IV, Флоренция 2010) // Вестник практического врача. — 2012. Спецвыпуск 1 — С. 6-30.


 На дыхательные тесты требуется время, они не показывают, насколько серьезна инфекция, и их трудно сделать у маленьких детей.
На дыхательные тесты требуется время, они не показывают, насколько серьезна инфекция, и их трудно сделать у маленьких детей.
 Д. Комбинация этих лекарств и H. pylori увеличивает риск развития язвы желудка.
Д. Комбинация этих лекарств и H. pylori увеличивает риск развития язвы желудка. pylori . Образец вашего дыхания анализируется после того, как вы выпьете особый напиток. Примечание : перед этим тестом вы не должны были принимать какие-либо антибиотики в течение как минимум четырех недель. Кроме того, вам не следует принимать ингибитор протонной помпы (ИПП) или антагонист рецепторов H 2 в течение как минимум двух недель. (Это препараты, подавляющие кислотность.) Кроме того, вы не должны ничего есть в течение шести часов до теста.Причина этих правил в том, что лекарства и еда могут повлиять на результат теста.
pylori . Образец вашего дыхания анализируется после того, как вы выпьете особый напиток. Примечание : перед этим тестом вы не должны были принимать какие-либо антибиотики в течение как минимум четырех недель. Кроме того, вам не следует принимать ингибитор протонной помпы (ИПП) или антагонист рецепторов H 2 в течение как минимум двух недель. (Это препараты, подавляющие кислотность.) Кроме того, вы не должны ничего есть в течение шести часов до теста.Причина этих правил в том, что лекарства и еда могут повлиять на результат теста.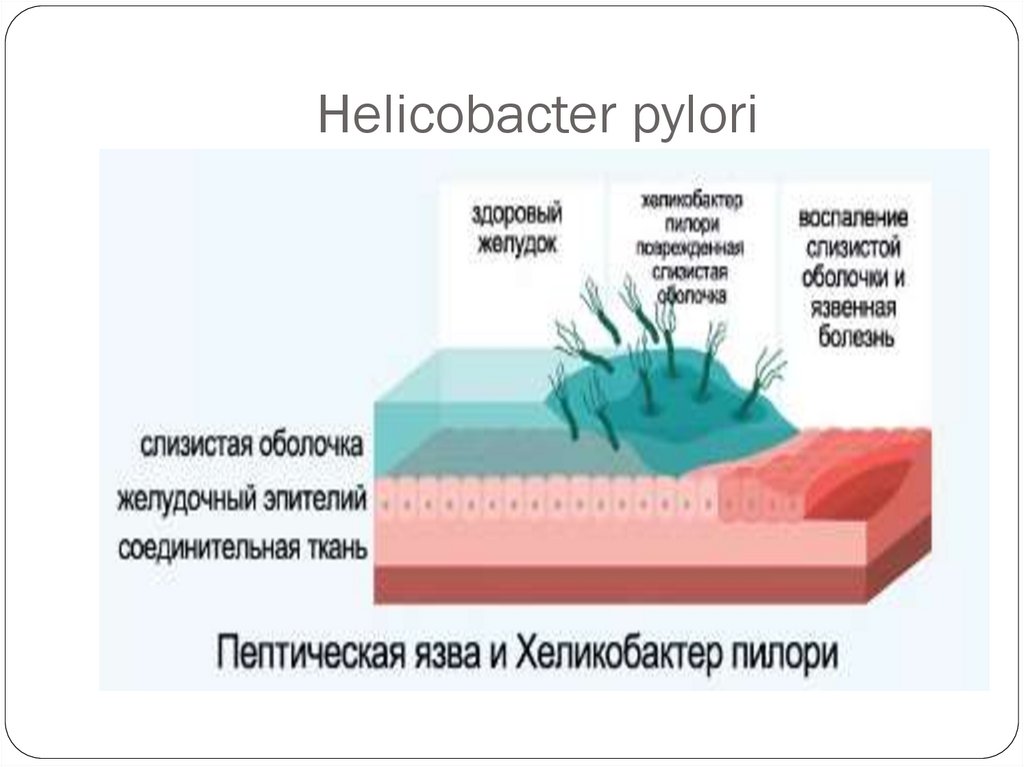
 Эти тесты выявляют антитела, указывающие на присутствие бактерии. Узнайте больше о анализах крови в CHOC.
Эти тесты выявляют антитела, указывающие на присутствие бактерии. Узнайте больше о анализах крови в CHOC. Эта ткань используется для:
Эта ткань используется для:  Небольшие образцы ткани могут быть взяты из стенки желудка, которые затем проверены на H. pylori .
Небольшие образцы ткани могут быть взяты из стенки желудка, которые затем проверены на H. pylori .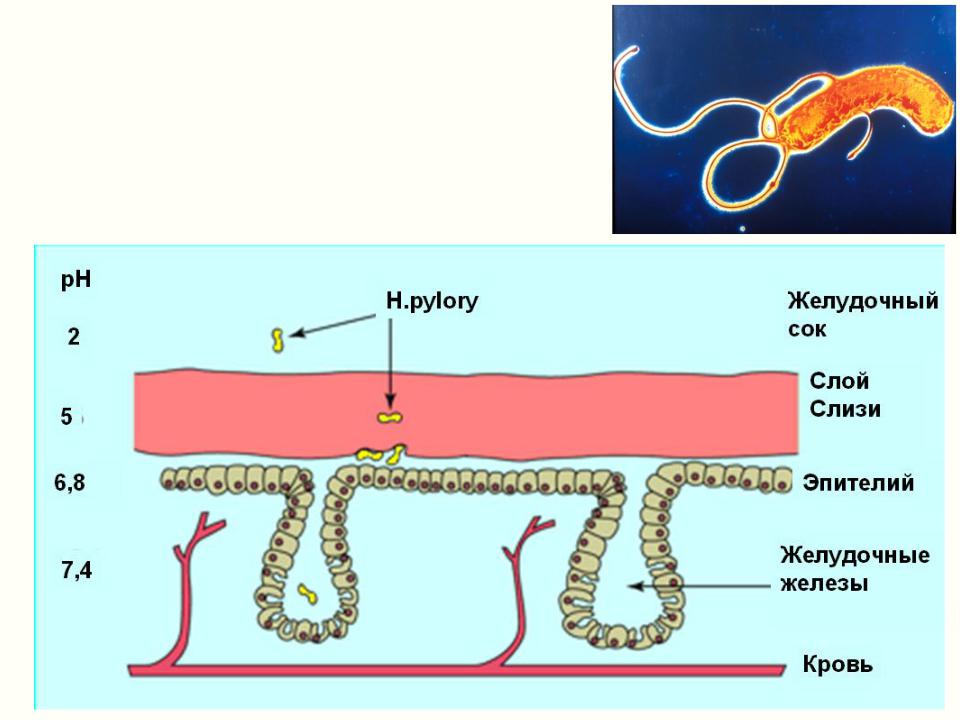 Am J Clin Dermatol 2002; 3: 273-82. Медлайн.
Am J Clin Dermatol 2002; 3: 273-82. Медлайн.