Симптомы остеосаркомы у детей: причины, симптомы, лечение
Возникновение первых симптомов остеосаркомы у детей наблюдается уже на поздних стадиях развития, когда заболевание поражает окружающие ткани. Встречается патология достаточно часто, отличается быстрым прогрессированием и высокой степенью агрессивности.
Понятие и причины
Остеогенная саркома у детей представляет собой новообразование, протекающее в злокачественной форме и поражающее костные ткани. Формироваться очаг поражения может в разных частях тела, но чаще всего страдают руки, ноги, челюсти. Остальные зоны организма затрагиваются редко.
Бесконтрольное деление клеток опухоли происходит по неизвестным причинам, механизм развития патологии еще не изучен.
Провоцирующие факторы следующие:
- Наследственность.
- Вредные привычки.
- Влияние на организм радиации, ядов, химикатов.
- Нерациональное питание.
- Заболевания костей.
Доброкачественные костные образования также могут перерасти в злокачественные формы.
Симптоматика
В начале развития остеосаркомы симптомы себя никак не проявляют. Только при наличии опухоли большого размера начинают возникать выраженные клинические признаки.
В первую очередь к ним относится болевой синдром. Его интенсивность увеличивается с каждой стадией, усиливается в ночное время суток. Болезненность трудно снимается простыми анальгетиками.
Помимо болезненных ощущений наблюдаются следующие симптомы остеосаркомы у детей:
- Ограничение подвижности сустава.
- Снижение прочности костей, что приводит к переломам.
- Хромота.
- Отечность мягких тканей, расположенных рядом с очагом.
- Покраснение кожного покрова в области поражения.
- Общая слабость.
- Ухудшение аппетита.
- Повышение температуры тела.
- Плаксивость, капризность.
Если поражены кости черепа, то возникают приступы головокружения, головная боль, тошнота, рвота.
Обследование
Для диагностики остеосаркомы применяют следующие методы:
- Лабораторное исследование крови.
- Рентгенография.
- Компьютерная томография.
- Магнитно-резонансная томография.
- Сцинтиграфия.
Также проводится биопсия с последующей гистологией. Именно этот метод помогает поставить окончательный диагноз, выявить злокачественные клетки в обнаруженной опухоли.
Лечебные мероприятия
Основные методы лечения остеосаркомы – оперативное вмешательство и химиотерапия. Облучение применяется в редких случаях. Как правило, сначала проводят химическое лечение, затем операцию по удалению опухоли, а после нее снова назначают химические препараты, чтобы уничтожить остаточные атипичные клетки.
На поздних стадиях при неоперабельности новообразования вылечить пациента не удается. В этом случае применяют химиотерапию в качестве основного метода лечения остеосаркомы, что позволяет уменьшить интенсивность симптомов и продлить жизнь больного.Прогноз
Прогноз излечения зависит от множества факторов. К ним относится следующее:
- Стадия развития патологии.
- Наличие сопутствующих заболеваний.
- Разновидность саркомы.
- Размер очага, его агрессивность.
- Состояние иммунной системы.
Исход болезни хороший при ранних стадиях заболевания, особенно если оно локализуется в области нижних и верхних конечностей. При выявлении опухоли в костях черепа, грудной клетки прогноз менее утешительный. При обнаружении патологии на поздних стадиях шанс на выздоровление очень низкий.
opake.ru
ОСТЕОГЕННАЯ САРКОМА У ДЕТЕЙ — Онкология
ОСТЕОГЕННАЯ САРКОМА — одна из основных форм первичных злокачественных новообразований костей у детей. Эта опухоль составляет от 50 до 80% всех сарком скелета и занимает 6-е место по частоте среди всех злокачественных опухолей детского возраста. Частота встречаемости заболевания составляет 0,4 на 100000 [2, 4]. Опухоль происходит из примитивной кость-формирующей мезенхимы, характеризуется продукцией остеоида при злокачественной пролиферации веретеноклеточной стромы. Кость-формирующая мезенхима может трансформироваться в костную, хрящевую или фиброзную ткани [7, 19].
Пик заболеваемости приходится на вторую декаду жизни (10 — 20 лет). Мальчики болеют чаще девочек (1,4:1). В более раннем возрасте (моложе 10 лет) преимущественно болеют девочки, у которых в этот период костный возраст больше, нежели у мальчиков. В более старшем возрасте (старше 30 лет), остеогенная саркома носит вторичный характер и возникает на почве другого патологического процесса (на фоне болезни Педжета, болезни Олье (дисхондроплазии), фибросаркомы, гигантоклеточной опухоли) [1,3,13].
Обязательным условием диагностирования остеосаркомы является формирование остеоида (патологической костной ткани).
Остеогенная саркома может быть обнаружена в любой части скелета, однако наиболее часто она поражает длинные трубчатые кости конечностей. Обычно опухоль локализуется в костях нижних конечностей (80-90%), в основном в костях, составляющих коленный сустав — в 60-80% случаев. Кости верхней конечности поражаются примерно у 1 0% больных, при этом наиболее частой локализацией опухоли является плечевая кость. В длинных трубчатых костях опухоль чаще располагается в области метафиза. Поражение плоских костей, костей стопы, кисти и позвоночника встречается крайне редко [5, 10].
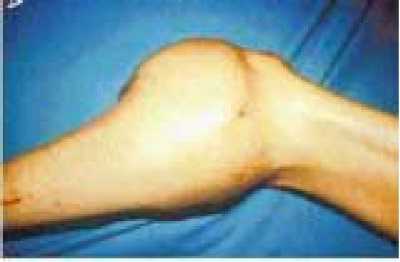
У детей средний срок появления первых симптомов заболевания до установления диагноза остеосаркомы составляет в среднем 3 месяца.
Клиническая триада остеогенной саркомы — припухлость, боли (характерны ночные боли), нарушение функции конечности. Чаще опухоль
проявляется увеличением объема конечности. При быстром росте опухоли возникает отечность мягких тканей и кожи, синюшность, что наиболее выражено в случаях поздней диагностики, когда опухоль сдавливает глубокие сосуды конечности. На 3-4 месяце от начала заболевания развивается болевая контрактура в ближайшем суставе; конечность из-за болей, как правило, не функциональна [6, 10].
Злокачественные опухоли костей, в отличие от злокачественных эпителиальных опухолей, метастазируют почти исключительно гематогенно, так как лимфатический дренаж костной ткани отсутствует. На ранних стадиях процесса гематогенное распространение опухоли проявляется метастатическим поражением легких, а затем вторичными метастазами в кости. Около 10-20% больных имеют клинически определяемые легочные метастазы в период установления диагноза.
Опухоль может давать очаги сателлиты (skip-метастазы). Skip-MTS представляют собой опухолевые очаги, располагающиеся в пределах той же самой кости, но не имеющие непосредственной связи с первичной опухолью. Как правило, они выявляются в губчатом веществе кости проксимальнее основного очага, небольших размеров, с относительно четкими контурами. Частота обнаружения skip-MTS составляет менее 1% [9].
Остеогенная саркома может поражать прилегающий сустав. Прямое прорастание через суставную поверхность наблюдается редко. Распространение опухоли на прилегающий сустав чаще всего происходит вследствие прямого перикапсульного проникновения. Трансартикулярные «прыгающие» метастазы обнаруживаются в 1% случаев. Поражение лимфатических узлов встречается в 1 0% случаев и является плохим прогностическим признаком [21].
Повышение эффективности диагностики остеогенной саркомы относится к числу весьма сложных и актуальных задач современной клинической онкологии. Знание истинного распространения опухоли необходимо как для оценки эффективности проводимой химиотерапии, так и для выбора оптимального вида оперативного вмешательства в первичном очаге. Трудности диагностики предопределили внедрение в клиническую практику специальных визуализирующих методов диагностики (КТ, МРТ, ОСГ, ангиография).
В диагностике остеогенной саркомы рентгенологический метод исследования позволяет обнаружить опухоль, выявить реакцию периоста, а также протяженность распространения не только в пределах кости, но и в мягких тканях. Проведение рентгенологического исследования в динамике позволяет судить об ответной реакции опухоли на проводимую предоперационную химиотерапию.
Рентгенологические признаки опухоли обусловлены в основном вариантом остеогенной саркомы, локализацией и распространенностью процесса.
Одним из наиболее патогномоничных рентгенологических признаков остеосаркомы принято считать наличие своеобразных остеофитов, возникающих на границе наружного дефекта компактного слоя кости и внекостного компонента опухоли, которые имеют вид характерного козырька, расположенного под углом к длинной оси кости («козырек» Кодмана). Другим симптомом, свидетельствующим о распространении опухолевого процесса за пределы кости, являются спикулы (очаги патологического костеобразования) — тонкие игольчатые участки обызвествления, располагающиеся перпендикулярно по отношению к оси кости.
Распространение опухолевого процесса на окружающие мягкие ткани приводит к образованию внекостного компонента, в котором развиваются поля оссификации разных размеров и плотности. При оценке состояния внекостного компонента саркомы выявленные в нем участки опухолевого костеобразования являются практически патогномоничным симптомом остеогенной саркомы. Внекостный компонент остеосаркомы, по данным литературы, на рентгенограммах определяется в 80-90% случаев. Все злокачественные опухоли в той или иной степени вызывают воспалительную реакцию вокруг очага, поэтому изображение внекостного компонента на рентгенограммах превышает его реальные размеры. Выраженность мягкотканого компонента прямо пропорциональна длительности опухолевого процесса.
Развитие компьютерной томографии (КТ) значительно расширило возможности определения границ распространения опухоли. Распространение мягкотканого компонента опухоли по данным КТ определяется более точно, чем на рентгенограммах за счет изменения коэффициента поглощения рентгеновских лучей опухолью. Возможности КТ ограничены лишь уточнением локализации, определением протяженности поражения кости и внекостного компонента опухоли. Магнитно-резонансная томография (МРТ) является более точным и специфичным исследованием, чем КТ. Информативность МРТ повышается благодаря отсутствию артефактов, которые имеют место при КТ-исследовании. МРТ дает хорошую дифференцировку мягких тканей, позволяя
различать нормальную, гиперваскуляризированную и опухолевую ткани. Благодаря широкому спектру регистрируемых сигналов (в частности, разности сигналов от воспалительной ткани и ткани опухоли) МРТ позволяет с большей точностью установить истинный размер и границы опухоли максимально приближенные к реальным, оценить взаимоотношение опухоли с магистральным сосудисто-нервным пучком. Исследование с контрастированием гадалиниумсодержащим препаратом (омнискан — накапливается в опухоли и четко отграничивает ее границы) улучшает изображение краев опухоли и позволяет детально исследовать распространение опухоли в пределах костномозгового канала. Интрамедуллярное распространение опухоли обычно бывает более обширным, чем мягкотканное или кортикальное поражение.
По данным МРТ можно оценить динамику опухолевого процесса после проведения предоперационной химиотерапии. В крупнейших онкологических центрах мира применяется усовершенствованный метод МРТ — DEMRI — динамический захват контрастного вещества в опухоли с определением процента его накопления, что позволяет оценить в динамике количество жизнеспособных опухолевых клеток [16]. По сравнению со всеми другими методами исследования данные МРТ подвержены наибольшим изменениям, связанным с предшествующей биопсией или манипуляцией в области опухоли.
Радионуклидная диагностика — остеосцинтиграфия (ОСГ) — получила широкое применение в выявлении различных костных заболеваний, в том числе и злокачественных опухолей. Принцип диагностики поражения кости состоит в том, что в очаге специфического поражения повышается процент накопления радиофармпрепарата (РФП), выраженность которого зависит от степени реактивного костеобразования. В настоящее время широкое применение находят фосфаты, меченные короткоживущим нуклидом 99mTc (Те- пирофосфат). Повышенное накопление РФП совершенно очевидно отражает степень интенсивности обменных процессов в участках поражения и поэтому является важным признаком активности патологического процесса. Из этого следует, что опухолевое поражение проходит раннюю стадию интенсификации обменных процессов, предшествующую развитию грубых морфологических изменений, которые удается определить рентгенологически. Тип патологического накопления РФП в большинстве случаев отмечается в виде очагов гиперфиксации. Сцинтиграфическая активность опухоли — важный индикатор ее агрессивности. Наибольшая фиксация РФП отмечалась при остеобластическом варианте остеосаркомы и относительно невысокое содержание — при остеолитическим варианте. Но некоторые очаги могут быть негативными.
Независимо от разновидности опухоли четкая визуализация контуров ее на сцинтиграммах соответствует границам интрамедуллярного и внекостного компонента новообразования.
Значительная диагностическая ценность ОСГ заключается в выявлении отдаленных метастазов остеогенной саркомы в кости и skip-метастазов. Установлено, что рентгенологическая картина метастазов в кости, как правило, соответствует типу первичной опухоли с преимущественным преобладанием остеобластических очагов.
По изменению процента накопления изотопа в динамике можно достаточно точно судить об эффективности химиотерапии. Значительное снижение процента накопления изотопа в очаге коррелирует с хорошим гистологическим ответом опухоли на химиотерапию.
Ангиография — вспомогательный метод в диагностике остеогенной саркомы. Исследование используется для более четкого определения состояния магистральных сосудов в области опухоли, а также, выявление опухолевых тромбов.
Некоторую помощь в диагностике остеогенной саркомы может оказывать определение активности щелочной фосфатазы (ЩФ). Повышение уровня ЩФ объясняют повышенной остеобластической активностью опухоли. Повышение уровня ЩФ — не абсолютный симптом.
Прогноз при генерализованных формах остеогенной саркомы у детей зависит от срока появления легочных метастазов. С целью раннего выявления легочных метастазов в детской онкологии традиционно всем больным проводится рентгенографическое исследование грудной клетки. Однако разрешающие возможности обычной рентгенографии следует считать недостаточными для ранней диагностики метастазов в легких. Срок рентгенологического выявления метастазов в легких составляет в среднем от 3-х до 8 месяцев от начала заболевания.
Для выявления легочных метастазов остеогенной саркомы методом рентгенографии необходимо, чтобы последний был представлен тенью более 10 мм в диаметре и был достаточно рентгеноконтрастен. С внедрением в клиническую практику КТ грудной клетки
стало возможным определять метастатические очаги менее 5 мм в диаметре у 10-15% пациентов, у которых метастазы не определяются на рентгенограммах. Причем, при использовании спиральной программы, стало возможным выявлять очаги в диаметре до 1 мм [12].
Биопсия необходима для морфологического подтверждения диагноза. Хирургическая стратегия предусматривает осуществление минимального вмешательства, обеспечивающего получение адекватного по объему биопсийного материала для окончательной диагностики. Лучевые методы диагностики осуществляются до проведения биопсии, т.к. хирургическая манипуляция в зоне опухоли влияет на результаты всех радиологических исследований, что затрудняет их интерпретацию [10].
Для сведения к минимуму потенциальной диссеминации опухоли, многие авторы рекомендуют предпринять попытку выполнения трепанобиопсии иглой Jamshidi. Если трепанобиопсия оказывается не адекватной, осуществляется небольшая ножевая биопсия. Аспирационная биопсия при остеогенной саркоме — мало информативна. Выполнение биопсии несоответствующими методами приводит к осложнениям в ране (диссеминация опухолевых клеток, инфицирование) у 20% пациентов. B 10% случаев неправильно спланированная и выполненная биопсия приводит к невозможности выполнить органосохраняющую операцию в первичном очаге.
Химиотерапия. До 1970 г. первичное лечение остеосаркомы конечностей без отдаленных метастазов состояло из удаления опухоли (ампутация) и/или облучения (в большой дозе) области основной опухоли. Ранние исследования роли химиотерапии при остеосаркомах были разочаровывающими; опухоль считалась химиорезистентной [11].
Сообщения об эффективных схемах химиотерапии при остеосаркоме появились в 80-х годах. В них описывалось успешное применение адриамицина, больших доз метотрексата под прикрытием лейковорина, препаратов платины и в последнее время ифосфамида. Было показано, что эти препараты способны устранить скрытые и микроскопические метастазы и улучшить выживаемость [14].
Предоперационная химиотерапия, предложенная играет основную роль в подавлении роста микрометастазов и способствует ограничению распространенности первичной опухоли. Реакция остеосаркомы на предоперационную химиотерапию может оцениваться на основании клинических, лабораторных, рентгенологических и патоморфологических характеристик. Клинически эффективность лечения проявляется уменьшением болей и отека. На лабораторном уровне о положительной реакции на лечение свидетельствует снижение ранее повышенного уровня щелочной фосфатазы. При проведении специальных методов исследования (МРТ, ОСГ) могут определяться уменьшение и/или полное исчезновение мягкотканого компонента опухоли, восстановление межмышечных промежутков, заживление патологических переломов и отложение кальция в неопластической костной ткани (кальцификация надкостницы). Ангиография представляет субъективный способ оценки выраженности реакции опухоли на химиотерапию.
«Золотым стандартом» оценки и определения реакции на лечение стали гистологические изменения, выявленные в удаленной первичной опухоли после проведения предоперационной химиотерапии. Для определения выраженности этих изменений был разработан целый ряд систем оценки, каждая из которых основывается на определении количества «жизнеспособных» опухолевых клеток в удаленных тканях. Выраженность лекарственного патоморфоза в опухоли признана главным возможным прогностическим фактором [17].
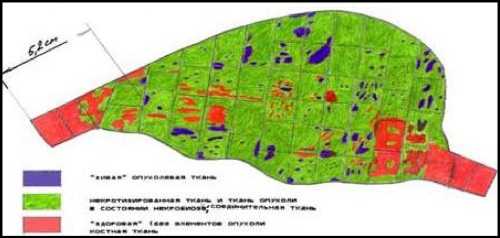
До появления эффективных противоопухолевых химиопрепаратов ряд исследователей отстаивали необходимость использования лучевой терапии в лечении первичной опухоли для того, чтобы избежать выполнения калечащих операций у больных с первоначально не определяемыми отдаленными метастазами. Но отдаленные метастазы у этих больных выявлялись в ближайшие 5-6 месяцев после окончания лучевого лечения. Во всех крупнейших зарубежных клиниках этот вопрос решен не в пользу данного метода лечения. В настоящее время, на основании проведенных исследований, доказано, что остеосаркома является высокорадиорезистентной опухолью [8]. В настоящее время лучевая терапия используется с симптоматической (противоболевой) целью, в основном, после выполнения нерадикальной операции при определенных локализациях остеосаркомы, например, в костях позвоночника или таза. И если очаг в легком находится в нерезектабельном месте, иногда решается вопрос о проведении лучевой терапии, даже учитывая, что остеогенная саркома резистентна к лучевому воздействию. Лучевая терапия может контролировать размеры огромной опухоли какое-то время (только при солитарном поражении) [8].
Хирургический этап лечения (первичный очаг).
Тщательное предоперационное планирование хирургического вмешательства и отбор больных — важнейшее условие успешного удаления первичной опухоли. Выбор метода оперативного вмешательства у больных с
остеогенной саркомой зависит главным образом от анатомической локализации. В настоящее время большинство ведущих центров, занимающихся лечением костных сарком, доказали, что органосохраняющие операции у детей являются целесообразным и адекватным методом лечения у части больных, но только при условии их правильного отбора.
Важнейшее хирургическое решение — определение границ резекции опухоли. Хотя выбор онкологической адекватности проксимальной границы резекции имеет решающее значение для предотвращения дальнейшего роста опухоли, не менее важно стремиться к «экономичности» хирургической операции, обеспечивающей максимальный потенциал для реабилитации больного. Исследования показывают, что физиологическая адаптация больных с ампутацией эквивалентна таковой у пациентов, подвергшихся органосохраняющей операции [18].
В определении уровня ампутации центральную роль играют два фактора. Первый фактор — протяженность мягкотканного компонента (полезную информацию дает КТ, МРТ) и связь с сосудисто-нервным пучком. Второй фактор — протяженность поражения кости, и, что еще важнее, степень интрамедуллярного распространения опухоли (ОСГ с 99mTc). Интрамедуллярное распространение опухоли обычно бывает более обширным, чем мягкотканный компонент. Традиционно уровень ампутации определяется примерно на 7 — 8 см выше проксимальной границы мягкотканного и интрамедуллярного компонентов опухоли. При хорошем ответе опухоли на предоперационную химиотерапию граница резекции может быть уменьшена до 3 — 5 см.
Сохраняющая конечность операция рассматривается в настоящее время как предпочтительный метод лечения у тщательно отобранных больных с остеогенной саркомой. Необходимо подчеркнуть, что в настоящее время метастазы в легкие не являются противопоказанием к выполнению органосохраняющих операций [5].
Ампутация (калечащая операция) осуществляется в тех случаях, когда первичная опухоль оказывается нерезектабильной. Основным фактором, побуждающим к проведению ампутации,
является вовлечение сосудисто-нервного пучка (особенно магистрального нерва). Вспомогательными факторами являются — значительное рассеивание опухолевых элементов вследствие плохо спланированной и проведенной биопсии или наличие патологического перелома [15].
Хирургическое лечение метастазов остеосаркомы в легкие. Последнее десятилетие характеризуется значительным прогрессом в лечении генерализованных форм остеогенной саркомы, прежде всего в тех случаях, когда имеются признаки метастатического поражения легких. Наметившиеся положительные тенденции в терапии этого контингента больных обусловлены появлением новых активных химиотерапевтических протоколов и возможностью определения гистологического ответа в метастатической опухоли на лечение. Применение химиотерапии и радикальное удаление солитарных и единичных метастазов позволили добиться 5-летней выживаемости у 30 — 35% больных с легочными метастазами [20].
Читайте также:
therapycancer.ru
симптомы, причины, лечение, профилактика, осложнения
Причины
Злокачественное образование, именуемое остеосаркомой, возникает при стремительном росте костей у детей. Такие больные отличаются высоким, не соответствующим возрасту ростом. Остеогенная саркома поражает растущие участки скелета.
Этот недуг может развиться на фоне полученной травмы, перелома либо ушиба кости.
В группе риска данного злокачественного процесса подростки, имеющие генетическую предрасположенность, или имеющие доброкачественные образования костных тканей.
Провоцирующим фактором является и ионизирующее излучение в период гормонального роста.
Симптомы
Симптоматическая картина не сразу позволяет заподозрить у ребёнка онкологическое заболевание, поэтому остеогенная саркома часто обнаруживается не на первой стадии, а позднее, когда признаки недуга довольно сильные:
- Первым признаком заболевания является появление боли. К сожалению, не всегда на болевой синдром обращают внимание родители, дети часто получают травмы и многие тянут до последнего, прежде, чем обратиться к врачу.
- Болевые ощущения локализуются вокруг сустава. Боль характеризуется тем, что не проходит с течением времени, а напротив, усиливается. Если держать поражённую конечность в состоянии покоя, то она всё равно будет болеть. Иногда болевой синдром становится более сильным в ночное время суток.
- Поражённое место может припухать, краснеть, на нём проявляется сетка вен и сосудов.
- Иногда у больных наблюдается повышение температуры.
Диагностика остеогенной саркомы у ребёнка
Врач беседует с пациентом и его родителями, изучает анамнез болезни и анамнез жизни больного, выслушивает имеющиеся жалобы. Особенно важно обследоваться ребёнка полностью:
- Рентгенографическое исследование, посредством него возможно выяснить наличие остеосаркомы у пациента, обнаружить мягкотканые компоненты, аномальные переломы, выявить размер образования. На рентгенографическом снимке можно наблюдать метафизарную локальность, формирующуюся в трубчатых костях; выяснить, имеется ли васкуляризация; игольчатый периостит; в ходе рентгена органов дыхания создаётся информация о мелких метастазах.
- Морфологические исследования остеогенной саркомы, представляющие собой выполнение биопсии и трепанобиопсии.
- Выполнение остеосцинтиграфии, которая позволяет выявить повышенное количество изотопов.
- Для выяснения локализации образования, его размеров, характере распространения на мягкие ткани и суставы, требуется пройти компьютерную томографию, метод позволяет обнаружить микрометастазы, не видные на рентгенографическом исследовании.
- Посредством МРТ-диагностики возможно выяснить каким именно образом злокачественное образование воздействует на окружающие ткани, сосудисто-нервные сплетения, а также наблюдать динамику злокачественного процесса после проведения химиотерапии, судить об её эффективности.
- Перед хирургическим вмешательством в обязательном порядке осуществляется ангиография, которая позволяет обнаружить, повлияло ли образование на сосуды, и тем самым планировать операцию с сохранением органов.
Особенно важным является дифференцировать данное онкологическое заболевание от других злокачественных процессов.
Осложнения
При своевременном обращении к врачу и проведении хирургической органосохраняющей операции осложнений удаётся избежать. При затягивании терапии и не соблюдении назначений специалистов остеосаркома может прорастать вглубь тканей, и тогда приходится ампутировать поражённую конечность. Выживаемость данного недуга равняется 80 процентам.
Лечение
Что можете сделать вы
При наличии болей у ребёнка необходимо сразу обращаться к врачу. Такой популярный симптом может сигнализировать о развитии остеосаркомы, в особенности это касается подростов в период их полового созревания.
Самолечение не рекомендуется проводить, так как эффекта таким образом вы не добьётесь, а навредить сможете.
Что делает врач
В случае возникновения злокачественных процессов в организме, включая появление остеогенной саркомы, как правило, используют три ключевых варианта лечения: оперативное вмешательство, химио- и лучевую терапию.
Перед тем как выполнить хирургическую операцию необходимо провести химиотерапию для того, чтобы снизить количество мелких метастазов в дыхательных путях, сократить объёмы имеющейся злокачественной опухоли и оценить гистологический результат онкообразования на выполнение химиотерапии. Всё это даёт возможность определить методику проводимого лечения.
Проведение операции. Этот способ лечения является обязательным и максимально эффективным. В настоящее время прибегают к органосохраняющим операциям, в результате которых иссекается лишь поражённый опухолевыми клетками сегмент костной ткани, который затем заменяется имплантатом. Если образование прорастает в мягкие ткани, возникают патологические переломы и другие аномальные процессы,осуществляется ампутация поражённой конечности. Возникновение метастазовне является препятствием для выполнения органосохраняющих операций.
После выполненного оперативного вмешательства назначается химиотерапия.
Осуществление лучевой терапии признано менее эффективным, чем выше перечисленные способы терапии, так как злокачественные клетки остеосаркомы не являются чувствительными к такому виду излучения. Курс лучевой терапии может быть показан, если противопоказано проведение операции.
Профилактика
Специальных профилактических мер, позволяющих не заболеть остеосаркомой, не имеется. Необходимо внимательно относится к здоровью своего ребёнка, при возникновении болей в костях и суставах обращается к врачу, лечить предраковые заболевания.
Оцените материал:
спасибо, ваш голос принят
Также смотрят
Вооружайтесь знаниями и читайте полезную информативную статью о заболевании остеогенная саркома у детей. Ведь быть родителями – значит, изучать всё то, что поможет сохранять градус здоровья в семье на отметке «36,6».
Узнайте, что может вызвать недуг , как его своевременно распознать. Найдите информацию о том, каковы признаки, по которым можно определить недомогание. И какие анализы помогут выявить болезнь и поставить верный диагноз.
В статье вы прочтёте всё о методах лечения такого заболевания, как остеогенная саркома у детей. Уточните, какой должна быть эффективная первая помощь. Чем лечить: выбрать лекарственные препараты или народные методы?
Также вы узнаете, чем может быть опасно несвоевременное лечение недуга остеогенная саркома у детей, и почему так важно избежать последствий. Всё о том, как предупредить остеогенная саркома у детей и не допустить осложнений.
А заботливые родители найдут на страницах сервиса полную информацию о симптомах заболевания остеогенная саркома у детей. Чем отличаются признаки болезни у детей в 1,2 и 3 года от проявлений недуга у деток в 4, 5, 6 и 7 лет? Как лучше лечить заболевание остеогенная саркома у детей?
Берегите здоровье близких и будьте в тонусе!
detstrana.ru
33. Остеогенная саркома. Виды. Клиника. Диагностика. Лечение.
Остеогенная саркома — саркома, злокачественные клетки которой происходят из костной ткани и продуцируют эту ткань. В некоторых из этих опухолей доминируют хондробластические или фибробластические компоненты.
Виды:рентгенологически подразделяется на:
-остеолитическую,
-остеопластическую (склеротическую)
-смешанную формы.
Кроме того выделяют:
1)Телеангиэктатическая остеосаркома. При рентгенологическом ее рассмотрении данная форма саркомы имеет сходство с гигантоклеточной опухолью и с аневризмальной костной кистой, особенности ее заключаются в формировании литических очагов, в которых отмечается слабо выраженная форма склерозирования. В целом же отличия от традиционного течения остеосаркомы в данном случае не наблюдается, равно, как и практически отсутствуют отличия по части ответа на производимое лечение (химиотерапия).
2)Параоссальная (юкстакортикальная) остеосаркома. Произрастает со стороны коркового костного слоя, ткань опухолевого образования может окружать кость по всем ее сторонам. В большинстве случаев не происходит произрастания данного процесса к костномозговому каналу. Мягкотканного компонента в этом случае нет, из-за чего существует возможность неверного дифференцирования опухолевого образования от такого образования как остеоид (под остеоидом понимается такая стадия формирования костной ткани, которая предшествует стадии минерализации за счет межклеточного ее вещества). Во многих случаях такая опухоль характеризуется низкой степенью собственной злокачественности, скорость течения патологического процесса незначительная, метастазов практически нет. Следует учитывать, что при неадекватной терапии опухоль склонна к рецидивированию, то есть к повторному росту и развитию, что допускается даже в таком случае, если хирургическое удаление опухолевого образованиябыло произведено неадекватным образом или с остатком одной/нескольких его клеток. Более того, в таком случае не только допускается рецидивирование, но и усиление злокачественности характера вновь образованного опухолевого образования, что, соответственно, ухудшает общую картину течения заболевания и прогноз по нему.
3)Периостальнаяостеосаркома. Аналогично предыдущему варианту, расположение опухолевого образования сосредотачивается вдоль костной поверхности, собственно и течение заболевание характеризуется сходством с вышеописанной формой процесса. Опухолевое образование располагает мягкотканным компонентом, проникновения к костномозговому каналу не происходит.
4)Интраоссальнаяостеосаркома. Данная форма опухолевого образования характеризуется низкой степенью собственной злокачественности и минимальной степенью атипичных процессов на клеточном уровне. По этой причине подобные опухолевые образования могут быть определены в качестве доброкачественных опухолей при диагностике. Между тем, здесь, как и в одном из рассмотренных выше вариантов, существует риск рецидивирования процесса, при котором опухолевое образование может перейти к более злокачественной форме прогрессирования.
5)Мультифокальная остеосаркома. Такого типа опухоль проявляется в качестве множественного типа очагов, формирующихся в костях, очаги эти схожи друг с другом. Прогноз по саркоме в данном случае рассматривается как фатальный для больных.
6)Экстраскелетнаяостеосаркома. Данного типа опухоль диагностируется достаточно редко. Ее особенность заключается в продуцировании остеоида либо костной ткани, в некоторых случаях в сочетании с хрящевой тканью, происходит это в мягких тканях, преимущественно в области нижних конечностей. Между тем, допускаются и другие варианты поражений, например, почек, кишечника, гортани, пищевода, сердца, мочевого пузыря, печени и пр. Для заболевания прогноз определяется плохой, проведение химиотерапии не сопровождается достаточной степенью чувствительности. Установление диагноза по данной форме саркомы может быть произведено лишь после того, как будет исключено наличие костных очагов опухолевого образования.
7)Мелкоклеточная остеосаркома. В данном случае речь идет о высокозлокачественной форме течения патологического процесса. Особенности морфологического строения отличают опухоль от остальных вариантов, в связи с чем и выделено именно такое ее определение. Чаще всего локализация опухолевого образования сосредотачивается со стороны бедренной кости, в обязательном порядке течение процесса сопровождается продуцированием остеоида.
8)Остеосаркома таза. Характерной особенностью опухолевого образования является стремительность его развития и общая широта его распространения по тканям и по областям, его окружающим. Объясняется это особенностями анатомического строения тазовой области, что, в свою очередь, обуславливает отсутствие анатомических и фасциальных барьеров для такого распространения. Возникая непосредственно из элементов кости, она характеризуется бурным течением и склонностью рано давать метастазы. Остеогенная саркома наблюдается в любом возрасте, но около 65 % всех случаев падает на период от 10 до 30 лет, и чаще всего развитие саркомы отмечается в конце полового созревания.Мужчиныпоражаются в два раза чаще, чемженщины. Излюбленной локализацией являются длинныетрубчатые кости; на долюплоскихикороткихкостейпадает не больше одной пятой части всех остеогенных сарком. Костинижних конечностейв 5-6 раз чаще поражаются, чем костиверхних конечностей, и 80 % всех опухолей нижних конечностей гнездятся в области коленного сустава. Первое место по частоте занимаетбедро, на долю которого падает половина всех остеогенных сарком, затем следует большеберцовая кость, плечевая, тазовые кости, малоберцовая, плечевой пояс, локтевая кость. Лучевая кость, где так часто наблюдаетсягигантоклеточная опухоль, исключительно редко дает рост остеогенной саркомы. Почти никогда остеогенная саркома не исходит из надколенника. Поражение черепа имеет место главным образом в детском возрасте, а также в старости в качестве осложнения обезображивающей остеодистрофии. Типичной локализацией остеогенной саркомы в длинных трубчатых костях является мета-эпифизарный конец, а у детей и юношей, до наступления синостоза, —метафизкости. В бедренной кости поражается обыкновенно дистальный конец, но около 10 % остеогенных сарком бедра гнездятся вдиафизеи оставляют метафизы нетронутыми. В большеберцовой кости остеогенная саркома только в одном случае из десяти располагается в дистальном конце — типичным местом служит проксимальный медиальныймыщелок. Таким же типичным местом для плечевой кости является область шероховатостидельтовидной мышцы.Начало заболевания не всегда удается точно определить. Неясные тупые боли появляются вблизи сустава, так как первично опухоль локализуется чаще всего вблизи метафизарного отдела трубчатой кости. Возникает боль в суставе без объективных признаков выпота в нём, часто после травмы в прошлом. По мере расширения границ опухоли и вовлечения в процесс соседних тканей боли усиливаются. Появляются отчётливое утолщение метадиафизарного отдела кости, выраженная пастозность тканей, венозная сеть кожи ясно определяется. К этому времени возникает контрактура в суставе, увеличивается хромота. При пальпации — резкая боль. Сильные ночные боли, не снимаемые анальгетиками и не связанные с функцией конечности и не утихающие даже при фиксации в гипсе. Опухоль стремительно распространяется по соседним тканям, быстро заполняет костномозговой канал, прорастает мышцы, очень рано дает обширные гематогенные метастазы, особенно в лёгкие, головной мозг; метастазы в кости крайне редки.
Диагностика:
1.Рентгенодиагностика остеогенных сарком несложна. Для начальных стадий характерен остеопороз кости, контуры опухоли смазаны, за пределы метафиза она не распространяется. Вскоре намечается дефект костной ткани. В некоторых опухолях отмечаются пролиферативные, остеобластические процессы. В этих случаях отслоенная надкостница веретенообразно вздута, иногда, прерываясь, дает картину «козырька» или «треугольника Кодмена». Характерен, особенно у детей, игольчатый периостит, когда остеобласты продуцируют костную ткань по ходу кровеносных сосудов, то есть перпендикулярно кортикальному слою, образуя так называемые спикулы.
2.Морфологическое исследование опухоли. Одной из частых причин невозможности проведения органосохраняющей операции является неудачно проведенная биопсия с местным обсеменением опухолевыми клетками, развитием патологического перелома. Поэтому биопсия должна проводиться хирургом и предпочтительнее проводить трепанобиопсию, нежели ножевую биопсия (для максимальной защиты прилежащих к опухоли тканей от контакта с биоптатом). 3. Остеосцинтиграфия (ОСГ) с Te-99 — позволяет выявить другие очаги в костях, хотя повышение накопления изотопа не является специфическим. При проведении ОСГ в динамике по изменению процента накопления изотопа в очаге до- и после химиотерапии, можно достаточно точно судить об эффективности химиотерапии. Значительное снижение процента накопления изотопа в очаге достаточно точно коррелирует с хорошим гистологическим ответом опухоли на химиотерапию. 4. Компьютерная томография (КТ) очага — позволяет выявить точную локализацию опухоли, ее размеры, отношение опухоли к окружающим тканям, распространение ее на сустав. КТ легких позволяет выявить микрометастазы, не выявляемые рентгенологически. 5. Магниторезонансная томография (МРТ). Наиболее точный метод контрастирования опухоли, выявляющий ее отношение к окружающим тканям, сосудисто-нервному пучку, а также позволяющий определить динамику процесса при проведении химиотерапии, ее эффективность и, соответственно, планировать объем операции. В настоящее время МРТ проводится с контрастом, содержащим гадолиниум, который накапливается по периферии опухоли, четко отграничивая ее. В крупнейших онкологических клиниках мира используется усовершенствованный метод — DEMRI — динамический захват контрастного вещества, определяемый при МРТ. С помощью компьютера производится количественное определение (в%) опухолевых клеток, накапливающих контраст до- и после химиотерапии, тем самым определяя гистологический ответ опухоли на лечение еще в предоперационный период. 6.Ангиография — проводится перед операцией. Этим методом выявляют свободны или нет сосуды от опухоли, что определяет объем операции. При наличии в сосудах опухолевых эмболов, проведение органосохраняющей операции невозможно.
Дифференциальный диагноз остеогенной саркомы проводят между хондросаркомой, эозинофильной гранулемой, хрящевыми экзостозами, остеобластокластомой.
Лечение остеогенной саркомы включает в себя следующие стадии: 1. Предоперационная химиотерапия для подавления микрометастазов в легких, уменьшения размеров первичного очага опухолеобразования и оценки гистологического ответа опухоли на химиотерапию, что определяет дальнейшую методику лечения. Для лечения остеогенной саркомы в настоящее используются следующие препараты: высокодозный метотрексат, адрибластин, ифосфамид, препараты платины, (карбоплатин, цисплатин), этопозид. 2. Обязательная операция. Если ранее прибегали к обширной операция, зачастую включающую в себя ампутацию всей конечности, то в настоящее время ограничиваются щадящей операцией. При этом удаляют лишь части кости с заменой её на имплантат из пластика, металла или трупной кости. От органосохраняющей операции отказываются в тех случаях, когда опухоль прорастает сосудисто-нервный пучок, если произошел патологический перелом, а также при больших размерах опухоли и её прорастании мягких тканей. Наличие метастазов не является противопоказанием к органосохраняющей операции. Крупные метастазы в легких также удаляются хирургически. 3. Послеоперационная химиотерапия с учетом результатов предоперационной химиотерапии. Лучевая терапия для лечения малоэффективна в силу того, что клетки остеогенной саркомы малочувствительны к ионизирующему излучению. Лучевую терапию проводят в том случае, если по какой-либо причине операция невозможна.
studfiles.net
Остеогенная саркома у детей — Детская хирургия
Остеогенная саркома у детей — злокачественная опухоль, переходящая из остеобластов, продуцирующих атипичное костное вещество.
Эпидемиология. У детей составляет 56% костных злокачественных опухолей. Ежегодно регистрируются 2-3 случая заболевания на миллион населения.
Более 50% остеогенных сарком у детей локализуются в зонах интенсивного роста костей: дистальный метафиз бедренной кости (50%), проксимальный метафиз большеберцовой кости (26%), метафизы плечевой кости (10%).
Морфология.
Макроскопически характеризуется узловатым образованием, белесоватой мягкой ткани, напоминающей рыбье мясо, внутри которого имеются очаги расплавления и кровоизлияний.
Микроскопически: полиморфные веретенообразные клетки; выраженным митотическим и амитотическим делением.
Симптомы остеогенной саркомы у детей
Боль в пораженной конечности — ранний и ведущий симптом. Особенностью ее является постоянный характер: она не стихает во время сна и в покое.
Припухлость в области расположения опухоли, без четких контуров, плотной консистенции, умеренно болезненная.
Нарушение функции конечности обусловлено прорастанием опухолью мягких тканей, их сдавлением и ограничением движения в суставе.
Диагностика остеогенной саркомы у детей
Лабораторная диагностика повышение уровня лактатдегидрогеназы, щелочной фосфатазы свидетельствует об интенсивности процессов костеобразования в опухоли.
Рентгенологическое исследование.
— Начальная стадия характеризуется остеопорозом, смазанностью и нечеткостью контуров опухоли.
— Остеолитическая форма характеризуется разрушением коркового слоя кости, отслоения надкостницы («симптом козырька»), наличием линейных теней, расположенных перпендикулярно кости, обусловленных образованием костных игл вдоль стенок кровеносных сосудов («симптом спикул»). Спикулы служат рентгенологическим признаком прорастания опухоли в мягкие ткани.
— Остеобластическая форма характеризуется преобладанием пролиферативных процессов и рентгенологически проявляется избыточной костной тканью.
— Смешанная форма проявляется симптомом игольчатого периостита, переходом опухоли в мягкие ткани, быстрым ростом, разрушением кортикального слоя кости и надкостницы, отсутствием распространения опухоли в эпифиз.
Лечение остеогенной саркомы у детей
Основной метод лечения — радикальная операция, направленная на удаление всей опухоли е пределах здоровой ткани. Химиотерапия — является важной частью комплексного лечения. Лучевая терапия используется в комбинации с химиотерапией.
Прогноз при остеогенной саркоме у детей — выживаемость в течение 5 лет после радикальной операции составляет 25-30%.
Статью подготовил и отредактировал: врач-хирург Пигович И.Б.
Видео:
Полезно:
surgeryzone.net
Остеогенная саркома — Новообразования остеогенного происхождения — Болезни костей у детей — Kelechek.ru
Остеогенная саркома — исключительно злокачественная и наиболее часто встречающаяся форма первичной злокачественной опухоли кости у детей. Согласно нашим данным она составляет 4,5% всех случаев диспластических заболеваний и 62% костных злокачественных опухолей у детей.
По нашим данным, на долю остеогенных сарком приходится 18% всех случаев злокачественных опухолей разных тканей. Если для людей пожилого возраста при злокачественном бластоматозном поражении костей характерны метастатические опухоли, то для детей и подростков — первичная остеогенная саркома.
К остеогенной саркоме относятся первичные новообразования, которые исходят из самой кости, развиваются из элементов собственно костной ткани (в том числе из надкостницы) и состоят из мезенхимальных недифференцированных клеток, участвующих в условиях нормального развития в образовании соединительной, хрящевой и костной ткани.
Термин «остеогенная саркома» предложен Ewing в 1920 г. Автор вкладывал в это название довольно широкое понятие. Так он обозначал все саркомы, возникающие в кости. Н. Н. Петров, Kolodny и др. под названием «остеогенная саркома» понимали злокачественные опухоли, образовавшиеся из клеток, которые потенциально могли стать костными, т. е. авторы включали в это понятие и соединительнотканные, и мукоидные, и хрящевые саркомы кости. Мы под этим наименованием имеем в виду первичные злокачественные опухоли кости, образующие опухолевую остеоидную или костную ткань.
Распространенный в литературе термин «остеосаркома» — понятие широкое и, с нашей точки зрения, нерациональное.
Под ним можно подразумевать любую форму саркомы скелета: остеогенную саркому, хондросаркому, фибросаркому, параоссальную саркому. Рассматривая саркомы с точки зрения их генеза, мы включили в группу остеогенных сарком злокачественные остеобластокластомы, клинико-рентгенологически ничем не отличающиеся от полиморфноклеточных остеогенных сарком и диагностированные лишь при тщательном изучении патологоанатомами. Хондросаркоме кости посвящена отдельная глава в книге.
«Болезни костей у детей», М.В.Волков
Лечение хондром длинных трубчатых костей в связи с возможными случаями малигнизации следует проводить с помощью резекций кости и удаления опухоли в пределах здоровых тканей. Рецидивировапие хондром — редкое явление. Оно возникает при заведомо неполном удалении опухоли. Резекция длинной трубчатой кости по поводу хондромы может носить характер краевой резекции, если есть уверенность в полном удалении опухоли….
Дифференциальную диагностику первичной хондросаркомы следует проводить с хондромой, остеогенной саркомой, хондробластомой и хондромиксоидной фибромой. Наибольшие трудности для распознавания представляют ранние формы опухолей. При этом основную помощь оказывает гистологическое исследование. Хондрома имеет не только доброкачественные признаки клинического и рентгенологического характера, но и приведенные выше морфологические особенности. Хондробластому легко отличить при гистологическом исследовании ввиду гигантоклеточного ее строения….
Прогноз при хондромах у детей следует определять осторожно, так как в функциональном отношении больных ожидают большие деформации, а прогноз для жизни плохой при хондромах длинных трубчатых костей и при множественных хондромах, которые могут малигпизироваться у взрослых. Herzog (1944) сообщил о 38-летнем больном, у которого в возрасте 1,5 лет были обнаружены множественные хондромы. В возрасте 16…
Лечение больных с хондросаркомой состоит в радикальном хирургическом вмешательстве в сочетании с лекарственной противоопухолевой терапией. Лучевая терапия, по единодушному мнению авторов, при хондросаркоме безуспешна. Она лишь временно ослабляет боли, слегка задерживая рост опухоли, что имело место в анемнезе у 2 наших больных. По данным некоторых исследователей (Hatcher, 1956), лучевая терапия даже вредна, так как приводит…
Хондробластома кости относится к новообразованиям скелета, довольно редко встречающимся и недостаточно изученным. Согласно нашим данным, она встретилась в 1,1% случаев среди истинных опухолей скелета и дисплазии у детей. По статистике Kunkell, Dahlin и Young (1956), у лиц разного возраста хондробластома составляет 1 % по отношению ко всем первичным опухолям костей. В 1931 г. Codman, располагая…
www.kelechek.ru
Остеогенная саркома (дифференциальная диагностика) — Новообразования остеогенного происхождения — Болезни костей у детей — Kelechek.ru
Если ранняя, своевременная диагностика сарком костей представляет у детей большие трудности, то дифференциальная диагностика является не менее сложным разделом костной, патологии детского возраста. Числу поступивших больных с различными саркомами костей на нашем материале приблизительно соответствует число детей, направленных с диагнозом злокачественной опухоли костей, который не подтвердился.
Большие трудности возникают при дифференциальной диагностике с саркомой Юинга и ретикулярной саркомой кости. Точное установление диагноза имеет важное практическое значение. В отличие от остеогенной саркомы опухоль Юинга поражает диафизы длинных трубчатых костей. Чаще болям предшествует появление опухоли. В отдельных случаях саркомы Юинга начало заболевания может напоминать острый воспалительный процесс, а в ранних стадиях остеогенной саркомы этого не наблюдается.
На рентгенограмме при саркоме Юинга полностью разрыхлен корковый слой кости и увеличена толщина кости в виде напластований коркового слоя, а также расширен костномозговой канал, так как он исходит из клеток костного мозга (эндотелиальиая миелома). Вместе с тем в отдельных случаях клинико-рентгенологическая близость остеогенной саркомы, опухоли Юинга и ретикулосаркомы столь велика, особенно при поражении плоских костей, что диагноз у ряда наших больных был правильно установлен лишь после биопсии или на секции.
Не меньшие трудности представляет дифференциация остеогенной саркомы с другими редко встречающимися в детском возрасте видами сарком, которым мы даем ниже краткую характеристику. Первичная хондросаркома кости (в том числе у детей) отличается большими размерами, так как опухоль определенное время может расти бессимптомно, долго не давая метастазов.
В ряде случаев диагноз уточняется только после гистологического исследования. Наличие хрящевых элементов в саркоматозной опухоли еще не говорит в пользу хондросаркомы. Такие элементы в пассивном, непролиферирующем состоянии могут быть и при остеогенной саркоме.
«Болезни костей у детей», М.В.Волков
Как и все первичные доброкачественные истинные новообразования, хондрома характеризуется солитарным очагом в одной кости. Так называемые множественные хондромы в подавляющем большинстве случаев являются вторичными новообразованиями, сопровождающими диспластический системный процесс скелета — дисхондроплазию (хондроматоз костей), экзостозную множественную хондроплазию, деформирующую суставную хондродисплазию. В этих случаях можно говорить об осложнении дисплазии и о переходе очага в истинную опухоль…
Большое значение в установлении правильного диагноза имеют общее состояние больного и специфические реакции, а также динамические изменения в очаге в ответ на иммобилизацию и специфическое лечение, тогда как последние совершенно не оказывают влияния на развитие опухоли. Солитарная энхондрома может быть принята за хондробластому вследствие возможных включений обызвествленного хряща в структуре опухоли, которые при хондроме грубее…
Локализация хондром существенно отличается от локализации костно-хрящевых экзостозов, что иногда является одним из клинических и диагностических признаков. Излюбленной локализацией хондром являются плюсневые и пястные кости, фаланги пальцев кистей и стоп, затем ребра и грудина, т. е. кости, имеющие наибольшее количество хрящевой ткани (суставные хрящи, хрящевой состав тела грудины, ребер). У половины наших больных были поражены…
Дифференциальная диагностика усложняется близостью гистологического строения хондробластомы и хондромиксоидной фибромы, а также возможностью существования смешанных форм, описанных Dahlin (1957), Lichtenstein и Bernstein (1957), Р. Е. Житницким (1964). В одном из наших случаев у мальчика 10 лет, которого мы наблюдаем в течение последних 9 лет, имела место хондробластома правой большеберцовой кости. Ему была произведена краевая резекция…
Энхондромы исходят из области кортикального слоя, примыкая как к диафизу, так и к метафизу. Боли при экхондромах возникают лишь после того, как последние достигают значительных размеров и наступает сдавление окружающих тканей, в то время как при энхондромах болезненность связана с разрушением надкостницы. В результате разрастания хондром на кистях и стопах образуются деформации, мешающие функции. При…
www.kelechek.ru