ЛЕКЦИЯ Гемобластозы
ГЕМОБЛАСТОЗЫ
• Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
В последние годы в литературе широко обсуждается вопрос о существовании предопухолевой стадии лейкозов и лимфом. Предлагаются термины «предлейкоз» и «предлимфома» для обозначения состояний с различными качественными и количественными изменениями кроветворной ткани, нередко предшествующими развитию гемобластозов.
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобластов Доказывается наблюдениями за пациентами, заболевшими лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатических препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобластного лейкоза и эритромиелоза.
Роль вирусов в качестве этиологического фактора гемобластозов трактуется неоднозначно. В развитии гемобластозов человека доказано участие лишь двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и Т-лимфоцитарного вируса лейкоза человека первого типа (Т-клеточная лимфома и Т-клеточные лейкозы). Имеются экспериментальные данные, доказывающие прямое канцерогенное действие вирусов на гемопоэтические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хромосом (болезни Клайнфелтера, Тернера), а также существованием «лейкозных семей». Нередко лейкозы развиваются у пациентов с наследственными дефектами иммунитета (атаксия телеагиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдриджа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздействуя на стволовые и полустволовые гемопоэтические клетки, пр» водят к одинаковым результатам — злокачественной трансформации. Следовательно, существует так называемое узкое место, через которое могут осуществлять свое воздействие различив агенты. Такое место, вероятнее всего, находится в геноме клеток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лимфоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген c-myc из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрокной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тирозинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лимфоцитарных лейкозах и лимфомах — в локусе 11q гена а-цепочек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигнизации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами где рост и дифференцировка клеток происходят только в Присутствии факторов роста или стромальных клеток. Стромальные клетки, вероятно, также выделяют факторы роста, святые с их клеточными мембранами, а также гепарансульфатами стромы, обеспечивая тем самым локальный рост.
Схема 34. Структура гемопоэтической системы
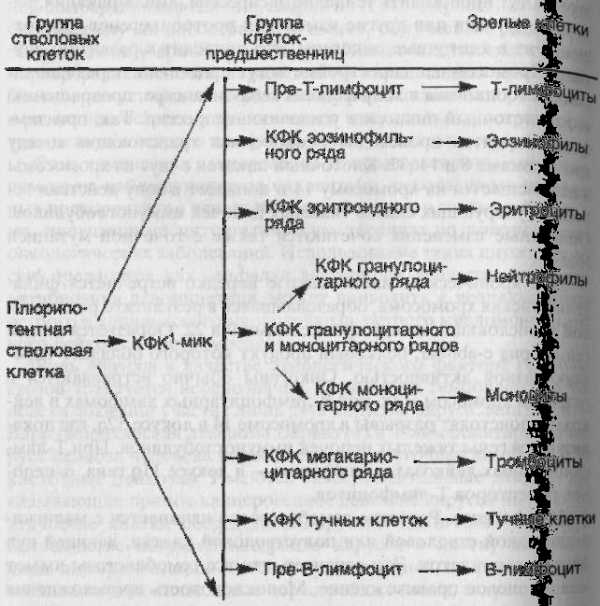
1 – Колониеформирующая клетка, син. колониеобразующая клетка (КОЕ).
Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мал изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лейкозных клеток с участием особых факторов и контактного торможения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и властные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритромиелобластный, мегакариобластный, недифференцированный. Иронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лимфоцитарного происхождения (хронический лимфолейкоз, парапротеинемические лейкозы: миеломная болезнь, первичная макроглобулинемия Вальденстрема, болезнь тяжелых цепей Франклина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарц 0, го происхождения (хронический моноцитарный лейкоз, гистиоцитоз X).
Иммунный фенотип опухолевых клеток в настоящее время стало возможным проводить более точное типирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50 — 80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Острые лейкозы
Различные формы острого лейкоза имеют стереотипные морфологические проявления: лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек. Размеры и очертания ядер, а также ширина ободка цитоплазмы могут варьировать. Бласты составляют 10—20 % костномозговых клеток. Цитогенетическую принадлежность бластов, как правило, можно выявить только с помощью специальных методов исследования — цитохимических и иммуногистохимических. Применяются реакции на пероксидазу, окраска на липиды Суданом черным, ШИК-реакция, гистоферментохимические реакции на выявление неспецифической эстеразы, хлорацетатэсте разы, кислой фосфатазы. Иммуногистохимически возможно определение маркеров В-, Т-лимфоцитов, клеток миелоидного моноцитарного рядов.
В периферической крови и в костном мозге описывается Феномен лейкемического провала («hiatus leucemicus»), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм.
В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретикулярных волокон, нередко развивается миелофиброз. При цитостатической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань.
Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. В связи с лейкозной инфильтрацией слизистых оболочек полости рта и ткани миндалин появляются некротический гингивит, тонзиллит — некротическая ангина. Иногда присоединяется вторичная инфекция и развивается сепсис, приводящий больных к смерти.
В результате тромбоцитопении, повреждения печени и стенок сосудов у больных острыми лейкозами нередко возникает геморрагический синдром вплоть до развития смертельных осложнений — кровоизлияний в головной мозг и желудочно-кишечных кровотечений.
Использование активной цитостатической терапии повлияло на течение острых лейкозов, т.е. привело к индуцированному лекарственному патоморфозу. В связи с этим в настоящее время выделяют следующие клинические стадии заболевания: первая атака, ремиссия (полная или неполная), рецидив (первый, повторный).
Наибольшее значение среди острых лейкозов имеют острый лимфобластный и острый миелобластный лейкозы.
Острый лимфобластный лейкоз. Самый распространенный лейкоз в детском и юношеском возрасте. Пик заболеваемости приходится на возраст от 1 года до 6 лет. Протекает с поражением костного мозга, лимфатических узлов, селезенки, вилочковой железы, а также других органов. Центральная нервная система обычно вовлекается при рецидивах заболевания после химиотерапии. В костном мозге, периферической крови и в других органах обнаруживаются опухолевые клетки типа лимфобластов с ШИК-положительными гранулами в цитоплазме, не дающие реакций на пероксидазу, эстеразы и не содержащие липиды.
В 2/3 случаев в опухолевых клетках обнаруживаются цитогенетические нарушения в виде полиплоидии, филадельфийской хромосомы и реципрокной транслокации между хромосомами 8 и 14.
Цитогенез острого лимфобластного лейкоза связан с предшественниками Т- и В-лимфоцитов. На Т-клеточные лейкозы в гранах Европы приходится 10—15 % наблюдений. Преобладают В-клеточные лейкозы.
Руководствуясь иммунологическими фенотипами опухолевых клеток выделяют несколько форм лимфобластного лейкоза, что имеет значение для выбора терапии и прогноза. Преобладающие В-лимфобластные лейкозы представлены ранним, промежуточным и поздним вариантами, отличающимися по экспрессии пара, глобулина CD 10, поверхностного иммуноглобулина и активности терминальной диоксинуклеотидтрансферазы. Маркерами Т-лимфобластного лейкоза являются антигены CD7 и Т-рецепторов.
У детей преобладает промежуточный вариант, у взрослых —_ ранний и промежуточный. Прогноз у детей значительно лучше чем у взрослых. Выживаемость составляет соответственно 60 и 30 %. Наихудший прогноз при Т-лимфобластном лейкозе.
Острый миелобластный лейкоз. Наиболее частая форма заболевания у взрослых с относительно хорошим прогнозом — ремиссии наступают у 70—80 % больных, полные ремиссии — у 25 % больных.
Описываются наблюдения развития острого миелобластного лейкоза у людей, подвергшихся радиационному воздействию, контактирующих с бензолом (кожевенная индустрия в Турции, производство синтетических клеев и др.), принимавших цитостатические препараты, а также у страдающих наследственными заболеваниями — болезнью Дауна, анемией Фанкони, синдромом Блума.
Опухолевые клетки имеют типичные для миелобластов цитохимические маркеры: ШИК-положительную диффузно окрашенную цитоплазму, содержат липиды, пероксидазу, эстеразы. Опухолевые клетки инфильтрируют костный мозг, приобретающий макроскопически пиоидный вид, селезенку, печень, лимфатические узлы, слизистую оболочку желудочно-кишечного тракта, что сопровождается язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев лейкозные инфильтраты обнаруживаются в легких («лейкозный пневмонит»), в 1/4 — в оболочках мозга («лейкозный менингит»). По иммунологическим фенотипам выделяют 6 вариантов заболевания.
Больные умирают от кровоизлияний в головной мозг, желудочно-кишечных кровотечений и инфекционных осложнений. Лечение цитостатиками изменило проявления заболевания, удлинило жизнь больным.
Хронические лейкозы
Хронические лейкозы отличаются от острых цитарной дифференцировкой опухолевых клеток, более длительным стадийным течением.
Первая стадия заболеваний характеризуется присутствием одного клона опухолевых клеток, течет годами, относительно доброкачественно, хронически и называется моноклоновой, доброкачественной.
Вторая стадия обусловлена появлением вторичных опухолевых клонов, характеризуется быстрым, злокачественным течением с появлением множества бластов и называется злокачественной, поликлоновой стадией, или стадией бластного криза. 80% больных хроническими лейкозами погибают в стадии бластного криза.
Результаты цитогенетических исследований показали, что злокачественная трансформация кроветворных клеток при хронических лейкозах может происходить на очень ранних стадиях — на стадиях стволовых клеток. Цитарный характер лейкозов обусловлен низким блоком дифференцировки в опухолевых клетках.
При хронических лейкозах лейкозные инфильтраты обнаруживаются в костном мозге, где в связи с длительными течением и цитостатической терапией нередко развивается миелофиброз в печени, селезенке и лимфатических узлах, которые иногда достигают значительных размеров.
Хронические лимфоцитарные лейкозы. Эти формы лейкозов объединяются в две группы. Первая — хронический лимфолейкоз и примыкающие к нему болезнь Сезари (лимфоматоз кожи), Т-клеточный лимфоцитарный лейкоз, пролимфоцитарный лейкоз (В-клеточный), волосато-клеточный лейкоз (В-клеточный). Вторая группа — парапротеинемические лейкозы. Наибольшее значение имеет хронический лимфолейкоз.
Хронический лимфолейкоз. Встречается обычно у лиц старше 40 лет, чаще в пожилом возрасте. Мужчины болеют в два раза чаще женщин. Заболеваемость достигает 6 случаев на 100 000 населения.
Цитогенез — в 95 % случаев из ранних В-клеток. Опухолевые клетки напоминают пролимфоциты и малые лимфоциты и экспрессируют параглобулины CD 19, CD20, CD5.
В клинической картине преобладают лимфаденопатия, анемия (нередко аутоиммунная), тромбоцитопения, гранулоцитопе-ния, имеются выраженная иммунодепрессия и предрасположенность к инфекционным осложнениям. Прогноз относительно хороший, заболевание протекает длительно с высокими показателями выживаемости. Однако в финале может развиться бласт-ный криз.
Лейкозные инфильтраты диффузно поражают костный мозг, лимфатические узлы, которые могут достигать значительных Размеров, образуя мягкие или плотноватые пакеты, а также одаривать соседние органы. Селезенка резко увеличена, в отдельных случаях ее масса составляет несколько килограммов. Печень увеличена в меньшей степени.
Больные умирают обычно от инфекционных осложнений. Описаны наблюдения трансформации хронического лимфолейкоза в неходжкинские лимфомы.
Парапротеинемические лимфолейкозы в эту группу входят три заболевания — миеломная болезнь, первичная макроглобулинемия Вальденстрема и болезнь тяжелы цепей Франклина. Особенностью парапротеинемических лейк0 зов, которые также называются злокачественными иммунопролиферативными заболеваниями, является способность опухолевых клеток синтезировать однородные иммуноглобулины ила их фрагменты — парапротеины, что связано с цитогенезом опухолевых клеток. Опухолевые клетки при парапротеинемических лейкозах дифференцируются по плазмоцитарному типу, сохраняя в извращенной форме особенность плазматических клеток синтезировать иммуноглобулины.
Наибольшее значение среди парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (болезнь Рустицкого — Калера, множественная миелома, генерализованная плазмоцитома) встречается в основном у взрослых. Описаны единичные наблюдения у людей моложе 30 лет. Свое название заболевание и опухолевая клетка получили в связи с преимущественной локализацией процесса на «территории» костного мозга (миелон — костный мозг).
Выделяют несколько вариантов миеломной болезни в зависимости от характера распространения миеломных инфильтратов в костном мозге, от характера миеломных клеток и от типа синтезируемого парапротеина.
По характеру распространенности опухолевого инфильтрата в костном мозге выделяют диффузную, диффузно-узловатую, множественно-узловатую формы миеломы; по клеточному составу — плазмоцитарную, плазмобластную, полиморфно-клеточную и мелкоклеточную миелому [Струков А.И., 1959]. В зависимости от способности секретировать различные типы парапротеинов различают несколько вариантов миеломной болезни: несекретирующие, диклоновые миеломы, миелому Бенс-Джонса, G-, А-, М-миеломы. Наиболее часто встречаются G-, А-миелома, миелома Бенс-Джонса, на долю которых приходится 75, 20 и 15 % наблюдений соответственно.
Опухолевая ткань разрастается преимущественно в плоских костях (череп, ребра, таз) и в позвоночнике, инициируя в них остеолизис, остеопороз. На рентгенограмме очаги поражения имеют вид гладкостенных пробоин. Полости образуются в местах роста миеломных клеток за счет активации ими остеокластов, осуществляющих лизис и резорбцию костной ткани (пазушно рассасывание). Высказываются предположения, что в качестве активирующих остеокласты субстанций могут выступать интерлейкин-1 и бета-трансформирующий фактор роста, выделяемые миеломными клетками. Помимо костного мозга, опухолевые инфильтраты могут обнаруживаться и в других органах.
Осложнения миеломной болезни развиваются вследствие деструкции костной ткани — патологические переломы, боли в костях, а также из-за продукции парапротеинов — амилоидоз (AL-амилоидоз), парапротеинемическая кома и парапротеиноз органов.
Хронические миелоцитарные лейкозы. Группа лейкозов, содержащих опухолевые клетки типа процитарных и цитарных предшественников миелоидного ряда. В эту группу входят хронический миелоцитарный лейкоз с или без филадельфийской хромосомы, ювенильный хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, первичный миелофиброз (мегакариоцитарная дифференцировка опухолевых клеток). Разнообразие форм хронических миелоцитарных лейкозов обусловлено существованием общей клетки-предшественницы гранулоцитарного, моноцитарного, мегакариоцитарного, эозинофильного и базофильного ростков. При развитии всех этих форм злокачественная трансформация, вероятно, происходит на уровне плюрипотентной стволовой клетки миелоидного ростка, так как цитогенетические маркеры можно обнаружить во всех ветвях этого ростка.
Хронический миелолейкоз представляет наибольший практический интерес. Это нередкое заболевание, на долю которого приходится 15 % всех случаев лейкоза. В США ежегодно регистрируется 2500 новых случаев. Встречается в любом возрасте, немного чаще у лиц мужского пола. В развитии заболевания имеют значение те же этиологические факторы, что и при остром миелобластном лейкозе.
Цитогенетическим маркером заболевания является филадельфийская хромосома, свидетельствующая также и о плохом прогнозе.
Заболевание протекает в две или даже три стадии: хроническая стадия, промежуточная (выделяется клиницистами, так как требует особых терапевтических мероприятий) и бласттранс-формации.
Хроническая стадия длится 3—4 года, нередко не имеет клинических проявлений. Морфологически в эту стадию обнаруживают сплено- и гепатомегалию, анемию. В костном мозге, периферической крови, в селезенке, печени и лимфатических узлах обнаруживают увеличение про- и цитарных форм миелоидного Ростка, имеющих маркеры одного опухолевого клона.
Промежуточная стадия сопровождается нарастанием слабости, повышением температуры тела, появлением клеток с новыми цитогенетическими отклонениями, резистентных к применявшимся ранее цитостатикам, прогрессированием сплено- и гепатомегалии. Эта стадия длится несколько месяцев, но при правильно назначенном лечении может быть пролонгирована.
Стадия бласттрансформации — властного криза — заканчивается смертью больных, несмотря на проводимую терапию, в очень короткие сроки. В инфильтратах в костном мозге и во вну тренних органах, а также в периферической крови появляются бластные формы (12—25 %), опухолевые клоны с новыми цито-генетическими нарушениями.
У 10 % больных заболевание заканчивается миелофиброзом обусловленным действием цитостатиков. Другой причиной миелофиброза может быть двухростковая пролиферация клеток типа цитарных предшественников грануло- и мегакариоцитарного ростков. Последние продуцируют фактор роста тромбоцитов, активирующий фибробласты.
На аутопсии имеются характерные изменения внутренних органов: пиоидный костный мозг, значительные сплено- и гепатомегалия, умеренное увеличение лимфатических узлов.
ЛИМФОМЫ
• Лимфомы — регионарные злокачественные опухоли лимфоидной ткани. Имеют моноклоновое происхождение, что используется при их диагностике и дифференциальной диагностике с реактивными гиперпластическими процессами в лимфоидной ткани.
Диагноз лимфом устанавливается прежде всего при биопсии лимфатических узлов.
Классификация. В настоящее время используется несколько классификаций лимфом: H.Rappoport (1966), R.G.Lukes — R.D.Collins (1973—1974), R.E.A.L., кильская и ВОЗ, включающая в себя обе эти классификации.
Классификация лимфом [R.E.A.L. и кильская, 1996]
НЕХОДЖКИНСКИЕ ЛИМФОМЫ | ХОДЖКИНСКИЕ ЛИМФОМЫ | ||
В —лимфоцитарные | Т—лимфоцитарные | классические варианты | неклассический вариант |
1. Из предшественников В-лимфоцитов (бластные В-лимфомы) | 1. Из предшественников Т-лимфоцитов (бластные Т-лимфомы) | 1. Лимфоцитарный (провизорный) 2. Нодулярный склероз | С преобладанием лимфоцитов |
2. Из периферических В-клеток (цитарные В-лимфомы) | 2. Из периферических Т-клеток (цитарные Т-лимфомы) | 3. Смешанно-клеточный 4. С подавлением лимфоидной ткани | |
studfiles.net
Гемобластозы
Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
В последние годы в литературе широко обсуждается вопрос о существовании предопухолевой стадии лейкозов и лимфом. Предлагаются термины «предлейкоз» и «предлимфома» для обозначения состояний с различными качественными и количественными изменениями кроветворной ткани, нередко предшествующими развитию гемобластозов.
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобласто-юв доказывается наблюдениями за пациентами, заболевшими
лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатиче-ских препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобласт-ного лейкоза и эритромиелоза.
Роль вирусов в качестве этиологического фактора гемобла-стозов трактуется неоднозначно. В развитии гемобластозов человека доказано участие лишь двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и Т-лимфоцитарного вируса лейкоза человека первого типа (Т-клеточная лимфома и Т-клеточные лейкозы). Имеются экспериментальные данные, доказывающие прямое канцерогенное действие вирусов на гемопо-этические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хро мосом (болезни Клайнфелтера, Тернера), а также существовани ем «лейкозных семей». Нередко лейкозы развиваются у пациен тов с наследственными дефектами иммунитета (атаксия-телеан гиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдрид жа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздейст вуя на стволовые и полустволовые гемопоэтические клетки, при водят к одинаковым результатам — злокачественной трансфор мации. Следовательно, существует так называемое узкое место через которое могут осуществлять свое воздействие различные агенты. Такое место, вероятнее всего, находится в геноме кле
ток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лим-фоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген с-тус из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрок-ной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тиро-зинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лим-фоцитарных лейкозах и лимфомах — в локусе llq гена а-цепо-чек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигни-зации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами, где рост и дифференцировка клеток происходят только в присутствии факторов роста или стромальных клеток. Стро-мальные клетки, вероятно, также выделяют факторы роста, свя-заные с их клеточными мембранами, а также гепарансульфата-ми стромы, обеспечивая тем самым локальный рост.
Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мало изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лей-козных клеток с участием особых факторов и контактного торможения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и бластные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритроми-елобластный, мегакариобластный, недифференцированный. Хронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лим-фоцитарного происхождения (хронический лимфолейкоз, пара-протеинемические лейкозы: миеломная болезнь, первичная мак-роглобулинемия Вальденстрема, болезнь тяжелых цепей Франкина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарно-го происхождения (хронический моноцитарный лейкоз, гистио-цитоз X).
Иммунный фенотип опухолевых клеток.В настоящее время стало возможным проводить более точное ти-пирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD 19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50—80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Острые лейкозы
Различные формы острого лейкоза имеют стереотипные морфологические проявления: лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек. Размеры и очертания ядер, а также ширина ободка цитоплазмы могут варьировать. Бласты составляют 10—20 % костномозговых клеток. Цитогенетическую принадлежность бластов, как правило, можно выявить только с помощью специальных методов исследования — цитохимических и иммуногистохимиче-ских. Применяются реакции на пероксидазу, окраска на липиды Суданом черным, ШИК-реакция, гистоферментохимические реакции на выявление неспецифической эстеразы, хлорацетатэсте-разы, кислой фосфатазы, Иммуногистохимически возможно определение маркеров В-, Т-лимфоцитов, клеток миелоидного и моноцитарного рядов.
В периферической крови и в костном мозге описывается феномен лейкемического провала («hiatus leucemicus»), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм.
В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретику-
лярных волокон, нередко развивается миелофиброз. При цито-статической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань.
Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. В связи с лейкоз-ной инфильтрацией слизистых оболочек полости рта и ткани миндалин появляются некротический гингивит, тонзиллит — некротическая ангина. Иногда присоединяется вторичная инфекция и развивается сепсис, приводящий больных к смерти.
В результате тромбоцитопении, повреждения печени и стенок сосудов у больных острыми лейкозами нередко возникает геморрагический синдром вплоть до развития смертельных осложнений — кровоизлияний в головной мозг и желудочно-кишечных кровотечений.
Использование активной цитостатической терапии повлияло на течение острых лейкозов, т.е. привело к индуцированному лекарственному патоморфозу. В связи с этим в настоящее время выделяют следующие клинические стадии заболевания: первая атака, ремиссия (полная или неполная), рецидив (первый, повторный).
Наибольшее значение среди острых лейкозов имеют острый лимфобластный и острый миелобластный лейкозы.
Острый лимфобластный лейкоз. Самый распространенный лейкоз в детском и юношеском возрасте. Пик заболеваемости приходится на возраст от 1 года до 6 лет. Протекает с поражением костного мозга, лимфатических узлов, селезенки, вилочковой железы, а также других органов. Центральная нервная система обычно вовлекается при рецидивах заболевания после химиотерапии. В костном мозге, периферической крови и в других органах обнаруживаются опухолевые клетки типа лимфобластов с ШИК-положительными гранулами в цитоплазме, не дающие реакций на пероксидазу, эстеразы и не содержащие липиды.
В 2/3 случаев в опухолевых клетках обнаруживаются цитоге-нетические нарушения в виде полиплоидии, филадельфийской хромосомы и реципрокной транслокации между хромосомами 8 и 14.
Цитогенез острого лимфобластного лейкоза связан с предшественниками Т- и В-лимфоцитов. На Т-клеточные лейкозы в странах Европы приходится 10—15 % наблюдений. Преобладают В-клеточные лейкозы.
Руководствуясь иммунологическими фенотипами опухолевых клеток, выделяют несколько форм лимфобластного лейкоза, что имеет значение для выбора терапии и прогноза. Преобладающие В-лимфобластные лейкозы представлены ранним, промежуточным и поздним вариантами, отличающимися по экспрессии пара-глобулина CD 10, поверхностного иммуноглобулина и активности терминальной диоксинуклеотидтрансферазы. Маркерами Т-лимфобластного лейкоза являются антигены CD7 и Т-рецепто-ров.
У детей преобладает промежуточный вариант, у взрослых — ранний и промежуточный. Прогноз у детей значительно лучше, чем у взрослых. Выживаемость составляет соответственно 60 и 30 %. Наихудший прогноз при Т-лимфобластном лейкозе.
Острый миелобластный лейкоз. Наиболее частая форма заболевания у взрослых с относительно хорошим прогнозом — ремиссии наступают у 70—80 % больных, полные ремиссии — у 25 % больных.
Описываются наблюдения развития острого миелобластного лейкоза у людей, подвергшихся радиационному воздействию, контактирующих с бензолом (кожевенная индустрия в Турции, производство синтетических клеев и др.), принимавших цитоста-тические препараты, а также у страдающих наследственными заболеваниями — болезнью Дауна, анемией Фанкони, синдромом Блума.
Опухолевые клетки имеют типичные для миелобластов цитохимические маркеры: ШИК-положительную диффузно окрашенную цитоплазму, содержат липиды, пероксидазу, эстеразы. Опухолевые клетки инфильтрируют костный мозг, приобретающий макроскопически пиоидный вид, селезенку, печень, лимфатические узлы, слизистую оболочку желудочно-кишечного тракта, что сопровождается язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев лейкозные инфильтраты обнаруживаются в легких («лейкозный пневмонит»), в 114— в оболочках мозга («лейкозный менингит»). По иммунологическим фенотипам выделяют 6 вариантов заболевания.
Больные умирают от кровоизлияний в головной мозг, желудочно-кишечных кровотечений и инфекционных осложнений. Лечение цитостатиками изменило проявления заболевания, удлинило жизнь больным.
Хронические лейкозы
Хронические лейкозы отличаются от острых цитарной диф-ференцировкой опухолевых клеток, более длительным стадийным течением.
Первая стадия заболеваний характеризуется присутствием одного клона опухолевых клеток, течет годами, относительно доброкачественно, хронически и называется м о н о -клоновой, доброкачественной.
Вторая стадия обусловлена появлением вторичных опухолевых клонов, характеризуется быстрым, злокачественным течением с появлением множества бластов и называется злокачественной, поликлоновой стадией, или стадией властного криза. 80% больных хроническими лейкозами погибают в стадии властного криза.
Результаты цитогенетических исследований показали, что злокачественная трансформация кроветворных клеток при хронических лейкозах может происходить на очень ранних стадиях — на стадиях стволовых клеток. Цитарный характер лейкозов обусловлен низким блоком дифференцировки в опухолевых клетках.
При хронических лейкозах лейкозные инфильтраты обнаруживаются в костном мозге, где в связи с длительными течением и цитостатической терапией нередко развивается миелофиброз в печени, селезенке и лимфатических узлах, которые иногда достигают значительных размеров.
Хронические лимфоцитарные лейкозы. Эти формы лейкозов объединяются в две группы. Первая — хронический лимфолей-коз и примыкающие к нему болезнь Сезари (лимфоматоз кожи), Т-клеточный лимфоцитарный лейкоз, пролимфоцитарный лейкоз (В-клеточный), волосато-клеточный лейкоз (В-клеточный). Вторая группа — парапротеинемические лейкозы. Наибольшее значение имеет хронический лимфолейкоз.
Хронический лимфолейкоз. Встречается обычно у лиц старше 40 лет, чаще в пожилом возрасте. Мужчины болеют в два раза чаще женщин. Заболеваемость достигает 6 случаев на 100 000 населения.
Цитогенез — в 95 % случаев из ранних В-клеток. Опухолевые клетки напоминают пролимфоциты и малые лимфоциты и экс-прессируют параглобулины CD 19, CD20, CD5.
В клинической картине преобладают лимфаденопатия, анемия (нередко аутоиммунная), тромбоцитопения, гранулоцитопе-ния, имеются выраженная иммунодепрессия и предрасположенность к инфекционным осложнениям. Прогноз относительно хороший, заболевание протекает длительно с высокими показателями выживаемости. Однако в финале может развиться властный криз.
Лейкозные инфильтраты диффузно поражают костный мозг, лимфатические узлы, которые могут достигать значительных размеров, образуя мягкие или плотноватые пакеты, а также сдавливать соседние органы. Селезенка резко увеличена, в отдельных случаях ее масса составляет несколько килограммов. Печень увеличена в меньшей степени.
Больные умирают обычно от инфекционных осложнений. Описаны наблюдения трансформации хронического лимфолеи-коза в неходжкинские лимфомы.
Парапротеинемические лимфолейкозы.В эту группу входят три заболевания — миеломная болезнь, первичная макроглобулинемия Вальденстрема и болезнь тяжелых цепей Франклина. Особенностью парапротеинемических лейкозов, которые также называются злокачественными иммунопро-лиферативными заболеваниями, является способность опухолевых клеток синтезировать однородные иммуноглобулины или их фрагменты — парапротеины, что связано с цитогенезом опухолевых клеток. Опухолевые клетки при парапротеинемических лейкозах дифференцируются по плазмоцитарному типу, сохраняя в извращенной форме особенность плазматических клеток синтезировать иммуноглобулины.
Наибольшее значение среди парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (болезнь Рустицкого — Калера, множественная миелома, генерализованная плазмоцитома) встречается в основном у взрослых. Описаны единичные наблюдения у людей моложе 30 лет. Свое название заболевание и опухолевая клетка получили в связи с преимущественной локализацией процесса на «территории» костного мозга (миелон — костный мозг).
Выделяют несколько вариантов миеломной болезни в зависимости от характера распространения миеломных инфильтратов в костном мозге, от характера миеломных клеток и от типа синтезируемого парапротеина.
По характеру распространенности опухолевого инфильтрата в костном мозге выделяют диффузную, диффузно-узловатую, множественно-узловатую формы миеломы; по клеточному составу — плазмоцитарную, плазмобластную, полиморфно-клеточную и мелкоклеточную миелому [Струков А.И., 1959].
В зависимости от способности секретировать различные типы парапротеинов различают несколько вариантов миеломной болезни: несекретирующие, диклоновые миеломы, миелому Бенс-Джонса, G-, А-, М-миеломы. Наиболее часто встречаются G-, А-миелома, миелома Бенс-Джонса, на долю которых приходится 75, 20 и 15 % наблюдений соответственно.
Опухолевая ткань разрастается преимущественно в плоских костях (череп, ребра, таз) и в позвоночнике, инициируя в них ос-теолизис, остеопороз. На рентгенограмме очаги поражения имеют вид гладкостенных пробоин. Полости образуются в местах роста миеломных клеток за счет активации ими остеокластов, осуществляющих лизис и резорбцию костной ткани (пазушное рассасывание). Высказываются предположения, что в качестве активирующих остеокласты субстанций могут выступать интер-лейкин-1 и бета-трансформирующий фактор роста, выделяемые миеломными клетками. Помимо костного мозга, опухолевые ин-фильтраты могут обнаруживаться и в других органах.
Осложнения миеломной болезни развиваются вследствие деструкции костной ткани — патологические переломы, боли в костях, а также из-за продукции парапротеинов — амилоидоз (AL-амилощоз), парапротеинемическая кома и парапротеиноз органов.
Хронические миелоцитарные лейкозы. Группа лейкозов, содержащих опухолевые клетки типа процитарных и цитарных предшественников миелоидного ряда. В эту группу входят хронический миелоцитарный лейкоз с или без филадельфийской хромосомы, ювенильный хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, первичный миелофиброз (мегакариоцитарная диффе-ренцировка опухолевых клеток). Разнообразие форм хронических миелоцитарных лейкозов обусловлено существованием общей клетки-предшественницы гранулоцитарного, моноцитарно-го, мегакариоцитарного, эозинофильного и базофильного ростков. При развитии всех этих форм злокачественная трансформация, вероятно, происходит на уровне плюрипотентной стволовой клетки миелоидного ростка, так как цитогенетические маркеры можно обнаружить во всех ветвях этого ростка.
Хронический миелолейкоз представляет наибольший практический интерес. Это нередкое заболевание, на долю которого приходится 15 % всех случаев лейкоза. В США ежегодно регистрируется 2500 новых случаев. Встречается в любом возрасте, немного чаще у лиц мужского пола. В развитии заболевания имеют значение те же этиологические факторы, что и при остром миелобластном лейкозе.
Цитогенетическим маркером заболевания является филадельфийская хромосома, свидетельствующая также и о плохом прогнозе.
Заболевание протекает в две или даже три стадии: хроническая стадия, промежуточная (выделяется клиницистами, так как требует особых терапевтических мероприятий) и бласттранс-формации.
Хроническая стадия длится 3—4 года, нередко не имеет клинических проявлений. Морфологически в эту стадию обнаруживают сплено- и гепатомегалию, анемию. В костном мозге, периферической крови, в селезенке, печени и лимфатических узлах обнаруживают увеличение про- и цитарных форм миелоидного ростка, имеющих маркеры одного опухолевого клона.
Промежуточная стадия сопровождается нарастанием слабости, повышением температуры тела, появлением клеток с новыми цитогенетическими отклонениями, резистентных к применявшимся ранее цитостатикам, прогрессированием сплено- и гепато-мегалии. Эта стадия длится несколько месяцев, но при правильно назначенном лечении может быть пролонгирована.
Стадия бласттрансформации — властного криза — заканчивается смертью больных, несмотря на проводимую терапию, в очень короткие сроки. В инфильтратах в костном мозге и во внутренних органах, а также в периферической крови появляются бластные формы (12—25 %), опухолевые клоны с новыми цито-генетическими нарушениями.
У 10 % больных заболевание заканчивается миелофиброзом, обусловленным действием цитостатиков. Другой причиной мие-лофиброза может быть двухростковая пролиферация клеток типа цитарных предшественников грануло- и мегакариоцитарного ростков. Последние продуцируют фактор роста тромбоцитов, активирующий фибробласты.
На аутопсии имеются характерные изменения внутренних органов: пиоидный костный мозг, значительные сплено- и генато-мегалия, умеренное увеличение лимфатических узлов.
ЛИМФОМЫ
• Лимфомы — регионарные злокачественные опухоли лимфо-идной ткани. Имеют моноклоновое происхождение, что используется при их диагностике и дифференциальной диагностике с реактивными гиперпластическими процессами в лимфоидной ткани.
Диагноз лимфом устанавливается прежде всего при биопсии
лимфатических узлов.
Классификация. В настоящее время используется несколько классификаций лимфом: H.Rappoport (1966), R.G.Lukes — R.D.Collins (1973—1974), R.E.A.L., кильская и ВОЗ, включающая в себя обе эти классификации.
Классификация лимфом [R.E.A.L. и кильская, 1996]
|
неклассический вариант С преобладани ем лимфоцитов |
|
классические варианты 1. Лимфоцитар-ный (провизорный) 2. Нодулярный склероз 3. Смешанно-клеточный 4. С подавлением лимфоид-ной ткани |
НЕХОЛЖКИНСКИЕ ЛИМФОМЫ ХОДЖКИНСКИЕ ЛИМФОМЫ
|
Т—лимфоцитарные
|
В—лимфоцитарные
1. Из предшественников В-лим-фоцитов (властные В-лим-фомы)
2. Из периферических В-клеток (цитарные В-лимфомы)
Основным принципам всех основных классификаций лимфом является подразделение их на: 1) ходжкинскую и неходжкинские лимфомы; 2) В- и Т-лимфоцитарные и неклассифицируемые по цитогенезу; 3) низкой, умеренной и высокой злокачественности по степени дифференцировки опухолевых клеток.
В терминальной стадии заболеваний возможна генерализация опухолевого процесса с развитием метастазов в костном мозге — «лейкемизация лимфом».
Лимфогранулематоз (болезнь Ходжкина). В 1832 г. врач и куратор анатомического музея одной из лондонских клиник T.Hodgkin описал 6 случаев своеобразного заболевания с лимф-аденопатией и необычной спленомегалией. Только в 1926 г. H.Fox из того же госпиталя изучил гистологические изменения, характерные для болезни Ходжкина.
Частота заболевания составляет до 3 случаев на 100 000 населения, т.е. 1 % всех злокачественных опухолей в развитых странах. Имеется два пика заболевания — в молодом и пожилом возрасте (в странах третьего мира страдают в основном дети).
Этиология заболевания неизвестна. Имеются указания на обнаружение у больных болезнью Ходжкина антител к вирусу Эп-штейна — Барр в 35 % случаев, нередко после перенесенного ими мононуклеоза. В многоядерных опухолевых клетках Березовского — Штернберга (Рида — Штернберга) были обнаружены мембранные протеины этого вируса. Вероятно, существует и определенная наследственная предрасположенность (судя но гаилотипу HLA).
Цитогенетическая принадлежность опухолевых клеток при классических вариантах болезни Ходжкина остается спорной. Клетки Березовского — Штернберга не имеют аналога среди нормальных клеток, так как постоянно экспрессируют маркер клеток лимфоидного ряда (CD30), маркер клеток гранулоцитар-ного ряда (CD15), а также маркеры Т- и В-лимфоцитов. Напротив, лимфогранулематоз с преобладанием лимфоцитов, не входящий в группу классических вариантов болезни, характеризуется наличием опухолевых клеток В-лимфоцитарной природы, экс-прессирующих маркеры В-лимфоцитов, а также белок J-цепочек IgG, секретируемый В-клетками.
Опухолевая ткань при лимфогранулематозе представлена тремя клетками: большими и малыми клетками Ходжкина с одним крупным ядром, содержащим ядрышки, и многоядерной клеткой Березовского — Штернберга. На определенной стадии опухолевой прогрессии в опухолевой ткани появляются массивные скопления и пролифераты неопухолевых клеток, гематогенного и местного, гистиогенного происхождения, вероятно, за счет выделения опухолевыми клетками хемотаксических и ростовых факторов: лимфоцитов, эозинофилов, плазматических клеток, нейтрофилов, фибробластов. Характерны некроз и склероз опухолевой ткани, а также пролиферация эндотелия венул.
Классификация лимфогранулематоза основывается на распространенности опухоли и гистопатологических изменениях. Выделяют изолированный вариант с поражением одной группы лимфатических узлов (шейных, медиастинальных, забрюшинных и др.) и генерализованный с распространением процесса на несколько групп лимфатических узлов и, как правило, с вовлечением селезенки.
Макроскопически лимфатические узлы увеличены в размерах, спаиваются между собой. Селезенка также увеличена, имеет характерный красный цвет с белыми прожилками — «порфировая селезенка».
Гистопатологические варианты лимфогранулематоза подразделяются на классические и с преобладанием лимфоцитов (см. классификацию лимфом). Классические варианты представлены: 1) лимфоцитарным; 2) нодулярным (узловатым) склерозом; 3) смешанно-клеточным; 4) с подавлением лимфоидной ткани. Описанные гистопатологические варианты могут быть последовательными стадиями прогрессирования заболевания.
Прогноз зависит от количества сохранившихся лимфоцитов.
Неходжкинские лимфомы. Это группа злокачественных опухолей В- и Т-клеточного происхождения. Среди неходжкинских В-лимфом выделяют злокачественную лимфоцитарную лимфо-му, злокачественную лимфоплазмоцитарную лимфому, злокачественную центроцитарную (центробластную лимфому), злокачественную лимфому Беркитта, злокачественную лимфобластную лимфому и злокачественную анапластическую крупноклеточную лимфому. Диагноз этих заболеваний требует обязательного морфологического исследования биоптатов лимфатических узлов, нередко с иммуногистохимическим анализом.
Т-клеточные лимфомы встречаются значительно реже и составляют 10—15 % от всех неходжкинских лимфом. Они подраз деляются на лимфобластные, лимфоцитарные и периферичес кие — грибовидный микоз (поражение кожи и лимфатических узлов) и болезнь Сезари (лимфома кожи с лейкемизацией).
dendrit.ru
-Лекция №4 ГЕМОБЛАСТОЗЫ
Лекция 4
ГЕМОБЛАСТОЗЫ
• Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
В последние годы в литературе широко обсуждается вопрос о существовании предопухолевой стадии лейкозов и лимфом. Предлагаются термины «предлейкоз» и «предлимфома» для обозначения состояний с различными качественными и количественными изменениями кроветворной ткани, нередко предшествующими развитию гемобластозов.
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобласто-юв доказывается наблюдениями за пациентами, заболевшими
311
лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатиче-ских препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобласт-ного лейкоза и эритромиелоза.
Роль вирусов в качестве этиологического фактора гемобла-стозов трактуется неоднозначно. В развитии гемобластозов человека доказано участие лишь двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и Т-лимфоцитарного вируса лейкоза человека первого типа (Т-клеточная лимфома и Т-клеточные лейкозы). Имеются экспериментальные данные, доказывающие прямое канцерогенное действие вирусов на гемопо-этические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хро мосом (болезни Клайнфелтера, Тернера), а также существовани ем «лейкозных семей». Нередко лейкозы развиваются у пациен тов с наследственными дефектами иммунитета (атаксия-телеан гиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдрид жа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздейст вуя на стволовые и полустволовые гемопоэтические клетки, при водят к одинаковым результатам — злокачественной трансфор мации. Следовательно, существует так называемое узкое место через которое могут осуществлять свое воздействие различные агенты. Такое место, вероятнее всего, находится в геноме кле
312
ток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лим-фоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген с-тус из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрок-ной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тиро-зинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лим-фоцитарных лейкозах и лимфомах — в локусе llq гена а-цепо-чек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигни-зации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами, где рост и дифференцировка клеток происходят только в присутствии факторов роста или стромальных клеток. Стро-мальные клетки, вероятно, также выделяют факторы роста, свя-заные с их клеточными мембранами, а также гепарансульфата-ми стромы, обеспечивая тем самым локальный рост.
313
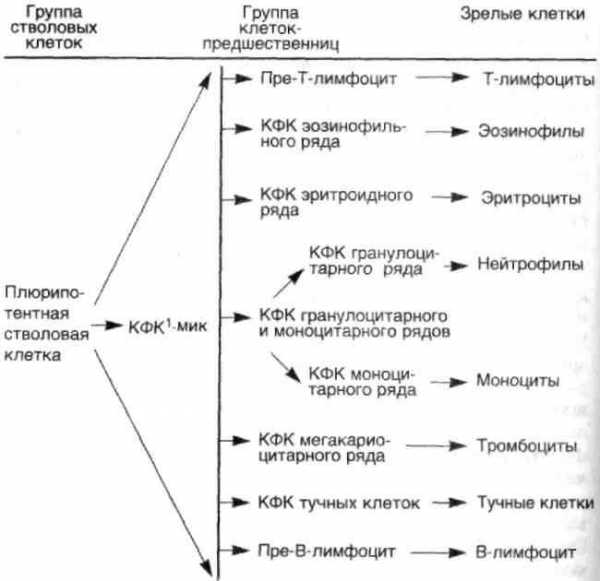
Схема 34. Структура гемопоэтической системы
1 Колониеформирующая клетка, син, колониеобразующая клетка (КОЕ).Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мало изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лей-козных клеток с участием особых факторов и контактного тор
314
можения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и бластные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритроми-елобластный, мегакариобластный, недифференцированный. Хронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лим-фоцитарного происхождения (хронический лимфолейкоз, пара-протеинемические лейкозы: миеломная болезнь, первичная мак-роглобулинемия Вальденстрема, болезнь тяжелых цепей Франк-
315
лина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарно-го происхождения (хронический моноцитарный лейкоз, гистио-цитоз X).
Иммунный фенотип опухолевых клеток.В настоящее время стало возможным проводить более точное ти-пирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD 19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50—80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Острые лейкозы
Различные формы острого лейкоза имеют стереотипные морфологические проявления: лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек. Размеры и очертания ядер, а также ширина ободка цитоплазмы могут варьировать. Бласты составляют 10—20 % костномозговых клеток. Цитогенетическую принадлежность бластов, как правило, можно выявить только с помощью специальных методов исследования — цитохимических и иммуногистохимиче-ских. Применяются реакции на пероксидазу, окраска на липиды Суданом черным, ШИК-реакция, гистоферментохимические реакции на выявление неспецифической эстеразы, хлорацетатэсте-разы, кислой фосфатазы, Иммуногистохимически возможно определение маркеров В-, Т-лимфоцитов, клеток миелоидного и моноцитарного рядов.
В периферической крови и в костном мозге описывается феномен лейкемического провала («hiatus leucemicus»), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм.
В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретику-
лярных волокон, нередко развивается миелофиброз. При цито-статической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань.
Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. В связи с лейкоз-ной инфильтрацией слизистых оболочек полости рта и ткани миндалин появляются некротический гингивит, тонзиллит — некротическая ангина. Иногда присоединяется вторичная инфекция и развивается сепсис, приводящий больных к смерти.
В результате тромбоцитопении, повреждения печени и стенок сосудов у больных острыми лейкозами нередко возникает геморрагический синдром вплоть до развития смертельных осложнений — кровоизлияний в головной мозг и желудочно-кишечных кровотечений.
Использование активной цитостатической терапии повлияло на течение острых лейкозов, т.е. привело к индуцированному лекарственному патоморфозу. В связи с этим в настоящее время выделяют следующие клинические стадии заболевания: первая атака, ремиссия (полная или неполная), рецидив (первый, повторный).
Наибольшее значение среди острых лейкозов имеют острый лимфобластный и острый миелобластный лейкозы.
Острый лимфобластный лейкоз. Самый распространенный лейкоз в детском и юношеском возрасте. Пик заболеваемости приходится на возраст от 1 года до 6 лет. Протекает с поражением костного мозга, лимфатических узлов, селезенки, вилочковой железы, а также других органов. Центральная нервная система обычно вовлекается при рецидивах заболевания после химиотерапии. В костном мозге, периферической крови и в других органах обнаруживаются опухолевые клетки типа лимфобластов с ШИК-положительными гранулами в цитоплазме, не дающие реакций на пероксидазу, эстеразы и не содержащие липиды.
В 2/3 случаев в опухолевых клетках обнаруживаются цитоге-нетические нарушения в виде полиплоидии, филадельфийской хромосомы и реципрокной транслокации между хромосомами 8 и 14.
Цитогенез острого лимфобластного лейкоза связан с предшественниками Т- и В-лимфоцитов. На Т-клеточные лейкозы в странах Европы приходится 10—15 % наблюдений. Преобладают В-клеточные лейкозы.
Руководствуясь иммунологическими фенотипами опухолевых клеток, выделяют несколько форм лимфобластного лейкоза, что имеет значение для выбора терапии и прогноза. Преобладающие
316
317
В-лимфобластные лейкозы представлены ранним, промежуточным и поздним вариантами, отличающимися по экспрессии пара-глобулина CD 10, поверхностного иммуноглобулина и активности терминальной диоксинуклеотидтрансферазы. Маркерами Т-лимфобластного лейкоза являются антигены CD7 и Т-рецепто-ров.
У детей преобладает промежуточный вариант, у взрослых — ранний и промежуточный. Прогноз у детей значительно лучше, чем у взрослых. Выживаемость составляет соответственно 60 и 30 %. Наихудший прогноз при Т-лимфобластном лейкозе.
Острый миелобластный лейкоз. Наиболее частая форма заболевания у взрослых с относительно хорошим прогнозом — ремиссии наступают у 70—80 % больных, полные ремиссии — у 25 % больных.
Описываются наблюдения развития острого миелобластного лейкоза у людей, подвергшихся радиационному воздействию, контактирующих с бензолом (кожевенная индустрия в Турции, производство синтетических клеев и др.), принимавших цитоста-тические препараты, а также у страдающих наследственными заболеваниями — болезнью Дауна, анемией Фанкони, синдромом Блума.
Опухолевые клетки имеют типичные для миелобластов цитохимические маркеры: ШИК-положительную диффузно окрашенную цитоплазму, содержат липиды, пероксидазу, эстеразы. Опухолевые клетки инфильтрируют костный мозг, приобретающий макроскопически пиоидный вид, селезенку, печень, лимфатические узлы, слизистую оболочку желудочно-кишечного тракта, что сопровождается язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев лейкозные инфильтраты обнаруживаются в легких («лейкозный пневмонит»), в 114 — в оболочках мозга («лейкозный менингит»). По иммунологическим фенотипам выделяют 6 вариантов заболевания.
Больные умирают от кровоизлияний в головной мозг, желудочно-кишечных кровотечений и инфекционных осложнений. Лечение цитостатиками изменило проявления заболевания, удлинило жизнь больным.
Хронические лейкозы
Хронические лейкозы отличаются от острых цитарной диф-ференцировкой опухолевых клеток, более длительным стадийным течением.
Первая стадия заболеваний характеризуется присутствием одного клона опухолевых клеток, течет годами, относительно доброкачественно, хронически и называется м о н о -клоновой, доброкачественной.
318
ь Вторая стадия обусловлена появлением вторичных опухолевых клонов, характеризуется быстрым, злокачественным течением с появлением множества бластов и называется злокачественной, поликлоновой стадией, или стадией властного криза. 80% больных хроническими лейкозами погибают в стадии властного криза.
Результаты цитогенетических исследований показали, что злокачественная трансформация кроветворных клеток при хронических лейкозах может происходить на очень ранних стадиях — на стадиях стволовых клеток. Цитарный характер лейкозов обусловлен низким блоком дифференцировки в опухолевых клетках.
При хронических лейкозах лейкозные инфильтраты обнаруживаются в костном мозге, где в связи с длительными течением и цитостатической терапией нередко развивается миелофиброз в печени, селезенке и лимфатических узлах, которые иногда достигают значительных размеров.
Хронические лимфоцитарные лейкозы. Эти формы лейкозов объединяются в две группы. Первая — хронический лимфолей-коз и примыкающие к нему болезнь Сезари (лимфоматоз кожи), Т-клеточный лимфоцитарный лейкоз, пролимфоцитарный лейкоз (В-клеточный), волосато-клеточный лейкоз (В-клеточный). Вторая группа — парапротеинемические лейкозы. Наибольшее значение имеет хронический лимфолейкоз.
Хронический лимфолейкоз. Встречается обычно у лиц старше 40 лет, чаще в пожилом возрасте. Мужчины болеют в два раза чаще женщин. Заболеваемость достигает 6 случаев на 100 000 населения.
Цитогенез — в 95 % случаев из ранних В-клеток. Опухолевые клетки напоминают пролимфоциты и малые лимфоциты и экс-прессируют параглобулины CD 19, CD20, CD5.
В клинической картине преобладают лимфаденопатия, анемия (нередко аутоиммунная), тромбоцитопения, гранулоцитопе-ния, имеются выраженная иммунодепрессия и предрасположенность к инфекционным осложнениям. Прогноз относительно хороший, заболевание протекает длительно с высокими показателями выживаемости. Однако в финале может развиться властный криз.
Лейкозные инфильтраты диффузно поражают костный мозг, лимфатические узлы, которые могут достигать значительных размеров, образуя мягкие или плотноватые пакеты, а также сдавливать соседние органы. Селезенка резко увеличена, в отдельных случаях ее масса составляет несколько килограммов. Печень увеличена в меньшей степени.
Больные умирают обычно от инфекционных осложнений. Описаны наблюдения трансформации хронического лимфолеи-коза в неходжкинские лимфомы.
319
Парапротеинемические лимфолейкозы.В эту группу входят три заболевания — миеломная болезнь, первичная макроглобулинемия Вальденстрема и болезнь тяжелых цепей Франклина. Особенностью парапротеинемических лейкозов, которые также называются злокачественными иммунопро-лиферативными заболеваниями, является способность опухолевых клеток синтезировать однородные иммуноглобулины или их фрагменты — парапротеины, что связано с цитогенезом опухолевых клеток. Опухолевые клетки при парапротеинемических лейкозах дифференцируются по плазмоцитарному типу, сохраняя в извращенной форме особенность плазматических клеток синтезировать иммуноглобулины.
Наибольшее значение среди парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (болезнь Рустицкого — Калера, множественная миелома, генерализованная плазмоцитома) встречается в основном у взрослых. Описаны единичные наблюдения у людей моложе 30 лет. Свое название заболевание и опухолевая клетка получили в связи с преимущественной локализацией процесса на «территории» костного мозга (миелон — костный мозг).
Выделяют несколько вариантов миеломной болезни в зависимости от характера распространения миеломных инфильтратов в костном мозге, от характера миеломных клеток и от типа синтезируемого парапротеина.
По характеру распространенности опухолевого инфильтрата в костном мозге выделяют диффузную, диффузно-узловатую, множественно-узловатую формы миеломы; по клеточному составу — плазмоцитарную, плазмобластную, полиморфно-клеточную и мелкоклеточную миелому [Струков А.И., 1959].
В зависимости от способности секретировать различные типы парапротеинов различают несколько вариантов миеломной болезни: несекретирующие, диклоновые миеломы, миелому Бенс-Джонса, G-, А-, М-миеломы. Наиболее часто встречаются G-, А-миелома, миелома Бенс-Джонса, на долю которых приходится 75, 20 и 15 % наблюдений соответственно.
Опухолевая ткань разрастается преимущественно в плоских костях (череп, ребра, таз) и в позвоночнике, инициируя в них ос-теолизис, остеопороз. На рентгенограмме очаги поражения имеют вид гладкостенных пробоин. Полости образуются в местах роста миеломных клеток за счет активации ими остеокластов, осуществляющих лизис и резорбцию костной ткани (пазушное рассасывание). Высказываются предположения, что в качестве активирующих остеокласты субстанций могут выступать интер-лейкин-1 и бета-трансформирующий фактор роста, выделяемые миеломными клетками. Помимо костного мозга, опухолевые ин-фильтраты могут обнаруживаться и в других органах.
Осложнения миеломной болезни развиваются вследствие деструкции костной ткани — патологические переломы, боли в ко-
320
стях, а также из-за продукции парапротеинов — амилоидоз (AL-амилощоз), парапротеинемическая кома и парапротеиноз органов.
Хронические миелоцитарные лейкозы. Группа лейкозов, содержащих опухолевые клетки типа процитарных и цитарных предшественников миелоидного ряда. В эту группу входят хронический миелоцитарный лейкоз с или без филадельфийской хромосомы, ювенильный хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, первичный миелофиброз (мегакариоцитарная диффе-ренцировка опухолевых клеток). Разнообразие форм хронических миелоцитарных лейкозов обусловлено существованием общей клетки-предшественницы гранулоцитарного, моноцитарно-го, мегакариоцитарного, эозинофильного и базофильного ростков. При развитии всех этих форм злокачественная трансформация, вероятно, происходит на уровне плюрипотентной стволовой клетки миелоидного ростка, так как цитогенетические маркеры можно обнаружить во всех ветвях этого ростка.
Хронический миелолейкоз представляет наибольший практический интерес. Это нередкое заболевание, на долю которого приходится 15 % всех случаев лейкоза. В США ежегодно регистрируется 2500 новых случаев. Встречается в любом возрасте, немного чаще у лиц мужского пола. В развитии заболевания имеют значение те же этиологические факторы, что и при остром миелобластном лейкозе.
Цитогенетическим маркером заболевания является филадельфийская хромосома, свидетельствующая также и о плохом прогнозе.
Заболевание протекает в две или даже три стадии: хроническая стадия, промежуточная (выделяется клиницистами, так как требует особых терапевтических мероприятий) и бласттранс-формации.
Хроническая стадия длится 3—4 года, нередко не имеет клинических проявлений. Морфологически в эту стадию обнаруживают сплено- и гепатомегалию, анемию. В костном мозге, периферической крови, в селезенке, печени и лимфатических узлах обнаруживают увеличение про- и цитарных форм миелоидного ростка, имеющих маркеры одного опухолевого клона.
Промежуточная стадия сопровождается нарастанием слабости, повышением температуры тела, появлением клеток с новыми цитогенетическими отклонениями, резистентных к применявшимся ранее цитостатикам, прогрессированием сплено- и гепато-мегалии. Эта стадия длится несколько месяцев, но при правильно назначенном лечении может быть пролонгирована.
Стадия бласттрансформации — властного криза — заканчивается смертью больных, несмотря на проводимую терапию, в
321
очень короткие сроки. В инфильтратах в костном мозге и во внутренних органах, а также в периферической крови появляются бластные формы (12—25 %), опухолевые клоны с новыми цито-генетическими нарушениями.
У 10 % больных заболевание заканчивается миелофиброзом, обусловленным действием цитостатиков. Другой причиной мие-лофиброза может быть двухростковая пролиферация клеток типа цитарных предшественников грануло- и мегакариоцитарного ростков. Последние продуцируют фактор роста тромбоцитов, активирующий фибробласты.
На аутопсии имеются характерные изменения внутренних органов: пиоидный костный мозг, значительные сплено- и генато-мегалия, умеренное увеличение лимфатических узлов.
ЛИМФОМЫ
• Лимфомы — регионарные злокачественные опухоли лимфо-идной ткани. Имеют моноклоновое происхождение, что используется при их диагностике и дифференциальной диагностике с реактивными гиперпластическими процессами в лимфоидной ткани.
Диагноз лимфом устанавливается прежде всего при биопсии
лимфатических узлов.
Классификация. В настоящее время используется несколько классификаций лимфом: H.Rappoport (1966), R.G.Lukes — R.D.Collins (1973—1974), R.E.A.L., кильская и ВОЗ, включающая в себя обе эти классификации.
Классификация лимфом [R.E.A.L. и кильская, 1996]
неклассический вариант
С преобладани ем лимфоцитов
studfiles.net
Лекция №4 ГЕМОБЛАСТОЗЫ
Лекция 4
ГЕМОБЛАСТОЗЫ
• Гемобластозы — опухолевые заболевания кроветворной и лимфатической ткани. Гемобластозы подразделяют на системные заболевания — лейкозы, а также регионарные — лимфомы.
Отличия между лейкозами и лимфомами заключаются не только в наличии или отсутствии системности поражения. Известно, что в терминальной стадии лимфомы дают обширное мета-стазирование, в том числе и в костный мозг. Другим важным отличием лейкозов от лимфом является то, что при лейкозах опухоль первично возникает на «территории» костного мозга, а при лимфомах костный мозг поражается вторично в результате ме-тастазирования.
При лейкозах опухолевые клетки, как правило, обнаруживаются в крови, поэтому в литературе используется термин для обозначения лейкозов, предложенный еще Р.Вирховым, «лейкемия».
В последние годы в литературе широко обсуждается вопрос о существовании предопухолевой стадии лейкозов и лимфом. Предлагаются термины «предлейкоз» и «предлимфома» для обозначения состояний с различными качественными и количественными изменениями кроветворной ткани, нередко предшествующими развитию гемобластозов.
Эпидемиология. Опухоли кроветворной и лимфоидной ткани в числе пяти самых распространенных опухолей человека. Среди опухолей детей первых 5 лет жизни на их долю приходится 30 % случаев.
Этиология. Как все опухоли, гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения, действующими на стволовые и полустволовые клетки-предшественницы. Большое значение в возникновении ряда гемобластозов имеет наследственный фактор.
Роль ионизирующей радиации в возникновении гемобласто-юв доказывается наблюдениями за пациентами, заболевшими
311
лейкозами и лимфомами через определенное время после атомной бомбардировки Японии, аварий на АЭС, ядерных испытаний. Описаны случаи заболеваний у людей, получавших радиотерапию, а также у врачей-радиологов. Известен цитогенетический маркер радиационного поражения — кольцевидная хромосома. Достоверно установлена связь между радиационным поражением и развитием острого и хронического миелолейкоза, острого эри-тромиелоза и острого лимфобластного лейкоза у детей.
Роль химических канцерогенов доказывается данными экспериментов, наблюдениями за пациентами, работавшими на вредных предприятиях с использованием бензола, а также за больными, получавшими цитостатическую терапию по поводу других онкологических заболеваний. Использование таких цитостатиче-ских препаратов, как мелфалан, азатиоприн, лейкеран, миелосан, антибиотика левомицетина, может приводить к возникновению острого и хронического миелолейкоза, острого миеломонобласт-ного лейкоза и эритромиелоза.
Роль вирусов в качестве этиологического фактора гемобла-стозов трактуется неоднозначно. В развитии гемобластозов человека доказано участие лишь двух вирусов: вируса Эпштейна — Барр (африканская лимфома Беркитта) и Т-лимфоцитарного вируса лейкоза человека первого типа (Т-клеточная лимфома и Т-клеточные лейкозы). Имеются экспериментальные данные, доказывающие прямое канцерогенное действие вирусов на гемопо-этические клетки посредством вирусных онкогенов. Однако в большинстве ситуаций внедрение вирусов в клетку вызывает лишь иммортализацию (бессмертие) последней, на фоне которой возникают дополнительные перестройки генома, ведущие к злокачественной трансформации (многоступенчатый канцерогенез).
Роль наследственности в развитии гемобластозов подтверждается частым развитием лейкозов у людей с наследственными заболеваниями со спонтанными разрывами хромосом (болезни Дауна, Блума, анемия Фанкони), с нерасхождением половых хро мосом (болезни Клайнфелтера, Тернера), а также существовани ем «лейкозных семей». Нередко лейкозы развиваются у пациен тов с наследственными дефектами иммунитета (атаксия-телеан гиэктазия, или синдром Луи-Бар, синдром Вискотта — Олдрид жа, болезнь Братона).
Патогенез. Множество этиологических факторов, воздейст вуя на стволовые и полустволовые гемопоэтические клетки, при водят к одинаковым результатам — злокачественной трансфор мации. Следовательно, существует так называемое узкое место через которое могут осуществлять свое воздействие различные агенты. Такое место, вероятнее всего, находится в геноме кле
312
ток, где располагаются протоонкогены и антионкогены. При этом могут происходить усиление экспрессии, амплификация, точечная мутация или другие изменения протоонкогенов, превращение их в клеточные онкогены, что приводит к развитию опухоли. Хромосомные перестройки могут привести к передислокации протоонкогена в зону влияния гена-энхансера, превращению его в клеточный онкоген и усилению экспрессии. Так, при лим-фоме Беркитта происходит реципрокная транслокация между хромосомами 8 и 14q32. Клеточный онкоген с-тус из хромосомы 8 перемещается на хромосому 14 и попадает в зону действия генов, регулирующих синтез тяжелых цепочек иммуноглобулинов. Описанные изменения сочетаются также с точечной мутацией N-ras.
При хроническом миелолейкозе нередко встречается филадельфийская хромосома, образовавшаяся в результате реципрок-ной транслокации между хромосомами 9 и 22. Образуется новый ген-гибрид c-abl-bcr, белковый продукт которого обладает тиро-зинкиназной активностью. Онкогены обычно встраиваются в разрывы хромосом. Так, при В-лимфоцитарных лимфомах и лейкозах происходят разрывы в хромосоме 14 в локусе 32q, где локализуются гены тяжелых цепочек иммуноглобулинов. При Т-лим-фоцитарных лейкозах и лимфомах — в локусе llq гена а-цепо-чек рецепторов Т-лимфоцитов.
Морфогенез. Развитие гемобластозов начинается с малигни-зации одной стволовой или полустволовой клетки, дающей пул опухолевых клеток. Это означает, что все гемобластозы имеют моноклоновое происхождение. Моноклоновость происхождения подтверждается экспериментальными и клиническими данными по обнаружению во всех опухолевых клетках одного и того же больного клоновой метки — хромосомной или изоферментной. Например, во всех опухолевых клетках при хроническом миелолейкозе присутствует филадельфийская хромосома.
Стволовые клетки составляют примерно 0,01—0,001 % всей популяции костномозговых клеток. Рост и дифференцировка стволовых и полустволовых клеток-предшественниц управляются факторами роста (схема 34) и стромальным микроокружением, что подтверждается экспериментами с клеточными культурами, где рост и дифференцировка клеток происходят только в присутствии факторов роста или стромальных клеток. Стро-мальные клетки, вероятно, также выделяют факторы роста, свя-заные с их клеточными мембранами, а также гепарансульфата-ми стромы, обеспечивая тем самым локальный рост.
313
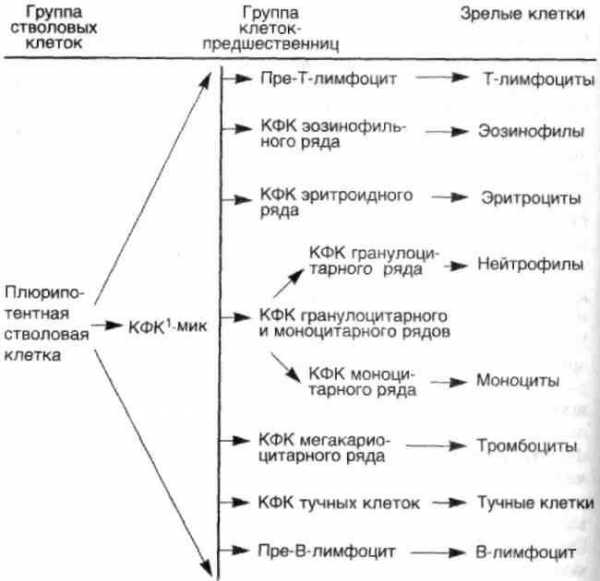
Схема 34. Структура гемопоэтической системы
1 Колониеформирующая клетка, син, колониеобразующая клетка (КОЕ).Результаты работ по изучению морфологии и клеточной кинетики гемобластозов, в первую очередь лейкозов, показали, что при развитии опухолей происходит не только малигнизация на уровне стволовых и полустволовых клеток-предшественниц, но также развивается блок дифференцировки в пуле опухолевых клеток.
ЛЕЙКОЗЫ
При лейкозах опухолевая ткань первоначально разрастается на «территории» костного мозга и постепенно замещает нормальные ростки кроветворения. Механизмы этого явления мало изучены. Вероятно, речь идет не о простом механическом вытеснении, а скорее о подавлении нормальных ростков клоном лей-козных клеток с участием особых факторов и контактного тор
314
можения. В результате этого процесса у больных лейкозами закономерно развиваются различные варианты цитопений — анемия, тромбоцитопения, лимфоцитопения, гранулоцитопения, что приводит к повышенной кровоточивости, кровоизлияниям, подавлению иммунитета с присоединением инфекционных осложнений.
Метастазирование при лейкозах сопровождается появлением лейкозных инфильтратов в различных органах — печени, селезенке, лимфатических узлах и др. В органах могут развиваться изменения, обусловленные обтурацией сосудов опухолевыми клетками — инфаркты, язвенно-некротические осложнения.
Принципы классификации лейкозов. Выделяют пять основных принципов классификации: по характеру течения лейкозов; по степени дифференцировки опухолевых клеток; в соответствии с цитогенезом; на основе иммунного фенотипа опухолевых клеток; по общему числу лейкоцитов и наличию бластных клеток в периферической крови.
По характеру течения выделяют острые, протекающие менее года, и хронические, существующие длительное время.
По степени дифференцировки опухолевых клеток выделяют недифференцированные, властные и цитарные лейкозы.
При высоком блоке дифференцировки лейкозные клетки могут напоминать стволовые и бластные клетки первых четырех классов клеток-предшественниц [Чертков И.Л., Воробьев А.И., 1993]. Поэтому по степени дифференцировки эти лейкозы называют властными и недифференцированными. Поскольку они протекают остро, то можно говорить, что острые лейкозы — это бластные и недифференцированные лейкозы.
При низком блоке дифференцировки лейкозные клетки напоминают процитарные и цитарные клетки-предшественницы, лейкозы протекают менее злокачественно, хронически и называются цитарными.
Цитогенетические варианты лейкозов основываются на представлениях о кроветворении (см. схему 34). Острые лейкозы по цитогенезу подразделяются на лимфобластный, миелобластный, монобластный, миеломонобластный, эритроми-елобластный, мегакариобластный, недифференцированный. Хронические лейкозы представлены лейкозами миелоцитарного происхождения (хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, хронический базофильный лейкоз, миелосклероз и др.), лим-фоцитарного происхождения (хронический лимфолейкоз, пара-протеинемические лейкозы: миеломная болезнь, первичная мак-роглобулинемия Вальденстрема, болезнь тяжелых цепей Франк-
315
лина; лимфоматоз кожи — болезнь Сезари и др.), моноцитарно-го происхождения (хронический моноцитарный лейкоз, гистио-цитоз X).
Иммунный фенотип опухолевых клеток.В настоящее время стало возможным проводить более точное ти-пирование опухолевых клеток в зависимости от их иммунного фенотипа по экспрессии CD 19, CD20, CD5, легких цепочек иммуноглобулинов и других антигенных маркеров.
По общему числу лейкоцитов в периферической крови и наличию лейкозных клеток выделяют лейкемические (более 50—80 • 109/л лейкоцитов, в том числе бластов), сублейкемические (50—80 • 109/л, в том числе бласты), лейкопенические (содержание лейкоцитов в периферической крови ниже нормы, но есть бласты), алейкемические (содержание лейкоцитов в периферической крови ниже нормы, бласты отсутствуют).
Морфологическое исследование имеет большое значение в диагностике лейкозов. Основными методами прижизненной морфологической диагностики являются исследования мазков периферической крови и биоптатов костного мозга, которые получают при трепанации гребешка подвздошной кости или пункции грудины, а также других органов.
Острые лейкозы
Различные формы острого лейкоза имеют стереотипные морфологические проявления: лейкозная инфильтрация костного мозга в виде очаговых и диффузных инфильтратов из клеток с крупными светлыми ядрами, содержащими по нескольку ядрышек. Размеры и очертания ядер, а также ширина ободка цитоплазмы могут варьировать. Бласты составляют 10—20 % костномозговых клеток. Цитогенетическую принадлежность бластов, как правило, можно выявить только с помощью специальных методов исследования — цитохимических и иммуногистохимиче-ских. Применяются реакции на пероксидазу, окраска на липиды Суданом черным, ШИК-реакция, гистоферментохимические реакции на выявление неспецифической эстеразы, хлорацетатэсте-разы, кислой фосфатазы, Иммуногистохимически возможно определение маркеров В-, Т-лимфоцитов, клеток миелоидного и моноцитарного рядов.
В периферической крови и в костном мозге описывается феномен лейкемического провала («hiatus leucemicus»), развивающийся за счет наличия только бластных и дифференцированных клеток и отсутствия промежуточных форм.
В костномозговой ткани происходят вытеснение нормальных клеток гемопоэза опухолевыми, истончение и резорбция ретику-
лярных волокон, нередко развивается миелофиброз. При цито-статической терапии происходит опустошение костного мозга с гибелью бластных форм, увеличивается число жировых клеток и разрастается соединительная ткань.
Лейкозные инфильтраты в виде диффузных или очаговых скоплений обнаруживаются в лимфатических узлах, селезенке и печени. Это приводит к увеличению размеров этих органов. В печени характерно развитие жировой дистрофии. В связи с лейкоз-ной инфильтрацией слизистых оболочек полости рта и ткани миндалин появляются некротический гингивит, тонзиллит — некротическая ангина. Иногда присоединяется вторичная инфекция и развивается сепсис, приводящий больных к смерти.
В результате тромбоцитопении, повреждения печени и стенок сосудов у больных острыми лейкозами нередко возникает геморрагический синдром вплоть до развития смертельных осложнений — кровоизлияний в головной мозг и желудочно-кишечных кровотечений.
Использование активной цитостатической терапии повлияло на течение острых лейкозов, т.е. привело к индуцированному лекарственному патоморфозу. В связи с этим в настоящее время выделяют следующие клинические стадии заболевания: первая атака, ремиссия (полная или неполная), рецидив (первый, повторный).
Наибольшее значение среди острых лейкозов имеют острый лимфобластный и острый миелобластный лейкозы.
Острый лимфобластный лейкоз. Самый распространенный лейкоз в детском и юношеском возрасте. Пик заболеваемости приходится на возраст от 1 года до 6 лет. Протекает с поражением костного мозга, лимфатических узлов, селезенки, вилочковой железы, а также других органов. Центральная нервная система обычно вовлекается при рецидивах заболевания после химиотерапии. В костном мозге, периферической крови и в других органах обнаруживаются опухолевые клетки типа лимфобластов с ШИК-положительными гранулами в цитоплазме, не дающие реакций на пероксидазу, эстеразы и не содержащие липиды.
В 2/3 случаев в опухолевых клетках обнаруживаются цитоге-нетические нарушения в виде полиплоидии, филадельфийской хромосомы и реципрокной транслокации между хромосомами 8 и 14.
Цитогенез острого лимфобластного лейкоза связан с предшественниками Т- и В-лимфоцитов. На Т-клеточные лейкозы в странах Европы приходится 10—15 % наблюдений. Преобладают В-клеточные лейкозы.
Руководствуясь иммунологическими фенотипами опухолевых клеток, выделяют несколько форм лимфобластного лейкоза, что имеет значение для выбора терапии и прогноза. Преобладающие
316
317
В-лимфобластные лейкозы представлены ранним, промежуточным и поздним вариантами, отличающимися по экспрессии пара-глобулина CD 10, поверхностного иммуноглобулина и активности терминальной диоксинуклеотидтрансферазы. Маркерами Т-лимфобластного лейкоза являются антигены CD7 и Т-рецепто-ров.
У детей преобладает промежуточный вариант, у взрослых — ранний и промежуточный. Прогноз у детей значительно лучше, чем у взрослых. Выживаемость составляет соответственно 60 и 30 %. Наихудший прогноз при Т-лимфобластном лейкозе.
Острый миелобластный лейкоз. Наиболее частая форма заболевания у взрослых с относительно хорошим прогнозом — ремиссии наступают у 70—80 % больных, полные ремиссии — у 25 % больных.
Описываются наблюдения развития острого миелобластного лейкоза у людей, подвергшихся радиационному воздействию, контактирующих с бензолом (кожевенная индустрия в Турции, производство синтетических клеев и др.), принимавших цитоста-тические препараты, а также у страдающих наследственными заболеваниями — болезнью Дауна, анемией Фанкони, синдромом Блума.
Опухолевые клетки имеют типичные для миелобластов цитохимические маркеры: ШИК-положительную диффузно окрашенную цитоплазму, содержат липиды, пероксидазу, эстеразы. Опухолевые клетки инфильтрируют костный мозг, приобретающий макроскопически пиоидный вид, селезенку, печень, лимфатические узлы, слизистую оболочку желудочно-кишечного тракта, что сопровождается язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев лейкозные инфильтраты обнаруживаются в легких («лейкозный пневмонит»), в 114 — в оболочках мозга («лейкозный менингит»). По иммунологическим фенотипам выделяют 6 вариантов заболевания.
Больные умирают от кровоизлияний в головной мозг, желудочно-кишечных кровотечений и инфекционных осложнений. Лечение цитостатиками изменило проявления заболевания, удлинило жизнь больным.
Хронические лейкозы
Хронические лейкозы отличаются от острых цитарной диф-ференцировкой опухолевых клеток, более длительным стадийным течением.
Первая стадия заболеваний характеризуется присутствием одного клона опухолевых клеток, течет годами, относительно доброкачественно, хронически и называется м о н о -клоновой, доброкачественной.
318
ь Вторая стадия обусловлена появлением вторичных опухолевых клонов, характеризуется быстрым, злокачественным течением с появлением множества бластов и называется злокачественной, поликлоновой стадией, или стадией властного криза. 80% больных хроническими лейкозами погибают в стадии властного криза.
Результаты цитогенетических исследований показали, что злокачественная трансформация кроветворных клеток при хронических лейкозах может происходить на очень ранних стадиях — на стадиях стволовых клеток. Цитарный характер лейкозов обусловлен низким блоком дифференцировки в опухолевых клетках.
При хронических лейкозах лейкозные инфильтраты обнаруживаются в костном мозге, где в связи с длительными течением и цитостатической терапией нередко развивается миелофиброз в печени, селезенке и лимфатических узлах, которые иногда достигают значительных размеров.
Хронические лимфоцитарные лейкозы. Эти формы лейкозов объединяются в две группы. Первая — хронический лимфолей-коз и примыкающие к нему болезнь Сезари (лимфоматоз кожи), Т-клеточный лимфоцитарный лейкоз, пролимфоцитарный лейкоз (В-клеточный), волосато-клеточный лейкоз (В-клеточный). Вторая группа — парапротеинемические лейкозы. Наибольшее значение имеет хронический лимфолейкоз.
Хронический лимфолейкоз. Встречается обычно у лиц старше 40 лет, чаще в пожилом возрасте. Мужчины болеют в два раза чаще женщин. Заболеваемость достигает 6 случаев на 100 000 населения.
Цитогенез — в 95 % случаев из ранних В-клеток. Опухолевые клетки напоминают пролимфоциты и малые лимфоциты и экс-прессируют параглобулины CD 19, CD20, CD5.
В клинической картине преобладают лимфаденопатия, анемия (нередко аутоиммунная), тромбоцитопения, гранулоцитопе-ния, имеются выраженная иммунодепрессия и предрасположенность к инфекционным осложнениям. Прогноз относительно хороший, заболевание протекает длительно с высокими показателями выживаемости. Однако в финале может развиться властный криз.
Лейкозные инфильтраты диффузно поражают костный мозг, лимфатические узлы, которые могут достигать значительных размеров, образуя мягкие или плотноватые пакеты, а также сдавливать соседние органы. Селезенка резко увеличена, в отдельных случаях ее масса составляет несколько килограммов. Печень увеличена в меньшей степени.
Больные умирают обычно от инфекционных осложнений. Описаны наблюдения трансформации хронического лимфолеи-коза в неходжкинские лимфомы.
319
Парапротеинемические лимфолейкозы.В эту группу входят три заболевания — миеломная болезнь, первичная макроглобулинемия Вальденстрема и болезнь тяжелых цепей Франклина. Особенностью парапротеинемических лейкозов, которые также называются злокачественными иммунопро-лиферативными заболеваниями, является способность опухолевых клеток синтезировать однородные иммуноглобулины или их фрагменты — парапротеины, что связано с цитогенезом опухолевых клеток. Опухолевые клетки при парапротеинемических лейкозах дифференцируются по плазмоцитарному типу, сохраняя в извращенной форме особенность плазматических клеток синтезировать иммуноглобулины.
Наибольшее значение среди парапротеинемических лейкозов имеет миеломная болезнь.
Миеломная болезнь (болезнь Рустицкого — Калера, множественная миелома, генерализованная плазмоцитома) встречается в основном у взрослых. Описаны единичные наблюдения у людей моложе 30 лет. Свое название заболевание и опухолевая клетка получили в связи с преимущественной локализацией процесса на «территории» костного мозга (миелон — костный мозг).
Выделяют несколько вариантов миеломной болезни в зависимости от характера распространения миеломных инфильтратов в костном мозге, от характера миеломных клеток и от типа синтезируемого парапротеина.
По характеру распространенности опухолевого инфильтрата в костном мозге выделяют диффузную, диффузно-узловатую, множественно-узловатую формы миеломы; по клеточному составу — плазмоцитарную, плазмобластную, полиморфно-клеточную и мелкоклеточную миелому [Струков А.И., 1959].
В зависимости от способности секретировать различные типы парапротеинов различают несколько вариантов миеломной болезни: несекретирующие, диклоновые миеломы, миелому Бенс-Джонса, G-, А-, М-миеломы. Наиболее часто встречаются G-, А-миелома, миелома Бенс-Джонса, на долю которых приходится 75, 20 и 15 % наблюдений соответственно.
Опухолевая ткань разрастается преимущественно в плоских костях (череп, ребра, таз) и в позвоночнике, инициируя в них ос-теолизис, остеопороз. На рентгенограмме очаги поражения имеют вид гладкостенных пробоин. Полости образуются в местах роста миеломных клеток за счет активации ими остеокластов, осуществляющих лизис и резорбцию костной ткани (пазушное рассасывание). Высказываются предположения, что в качестве активирующих остеокласты субстанций могут выступать интер-лейкин-1 и бета-трансформирующий фактор роста, выделяемые миеломными клетками. Помимо костного мозга, опухолевые ин-фильтраты могут обнаруживаться и в других органах.
Осложнения миеломной болезни развиваются вследствие деструкции костной ткани — патологические переломы, боли в ко-
320
стях, а также из-за продукции парапротеинов — амилоидоз (AL-амилощоз), парапротеинемическая кома и парапротеиноз органов.
Хронические миелоцитарные лейкозы. Группа лейкозов, содержащих опухолевые клетки типа процитарных и цитарных предшественников миелоидного ряда. В эту группу входят хронический миелоцитарный лейкоз с или без филадельфийской хромосомы, ювенильный хронический миелоцитарный лейкоз, хронический нейтрофильный лейкоз, хронический эозинофильный лейкоз, первичный миелофиброз (мегакариоцитарная диффе-ренцировка опухолевых клеток). Разнообразие форм хронических миелоцитарных лейкозов обусловлено существованием общей клетки-предшественницы гранулоцитарного, моноцитарно-го, мегакариоцитарного, эозинофильного и базофильного ростков. При развитии всех этих форм злокачественная трансформация, вероятно, происходит на уровне плюрипотентной стволовой клетки миелоидного ростка, так как цитогенетические маркеры можно обнаружить во всех ветвях этого ростка.
Хронический миелолейкоз представляет наибольший практический интерес. Это нередкое заболевание, на долю которого приходится 15 % всех случаев лейкоза. В США ежегодно регистрируется 2500 новых случаев. Встречается в любом возрасте, немного чаще у лиц мужского пола. В развитии заболевания имеют значение те же этиологические факторы, что и при остром миелобластном лейкозе.
Цитогенетическим маркером заболевания является филадельфийская хромосома, свидетельствующая также и о плохом прогнозе.
Заболевание протекает в две или даже три стадии: хроническая стадия, промежуточная (выделяется клиницистами, так как требует особых терапевтических мероприятий) и бласттранс-формации.
Хроническая стадия длится 3—4 года, нередко не имеет клинических проявлений. Морфологически в эту стадию обнаруживают сплено- и гепатомегалию, анемию. В костном мозге, периферической крови, в селезенке, печени и лимфатических узлах обнаруживают увеличение про- и цитарных форм миелоидного ростка, имеющих маркеры одного опухолевого клона.
Промежуточная стадия сопровождается нарастанием слабости, повышением температуры тела, появлением клеток с новыми цитогенетическими отклонениями, резистентных к применявшимся ранее цитостатикам, прогрессированием сплено- и гепато-мегалии. Эта стадия длится несколько месяцев, но при правильно назначенном лечении может быть пролонгирована.
Стадия бласттрансформации — властного криза — заканчивается смертью больных, несмотря на проводимую терапию, в
321
очень короткие сроки. В инфильтратах в костном мозге и во внутренних органах, а также в периферической крови появляются бластные формы (12—25 %), опухолевые клоны с новыми цито-генетическими нарушениями.
У 10 % больных заболевание заканчивается миелофиброзом, обусловленным действием цитостатиков. Другой причиной мие-лофиброза может быть двухростковая пролиферация клеток типа цитарных предшественников грануло- и мегакариоцитарного ростков. Последние продуцируют фактор роста тромбоцитов, активирующий фибробласты.
На аутопсии имеются характерные изменения внутренних органов: пиоидный костный мозг, значительные сплено- и генато-мегалия, умеренное увеличение лимфатических узлов.
ЛИМФОМЫ
• Лимфомы — регионарные злокачественные опухоли лимфо-идной ткани. Имеют моноклоновое происхождение, что используется при их диагностике и дифференциальной диагностике с реактивными гиперпластическими процессами в лимфоидной ткани.
Диагноз лимфом устанавливается прежде всего при биопсии
лимфатических узлов.
Классификация. В настоящее время используется несколько классификаций лимфом: H.Rappoport (1966), R.G.Lukes — R.D.Collins (1973—1974), R.E.A.L., кильская и ВОЗ, включающая в себя обе эти классификации.
Классификация лимфом [R.E.A.L. и кильская, 1996]
неклассический вариант
С преобладани ем лимфоцитов
studfiles.net
причины, симптомы, диагностика и лечение
Гемобластозы – костномозговые и внекостномозговые неопластические процессы, представленные двумя группами заболеваний — миелопролиферативными (лейкозами) и лимфопролиферативными (гематосаркомами). Общими для всех форм гемобластозов являются гиперпластический, интоксикационный, геморрагический, анемический, иммунодефицитный синдромы. Диагностика гемобластозов включает общий анализ крови; проведение стернальной пункции, трепанобиопсии, биопсии лимфоузлов с исследованием материала; инструментальных исследований (УЗИ, рентгенографии, МСКТ). Лечение гемобластозов, главным образом, химиолучевое; в некоторых случаях может быть показана трансплантация костного мозга.
Общие сведения
Гемобластозы – злокачественные опухолевые заболевания, характеризующиеся первичным поражением кроветворной и лимфатической тканей. За последние десятилетия частота гемобластозов неуклонно растет: ежегодно в России, западноевропейских странах и США регистрируется 7-11 случаев опухолей кроветворной ткани на 100 тыс. населения. В структуре онкологической заболеваемости, среди злокачественных опухолей прочих локализаций, гемобластозы занимают 5-6 место. Замечено, что мужчины болеют гемобластозами чаще женщин, а сельские жители реже, чем городское население. У детей первых 5 лет жизни с абсолютной частотой преобладает острый лимфобластный лейкоз, у лиц в возрасте 20-45 лет – хронический миелолейкоз. Поиск адекватных путей профилактики, раннего выявления и эффективного лечения гемобластозов является острейшей проблемой онкогематологии.
Гемобластозы
Классификация гемобластозов
В структуре гемобластозов выделяют миелопролиферативные и лимфопролиферативные заболевания. Первые представлены лейкозами (лейкемией) – злокачественными опухолями кроветворной ткани с первичным поражением костного мозга; вторые – гематосаркомами, или лимфомами – внекостномозговыми объемными образованиями с первичным локальным ростом, преимущественно в лимфоузлах.
При этом по мере прогрессирования, лейкозы и гематосаркомы могут трансформироваться друг в друга. Так, при лейкозах может возникать метастазирование опухолевых клеток в плевру, брюшину, яички, лимфоузлы, мозговые оболочки. В то же время, на определенном этапе развития гематосаркомы в патологические процессы может вовлекаться костный мозг, т. е. происходить лейкемизация с развитием изменений крови, характерных для лейкоза. В некоторых случаях гемобластоз изначально развивается, как лимфома-лейкоз – заболевание, сочетающее признаки костномозгового и внекостномозгового поражения.
На основании морфологических различий клеток, образующих опухолевый субстрат, лейкозы делятся на острые и хронические. В основе острых лейкозов лежит пролиферация бластных клеток, хронических — преимущественно зрелых и промежуточных клеток. Основные клинико-гематологические формы острого лейкоза представлены: о. лимфобластным лейкозом детей и взрослых, о. миелобластным, о. монобластным, о. миеломонобластным, о. мегакариобластным и другими лейкозами.
Хронические лейкозы подразделяются на миелопролиферативные и лимфопролиферативные. К ним относятся следующие виды гемобластозов: хронический миелолейкоз, хронический лимфолейкоз, хр. эритромиелоз, полицитемия, миеломная болезнь и пр. Другая группа гематобластозов – гематосаркомы представлены лимфогранулематозом (лимфомой Ходжкина) и нелимфогранулематозными/неходжкинскими лимфомами.
Причины гемобластозов
Гемобластозы принадлежат к заболеваниям полиэтиологического характера с окончательно невыясненными причинами. Тем не менее, доподлинно установлены некоторые канцерогенные факторы, увеличивающие риск возникновения гематобластозов. В первую очередь, это радиационное воздействие на организм различного происхождения: ультрафиолетовое и ионизирующее излучение, лучевая и радиоизотопная диагностика, лучевая терапия по поводу других онкологических заболеваний.
Мутагенным действием на клетки обладают химические вещества (бензол), многие лекарственные препараты (хлорамфеникол, фенилбутазон и др.), в том числе, цитостатики (метотрексат, циклофосфан, хлорамбуцил и др.). Этим объясняется тот факт, что у онкобольных, получающих химиолучевую терапию по поводу первичной злокачественной опухоли, нередко развиваются вторичные гемобластозы.
Повышенную вероятность лейкозной трансформации миелоидных или лимфоидных клеток предопределяют некоторые хромосомные дефекты, в частности, синдром Дауна, синдром Луи-Бар, анемия Фанкони, синдром Клайнфельтера и др. В происхождении гемобластозов доказана этиологическая роль вирусных факторов (вируса Эпштейна-Барра, ретровирусов) и обменных нарушений (расстройства метаболизма триптофана и тирозина).
Симптомы гемобластозов
Гемобластозы сопровождаются многочисленными местными и системными проявлениями. Манифестация гемобластозов может быть острой, напоминающей клинику ОРВИ, или медленной, латентной. Наиболее типичными для различных форм гемобластозов являются интоксикационный, пролиферативный (гиперпластический), геморрагический, анемический синдромы и синдром инфекционных осложнений.
В большинстве случаев первыми признаками гемобластозов служат неспецифические симптомы общей интоксикации – длительное немотивированное повышение температуры, утомляемость, потливость, астенизация. Гиперпластический синдром при гемобластозах характеризуется генерализованной лимфаденопатией (увеличением шейных, подмышечных, паховых лимфоузлов), гепато- и спленомегалией. Типичны оссалгии, вызванные увеличением объема костного мозга. Вследствие сдавления верхней полой вены увеличенными внутригрудными лимфоузлами появляются отеки лица, шеи, верхних конечностей, одышка (т. н. синдром верхней полой вены).
Геморрагические проявления гемобластозов включают повышенную склонность к образованию подкожных и подслизистых кровоизлияний, возникновению десневых, носовых, желудочно-кишечных кровотечений, ДВС-синдрома. Вследствие вторичного иммунодефицита у больных с гемобластозами снижается сопротивляемость к инфекциям, поэтому у них легко возникают пневмонии, септицемия, внутрибольничные инфекции, которые могут иметь молниеносное течение и заканчиваться летально.
В течении гемобластозов выделяют стадии обострения и ремиссии (полной и неполной). О полной ремиссии говорят в случае отсутствия клинических признаков гемобластоза в течение месяца, нормализации картины крови, определения в миелограмме менее 5% бластных клеток.
Диагностика гемобластозов
Основанием для подозрения на гемобластоз (кроме клинической картины заболевания), служат изменения гемограммы (количества эритроцитов и тромбоцитов, количества и морфологии лейкоцитов, лимфоцитов). Эти отклонения от нормы могут быть различны, в зависимости от формы и вида гемобластоза. Все пациенты с отклонениями в общем анализе крови для уточнения диагноза должны направляться к гематологу.
На следующем диагностическом этапе для оценки кроветворения и определения характера гемобластоза проводится стернальная пункция или трепанобиопсия, пункционная или открытая биопсия лимфатических узлов. Полученный материал подвергается цитохимическому, цитогенетическому, гистологическому исследованиям. По показаниям выполняется УЗИ печени и селезенки, рентгенография ОГК и МСКТ грудной клетки, рентгенография черепа, ребер, позвоночника, костей таза. Проведение дифференциальной диагностики требуется, главным образом, между различными формами гемобластозов.
Лечение гемобластозов
Лечение гемобластозов осуществляется длительно и поэтапно: сначала в специализированном отделении стационара, затем – в гематологическом кабинете поликлиники. Для различных видов гемобластозов разработаны стандартизованные программы лечения. К общим принципам относится помещение больного в асептические условия (изолированные палаты с повышенным уровнем защиты от проникновения инфекции), проведение терапии, направленной на индукцию и консолидацию ремиссии. Обычно в качестве первой линии терапии гемобластозов избирается высокодозная моно- или полихимиотерапия цитостатическими препаратами. При достижении положительной динамики по результатам миелограммы, дозировка химиопрепаратов снижается до поддерживающей. С целью коррекции картины крови осуществляется заместительная гемотрансфузионная терапия (переливание эритро-, тромбомассы). Профилактика инфекционных осложнений предполагает назначение антибактериальных и антимикотических препаратов. В дополнение к цитостатической терапии может быть показано проведение гормональной терапии, локального облучения лимфоузлов, селезенки, выполнение спленэктомии.
Лекарственная терапия гемобластозов может осложняться цитостатической болезнью, включающей агранулоцитоз, септицемию, некротическую энтеропатию; сывороточным гепатитом, дистрофическими изменениями печени, апластической анемией и др. Эффективным и перспективным методом лечения гемобластозов является трансплантация костного мозга, однако основная сложность данной процедуры заключается в подборе HLA-совместимого донора.
Прогноз и профилактика гемобластозов
Прогноз зависит от формы гемобластоза, своевременности, правильности и полноты проведенных лечебных курсов. Так, при лимфогранулематозе полную ремиссию удается достичь у более 90% больных, при остром лейкозе – у 60-70%, что позволяет продлить жизнь пациентов на годы. Многим больным гемобластозами удается преодолеть 5-летний порог выживаемости и даже добиться полного выздоровления. Между тем, анализ эпидемиологических данных за последние десятилетия позволяет прогнозировать увеличение числа случаев гемобластозов в ближайшее время.
О профилактике гемобластозов можно говорить только с позиции снижения контакта с потенциально опасными факторами — источниками ионизирующего излучения, химическими веществами, вирусными агентами. Практически здоровым людям ежегодно рекомендуется сдавать общий анализ крови.
www.krasotaimedicina.ru
Гемобластозы
5
Лекция
Гемобластозы.
Определение: это опухолевые заболевания кроветворной и лимфатической ткани. Они подразделяются на системные заболевания – лейкозы и регионарные лимфомы.
Отличия между ними заключаются : 1)в системности поражения при лейкозах; 2) лимфомы в терминальной фазе дают обширное метастазирование; 3) при лейкозах костный мозг поражается первично; 4) при лимфомах – вторично вследствие метастазирования; 5) При лекозах опухолевые клетки циркулируют в крови – проявления лейкемии, термин предложенный впервые Р. Вирховым.
Развитию гемобластозов, как и многим другим опухолевым процессам предшествуют стадии: а) «предлейкоза», б) «предлимфомы» с количественными и качественными изменениями кроветворной ткани.
Этиология. Как и все опухоли гемобластозы могут вызываться разнообразными мутагенными факторами экзогенного и эндогенного происхождения оказывающими канцерогенное действие на стволовые и полустволовые клетки предшественники. Большое значение в развитии ряда лейкозов имеет наследственный фактор.
Определенную роль в развитии лейкозов играет ионизирующая радиация – атомная бомбардировка Японии, аварии на АЭС, ядерные испытания, радиотерапия.
Известен цитогенетический маркер радиационного поражения организма-кольцевидная хромосома в кроветворных клетках. Установлена четкая связь радиационного поражения с развитием острого и хронического миелолейкоза у взрослых, а у детей – острого эритромиелоза и острого лимфобластного лейкоза.
Роль химических канцерогенов: Установлено, что такие химические вещества как а) бензол, б) лекарственные цитостатики: мелфалан, азотиоприн, лейкеран, миелосан, в) антибиотик левомицетин вызывают острый и хронический миелолейкоз, миелобластный лейкоз и эритромиэлоз.
Роль вирусов трактуется неоднозначно. Пока точно доказано участие в развитии лейкозов только двух вирусов: а) Эпштей-Барра, имеющего отношение к Африканской лимфоме Беркитта; б) вируса Т-лимфоцитарного лейкоза человека первого типа –Т-клеточного лейкоза, Т-клеточной лимфомы.
Внедрение вирусов в клетку вызывает посредством многоступенчатого канцерогенеза перестройку генома, ведущую к злокачественной трансформации клеток крови.
Роль наследственности: а) отмечено частое развитие лейкозов при наследственных заболеваниях, сопровождающихся спонтанными разрывами хромосом — это болезни Дауна, Блума, анемия Фанкони; б) с нерасхождением половых хромосом – болезни Клайнфельтера, Тернера: в) существование «лейкозных семей»; г) развитие лейкозов у лиц с наследственными дефектами иммунной системы: синдромы –Луи-Бара, Вискотта-Олдриджа, Братона.
Патогенез. Изучение механизмов развития лейкозов показало, что этиологические факторы действуют на протоонкогены и антионкогены генома клетки, вызывая усиление: а) экспрессии, б) амплификацию, в) точковую мутацию, г) другие изменения протоонкогенов, превращая их в клеточные онкогены, что приводит к развитию опухоли, исходящей из кроветворной ткани.
Морфогенез лейкозов. Развитие гемобластозов начинается с малигнизации ОДНОЙ стволовой или полустволовой клетки, дающих моноклоновый пул опухолевых клеток. Моноклоновость подтверждается экспериментом и клиникой. При этом малигнизация происходит не только на уровне стволовых и полустволовых клеток, но и блокирование дифференцировки в клоне опухолевых клеток.
Лейкозы.
Первоначальный рост лейкозных клеток происходит в костном мозге с замещением нормальных ростков кроветворения. Механизмы этого явления мало изучены. В результате вытеснения нормального кроветворения развиваются различные варианты цитопении:
а) эритропении, за которой следуют: прогрессирующая анемия, гипоксия, дистрофии; б) тромбоцитопения, способствующая развитию геморрагического синдрома; в) гранулоцитопения, для которой характерно подавление неспецифической защиты организма от инфекций, развитие инфекционных осложнений, в том числе и сепсиса.
Метастазирование лейкозов имеет свои характерные отличия от других видов злокачественных опухолей, обусловленные особенностями строения кроветворной ткани, в которой клетки располагаются свободно, не имея межклеточных контактов. Лейкозные метастазы – это лейкемические диффузные или очаговые инфильтраты, образованные опухолевыми клетками, обтурация сосудов клеточными эмболами, вызывающая образование инфарктов, язвенно-некротические осложнения в полых органах.
Принципы классификации лейкозов.
В основу классификаци лейкозов положены пять основных принципов:
деление по характеру клинического течения: а) острые – менее года, б) хронические – длительно с ремиссиями и рецидивами;
по степени дифференцировки опухолевых клеток, связанной с уровнем блока дифференцировки: а) недифференцированные, бластные лейкозы, напоминающие при микроскопии по своему строению и гистохимическим характеристикам клетки первых четырех классов клеток-предшественников дифферона нормального кроветворения; для них характерен высокий блок дифференцировки, «лейкемический провал» в гемограмме и острое клиническое течение;
б) хронические процитарные и цитарные «пестрые» лейкозы, с низким блоком дифференцировки, менее злокачественным хроническим течением заболевания.
3. по цитогенезу: острые: недифференцируемый, лимфобластные, миелобластные, монобластные, миеломонобластные, эритромиелобластные, мегакариобластный;
хронические: а).миелоцитарные: миелоцитарный, нейтрофильный, эозинофильный, базофильный, миелосклероз и др.;
б). лимфоцитарные: лимфолейкоз, миеломная болезнь, макроглобулинемия Вальденстрема, болезнь тяжелых цепей Франклина, лимфатоз кожи – болезнь Сезари и др.;
в). моноцитарные: моноцитарный , гистиоцитоз Х ;
по иммунному фенотипу опухолевых клеток, выявляемых антигенными маркерами: а) СД-19. б) СД-20, в) СД-5, г) легких цепей Ig, д) других антигенных маркеров;
по общему числу лейкоцитов и бластных опухолевых клеток в периферической крови при определении гемограммы:
а) лейкемические – более 50-80 х 10 клеток, включая бласты,
б) сублейкемические -50-80 х 10 клеток, включая бласты,
в) лейкопенические – число нейкоцитов ниже нормы, но есть бласты,
г) алейкемические – число лейкоцитов ниже нормы, но бласты отсутствуют.
Острые лейкозы.
Имеют стереотипные морфологические проявления:
очаговая, либо диффузная лейкозная инфильтрация кроветворного костного мозга, от которого остается не более 10-20% костномозговых клеток.
В периферической крови «лейкемический провал».
Опустошение гемопоэза с миелофиброзом, особенноо при цитостатической терапии.
Лейкозные инфильтраты в лимфатических узлах, селезенке, печени, слизистой полости рта — некротический гингивит, тонзиллит- некротическая ангина, сепсис.
Тромбоцитопения — геморрагическмй синдром, кровоизлияния в головной мозг, желудочно-кишечные кровотечения.
Проявления индуцированного патоморфоза под влияеием цитостатической терапии протекающего стадийно: а) первая атака, б) ремиссия полная, не полная, в) рецидив — первый, повторный, бластный криз.
Наибольшее клиническое значение имеют следующие лейкозы:
А) острый лимфобластный, самый распространенный в детском и юношеском возрастах, пик заболевания от 1 до 6 лет. Протекает с поражением костного мозга, л / узлов, селезенки, вилочковой железы и других органов. ЦНС вовлекается при рецидивах после химиотерапии. По иммунологическим фенотипам опухолевых клеток выделяют следующие формы: ранний, промежуточный, поздний. У детей преобладает промежуточная форма, у взрослых – ранняя и промежуточная.
Б) Острый миелобластный лейкоз.
Наиболее частая форма лейкоза взрослых с относительно хорошим прогнозом – ремиссии у 70-80% больных, полные длительные ремиссии у 25% больных. Характеризуется инфильтрацией костного мозга, который приобретает вид пиоидного (гноевидного), селезенки, печени, лимфузлов, слизистой ЖКТ с язвенно-некротическими и геморрагическими осложнениями. В 1/3 случаев в легких развивается «лейкозный» пневмонит, в ¼ формируется «лейкозный» менингит. По иммунологическим фенотипам выделяют 6 вариантов заболевания. Причина смерти: а) кровоизлияния в головной мозг,
б) кровотечения в ЖКТ,
в) инфекционные осложнения, включая сепсис.
Применение цитостатиков продлевает жизнь.
Хронические лейкозы.
Характерным отличием от острых лейкозов являются: 1) цитарная дифференцировка опухолевых клеток, 2) длительное стадийное течение: а) первая стадия моноклоновая, б) вторая стадия – бластного криза, во время которой погибают до 80% всех больных.
3. отличие от острых форм – злокачественная трансформация лейкозных клеток происходит на стадиях стволовых клеток, а блок дифференцировки на уровне цитарных клеток гемопоэтического дифферона.
Выраженные лейкемические инфильтраты с превращением а) костного мозга в пиоидный, б) печени в гепатомегалическую, в) селезенки в спленомегалическую. Лимфоузлы в гиперпластические. Г) развитие лекарственного патоморфоза под влиянием цитостатиков, проявляющегося в виде миелофиброза.
Из хронических лимфоцитарных лейкозов наибольшее клиническое значение имеет хронический лимфолейкоз. Он развивается обычно у лиц старше 40 лет, чаще в пожилом возрасте, у мужчин в два раза чаще, чем у женщин. Клиническое течение этой формы лейкоза характеризуется проявлением: лимфоаденопатии, анемии, тромбоцитопении, гранулоцитопении, выраженной иммунодепресии, предрасположенностью к инфекционным осложнениям. Тем не менее, прогноз хороший, высокие показатели выживаемости. В финале заболевания может развиться бластный криз. Диффузные лейкозные инфильтраты (своеобразная форма метастазов) выявляются : в костном мозге, лимфоузлах, достигающих больших размеров, в увеличенной до нескольких кг селезенке (спленомегалия), в увеличенной печени (гепатомегалия). Иногда отмечается трансформация хронического лимфоцитарного лейкоза в неходженские лимфомы. Смерть наступает от инфекционных осложнений.
Парапротеинемические лейкозы.
В эту группу входят три заболевания: макроглобулинемия Вальденстрема, болезнь Франклина и миеломная болезнь Рустицкого –Калера. Миеломная болезнь встречается в основном у взрослых, редко у людей моложе 30 лет, имеет наибольшее клиническое значение. Выделяют три формы проявления: а) диффузную, б) диффузно-узловатую и в) множественно-узловатую. По клеточному составу различают: а) плазмоцитарную, б) плазмобластную, в) полиморфноклеточную, г) мелкоклеточную. По способности секретировать парапротеины: а) не секретирующие, б) диклоновые, в)миелома Бенс-Джонса, г) миеломы IgG,IgA,IgMпродуцирующие. Наиболее часто втречаются продуцирующиеIgG(75%),A(20%), Бенс-Джонса (15%) миеломы. Опухолевая ткань разрастается в плоских костях черепа, ребер, таза, реже других органов. Осложнения: а) патологические переломы, б) амилоидоз, в)парапротеинемичекая кома, в) парапротеиноз внутренних органов.
Миелоцитарные лейкозы.
Из этой группы лейкозов наибольшее клиническое значение имеет хронический миелолейкоз. На его долю приходится 15% всех лейкозов. Встречается в любом возрасте, чаще у мужчин. Цитологическим маркером является филадельфийская хромосома. Заболевание протекает стадийно: а) хроническая стадия продолжительностью 3-4 года со сплено- и гепатомегалией, б) промежуточная – несколько месяцев, в) стадия бласттрансформации – в короткий срок наступает смерть. На секции обнаруживают : пиоидный костный мозг, гепато- спленомегалию, умерено выраженное увеличение лимфатических узлов.
Лимфомы.
Определение — лимфопролиферативные очаговые злокачественные процессы исходящие из лимфоидной ткани.
Происхождение – моноклональное. Подразделяются на:
1. а)Ходжскинскую лимфому или лимфогранулематоз и б) неходжскинские лимфомы.
2. а) В и Т- лимфоцитарные, б) неклассифицируемые,
3. а) низкой, б) умеренной, в) высокой злокачественности по степени дифференцировки опухолевых клеток.
В терминальной стадии заболевания возможна генерализация процесса – «лейкемизация лимфомы».
Лимфогранулематоз. Одно из загадочных заболеваний. Впервые 6 наблюдений описал в 1832 году англичанин Ходжкин. Спустя 94 года – в 1926 году характерные морфологические проявления изучил англичанин Фокс. У этой болезни отмечаются два возрастных пика – в молодом (30 лет) и пожилом (после 60) возрасте. Этиология не известна, хотя у 35% больных выявлены антитела к вирусу Эпштейн-Барра, а в диагностических клетках Березовского -_Штернберга — Рид_-Пальтауфа обнаружены мембранные протеины этого вируса. Диагностические клетки Березовского -_Штернберга — Рид-Пальтауфа не имеют аналога среди нормальных клеток человеческого организма, что дает повод считать их гибридомами, так как они постоянно экспрессируют маркеры клеток лимфоидного ряда – СД-30, гранулоцитарного ряда – СД- 15, Т- и В-лимфоцитов.
Выделяют: 1. изолированный вариант течения с поражением одной группы лмфоузлов, шейных. Медиастинальных, забрюшинных и т.д.,
2. генерализованный с распространением процесса на несколько групп лимоузлов с вовлечением селезенки («порфировая» селезенка).
Гистологические варианты и стадии:
лимфогистиоцитарный с преобладанием лимфоидной ткани – первая стадия
нодулярный (узловой) склероз, — вторая стадия.
смешанно-клеточный вариант – третья стадия (гранулематозная).
с подавлением лимфоидной ткани – четвертая стадия (гранулематозно-некротическая). Прогноз зависит от числа сохранившихся лимфоцитов.
Неходжскинские лимфомы.
Неходжкинские лимфомы (НХЛ) – это гетерогенная группа злокачественных лимфопролиферативных опухолей, отличающихся по биологическим свойствам, морфологическому строению, клиническим проявлениям, ответу на терапию и прогнозу. Выделение различных вариантов НХЛ базируется на иммунофенотипических характеристиках опухолевых клеток, учитывающих клиническую картину и другие биологические особенности.
Среди В-лимфом выделяют: А) лимфоцитарную, Б) лимфоплазмоцитарную, В) центроцитаорную(центробластную) Г)лимфому Беркитта, Д) лимфобластную, Е) анапластическую крупноклеточную.
Т-лимфомы встречаются реже- не более 10-15%. Их делят на :А) лимфобластные, Б) лимфоцитарные, В) периферические – лимфома кожи с лейкемизацией.
Наиболее значимыми факторами неблагоприятного прогноза являются: возраст старше 60 лет, повышение уровня ЛДГ, общее состояние больного, соответствующее 2-4 степени, III-IVстадия болезни, наличие более одного экстранодального очага поражения, вовлечение костного мозга. Это было положено в основу Международного прогностического индекса – МПИ .
На основании количества имеющихся неблагоприятных факторов прогноза выделяют 4 степени риска раннего прогрессирования болезни:
низкая степень риска – отсутствие или присутствие лишь одного неблагоприятного признака,
низкая/промежуточная – наличие 2 факторов, промежуточная/высокая –наличие 3 факторов
высокая –наличие 4 факторов.
Наличие двух и более факторов отрицательно сказывается на прогнозе заболевания независимо от морфологического варианта опухоли. Все морфологические варианты разделены по степени злокачественности. Опухоли низкой степени злокачественности характеризуются медленным прогрессированием, длительной выживаемостью (годы), умеренной чувствительностью к химиотерапии и отсутствием возможности излечения при использовании стандартной химиотерапии.
Высокоагрессивные лимфомы быстро прогрессируют, выживаемость составляет лишь месяцы, они умеренно- и высокочувствительны к химиотерапии и могут быть излечены стандартными методами химиотерапии. Клиническими особенностями НХЛ высокой степени злокачественности является быстрый рост опухолевых образований и склонность к раннему прогрессированию.
studfiles.net
testy_patanatomia (1)
АЛЬТЕРАЦИЯ. ДИСТРОФИИ. НЕКРОЗ
1. Какую сущность отражает термин «дистрофия»:
1) некроз;
2) нарушение метаболизма;
3) воспаление.
2. Выберите морфогенетический механизм развития дистрофий:
1) повреждение;
2) некроз;
3) фанероз;
4) воспаление.
3. Исходом гиалиново-капельной дистрофии чаще всего является:
1) возврат к нормальному состоянию;
2) гибель клетки;
3) переход в другие формы дистрофий.
4. Понятие «паренхиматозные дистрофии» относится к классификации:
1) по локализации процесса;
2) по виду нарушенного обмена;
3) по распространенности процесса.
5. Какой из перечисленных органов прежде всего подвергается диабетической микроангиопатии:
1) головной мозг;
2) печень;
3) почки;
4) сердце
6. Наличие вакуолей в клетке характерно: 1) для гиалиново-капельной дистрофии;
2) роговой дистрофии;
3) гидропической дистрофии.
7. Укажите орган, в котором коллоидная дистрофия имеет яр — кое выражение:
1) печень;
2) щитовидная железа;
3) вилочковая железа;
4) кости скелета.
8. Укажите макроскопический вид сердца со стороны эндокарда при жировой паренхиматозной дистрофии:
1) желтое сердце;
2) тигровое сердце;
3) бычье сердце.
9. При жировой дистрофии орган имеет консистенцию
1) плотную;
2) дряблую;
3) нормальную.
10. Какие дистрофии из ниже перечисленных являются стромально-сосудистыми:
1) мутное набухание органа;
2) амилоидоз;
3) гидропическая;
4) мукоидное набухание;
5) фибриноидное набухание.
11. Ожирение сердца является проявлением:
1) жировой дистрофии;
2) тучности;
3) нарушения обмена холестерина;
4) «тигрового» сердца;
5) атеросклероза.
12. Какая из перечисленных дистрофий не относится к стромально-сосудистым:
1) жировая дистрофия;
2) простое ожирение сердца;
3) тучность;
4) липоматоз;
5) атеросклероз.
13. Какова причина первичного ожирения:
1) алиментарная;
2) метаболическая;
3) эндокринная;
4) наследственная;
5) неизвестная.
14. Укажите характерную черту мукоидного набухания по локализации изменений:
1) клетки соединительной ткани;
2) основное вещество соединительной ткани;
3) паренхиматозные клетки глии;
4) накопление липидов в строме.
15. Гиалиноз может развиться в исходе:
1) амилоидоза;
2) ожирения;
3) фибриноидного набухания;
4) лейкоплакии.
16. Какой краситель элективно выявляет амилоид:
1) судан III;
2) толуидиновый синий;
3) гематоксилин-эозин;
4) конго красный;
5) пикрофуксин.
17. Биохимическая природа амилоида:
1) животный крахмал;
2) белок;
3) белково-полисахаридный комплекс;
4) мукопротеид;
5) хромопротеид.
18. Какой краситель необходимо применить для выявления мукоидного набухания:
1)гематоксилин-эозин;
2)судан III;
3)йодгрюн;
4)пикрофуксин;
5)толуидиновый синий.
19. Какая разновидность амилоидоза всегда является осложнением, а не основным заболеванием:
1)идиопатический;
2)приобретенный;
3)старческий;
4)наследственный;
5)локальный,
20. Какие липиды откладываются в стенках артерий при атеросклерозе:
1)фосфатиды;
2)лецитины;
3)сфинголипиды;
4) воска;
5) стерины и стероиды.
21. «Сальная» селезенка характерна:
1)для мукоидного набухания;
2)фибриноидного набухания;
3)гиалиноза;
4)амилоидоза;
5)мутного набухания.
22. Назовите желтуху, которая может наблюдаться при гепатите и циррозе печени:
1)надпеченочная;
2)печеночная;
3)подпеченочная.
23. Назовите виды желтух по механизму развития: 1) гипостатическая;
2) токсическая;
3) надпеченочная;
4) бактериальная;
5) печеночная;
6) подпеченочная.
24. Назовите процесс, относящийся к местному меланозу:
1) лейкоплакия;
2) невус;
3) витилиго;
4) карциноид.
НАРУШЕНИЕ КРОВООБРАЩЕНИЯ
1. Какой процесс ведет к развитию общего гемосидероза:
1) экстраваскулярный гемолиз;
2) некроз стенки сосуда;
3) интраваскулярный гемолиз;
4) образование гематомы;
5) диапедезные кровоизлияния.
2. Какие процессы развиваются в печени при хроническом венозном полнокровии:
1) стаз;
2) полнокровие в центре дольки и склероз;
3) артериальное полнокровие;
4) кровоизлияния.
3. Что такое анасарка:
1) отек кожи и подкожной клетчатки;
2) накопление транссудата в плевральной полости;
3) накопление отечной жидкости в полости перикарда.
4. Укажите виды отеков:
1) сердечные;
2) легочные;
3) печеночные;
4) почечные;
5) застойные;
6) белые.
5. Какие 4 процесса имеют значение в морфогенезе бурой индурации легких:
1) артериальное полнокровие;
2) хроническое венозное полнокровие;
3) гемосидероз;
4) диапедезные кровоизлияния;
5) фиброз;
6) стаз.
6. Что такое гематома?
1) геморрагическая инфильтрация;
2) точечные кровоизлияния;
3) внутреннее кровотечение;
4) скопление свернувшейся крови в ткани с нарушением ее целости.
7. Дайте определение кровоизлияния
1) истечениекрови из сосудов;
2) истечение крови из сердца
3) скопление крови в тканях,
8. Какое нарушение стенки сосуда происходитприаневризме аорты:
1) разрыв;
2) разъедание;
3) повышение проницаемости.
ВОСПАЛЕНИЕ
1. Что такое транссудат:
1) кровь без фибриногена;
2) накопление крови в серозной оболочке;
3) отечная жидкость;
4) воспалительный выпот.
2. Назовите причину кровотечения:
1) снижение проницаемости сосуда;
2) склероз сосуда;
3) разрыв сосуда;
4) гиалиноз сосуда.
3. Что такое малокровие:
1) уменьшение кровенаполнения органа в результате недостаточного притока крови;
2) уменьшение кровенаполнения органа вследствие снижения оттока крови;
3) уменьшение объема циркулирующей крови.
4. Дайте определение инфаркта:
1) сосудистый некроз;
2) сосудистый склероз;
3) дистрофия;
4) воспаление сосуда.
5. Что такое тромбоз:
1) прижизненное свертывание крови;
2) посмертное свертывание крови;
3) прижизненный гемолиз;
4) посмертный гемолиз.
6. Что такое эмболия:
1) циркуляция в крови не встречающихся в норме частиц и закупорка ими сосудов;
2) циркуляция в крови не встречающихся в норме частиц и обтурация серозных полостей;
3) циркуляция в крови не встречающихся в норме частиц и развитие диапедезных кровоизлияний.
7. Выберите вид малокровия:
1) вакатное;
2) тканевое;
3) компрессионное;
4) коллатеральное.
8. Что такое ретроградная эмболия:
1) движение эмбола по току крови;
2) движение эмбола против тока крови;
3) перемещение эмбола из вен большого круга в артерии, минуя легкие.
9. Назовите вид тромба по цвету:
1) черный;
2) белый;
3) синий;
4) зеленый.
10. Какой вид кровоснабжения преобладает в органах, для которых характерны клиновидные инфаркты:
1) магистральный;
2) рассыпной;
3) коллатеральный.
11. Какой некроз характерен для туберкулеза:
1) казеозный;
2) марантический;
3) нейрогенный;
4) ишемический;
5) ценкеровский.
12. В каком из перечисленных органов может развиться гангрена:
1) селезенка;
2) печень;
3) желчный пузырь;
4) головной мозг;
5) кость.
13. В каком из перечисленных органов развивается колликвационный некроз:
1) селезенка;
2) легкие;
3) почка;
4) головной мозг;
5) надпочечник.
14. Как называется самопроизвольное отторжение конечности:
1) ампутация;
2) демаркация;
3) мутиляция;
4) секвестрация.
15. Какие из перечисленных камней могут встречаться в почках:
1) пигментные;
2) копролиты;
3) холестериновые;
4) ураты;
5) флеболиты.
16. Какие тромбы образуются при очень медленном токе крови в сосудах:
1) красные;
2) пристеночные;
3) белые;
4) мигрирующие.
17. Назовите части смешанного тромба:
1) головка;
2) брюшко;
3) тело;
4) хвост;
5) придатки.
18. Какой вид инфаркта характерен для миокарда:
1) белый;
2) белый с геморрагическим венчиком;
3) красный.
19. Какие из перечисленных клеток выбрасывают медиаторы воспаления:
1) лаброциты;
2)базофилы;
3)тромбоциты;
4)нейтрофилы;
5)макрофаги.
20. Как называется воспаление полостей со скоплением в них гноя:
1)абсцесс;
2)эмпиема;
3)пневмония;
4)фурункул.
21. Перечислите 2 вида клеток, осуществляющих фагоцитоз:
1)фагосома;
2)микрофаги;
3)фаголизосома;
4)макрофаги.
22. Чем характеризуется фаза пролиферации:
1)повреждением ткани;
2)фагоцитозом;
3)образованием экссудата;
4)размножением клеток.
23. Назовите вид фибринозного воспаления:
1)крупозное;
2)флегмонозное;
3)катаральное;
4)абсцесс.
24. Назовите 2 процесса, характеризующих эмиграцию клетоккрови при экссудации:
1)воспалительная гиперемия;
2)лейкодиапедез;
3)пиноцитоз;
4)эритродиапедез;
5)выброс медиаторов.
25. Назовите вид гнойного воспаления: 1) серозное;
2) крупозное;
3) дифтеритическое;
4) катаральное;
5) абсцесс.
26. Чем характеризуется фаза экссудации:
1) размножением клеток;
2) дистрофией;
3) эмиграцией клеток крови;
4) образованием медиаторов;
5) некрозом.
27. Что такое флегмона:
1) очаговое гнойное воспаление;
2) разлитое гнойное воспаление;
3) гнойное воспаление кожи;
4) гнойное воспаление подкожной клетчатки.
28. Укажите локализацию дифтеритического воспаления:
1) слизистые оболочки;
2) серозные оболочки;
3) кожа;
4) подкожная клетчатка.
29. Чем характеризуется фаза альтерации:
1) нарушением кровообращения;
2) образованием экссудата;
3) некрозом;
4) фагоцитозом.
30. Назовите оболочку абсцесса:
1) базальная мембрана;
2) пиогенная мембрана;
3) серозная мембрана;
4) фибринозная мембрана.
31. Чем характеризуется продуктивное воспаление:
1) преобладание альтерации;
2) преобладание экссудации;
3) преобладание пролиферации;
4) размножение эпителиальных клеток кожи.
32. Назовите отличие специфических гранулем от неспецифических:
1) вызываются любым возбудителем;
2) вызываются определенным возбудителем;
3) развитием нагноения.
33. Какие клеточные инфильтраты образуются при продуктивном воспалении:
1) нейтрофильные;
2) тромбоцитарные;
3) эпителиоидноктеточные;
4) эритроцитарные:
5) эозинофильные.
34. Для какого заболевания характерно развитие специфической гранулемы:
1) аппендицит;
2) сифилис;
3) ангина;
4) перитонит.
35. Укажите виды продуктивного воспаления:
1) катаральное, крупозное;
2) альтеративное, экссудативное;
3) гнойное, гнилостное;
4) межуточное, гранулематозное.
36. Укажите локализацию продуктивного воспаления с образованием полипов и остроконечных кондилом:
1) серозные оболочки;
2) слизистые оболочки;
3) печень;
4) почка;
5) селезенка.
37. Какие клетки встречаются в туберкулезной гранулеме: 1) клетки Вирхова;
2) клетки Микулича;
3) клетки Пирогова-Лангханса.
38. Назовите клетки характерные для лепромы:
1) клетки Вирхова;
2) клетки Микулича;
3) клетки Пирогова-Лангханса.
39. Назовите клетки, характерные для риносклеромы:
1) клетки Вирхова;
2) клетки Микулича;
3) клетки Пирогова-Лангханса.
40. Укажите вид продуктивного воспаления:
1) дифтеритическое;
2) гранулематозное;
3) геморрагическое.
РЕГЕНЕРАЦИЯ. ПРИСПОСОБЛЕНИЕ. КОМПЕНСАЦИЯ
1. За счет чего происходит восстановление ткани или органа при реституции:
1) счет клеток крови;
2) счет ткани, идентичной погибшей;
3) счет опухолевой ткани.
2. Назовите вид заживления раны:
1) непосредственное закрытие дефекта эпителиального покрова;
2) метаплазия;
3) формирование новообразованных сосудов;
4) замещение раневого дефекта гиалиновым хрящом.
3. Назовите вид нейрогуморальной гипертрофии:
1) ложная гипертрофия;
2) акромегалия;
3) гепатомегалия;
4) вакатная гипертрофия.
4. Какие формы регенерации различают по виду гиперпластических процессов:
1) полная, неполная;
2) клеточная, внутриклеточная;
3) ложная, истинная.
5. Чем отличается заживление ран вторичным натяжением от заживления первичным натяжением:
1) развитием нагноения;
2) развитием гранулем;
3) появлением грануляционной ткани.
6. За счет чего осуществляется клеточная форма регенерации:
1) митоз, амитоз;
2) увеличение числа ядер в клетках;
3) увеличение объема клетки.
7. Как называются клетки, размножающиеся в фазе пролиферации при регенерации:
1) гематогенные;
2) клетки-предшественники;
3) клетки-посредники.
8. За счет чего осуществляется внутриклеточная форма регенерации:
1) митоз, амитоз;
2) разрастание и лизис ультраструктур;
3) дисплазия и метаплазия эпителия;
4) гипертрофия и гиперплазия ультраструктур.
9. Что характерно для патологической регенерации:
1) нарушение процессов метаболизма;
2) увеличение числа хромосом в клетках новообразованной ткани;
3) увеличение массы оставшейся специализированной ткани;
4) нарушение смены фаз пролиферации и дифференцировки.
10. Что такое гипертрофия:
1) увеличение кровенаполнения органа или ткани;
2) увеличение объема органа или ткани;
3) усиление функции органа или ткани.
11. Для каких органов и тканей характерна внутриклеточная форма регенерации:
1) мезотелий, почки;
2) миокард:
3) эндотелий, гладкие мышцы.
12. Что такое цирроз:
1) умеренно выраженный склероз без уплотнения ткани;
2) выраженный склероз с участками петрификации и гиалиноза;
3) выраженный склероз с деформацией и перестройкой органа;
4) облитерация полости.
13. Что образуется при неполной репаративной регенерации:
1) некроз и дистрофия;
2) экссудат и транссудат;
3) рубец на месте дефекта;
4) гиалиноз.
14. Что такое атрофия:
1) прижизненное омертвение органа или ткани;
2) прижизненное уменьшение объема органа или ткани;
3) неполное развитие органа в ходе онтогенеза;
4) разрастание железистой ткани на месте некроза.
15. Как рассматриваются изменения при тяжелой дисплазии:
1) истощение компенсации;
2) закрепление компенсации;
3) прозоплазия;
4) предрак.
16. Что такое грануляционная ткань:
1) ткань, содержащая большое число неспецифических гранулем;
2) ткань, состоящая из специфических гранулем;
3) молодая соединительная ткань, богатая клетками и сосудами.
17. Назовите степени дисплазии:
1) легкая, умеренная, тяжелая;
2) клеточная, внутриклеточная;
3) физиологическая, репаративная, патологическая.
18. Из каких фаз складывается процесс регенерации:
1) дистрофия, некроз;
2) организация, инкапсуляция;
3) экссудативная, пролиферация;
4) пролиферация, дифференцировка.
19. Назовите виды регенерации:
1) морфологическая, биохимическая, гистохимическая;
2) физиологическая, репаративная, патологическая;
3) дистрофическая, воспалительная.
20. Назовите вид атрофии:
1) анатомическая;
2) гистологическая;
3) биохимическая;
4) дисфункциональная.
21. Назовите вид компенсаторной гипертрофии:
1) рабочая;
2) нейрогуморальная;
3) нейротическая.
ОПУХОЛИ
1. Какой атипизм характерен для злокачественных опухолей:
1) клеточный;
2) тканевой;
3) клеточный и тканевой.
2. Как называется опухоль, в которой хорошо выражена строма и паренхима:
1) гистиоидная;
2) органоидная.
3. Выберите признаки тканевого атипизма:
1) неравномерное соотношение стромы и паренхимы;
2) полиморфизм ядер и клеток;
3) беспорядочное расположение сосудов;
4) гиперхромия ядер.
4. Назовите злокачественную опухоль из гладкой мускулатуры:
1) лейомиома;
2) рабдомиосаркома;
3) лейомиосаркома;
4) фибросаркома.
5. Укажите характер роста, присущий злокачественным опухолям:
1) экспансивный;
2) инфильтрирующий.
6. Какие опухоли дают метастазы:
1) злокачественные;
2) доброкачественные.
7. Укажите преимущественный путь метастазирования сарком:
1) лимфогенный;
2) гематогенный;
3) имплантационный.
8. Для каких опухолей характерен рецидив:
1) злокачественных;
2) доброкачественных.
9. Выберите признаки, характерные для злокачественных опухолей:
1) клеточный атипизм;
2) наличие капсулы;
3) инфильтрирующий рост;
4) экспансивный рост;
5) наличие патологических митозов.
10. Как называется рост опухоли в просвет органа:
1) экзофитный;
2) эндофитный;
3) инфильтрирующий;
4) аппозиционный.
11. Выберите признаки клеточного атипизма:
1) полиморфизм клеток и ядер;
2) неправильное соотношение стромы и паренхимы;
3) патологические митозы;
4) беспорядочное расположение сосудов в опухоли.
12. Какой атипизм характерен для доброкачественных опухолей:
1) тканевой и клеточный;
2) тканевой:
3) клеточный.
13. Может ли саркома развиваться из эпителия:
1) да;
2) нет.
14. Как называется злокачественная опухоль из волокнистой соединительной ткани:
1) фиброма;
2) фибросаркома;
3) фибромиома;
4) фиброаденома.
15. Перечислите доброкачественные опухоли мезенхимального происхождения:
1) остеосаркома;
2) липосаркома;
3) капиллярная гемангиома;
4) остеома.
16. Назовите доброкачественную опухоль из поперечно-полосатой мышечной ткани:
1) лейомиосаркома;
2) рабдомиосаркома;
3) лейомиома;
4) рабдомиома.
17. Как называется рост опухоли в толщину стенки органа:
1) экзофитный;
2) эндофитный.
18. Что лежит в основе метастазирования:
1) тромбоэмболия;
2) тканевая эмболия;
3) воздушная эмболия;
4) жировая эмболия.
19. Укажите вид роста, характерный для злокачественной опухоли:
1) экзофитный;
2) инфильтрирующий;
3) эндофитный;
4) экспансивный.
20. Перечислите опухоли из жировой ткани:
1) липома;
2) гибернома;
3) липосаркома;
4) фиброма.
21. Назовите доброкачественную опухоль из гладкой ткани:
1) лейомиома;
2) рабдомиосаркома;
3) лейомиосаркома;
4) фиброма.
22. Выберите доброкачественные опухоли из костной ткани:
1) фиброма;
2) остеома;
3) липома;
4) остеобластома;
5)хондрома;
6)остеосаркома.
23. Назовите злокачественную опухоль из хрящевой ткани:
1) остеома;
2) синовиома;
3) хондросаркома.
24. Выберите опухоли сосудистого происхождения:
1)фибромиома;
2)кавернозная гемангиома;
3)липосаркома;
4)капиллярная гемангиома.
25. Назовите опухолевидное образование из меланинобразующей ткани:
1)меланодермия;
2)невус;
3)меланома;
4) фибриноид.
26. Назовите виды опухолей ЦНС:
1) органоспецифические и мезенхимальные;
2) нейроэндокринные и нейротические;
3) нейроэктодермальные и менингососудистые.
27. Выберите виды невуса:
1)пограничный;
2)мезенхимальный;
3)внутриклеточный;
4)внутридермальный.
28. В каких органах из перечисленных может первично возникнуть рак:
1)кожа;
2)легкие;
3)мягкие ткани бедра;
4) скелет.
29. Что такое рак:
1)доброкачественная опухоль из эпителия;
2) злокачественная опухоль из эпителия;
3) злокачественная опухоль из тканей мезенхимального происхождения.
30. Назовите доброкачественную опухоль, которая развивается из плоского эпителия:
1) полип;
2) аденома;
3) папиллома;
4) скирр.
31. Выберите признаки, характерные для фиброзного рака:
1) наличие «раковых жемчужин»;
2) полиморфизм клеток;
3) преобладание паренхимы;
4) преобладание стромы.
32. Для какой из перечисленных опухолей характерно образование «раковых жемчужин»:
1) фиброзный рак;
2) медуллярный рак;
3) плоскоклеточный ороговевающий рак;
4) аденокарцинома.
33. Назовите разновидности астроцитом:
1) фибриллярная;
2) протоплазматическая;
3) недифференцированная;
4) фиброзная.
34. Укажите источники развития рака:
1) железистый эпителий органов ЖКТ;
2) железистый эпителий эндометрия;
3) плоский эпителий шейки матки;
4) трубчатые кости;
5) губчатые кости.
35. Укажите преимущественный путь метастазирования рака:
1) имплантационный;
2) гематогенный;
3) лимфогенный;
4) смешанный.
36. Выберите из перечисленных опухолей злокачественные эпителиальные:
1) папиллома;
2) скирр;
3) фиброаденома;
4) аденокарцинома.
37. Укажите источник развития аденокарциномы:
1) плоский и переходный эпителий;
2) призматический эпителий и эпителий желез;
3) мезотелий и эпендима желудочков.
38. Назовите истинную опухоль из меланинобразующей ткани:
1) невус;
2) меланома;
3) альбинизм;
4) лейкоплакия.
39. В каком возрасте встречается глиобластома:
1) до 15 лет;
2) 20-35 лет;
3) 40-60 лет.
40. Что характерно для острого лейкоза:
1) пролиферация недифференцированных клеток;
2) пролиферация малодифференцированных клеток;
3) пролиферация высокодифференцированных клеток.
41. Какие факторы способны вызвать мутацию клеток кроветворной системы:
1) ионизирующее излучение;
2) вирусы;
3) химические вещества;
4) ишемия.
42. Возможна ли трансформация лимфосаркомы в лейкоз:
1) да;
2) нет.
43. Какие 4 признака наблюдаются при недифференцированном лейкозе:
1) клетки костного мозга не поддаются идентификации;
2) некротический гингивит;
3) геморрагический диатез;
4) сепсис;
5) лейкемические инфильтраты состоят из клеток миелоидного ряда.
44. Выберите хронические лейкозы лимфоцитарного происхождения:
1) хронический лимфолейкоз;
2) лимфоматоз кожи;
3) хронический эритромиелоз.
45. Выберите 3 разновидности острых лейкозов:
1) миелобластный;
2) лимфобластный;
3) мегакариобластный;
4) парапротеинемические гемобластозы.
46. Какие из перечисленных признаков характерны для лейкоза:
1) анемия;
2) лейкемические инфильтраты;
3) неизмененная костно-мозговая ткань;
4) геморрагический синдром.
47. Какие клетки характерны для лимфогранулематоза:
1) Березовского—Штернберга;
2) клетки Вирхова;
3) Пирогова—Лангханса;
4) Русселя.
48. Какие патологические процессы развиваются в костях при разрастании миеломных клеток:
1) остеолизис;
2) остеопороз;
3) остеомиелит.
49. Назовите морфологические виды лимфогранулематоза:
1) изолированный;
2) дифференцированный;
3) плазмоклеточный;
4) генерализованный.
50. Что лежит в основе парапротеинемического нефроза:
1) инфильтрация гликогеном;
2) инфильтрация белком Бене—Джонса;
3) инфильтрация клетками Березовского—Штернберга.
51. Выберите 3 вида хронических лейкозов:
1) лимфобластный;
2) лимфоцитарный;
3) миелоцитарный;
4) моноцитарный;
5) мегакариобластный.
52. Какие из названных заболеваний относятся к злокачественным лимфомам:
1) лимфолейкоз;
2) ретикулосаркома;
3) лимфогранулематоз;
4) лимфангиосаркома.
БОЛЕЗНИ ОРГАНОВ ДЫХАНИЯ
1. Выберите термин, обозначающий воспаление всех слоев стенки бронха:
1) эндобронхит;
2) мезобронхит;
3) панбронхит;
4) перибронхит.
2. Выберите признаки, характерные для крупозной пневмонии:
1) поражается целая доля легкого;
2) воспаление начинается с бронхов;
3) пневмония протекает в 4стадии;
4) вызывается пневмококками.
3. Что является причиной уплотнения легкого в фазу опеченения:
1) карнификация;
2) накопление фибрина в альвеолах;
3) спадение легочной ткани.
4. Какие 2 признака характеризуют стадию прилива крупозной пневмонии:
1) гиперемия;
2) усиление диапедеза эритроцитов;
3) воспалительный отек;
4) образование гнойного экссудата.
5. Какие элементы экссудата преобладают в стадию серого опеченения крупозной пневмонии:
1) фибрин;
2) лейкоциты;
3) эритроциты.
6. Какие элементы экссудата преобладают в стадию красного опеченения крупозной пневмонии:
1) фибрин;
2) лейкоциты;
3) эритроциты.
7. Выберите признак, характерный для бронхопневмонии:
1) поражается сегмент легкого;
2) вызывается стафилококком;
3) протекает в 4 стадии;
4) воспаление начинается с бронхов.
8. Укажите 2 внелегочных осложнения крупозной пневмонии при лимфогенном распространении:
1) гнойный менингит;
2) перитонит;
3) медиастинит;
4) перикардит.
9. Назовите легочные осложнения при крупозной пневмонии:
1) карнификация;
2) абсцесс;
3) гангрена;
4) серое опеченение.
10. В какие сроки наступает стадия разрешения крупозной пневмонии:
1) на 4—6 день;
2) 7—8 день;
3) 9—11 день;
4) 14-18 день.
11. Какое из перечисленных заболеваний имеет существенное значение в развитии рака легкого:
1) крупозная пневмония;
2) бронхопневмония;
3) хронический бронхит;
4) интерстициальная пневмония.
12. Что такое коллапс легкого:
1) активное спадение респираторного отдела легких;
2) сдавление легких со стороны плевральной полости.
13. Какие процессы лежат в основе формирования легочного сердца при ХНЗЛ:
1) склероз сосудов малого круга;
2) гипоксия;
3) гнойное расплавление экссудата в альвеолах;
4) лейкоцитарная инфильтрация.
14. Что такое ателектаз легкого:
1) активное спадение респираторного отдела легких;
2) сдавление легких со стороны плевральной полости.
15. Какой процесс является причиной развития уремии при бронхоэктатической болезни:
1) некротический нефроз;
2) амилоидный нефроз;
3) гломерулонефрит.
16. Чем отличается хронический абсцесс от острого:
1) наличием пиогенной мембраны;
2) наличием фиброзной капсулы;
3) размерами.
17. Какой рак легкого чаще встречается:
1) бронхогенный;
2) пневмониогенный.
18. При какой эмфиземе расширяется весь ацинус:
1) старческой;
2) панацинарной;
3) викарной;
4) межуточной.
19. Назовите 5 сегментов легкого, в которых наиболее часто локализуются хронические абсцессы:
1) I; III; VII; IV; X;
2) II; VI; VIII; IX; X.
20. Какой процесс в легких сопровождается фиброзом, эмфиземой, деструкцией, репарацией, перестройкой и деформацией:
1) пневмофиброз;
2) пневмоцирроз;
3) карнификация.
21. В основе какого вида эмфиземы лежит вентильный механизм:
1) межуточная;
2) обструктивная;
3) старческая.
22. Какое изменение эпителия слизистой оболочки бронхов имеет существенное значение в развитии рака легкого:
1) атрофия;
2) десквамация;
3) метаплазия;
4) гиперплазия бокаловидных клеток.
23. Назовите абсцессы по происхождению:
1) пневмониогенные;
2) интерстициальные;
3) бронхогенные;
4) периферические.
БОЛЕЗНИ СЕРДЕЧНО-СОСУДИСТОЙ СИСТЕМЫ
1. Артерии каких органов наиболее часто поражаются при атеросклерозе:
1) печени, селезенки;
2) головного мозга, сердца;
3) почек, надпочечников;
4) легких, поджелудочной железы.
2. Выберите морфологический тип идиопатического миокардита:
1) сердечный;
2) сосудистый;
studfiles.net