Липиды и клеточная мембрана | Селекция привлекательных состояний

Есть такие модные для поедания омега-3 полиненасыщенные жирные кислоты, и теперь уже немного понятно, что означает это название. Давай разберемся с остальными его частями, ведь эти кислоты играют важную роль в работе твоего организма. Просто «ненасыщенной» называют жирную кислоту с одной двойной связью между атомами углерода в ее хвосте. А приставка «поли-» означает, что таких связей минимум две. Чем больше двойных связей, тем более причудливо изогнут хвост жирной кислоты, а значит тем сложнее такие хвосты плотно упаковывать вместе. Зато прямые хвосты насыщенных кислот вроде пальмитиновой отлично прижимаются друг к другу. Это приводит к тому, что ненасыщенные кислоты образуют жидкие масла, а твердые образованы в основном насыщенными. Ты сама можешь увидеть через прозрачную оболочку капсул с рыбьим жиром, что он остается жидким даже когда в комнате по-осеннему холодно. Сливочное масло при такой температуре совсем твердое, и чтобы оно приобрело консистенцию рыбьего жира его придется бросить на разогретую сковородку. При этом и масло, и рыбий жир состоят из жирных кислот, разница только в том, что в рыбьем жире они полиненасыщенные и прижимаются друг к другу с трудом, с большими промежутками. А в масле другие, насыщенные жирные кислоты, для которых не возникает проблем прижаться поближе.
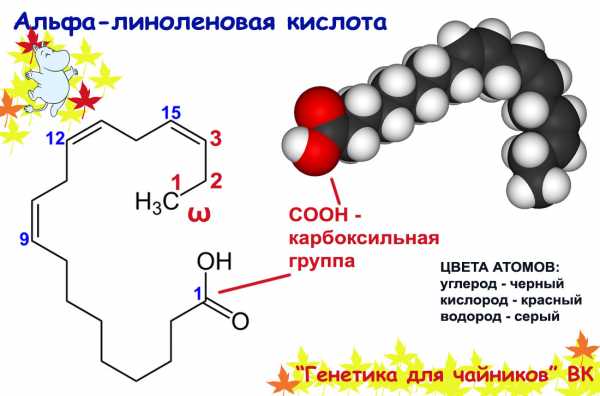
Вот альфа-линоленовая жирная кислота как раз полиненасыщенная. На ее схемах видно, как ее молекула изгибается в местах двойных связей.
Из всего названия «модных» жирных кислот осталось неразобранным самое начало: почему они именно «омега-3», а не «лямбда-5»? Оказывается, это просто следствие того, что для разных целей ученые присваивают атомам углерода в молекулах разные номера. И когда-то давно, когда жирные кислоты только начали изучать и еще не заморачивались всякой их насыщенностью, вполне логично решили считать атомы углерода от «головы», то есть карбоксильной группы.
На шариковой модели входящий в эту СООН-группу атом углерода номер один почти полностью скрыт под прилепленными красными кислородами. А на палочковой схеме возле него стоит синяя единица. Соответственно если считать от головы, то первая двойная связь у альфа-линоленовой кислоты будет между атомами углерода девять и десять. Тут ученые тоже договорились, что кто первый встал, того и тапк.. то есть номер этой двойной связи будет совпадать с номером меньшего по порядку углерода. Поэтому эту двойную связь обозначают Δ9. А потом решили, что удобнее считать углероды ненасыщенных жирных кислот, начиная от хвостов. А чтобы отличать хвосто-нумерацию от обычной, к номерам приписывают последнюю букву греческого алфавита: омега (ω). Так что омега-3 полиненасыщенная жирная кислота — эта такая, у которой первая из двойных связей между углеродами находится между третьим и четвертым атомами, если считать с конца. Первая, но не единственная, ведь кислота ПОЛИненасыщенная.
Теперь мы знаем, что из жирных кислот состоят жиры и масла. Но мы еще не знаем — как именно эти жирные кислоты при этом скомпонованы. Жирные кислоты запасаются в цитоплазме многих клеток не в виде отдельных молекул, а в виде более сложной конструкции — в виде молекул триглицеридов, собранных в мелкие капельки. Триглицерид ( triglyceride [trʌɪ’glɪsərʌɪd] ) — это молекула, состоящая из трех жирных кислот, присоединенных к одной молекуле глицерина, и именно из таких молекул и состоят животные жиры и растительные масла.
Я понимаю, что мы пока еще не знаем — что такое глицерин ( glycerin [‘glɪs(ə)rɪn] ) и каковы его свойства, но все в одну кучу валить невозможно, потому просто можно посмотреть на внешний вид глицерина — см. на рисунке — и представить себе, что на этой «вешалке» висит три жирных кислоты, что и является молекулой триглицерида. Не забываем про атомы водорода, присоединенные к атомам углерода, так что формула глицерина (следи по картинке слева направо по мере чтения химической формулы): HOCH 2-CH(OH)-CH2OH
Если клетке требуется энергия, то она берет молекулы триглицеридов из своего запаса и разрывает их, отрывая жирные кислоты и расщепляя их на мелкие кусочки, содержащие два атома углерода. Эти мелкие кусочки представляют собою такое же топливо, какое образуется из молекул глюкозы: они вступают в химические реакции, в результате которых клетка и получает энергию. Но триглицериды представляют собой более серьезный запас энергии: из них клетка получает в 6 раз больше энергии, чем она могла бы получить из глюкозы той же массы.
Жирные кислоты и разные жироподобные вещества, получаемые из них, имеют название «липиды» ( lipid [‘lipid] ). Также вместо термина «липиды» иногда говорят «жиры», но надо каждый раз понимать — что именно имеется в виду: та или иная жирная кислота или триглицерид или еще более сложные комплексы.
Липиды играют в клетках огромную роль — в частности, они являются основным строительным материалом мембран клеток. Если бы не было мембран, то клетки попросту не могли бы существовать: все их содержимое свободно уплывало бы в разные стороны. Мембрана образует прочную пленку, внутри которой и находится содержимое клетки.
Для построения мембраны используется довольно сложные липиды: фосфолипиды ( phospholipid [fɒsfə’lɪpɪd] ). Для того, чтобы построить молекулу фосфолипида, необходимо для начала взять молекулу триглецерида и оторвать от неё одну из жирных кислот. Затем к глицерину надо прицепить фосфатную группу — уже знакомое нам соединение фосфора и атомов кислорода — см. на картинке слева. И уже к фосфатной группе присоединяем еще одну группу молекул, азотсодержащую, называемую «холин» ( choline [‘kəʊliːn] ). Я не думаю, что стоит сейчас вдаваться в структуру и свойства холина, поскольку нашей задачей сейчас является лишь общее понимание того, как устроена молекула фосфолипида. Роль холина в работе нашего организма очень велика помимо его участия в структуре фосфолипидов. Надо только отдавать себе отчет в том, что и фосфат, и холин являются гидрофильными, и таким образом вместе они образуют «гидрофильную головку» фосфолипида, и в итоге молекула фосфолипида представляет собою объект, один конец которого гидрофобный, а другой — выраженно гидрофильный. Именно это качество фосфолипидов и делает их такими удобными для постройки мембран.
Я думаю, что если теперь посмотреть на изображения фосфолипидов, то можно уже без труда понять и запомнить то, как они устроены. Ниже размещены две картинки специально для этой цели.
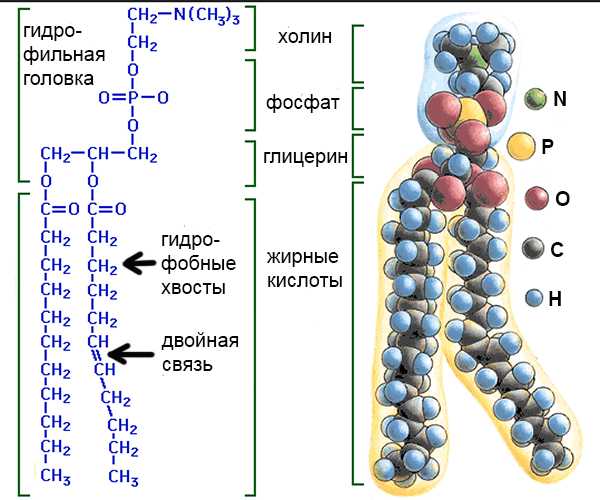
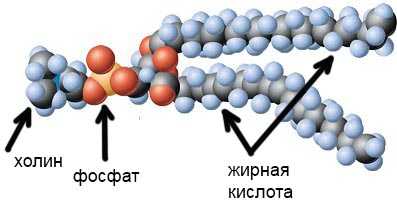
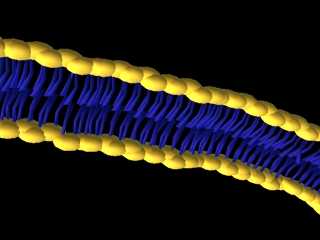
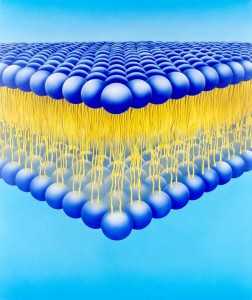
На следующих картинках видно — каким образом два слоя, состоящих из фосфолипидов, образуют мембрану клетки. Своими гидрофильными головками фосфолипиды направлены, разумеется, внутрь и вовне клетки, поскольку внутри клетки — цитоплазма, состоящая в основном из воды, а вовне — внеклеточная жидкость, тоже состоящая в основном из воды.
Своими гидрофобными хвостами фосфолипиды направлены внутрь мембраны.
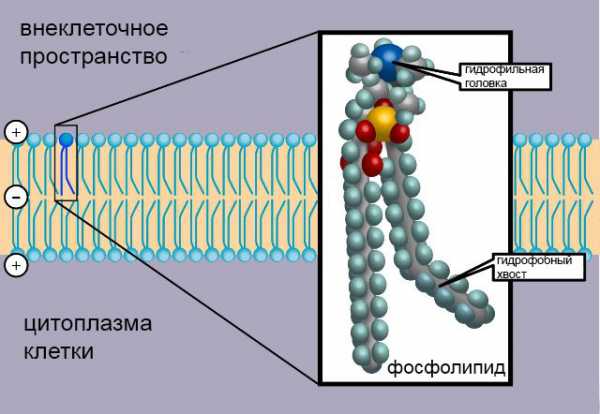
Молекулы, имеющие в своем составе как гидрофильные, так и гидрофобные области, называются амфифильными ( amphiphilic [amfə’filik] ). Таким образом, фосфолипиды являются амфифильными молекулами. Молекулы мыла — тоже. Фосфолипиды являются гораздо более выраженными амфифильными молекулами, чем триглицериды, поскольку комплекс «фосфат+холин» является намного более гидрофильным, чем глицерин. Когда фосфолипиды растекаются по поверхности воды, их гидрофильные концы сильно притягиваются к воде, так что они сразу же располагаются так, что их головки погружены в воду, а хвосты торчат наружу. Так образуется жирная пленка — нечто похожее на жир, плавающий на поверхности воды в процессе ее превращения во вкусный куриный бульон.
Гидрофобные хвосты хотя и не сильно, но все же притягиваются друг к другу, и кроме того молекулы воды оттесняют их, так что в результате группа фосфолипидов легко сворачивается в шарик с торчащими наружу головками — и такая жировая капля (отмечена цифрой 2 на рисунке) может спокойно плавать в толще воды, спрятав хвосты внутрь. В клетке возникает двойной липидный бислой (отмечен цифрой 1), который служит отличной преградой, мешающей бесконтрольно смешиваться жидкостям, находящимся внутри и снаружи клетки.
bodhi.name
Транспорт веществ через биологические мембраны.
Тема. Субклеточный и клеточный уровни организации живого.
Строение биологических мембран.
Основа биологической мембраны всех живых организмов- это двойная фосфолипидная структура. Фосфолипиды клеточных мембран представляют собой триглицериды, у которых одна из жирных кислот замещена на фосфорную кислоту. Гидрофильные «головки» и гидрофобные «хвостики» фосфолипидных молекул ориентированы так, что возникает два ряда молекул, головки которых прикрывают от воды «хвостики».
В такую фосфолипидную структуру интегрированы разные по величине и форме белки.
Индивидуальные свойства и особенности мембраны определяются преимущественно белками. Разный белковый состав определяет разницу строения и функций органоидов любых видов животных. Влияние состава липидов мембран на их свойства значительно ниже.
Транспорт веществ через мембрану делят на пассивный (без затрат энергии по градиенту концентрации) и активный (с затратами энергии).
Пассивный транспорт: диффузия, облегченная диффузия, осмос.
Диффузия — это движение растворенных в среде частиц из зоны с высокой концентрацией в зону с низкой концентрацией (растворение сахара в воде).
Облегченная диффузия — это диффузия с помощью белка-канала (поступление глюкозы в эритроциты).
Осмос — это движение частиц растворителя из зоны с меньшей концентрацией растворенного вещества в зону с высокой концентрацией (эритроцит в дистиллированной воде набухает и лопается).
Активный транспорт делят на транспорт, связанный с изменением формы мембраны и транспорт белками-ферментами-насосами.
В свою очередь, транспорт, связанный с изменением формы мембран, делят на три вида.
Фагоцитоз — это захват плотного субстрата (лейкоцит-макрофаг захватывает бактерию).
Пиноцитоз — это захват жидкостей (питание клеток зародыша на первых стадиях внутриутробного развития).
Транспорт белками-ферментами-насосами — это передвижение вещества через мембрану с помощью белков-переносчиков, интегрированных в мембрану (транспорт ионов натрия и калия «из» и «в» клетку, соответственно).
По направлению транспорт делят на экзоцитоз (из клетки) и эндоцитоз (в клетку).
Классификация составных частей клетки проводится по различным критериям.
По наличию биологических мембран органоиды делят на двумембранные, одномембранные и немембранные.
По функциям органоиды можно разделить на неспецифические (универсальные) и специфические (специализированные).
По значению при повреждении на жизненноважные и восстановимые.
По принадлежности к разным группам живых существ на растительные и животные.
Мембранные (одно- и двумембранные) органоиды имеют сходное с точки зрения химии строение.
Двумембранные органоиды.
Ядро. Если клетки организма имеют ядро, то их называют эукариотами. Ядерная оболочка имеет две близкорасположенные мембраны. Между ними находится перинуклеарное пространство. В ядерной оболочке есть отверстия — поры. Ядрышки — это части ядра ответственные за синтез РНК. В ядрах некоторых клеток женщин в норме выделяется 1 тельце Барра — неактивная Х-хромосома. При делении ядра становятся заметны все хромосомы. Вне деления хромосомы, как правило, не видны. Ядерный сок — кариоплазма. Ядро обеспечивает хранение и функционирование генетической информации.
Митохондрии. Внутренняя мембрана имеет кристы, которые увеличивают площадь внутренней поверхности для ферментов аэробного окисления. Митохондрии имеют свою ДНК, РНК, рибосомы. Главная функция — завершение окисления и фосфорилирование АДФ
АДФ+Ф=АТФ.
Пластиды (хлоропласты, хромопласты, лейкопласты). Пластиды имеют собственные нуклеиновые кислоты и рибосомы. В строме хлоропластов имеются дискообразные мембраны, собранные в стопки, где находится хлорофилл, ответственный за фотосинтез.
Хромопласты имеют пигменты, которые определяют желтую, красную, оранжевую окраску листьев, цветков и плодов.
Лейкопласты запасают питательные вещества.
studfiles.net
Введение в биологию (V) — caenogenesis — LiveJournal
Тема VЛИПИДЫ И МЕМБРАНЫ
В отличие от белков или углеводов, липиды не имеют никакой общей формулы. Это просто собирательное название всех гидрофобных биологически активных соединий. Вот, например, холестерин, спирт с огромной гидрофобной частью. Его производные — стероидные гормоны, которые вырабатываются у человека корой надпочечников и половыми железами. Все они относятся к липидам.
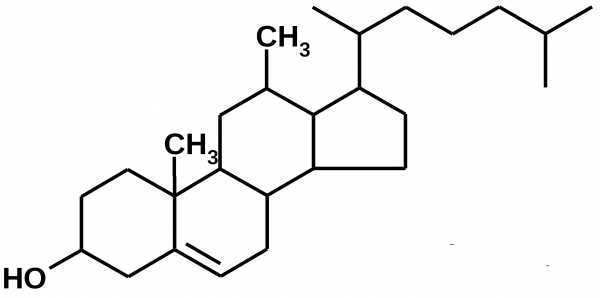
Заодно начнем привыкать к тому, что такие сложные формулы, как правило, не рисуют целиком, до каждого атома. На подобной формуле любой уголок обозначает атом углерода, у которого все свободные валентности по умолчанию заполнены атомами водорода. А если убрать единственную здесь двойную связь, то оставшееся ядро из четырех колец (трех шестиугольников и одного пятиугольника) будет называться замечательным словом “циклопентанпергидрофенантрен”. Это и есть основа для создания разнообразных стероидов, формулами которых загромождать изложение не будем.
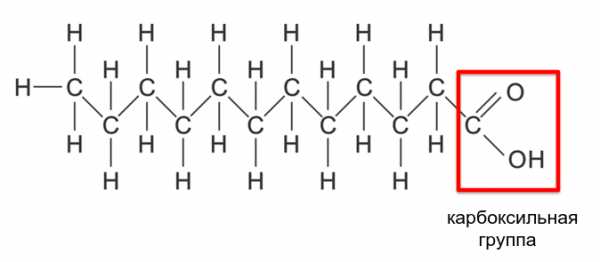
Другая важная группа липидов — жирные кислоты, то есть карбоновые кислоты с длинными (10-20 атомов углерода и больше) углеводородными “хвостами”. Чем длиннее “хвост”, тем хуже кислота растворяется в воде. Жирные кислоты, у которых в цепочке более 12 атомов углерода, называют высшими. 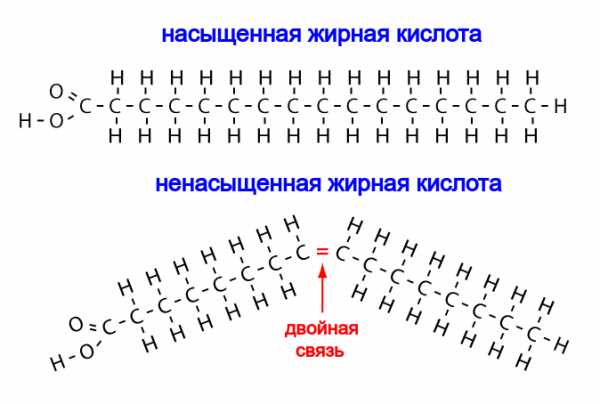
Жирные кислоты бывают насыщенные (без двойных связей в углеводородной цепочке) или ненасыщенные (с двойными связями). Насыщенные высшие жирные кислоты при комнатной температуре — твердые вещества, а ненасыщенные — жидкости. Связано это с более компактной упаковкой насыщенных «хвостов», в которых нет создаваемых двойными связями изломов и изгибов.
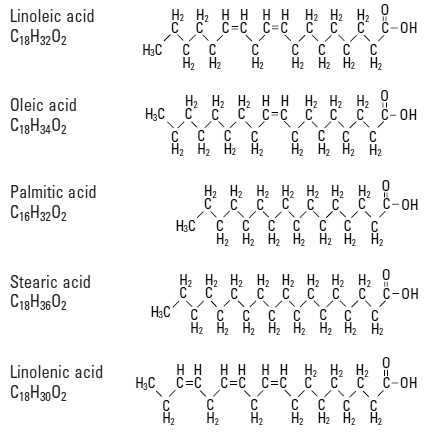
Несколько примеров жирных кислот: линолевая, олеиновая, пальмитиновая, стеариновая, линоленовая. Ненасыщенные жирные кислоты особенно распространены у растений (например, в растительных маслах).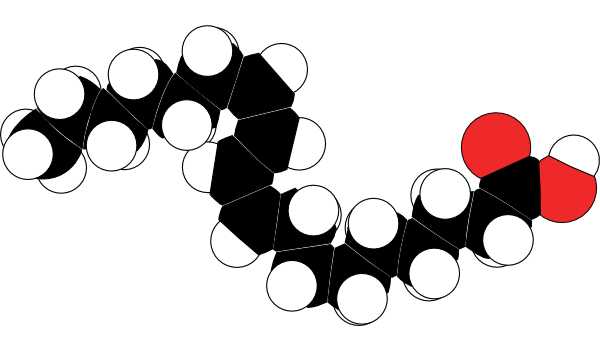
У насыщенных жирных кислот «хвосты» прямые, у ненасыщенных изогнутые в местах двойных связей. Из-за этого молекула может приобрести причудливую форму, особенно если двойных связей несколько. На картинке — модель молекулы линоленовой кислоты, у которой в «хвосте» три двойных связи.
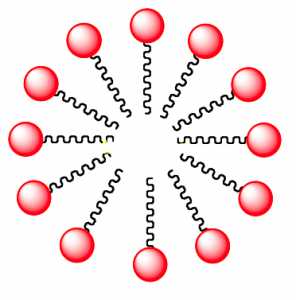
В водном растворе молекулы жирных кислот и их солей образуют мицеллы — шарообразные скопления, где гидрофобные “хвосты” обращены внутрь, минимизируя контакт с водой, а гидрофильные “головки” — наружу, поскольку они-то взаимодействуют с водой хорошо. Это довольно обычное поведение вещества, в молекуле которого есть одновременно гидрофобная и гидрофильная группы.
Жирные кислоты, а вернее их соли, постоянно используются человеком в качестве моющих средств. На картинке — один из самых распространенных компонентов мыла, стеарат натрия (соль стеариновой кислоты). Четко выделена гидрофильная головка, а остальная часть молекулы представляет собой гидрофобный хвост.
Механизм моющего действия мыла следующий. В сосуде слева молекулы мыла просто образуют мицеллу. В сосуде справа они растворяют свои углеводородные хвосты в капле “грязи” (которая, как правило, гидрофобна) и разбивают ее на мелкие капельки, которые легко смыть. Вещества с такой активностью называются детергентами.

Детергенты бывают очень разными по химической структуре; их гидрофильные части могут быть положительно заряженными, отрицательно заряженными или вовсе незаряженными, а просто полярными. Но молекула любого детергента обязательно включает гидрофобный «хвост» и гидрофильную «головку». Довольно много соединений такого типа входит в состав живых организмов.
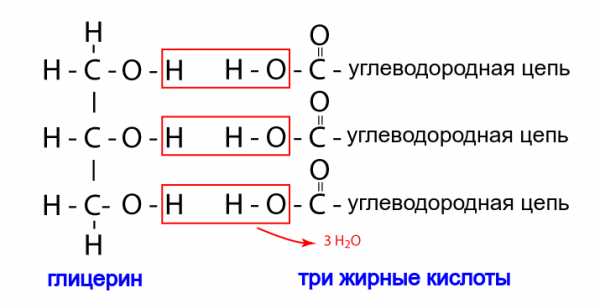
Вспомним, что любая карбоновая кислота может образовать с любым спиртом сложный эфир. При этом от кислоты отщепится -OH, от спирта -H, они образуют воду, а остатки кислоты и спирта замыкаются в единую молекулу со сложноэфирной группой -CO-O- посредине. Спиртом, участвующим в этой реакции, вполне может быть и глицерин, у которого гидроксильных групп три. Сложный эфир глицерина и трех жирных кислот называется жиром.
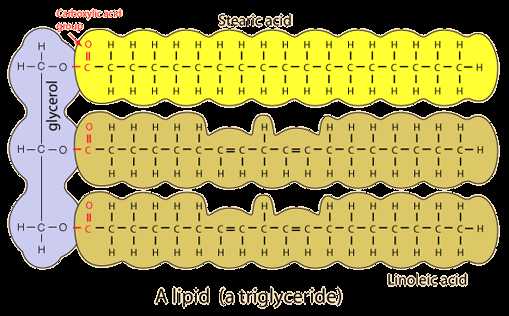
Типичный пример жира, в данном случае ненасыщенного (из трех остатков жирных кислот ненасыщенных тут два). Растительные масла — жидкие, потому что в них больше ненасыщенных жиров, чем у животных. Хотя в целом и насыщенные, и ненасыщенные жирные кислоты есть и у тех и у других, различается только их вклад.

Жиры — ценные источники энергии, именно поэтому они часто запасаются в клетках соединительной ткани у животных, как вот, например, у суслика.
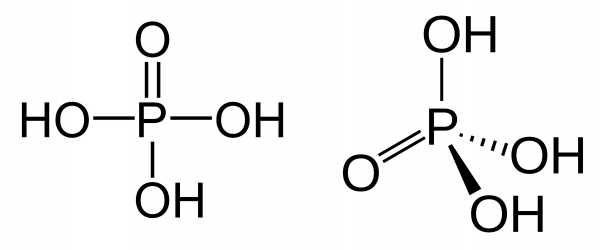
А теперь познакомимся с еще одним важным для нас соединением — фосфорной кислотой (H3PO4). Напомним, что валентность фосфора — 5. На картинке присутствуют два способа изображения молекулы: графическая формула, игнорирующая пространственное расположение связей, и структурная, показывающая его. Вновь будем иметь в виду, что “фосфорная кислота” и “фосфат” (то есть ее соль) в биохимии практически синонимы, в подавляющем большинстве случаев эти понятия свободно заменяются друг на друга.
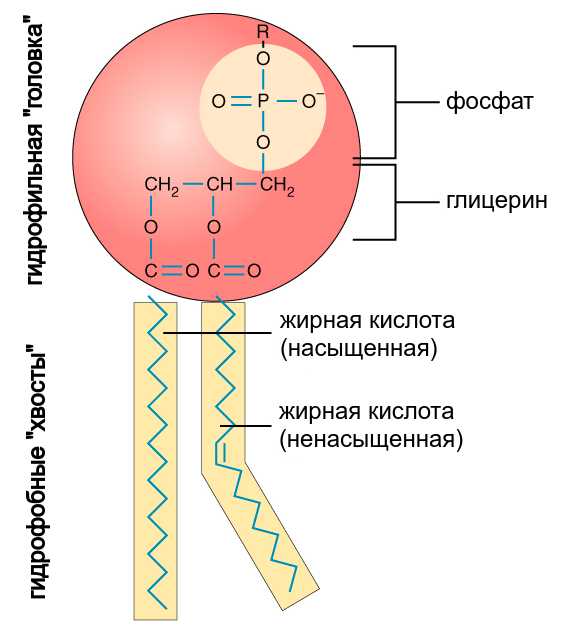
Сложный эфир глицерина, двух жирных кислот и фосфорной кислоты называется фосфолипидом. Можно сказать, что фосфолипид — это как бы жир, у которого вместо одного из остатков жирных кислот тем же способом присоединен фосфат. Такая молекула состоит из гидрофильной “головки” (включающей остатки глицерина и фосфата) и двух гидрофобных “хвостов” (жирных кислот). При фосфате бывают еще дополнительные боковые цепи, у разных фосфолипидов разные.
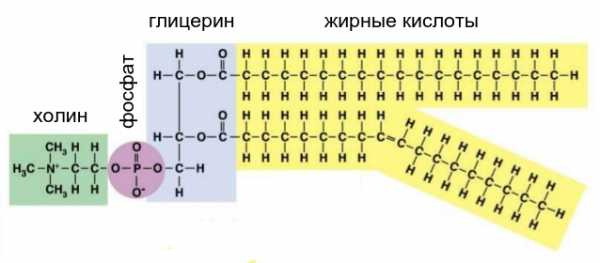
Один из самых распространенных фосфолипидов — фосфатидилхолин. Он приведен только в качестве примера. В других фосфолипидах на месте холина может быть аминокислота серин или что-нибудь еще.
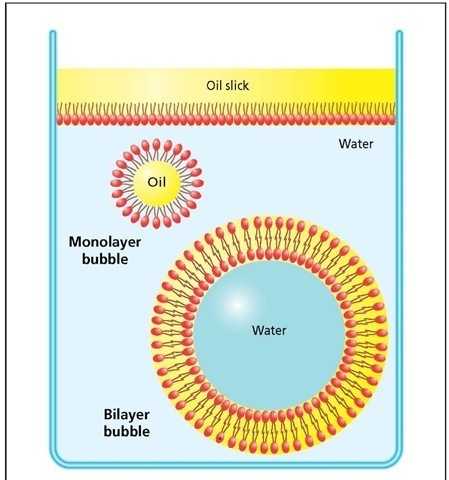
Именно из фосфолипидов в основном состоят клеточные мембраны. Тут используется их физическое свойство: собираться в воде в двойной слой гидрофобными “хвостами” внутрь и гидрофильными “головками” наружу. Замкнутый пузырек, образованный таким двойным слоем молекул, называется везикулой. Вся клеточная мембрана — это в некотором смысле сильно разросшаяся везикула.
На картинке показано, как на границе гидрофильного раствора (вода) и гидрофобного (масло) молекулы фосфолипидов ориентируются хвостами в сторону масла, а головками в сторону воды. Если же никакого масла поблизости нет, то молекулы фосфолипидов располагаются головками в сторону воды, а хвостами друг к другу, и получается двойной слой, который сразу замыкается в везикулу, чтобы не было неустойчивых свободных краев. Это чисто физическое явление, которое запросто может иметь место и вне живых клеток.
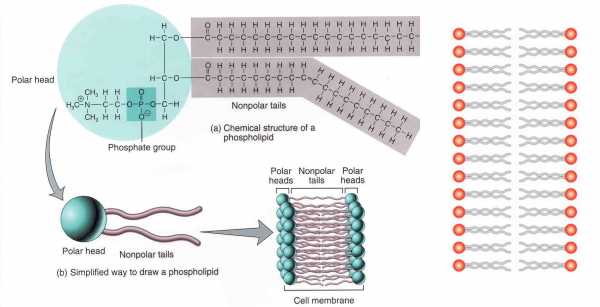
Вот схема того, как фосфолипиды «собираются» в клеточную мембрану. Молекула фосфолипида нарисована двумя способами — во всех деталях (в качестве примера тут взят уже знакомый нам фосфатидилхолин) и в виде головки с двумя хвостиками. Таким молекулы собираются в двойной слой хвостиками друг к другу, головками к воде. Справа — простейшая схема участка типичной мембраны.
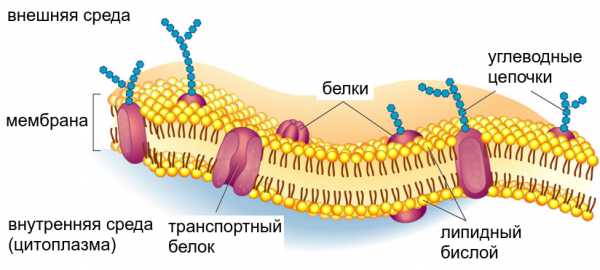
На самом деле биологические мембраны никогда не состоят только из одних фосфолипидов. Типичная клеточная мембрана — фосфолипидный бислой во встроенными в него интегральными белками, которые обычно являются или рецепторными (принимают сигналы из внешней среды и передают их внутрь клетки), или транспортными (переносят те или иные молекулы с одной стороны мембраны на другую). Часть белка, проходящая сквозь образованный «хвостами» внутренний слой мембраны, как правило, представляет собой альфа-спираль, целиком состоящую из гидрофобных аминокислот, боковые цепи которых торчат наружу. Если белок достаточно сложный, таких альфа-спиралей вполне может быть несколько. Кроме того, к мембранным белкам снаружи часто прикреплены ковалентными связями дополнительные цепочки, состоящие не из аминокислот, а из углеводов. Они бывают нужны в первую очередь для взаимодействия между клетками.
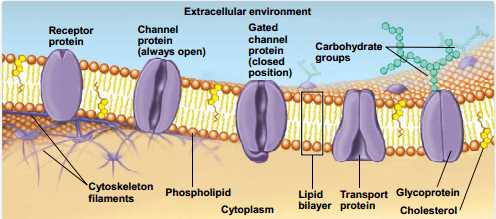
Тут мы видим кое-какие дополнительные детали. Во-первых, кроме фосфолипидов в мембране есть холестерин — его молекулы раскрашены желтым (если сравнить с уже знакомой нам формулой холестерина, видно, что каждая молекула своей гидроксильной группой обращена к воде, а массивной гидрофобной частью внутрь мембраны). Во-вторых, изнутри ко многим интегральным белкам прикреплены элементы цитоскелета — внутриклеточной системы опорных структур, тоже состоящей из белков. Но обе эти особенности есть далеко не у всех клеток.
В целом можно назвать как минимум три основные функции липидов: энергетическая (жиры), структурная (фосфолипиды, холестерин) и сигнальная (стероиды). Но надо иметь в виду, что липиды в силу самой природы этого сборного понятия крайне разнообразны, даже при том, что они (в отличие от белков) не являются полимерами. Мы обсудили далеко не все их группы.
caenogenesis.livejournal.com
Полярные головки — Большая Энциклопедия Нефти и Газа, статья, страница 1
Полярные головки
Cтраница 1
Полярные головки, в которых положительно заряженные аммонийподобные группы связаны с отрицательно заряженными ортофосфатными группами, представляют собой цвиттер-ионы, имеют большие электрические дипольные моменты и поэтому хорошо смачиваются водой. В клеточной мембране они обращены в сторону внешней или внутриклеточной водной среды. Такая двухслойная конструкция мембран образуется самопроизвольно. Значительная толщина углеводородного среднего слоя создает необходимую клеткам непроницаемость мембран по отношению к случайным молекулам, способным нарушить работу механизмов клетки. [2]
Полярные головки молекул окружены двойными слоями и находятся в воде, в то время как углеводородные хвосты собраны вместе в области, в которой отсутствует вода. [3]
В обычных мнцеллвх гидрофильные полярные головки лнпндных молекул обращены в сторону водной фазы, тогда как неполярные углеводородные цепи образуют гидрофобное ядро, изолированное от водного окружения. В обращенных мицеллах, существующих а таких растворителях, как бензол, гексан н др., молекулы лнпндов имеют иную ориентацию: их гидрофобные цепн направлены в растворитель, а полярные головки формируют центральную гидрофильную область мицеллы. Образование обращенных мнцелл значительно облегчается при добавлении следовых количеств воды в неполярный растворитель. [4]
В этой модели также предполагается, что молекулы липидов расположены в виде двойного слоя и их полярные головки направлены к поверхности мембраны, как показано на схеме, приведенной на рис. 3.4. Однако при этом молекулы белка не образуют непрерывного слоя на поверхности мембраны, а располагаются через неровные интервалы. В некоторых случаях они частично экспонированы на поверхности мембраны, а частично спрятаны в ней, а в других они полностью погружены в мембрану таким образом, что одна часть молекулы белка может высовываться с одной стороны мембраны, а другая — с другой. Следовательно поверхность мембраны состоит из полярных липидных головок, между которыми в разных местах выступают участки молекул глобулярных белков. [5]
В растворах амфифила в органическом растворителе возможно образование и инвертированных ламеллярных фаз, в которых двойные слои амфифила имеют инвертированную структуру, т.е. полярные головки в этом двойном слое обращены друг к другу, а гидрофобные хвосты погружены в соседние слои растворителя. [6]
Если в водном растворе липидных молекул становится больше, то эти молекулы собираются вместе так, что гидрофобные углеводородные цепи закрыты от воды, а полярные головки, наоборот, выставлены в воду, рис. 16.26. Такая модель позволяет изучать ионную проницаемость, генерацию электрического потенциала на мембране. [8]
Мицелла представляет собой компактное, примерно сферическое образование с упорядоченной центральной областью ( ядром), состоящим из углеводородных цепей молекул ПАВ. Полярные головки образуют шероховатую поверхность мицеллы. Значительное число противоионов связано с поверхностью и составляет как бы часть мицеллы. Остальные противоионы образуют диффузный электрический слой. [9]
Липиды ( вещества на основе жирных кислот) построены из полярной головки ( содержащей атомы водорода, углерода, азота, фосфора) и двух длинных неполярных углеводородных хвостов. Полярные головки гидрофильны, то есть могут притягивать к себе дипольные молекулы воды. Хвосты обладают гидрофобными свойствами, то есть не любят взаимодействовать с водой. [10]
Так, Ф. С. Шестранд в 1963 г. предположил, что глобулярные частицы в мембране представляют собой липнды в форме мицелл. Полярные головки лнпндных молекул находятся на поверхности мицелл, покрытых слоем белка. Люси ( 1464), мицеллярная форма приписывалась не только липидам, но и белкам, а вся мембрана рассматривалась как структура, построенная из чередующихся липидных мицелл и белковых глобул. Пердью ( 1966), предложенной прежде всего применительно к митохондриям, основой мембраны является регулярно построенный ассоциат липопротеиновых субъеднниц довольно сложной конфигурации. [11]
Сердцевину мембраны составляет бимолекулярный ли-пидный слой, в котором молекулы липидов ориентированы перпендикулярно поверхности мембраны. Полярные головки липидных молекул направлены наружу, в сторону водной фазы, а гидрофобные остатки жирных кислот, спиртов, альдегидов обращены внутрь бимолекулярного слоя. Белки, входящие в состав мембраны, находятся в растянутой по поверхности липида форме и имеют р-конформацию. Белок по обеим сторонам мембраны может быть не одинаков, что определяет ее асимметричность. Мембрана стабилизирована за счет взаимодействия ионных групп липидов и белка. [12]
Не только цепи жирных кислот, но и полярные группы липи-дов характеризуют мембрану. При этом именно полярные головки могут резче различаться в индивидуальных биологических мембранах. Они могут быть более существенными для липид-белковых, чем для липид-липидных взаимодействий, и для нормального функционирования отдельные белки могут нуждаться в специфических липидных полярных группах. [13]
Поверхность реального фосфолипидного бислоя представляет собой довольно сложное образование. Граничащие с электролитом полярные головки фосфолипидных молекул образуют поверхностный слой ( толщиной 0 6 — 1 нм), заполненный электрическими зарядами и диполями. Часть — этих зарядов и диполей принадлежит самим головкам, другую часть составляют молекулы воды и ионы электролита. Поэтому термины поверхностные заряды, поверхностные диполи в значительной степени условны. Заряды и диполи реальных фосфолипидных поверхностей распределены в приповерхностном слое. Происхождение такого распределения является результатом рыхлости поверхности, позволяющей молекулам воды и ионам электролита проникать в глубь поверхности. [14]
Поверхность реального фосфолипидного бислоя представляет собой довольно сложное образование. Граничащие с электролитом полярные головки фосфолипидных молекул образуют поверхностный слой ( толщиной 0 6 — 1 нм), заполненный электрическими зарядами и диполями. Часть этих зарядов и диполей принадлежит самим головкам, другую часть составляют молекулы воды и ионы электролита. Поэтому термины поверхностные заряды, поверхностные диполи в значительной степени условны. Заряды и диполи реальных фосфолипидных поверхностей распределены в приповерхностном слое. Происхождение такого распределения является результатом рыхлости поверхности, позволяющей молекулам воды и ионам электролита проникать в глубь поверхности. [15]
Страницы: 1 2 3
www.ngpedia.ru
Глава 12. Общие свойства биологических мембран
Все без исключения клеточные мембраны построены по общему принципу: это тонкие липопротеидные пленки, состоящие из двойного слоя липидных молекул, в который включены молекулы белка. В весовом отношении в зависимости от типа мембран на долю липидов приходится 25-60%, на долю белков 40-75%. В состав многих мембран входят углеводы, количество которых может достигать 2-10%.
Структурной основой мембран является двойной слой липидов
К липидам относится большая группа органических веществ, обладающих плохой растворимостью в воде (гидрофобность) и хорошей растворимостью в органических растворителях (липофильность). Состав липидов, входящих в мембраны клетки, очень разнообразен (рис. 116). Характерными представителями липидов, встречающихся в клеточных мембранах, являются фосфолипиды (глицерофосфатиды), сфингомиелины и из стероидных липидов — холестерин.
Глицерофосфатиды, или глицеролипиды, представляют собой сложные эфиры трехатомного спирта глицерина с двумя жирными кислотами и с фосфорной кислотой, которая в свою очередь может быть связана с различными химическими группами (холин, серин, инозит, этаноламин и др.). Так, например, в структуру наиболее часто встречающегося в мембранах глицеролипида лецитина входят участки двух жирных кислот, глицерина, фосфорной кислоты и холина.
Другая группа мембранных липидов называется сфингомнелиновой, в ней глицерин замещен аминоспиртом сфингозином.
Из липидов, относящихся к стероидам, больше всего в мембранах холестерина. В растительных клетках холестерин не обнаружен, его там заменяют фитостерины. У бактерий стерины отсутствуют.
Характерной особенностью липидов мембран является разделение их молекулы на две функционально различные части: неполярные (не несущие зарядов) хвосты, состоящие из жирных кислот, и заряженные полярные головки (рис. 117). Полярные головки несут на себе отрицательные заряды или могут быть нейтральными (в случае, если они имеют одновременно положительные и отрицательные заряды). Наличие неполярных хвостов липидов объясняет их хорошую растворимость в жирах и органических растворителях.
Если полярные липиды смешать с водой, то образуется эмульсия, состоящая из мицелл. При этом незаряженные (гидрофобные) хвосты будут стремиться образовывать однородную фазу в центре мицеллы, и заряженные, гидрофильные, головки будут торчать в водную фазу. Холестерин сам по себе мицелл не образует, но легко включается в мицеллы полярных липидов, в результате чего образуются мицеллы смешанного типа. Если, наоборот, к липидам добавить немного воды, то образуются мицеллы, как бы вывернутые наизнанку: их гидрофобные хвосты будут торчать в масляную фазу, а заряженные (гидрофильные) головки будут располагаться внутри мицеллы (рис. 118).
На поверхности воды растворы полярных липидов, растекаясь, образуют мономолекулярную пленку, в которой в водную фазу будут направлены заряженные (гидрофильные) головки, а неполярные хвосты будут обращены в сравнительно гидрофобную воздушную фазу. Смешивая с водой экстрагированные из мембран липиды или беря смеси разных липидов, можно получить бимолекулярные слои или мембраны толщиной около 3,5 нм, где периферические зоны слоя, смотрящие в водную фазу, будут содержать исключительно полярные головки, а незаряженные хвосты будут образовывать общую гидрофобную центральную зону такой образовавшейся мембраны (рис. 119).
Эта способность липидов самопроизвольно образовывать мембранные структуры определяется свойствами самих липидов, а именно наличием в их структуре полярных головок и неполярных хвостов.
В таких искусственные системах липидные мицеллы и мембраны могут взаимодействовать с белками своими полярными зонами или гидрофобными хвостами, при этом образуются искусственные липопротеидные мембраны, сходные с теми мембранами, которые можно выделить из клеток. Они имеют толщину около 7,5 нм. При окраске четырехокисью осмия искусственные мембраны обнаруживают в электронном микроскопе трехслойную структуру: два темных периферических слоя по 2,5 нм и светлый, центральный, примерно такой же толщины. Естественные клеточные мембраны имеют такое же строение.
Необходимо подчеркнуть, что как искусственные, так и естественные мембраны не представляют собой плоские слои, они всегда замкнуты сами на себя, образуя полые вакуоли, пузырьки, везикулы, плоские замкнутые мешки или трубчатые образования.
Представление о том, что в основе клеточных мембран лежит двойной липидный слой, было получено еще в 20-х гг. Было найдено, что если экстрагировать липиды из оболочки эритроцитов, а затем поместить липиды на поверхность водного мениска, то можно рассчитать площадь, занимаемую образовавшимся монослоем липидов. Оказалось, что эта площадь вдвое больше площади, занимаемой поверхностью эритроцитов, из которых были экстрагированы липиды. Было сделано предположение, что в мембранах эритроцитов липиды располагаются в два слоя. К тому же оказалось, что поверхностное натяжение мембраны клетки (1-2 дин/см2) гораздо ниже, чем поверхностное натяжение искусственного липидного слоя (7-15 дин/см2). Было обнаружено, что при добавлении белка к липидам поверхностное натяжение снижается до величины, характерной для поверхностного натяжения клеток.
Образовавшиеся искусственные липидные мембраны служат непроницаемым барьером для любых заряженных молекул, даже для ионов солей. Это определяет основное функциональное свойство мембран — служить преградой для свободной диффузии через слой липидов. Это свойство может быть использовано для практических целей. Так при смешивании липидов в водной среде образуется масса полых мембранных пузырьков, липосом (рис. 120). Жидкость, попавшая внутрь этих пузырьков, уже не может свободно обмениваться с жидкостью, находящейся снаружи. Таким образом искусственные мембраны липосом можно “загрузить” лекарственными веществами, которые могут в нужных концентрациях поступать к клеткам.
Мембранные белки встроены в билипидный слой
В среднем в липопротеидных мембранах белки по весу составляют 50%. Но количество белков в разных мембранах может быть различным. Так в мембранах митохондрий на долю белков приходится около 75%, а в плазматической мембране клеток миелиновой оболочки — около 25%. Но так как липидные молекулы имеют небольшой размер (около 0,5 нм) и молекулярный вес, их число по отношению к числу белковых молекул выше в 50 раз. Поэтому белковые молекулы как бы вкраплены в билипидный слой мембраны. Часть из них связана с липидными головками с помощью ионных (солевых) связей и поэтому легко экстрагируется из мембран растворами солей. Другие образуют солевые связи с полярными участками липидов через взаимодействие с ионами Mg++ или Ca++, такие белки экстрагируются с помощью хелатных соединений, таких, как версен (ЭДТА). Такие легко экстрагируемые белки большей частью расположены на мембранах со стороны цитоплазмы. В цитоплазматической мембране эти белки тесно связаны с белковыми структурами цитоскелета.
Большая часть белков взаимодействует с липидами в составе мембран на основе гидрофобных связей. Оказалось, что многие мембранные белки состоят как бы из двух частей: из участков, богатых полярными (несущими заряд) аминокислотами, и участков, обогащенных неполярными аминокислотами (глицином, аланином, валином, лейцином). Такие белки в липидных слоях мембран располагаются так, что их неполярные участки как бы погружены в “жирную” часть мембраны, где находятся гидрофобные участки липидов (рис. 121). Полярная (гидрофильная) же часть таких белков взаимодействует с головками липидов и обращена в сторону водной фазы (рис. 122), поэтому такие белки, связанные с липидами путем гидрофобных взаимодействий, практически не экстрагируются в водных фазах. Их можно выделить, лишь разрушая мембрану, экстрагируя из нее липиды или органическими растворителями, или детергентами. Поэтому эти белки мембран и называют интегральными.
Размер интегральных мембранных белков в среднем равен 8 нм, но встречаются крупные белки — до 35 нм величиной (белок тилакоидов хлоропластов). Обычно это очень асимметричные по своей природе белки и соответственно асимметрично локализованы в мембране (рис. 123): их разные функциональные части локализованы по обе стороны мембраны, и все белки данного типа расположены одинаково. С цитоплазматической стороны мембраны интегральные белки связаны с периферическими белками.
Эти представления, полученные при изучении химии клеточных мембран, были блестяще подтверждены морфологическими исследованиями. При использовании метода замораживания-скалывания, скол через мембраны может идти через центральную, липидную, зону. В этом случае обнажается масса глобул, белковой природы, находящихся в составе липидного слоя. Размер таких глобул около 4-8 нм. Эти и другие биохимические данные послужили основой для создания модели мембраны с мозаичной укладкой: мембрана состоит из неплотно упакованных белковых глобулярных белков, свободное пространство между которыми заполнено липидными молекулами (рис. 121). При этом часть белков может быть связана только с полярными группами липидов и может находиться на поверхности билипидного слоя; другие белки могут частично или даже полностью погружены из-за гидрофобных свойств своих участков в липидный слой; третьи — могут пронизывать мембрану насквозь. Интересно, что большая часть липидных молекул (70%) не связана с белками, так что белковые молекулы как бы плавают в “липидном озере”.
Липиды и белки мембран обладают латеральной подвижностью
Исследование искусственных липидных бислоев показало, что эти мембраны представляют собой двумерную жидкость, обладающую вязкостью, сравнимую с вязкостью оливкового масла. В составе таких и естественных мембран молекулы липидов постоянно движутся с огромной скоростью (коэффициент диффузии для них равен 10-8 см2 х с-1),достигающей 2 мкм за 1 с.
Липидные молекулы двигаются вдоль липидного слоя, могут вращаться вокруг своей оси, а также переходить из слоя в слой, что происходит редко и с помощью специальных переносчиков. Белки плавающие в “липидном озере” также обладают латеральной, продольной подвижностью, но скорость их перемещения в десятки и сотни раз ниже. Изучать перемещение белковых молекул в составе мембран на живых клетках проще на примере плазматической мембраны. Белки плазматической мембраны, гликопротеины, часто имеют олигосахаридные цепочки, смотрящие на внеклеточную среду.
Для исследования свойств плазматической мембраны широко используются лектины, белки растительного происхождения, которые специфически связываются с олигосахаридами мембранных белков. Так, лектин конканавалин А (КонА), выделенный из растения канавалии мечевидной, связывается с олигосахаридами, имеющими на концах глюкозу или маннозу. Лектин из бобов сои связывается с N-ацетилглюкозамином, а лектин из проростков пшеницы, кроме того, и с галактозой. На поверхности белков-лектинов имеются два или более района специфического связывания с углеводами. Если лектины добавлять к взвеси эритроцитов, то это вызывает их осаждение, сопровождающееся слипанием — агглютинация. Поэтому лектины еще называют агглютининами.
Такая реакция агглютинации эритроцитов вызвана тем, что лектин, например КонА, взаимодействуя с концевыми сахарами углеводов гликопротеидов, как бы сшивает эритроциты друг с другом, чем и вызывает их осаждение. Так как полисахариды есть на поверхности плазматической мембраны любых клеток, то лектины могут связываться с ними. Места посадки лектинов можно увидеть в электронном микроскопе, если связать лектины с электронноплотным белком ферритином. Более удобно регистрировать лектины на поверхности клеток с помощью иммунофлуоресцентного метода (см. выше). Использование этого метода позволило проследить за поверхностью белков в плоскости мембран. Так, оказалось, что при добавлении к клеткам, поверхность которых связана с КонА, антител против КонА, меченных флуорохромом, обнаруживается свечение по всей поверхности клетки. Это значит, что белки-гликопротеиды, полисахаридные цепи которых образуют слой, равномерно разбросаны по поверхности клеток. Однако через некоторое время на поверхности клетки видно не сплошное свечение, а отдельные множественные пятна или точки (их назвали “заплатками”, по-английски patch). Затем эти пятна собираются в одну зону — “колпачок”. Следовательно, белки, связанные с лектинами, могут быстро перемещаться в плоскости плазматической мембраны. Интересно, что “колпачок” всегда формируется над тем местом клетки, где находятся центриоли и аппарат Гольджи. Дальнейшая судьба этого колпачка может быть у разных клеток различной: у фибробластов колпачки могут отделяться и отрываться от тела при движении клетки, у других (лимфоциты) происходит поглощение этих участков внутрь клетки (эндоцитоз) и переваривание их там (рис. 124).
Латеральную подвижность белковых (гликопротеидных) молекул плазматической мембраны можно наблюдать при изучении клеточных гибридов, имеющих разные поверхностные антигены, которые можно пометить. В этом случае сначала в гибридной клетке антигены поверхностей были разобщены, а через некоторое время они равномерно распределились по всей поверхности гетерокариона .
Клеточные мембраны асимметричны
Состав липидов по обе стороны мембраны различен, что определяет асимметричность в строении билипидного слоя. Так, с помощью химического маркирования было найдено, что 80% сфингомиелина и 75% фосфатидилхолина, и 20% фосфатидилэтаноламина локализованы на наружной поверхности плазматической мембраны, на внутренней же — располагается весь фосфатидилсерин и 80% фосфатидилэтаноламина. Примерно такую же композицию имеют мембраны эндоплазматического ретикулума (для них наружной надо считать ту поверхность, которая обращена внутрь полости).
Особенно выражена асимметрия мембран в отношении интегральных белков. В составе естественных мембран белки строго ориентированы. Большей частью их N-концы смотрят в полость вакуолей или в случае плазматической мембраны, во внешнюю для клетки среду. Такое полярное расположение цепи белковой молекулы в липидном бислое создается в процессе синтеза мембранного белка на рибосоме (см. ниже). Полуинтегральные и примембранные белки также асимметрично расположены в мембранах. Так в эндоплазматическом ретикулуме белки-ферменты, синтезирующие липиды, расположены на цитозольной стороне мембран, а ферменты, пришивающие сахара к белковым цепочкам, гликозидазы, локализованы на внешней стороне мембраны.
Наличие углеводного компонента характерно практически для всех мембран клетки, но особенно для мембран вакуолярной системы и плазматической мембраны. Углеводный компонент мембран представлен главным образом гликопротеинами — молекулами белков, ковалентно (в отличие от нуклеопротеидов) связанных с цепочками углеводов. Как правило, цепочки углеводов расположены в наружных слоях мембран (для цитоплазматических вакуолей наружными считают слои, обращенные не к матриксу цитоплазмы, а в полость везикул или вакуолей). Они имеют ковалентные связи с интегральными белками, образуя гликопротеиды, или с липидами (гликолипиды). Углеводы мембран представляют собой короткие линейные или разветвленные цепочки, в состав которых входят галактоза, манноза, фруктоза, сахароза, N-ацетилглюкозамин, N-ацетилгалактозамин, пентозы — арабиноза и ксилоза, а также нейраминовая (сиаловая) кислота. Значение этого компонента очень велико для функционирования плазматической мембраны.
Разные мембраны имеют различные свойства
Несмотря на поразительную схожесть строения различных мембран, построенных по принципу липидного бислоя с вмонтированными в него белками, физические и химические свойства разных мембран различны. Это связано с тем, что в разных мембранах общий состав липидов значительно различается, что определяет особые свойства мембран.
Разные мембраны клетки могут отличаться друг от друга по количеству липидов. Так, плазматическая мембрана содержит 35-40% липидов, а мембраны митохондрий — 27-29%. Самое высокое содержание липидов в плазматической мембране шванновских клеток, образующих миелиновую оболочку нервов, — дл 80%.
Было обнаружено, что клеточные мембраны сильно отличаются друг от друга по составу липидов. Так, плазматические мембраны клеток животных богаты холестерином (до 30%) и в них мало лецитина, в то время как мембраны митохондрий, наоборот, богаты фосфолипидами и бедны холестерином. Из общего количества липидов содержание фосфатидилхолина (лецитина) во фракциях эндоплазматической сети составляет 60-70% от всех фосфолипидов, в то время как в плазматической мембране его может быть 25-35%.
В целом для плазматической мембраны характерно высокое содержание холестерина и сфинголипидов, а также преобладание насыщенных и мононенасыщенных жирных кислот в составе фосфолипидов, тогда как в митохондриях, эндоплазматической сети и во многих других цитоплаззматических мембранах содержится мало холестерина и сфинголипидов и сравнительно много полиненасыщенных жирных кислот. Видимо, в связи с этим мембраны цитоплазмы менее жесткие, чем плазматическая мембрана, они более “легкоплавки”.
Особенно отличаются мембраны по составу белков, которые, главным образом, определяют функциональные свойства мембран.
По биологической роли мембранные белки можно разделить на три группы: ферменты, рецепторные белки и структурные белки.
Набор ферментов в составе мембран может быть очень велик и разнообразен (например, в плазматической мембране клеток печени обнаружено не менее 24 различных ферментов). В разных мембранах существует характерный набор ферментов. Например, в плазматической мембране, как и во многих других, локализуется K+-Na+-зависимая АТФаза, участвующая в транспорте ионов. В митохондриях специфическим является набор белков — переносчиков электронов и феремент АТФ-синтетаза, обеспечивающие окислительное фосфорилирование и синтез АТФ.
Рецепторные белки специфически связываются с теми или иными веществами и как бы их узнают. Это белки-рецепторы для гормонов, для узнавания поверхности соседних клеток, вирусов, фагов у бактерий и т.д. К этой группе относятся фоторецепторные белки. Вообще же рецепторные белки входят в состав любых мембран. Так на внешней мембране митохондрий расположены рецепторы, участвующие в узнавании и транспорте митохондриальных белков, переносимых из цитозоля в митохондрии. На мембранах эндоплазматического ретикулума находятся рецепторы, узнающие и связывающие рибосомы, на ядерной оболочке — рецепторы кариофильных белков и т.д. На плазматической мембране расположены как рецепторы, узнающие соседние клетки или даже отдельные ионы солей (переносчики), так и белки, узнающие белки цитоскелета в цитоплазме.
Мембраны ассоциированы с цитоплазматическими белками
Со стороны цитоплазмы мембраны связаны через примембранные или собственно мембранные интегральные белки с разнообразными белковыми структурами цитоплазмы. К ним относятся в первую очередь компоненты цитоскелета. Это позволяет не только сделать мембраны более жесткими, но и обеспечивает подвижность мембран, создавая возможности для их транспортных функций. Например, жесткость плазматической мембраны безъядерных эритроцитов создается за счет связывания сети цитоплазматических белков с интегральными белками плазмолеммы. В ее состав входит белок, т.н. “белок полосы III”, который обеспечивает транспорт ионов через бислой, но одновременно через ряд белков связывается с сетью белков-спектринов, которые создают жесткую подмембранную сеть (рис. 125). Во многих эпителиальных клетках специальные белки плазматической мембраны связываются с элементами цитоскелета и участвуют в образовании целого ряда межклеточных соединений (десмосомы, адгезивный контакт и др.). С элементами цитоскелета связаны также оболочки клеточного ядра :внешняя ядерная мембрана тесно ассоциирована с промежуточными филаментами, которые фиксируют ядро в объеме цитоплазмы. Внутриклеточные вакуоли могут перемещаться в клетке только при взаимодействии с фибриллярными компонентами, такими как микротрубочки и микрофиламенты. Митохондрии перемещаются в клетке также за счет ассоциации с элементами цитоскелета.
Рост мембран происходит за счет встраивания готовых мембранных пузырьков
После деления клеток происходит увеличение объемов растущих дочерних клеток и тем самым рост клеточной поверхности, увеличение площади плазматической мембраны. Но это не единственный пример быстрого роста объема и поверхности. Поверхность быстро растущих клеток в тычиночных нитях злаков может за 1 ч увеличиться в 65 раз, т.е. каждую минуту плазмолемма нарастает на ее первоначальную величину. Такую большую скорость роста плазматической мембраны можно объяснить только тем, что происходит быстрое встраивание, интеркаляция, пузырьков в растущую плазматическую мембрану. Здесь, внутриклеточные мембранные пузырьки подходят к внутренней стороне плазматической мембраны (возможно, их подгоняют к себе микрофиламенты кортикального слоя), происходит слияние мембран и тем самым увеличение поверхности плазматической мембраны (рис. 126).
Откуда же берутся эти готовые блоки, мембранные пузырьки? Удалось проследить (см. ниже), что первичный генезис мембран происходит в гранулярном эндоплазматическом ретикулуме, который является источником всех клеточных мембран, кроме мембран митохондрий и пластид. От мембран гранулярного ЭПР отщепляются мелкие вакуоли, которые сливаются с мембранами аппарата Гольджи, от которого в свою очередь, отщепляются мелкие мембранные вакуоли, сливающиеся или с лизосомами, или с плазматической мембраной, или с секреторными вакуолями.
Таким образом, наблюдается последовательный каскад переходов одних мембран в другие. Первичные же мембранные вакуоли строятся за счет синтеза белка и липидов на мембранах гранулярного ЭПР.
Рост мембран митохондрий и пластид иного характера. Увеличение площади мембран митохондрий происходит за счет синтеза основной массы белков и липидов в гиалоплазме клетки, вслед за чем эти митохондриальные белки и липиды транспортируются через мембранную оболочку митохондрий и встраиваются в их компоненты.
studfiles.net
Введение в биологию. Часть №4: evan_gcrm — LiveJournal
Оригинал взят у caenogenesis
Введение в биологию (начало)
Введение в биологию. Часть №1
Введение в биологию. Часть №2
Введение в биологию. Часть №3
Тема V
ЛИПИДЫ И МЕМБРАНЫ
В отличие от белков или углеводов, липиды не имеют никакой общей формулы. Это просто собирательное название всех гидрофобных биологически активных соединий. Вот, например, холестерин, спирт с огромной гидрофобной частью. Его производные — стероидные гормоны, которые вырабатываются у человека корой надпочечников и половыми железами. Все они относятся к липидам.
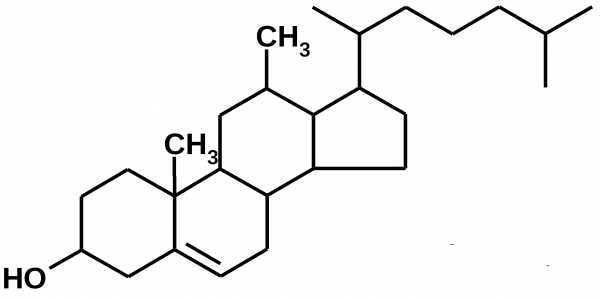
Заодно начнем привыкать к тому, что такие сложные формулы, как правило, не рисуют целиком, до каждого атома. На подобной формуле любой уголок обозначает атом углерода, у которого все свободные валентности по умолчанию заполнены атомами водорода. А если убрать единственную здесь двойную связь, то оставшееся ядро из четырех колец (трех шестиугольников и одного пятиугольника) будет называться замечательным словом “циклопентанпергидрофенантрен”. Это и есть основа для создания разнообразных стероидов, формулами которых загромождать изложение не будем.

Другая важная группа липидов — жирные кислоты, то есть карбоновые кислоты с длинными (10-20 атомов углерода и больше) углеводородными “хвостами”. Чем длиннее “хвост”, тем хуже кислота растворяется в воде. Жирные кислоты, у которых в цепочке более 12 атомов углерода, называют высшими. 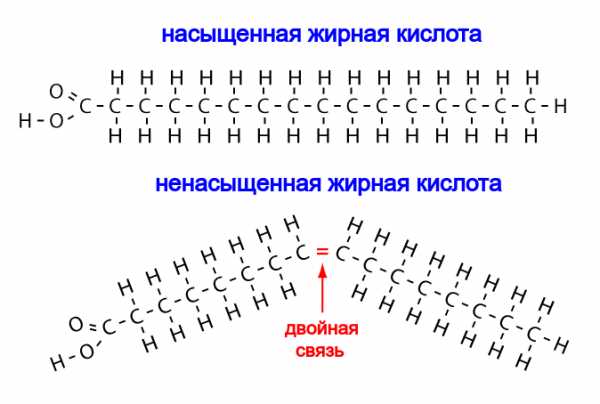
Жирные кислоты бывают насыщенные (без двойных связей в углеводородной цепочке) или ненасыщенные (с двойными связями). Насыщенные высшие жирные кислоты при комнатной температуре — твердые вещества, а ненасыщенные — жидкости. Связано это с более компактной упаковкой насыщенных «хвостов», в которых нет создаваемых двойными связями изломов и изгибов.
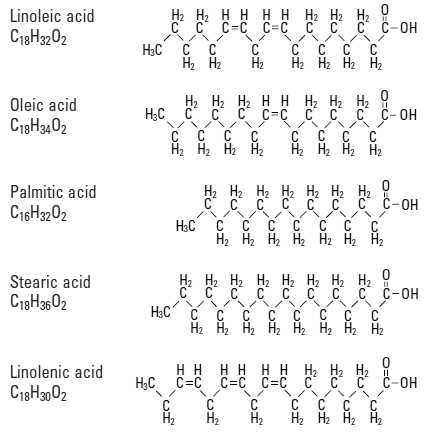
Несколько примеров жирных кислот: линолевая, олеиновая, пальмитиновая, стеариновая, линоленовая. Ненасыщенные жирные кислоты особенно распространены у растений (например, в растительных маслах).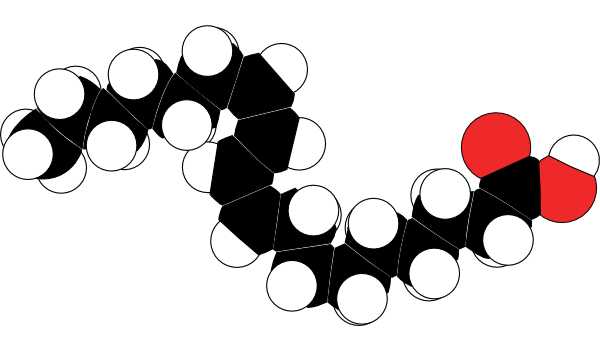
У насыщенных жирных кислот «хвосты» прямые, у ненасыщенных изогнутые в местах двойных связей. Из-за этого молекула может приобрести причудливую форму, особенно если двойных связей несколько. На картинке — модель молекулы линоленовой кислоты, у которой в «хвосте» три двойных связи.

В водном растворе молекулы жирных кислот и их солей образуют мицеллы — шарообразные скопления, где гидрофобные “хвосты” обращены внутрь, минимизируя контакт с водой, а гидрофильные “головки” — наружу, поскольку они-то взаимодействуют с водой хорошо. Это довольно обычное поведение вещества, в молекуле которого есть одновременно гидрофобная и гидрофильная группы.
Жирные кислоты, а вернее их соли, постоянно используются человеком в качестве моющих средств. На картинке — один из самых распространенных компонентов мыла, стеарат натрия (соль стеариновой кислоты). Четко выделена гидрофильная головка, а остальная часть молекулы представляет собой гидрофобный хвост.
Механизм моющего действия мыла следующий. В сосуде слева молекулы мыла просто образуют мицеллу. В сосуде справа они растворяют свои углеводородные хвосты в капле “грязи” (которая, как правило, гидрофобна) и разбивают ее на мелкие капельки, которые легко смыть. Вещества с такой активностью называются детергентами.
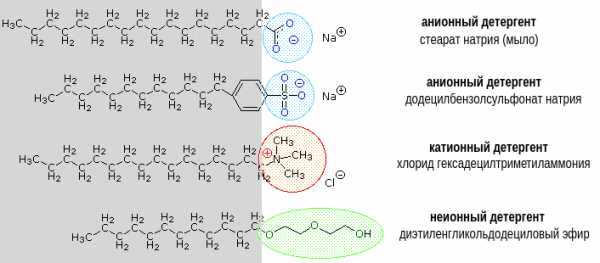
Детергенты бывают очень разными по химической структуре; их гидрофильные части могут быть положительно заряженными, отрицательно заряженными или вовсе незаряженными, а просто полярными. Но молекула любого детергента обязательно включает гидрофобный «хвост» и гидрофильную «головку». Довольно много соединений такого типа входит в состав живых организмов.

Вспомним, что любая карбоновая кислота может образовать с любым спиртом сложный эфир. При этом от кислоты отщепится -OH, от спирта -H, они образуют воду, а остатки кислоты и спирта замыкаются в единую молекулу со сложноэфирной группой -CO-O- посредине. Спиртом, участвующим в этой реакции, вполне может быть и глицерин, у которого гидроксильных групп три. Сложный эфир глицерина и трех жирных кислот называется жиром.
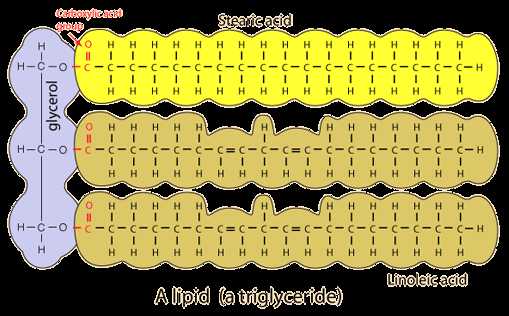
Типичный пример жира, в данном случае ненасыщенного (из трех остатков жирных кислот ненасыщенных тут два). Растительные масла — жидкие, потому что в них больше ненасыщенных жиров, чем у животных. Хотя в целом и насыщенные, и ненасыщенные жирные кислоты есть и у тех и у других, различается только их вклад.

Жиры — ценные источники энергии, именно поэтому они часто запасаются в клетках соединительной ткани у животных, как вот, например, у суслика.

А теперь познакомимся с еще одним важным для нас соединением — фосфорной кислотой (H3PO4). Напомним, что валентность фосфора — 5. На картинке присутствуют два способа изображения молекулы: графическая формула, игнорирующая пространственное расположение связей, и структурная, показывающая его. Вновь будем иметь в виду, что “фосфорная кислота” и “фосфат” (то есть ее соль) в биохимии практически синонимы, в подавляющем большинстве случаев эти понятия свободно заменяются друг на друга.

Сложный эфир глицерина, двух жирных кислот и фосфорной кислоты называется фосфолипидом. Можно сказать, что фосфолипид — это как бы жир, у которого вместо одного из остатков жирных кислот тем же способом присоединен фосфат. Такая молекула состоит из гидрофильной “головки” (включающей остатки глицерина и фосфата) и двух гидрофобных “хвостов” (жирных кислот). При фосфате бывают еще дополнительные боковые цепи, у разных фосфолипидов разные.
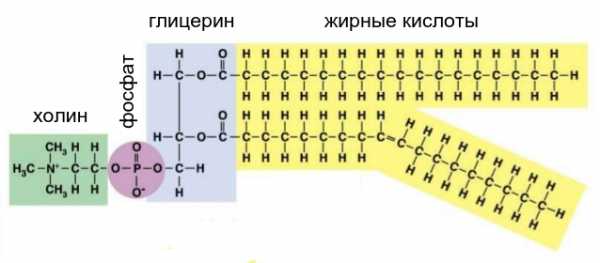
Один из самых распространенных фосфолипидов — фосфатидилхолин. Он приведен только в качестве примера. В других фосфолипидах на месте холина может быть аминокислота серин или что-нибудь еще.

Именно из фосфолипидов в основном состоят клеточные мембраны. Тут используется их физическое свойство: собираться в воде в двойной слой гидрофобными “хвостами” внутрь и гидрофильными “головками” наружу. Замкнутый пузырек, образованный таким двойным слоем молекул, называется везикулой. Вся клеточная мембрана — это в некотором смысле сильно разросшаяся везикула.
На картинке показано, как на границе гидрофильного раствора (вода) и гидрофобного (масло) молекулы фосфолипидов ориентируются хвостами в сторону масла, а головками в сторону воды. Если же никакого масла поблизости нет, то молекулы фосфолипидов располагаются головками в сторону воды, а хвостами друг к другу, и получается двойной слой, который сразу замыкается в везикулу, чтобы не было неустойчивых свободных краев. Это чисто физическое явление, которое запросто может иметь место и вне живых клеток.
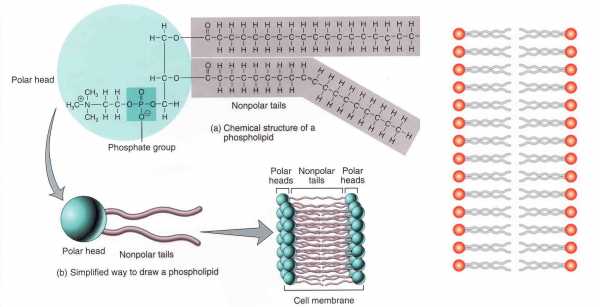
Вот схема того, как фосфолипиды «собираются» в клеточную мембрану. Молекула фосфолипида нарисована двумя способами — во всех деталях (в качестве примера тут взят уже знакомый нам фосфатидилхолин) и в виде головки с двумя хвостиками. Таким молекулы собираются в двойной слой хвостиками друг к другу, головками к воде. Справа — простейшая схема участка типичной мембраны.
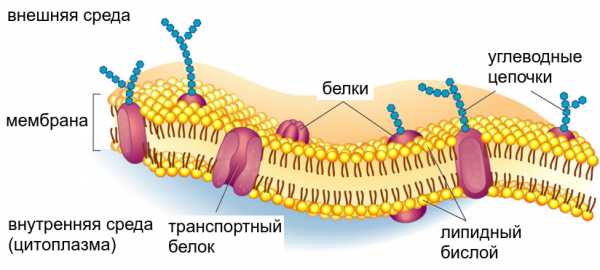
На самом деле биологические мембраны никогда не состоят только из одних фосфолипидов. Типичная клеточная мембрана — фосфолипидный бислой во встроенными в него интегральными белками, которые обычно являются или рецепторными (принимают сигналы из внешней среды и передают их внутрь клетки), или транспортными (переносят те или иные молекулы с одной стороны мембраны на другую). Часть белка, проходящая сквозь образованный «хвостами» внутренний слой мембраны, как правило, представляет собой альфа-спираль, целиком состоящую из гидрофобных аминокислот, боковые цепи которых торчат наружу. Если белок достаточно сложный, таких альфа-спиралей вполне может быть несколько. Кроме того, к мембранным белкам снаружи часто прикреплены ковалентными связями дополнительные цепочки, состоящие не из аминокислот, а из углеводов. Они бывают нужны в первую очередь для взаимодействия между клетками.
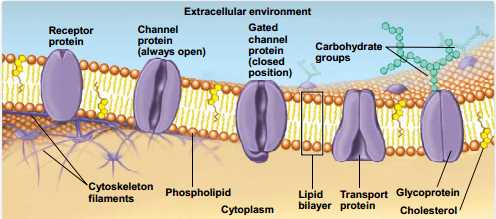
Тут мы видим кое-какие дополнительные детали. Во-первых, кроме фосфолипидов в мембране есть холестерин — его молекулы раскрашены желтым (если сравнить с уже знакомой нам формулой холестерина, видно, что каждая молекула своей гидроксильной группой обращена к воде, а массивной гидрофобной частью внутрь мембраны). Во-вторых, изнутри ко многим интегральным белкам прикреплены элементы цитоскелета — внутриклеточной системы опорных структур, тоже состоящей из белков. Но обе эти особенности есть далеко не у всех клеток.
В целом можно назвать как минимум три основные функции липидов: энергетическая (жиры), структурная (фосфолипиды, холестерин) и сигнальная (стероиды). Но надо иметь в виду, что липиды в силу самой природы этого сборного понятия крайне разнообразны, даже при том, что они (в отличие от белков) не являются полимерами. Мы обсудили далеко не все их группы.
ЛИПИДЫ
Молекулу, в которой есть гидрофильная и гидрофобная части, для краткости называют амфифильной. Известно, что при смешивании амфифильного вещества с водой оно может спонтанно «собраться» в везикулы. При этом молекулы липидов образуют двойной слой, очень похожий на липидный бислой клеточных мембран, и можно экспериментально подобрать условия, в которых такое возникновение везикул ускоряется. Искусственные везикулы могут «расти», избирательно пропуская через мембрану и удерживая в себе разные вещества, и могут «делиться» наподобие клеток. Из-за частичной проницаемости мембран внутри везикул поддерживается среда, отличающаяся от окружающего раствора, в которой идут собственные химические реакции. Получается, что простая самоорганизация растворенных липидов внезапно дает свойства, привычные для живых систем — рост, размножение, обмен веществ, поддержание внутренней среды.
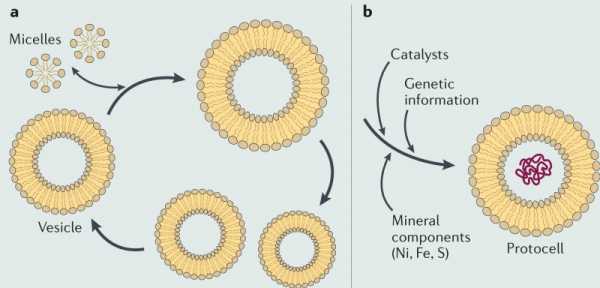
Сейчас можно уверенно сказать, что по части мембранной организации между живой и неживой природой нет особого разрыва. На картинке — вероятная эволюция от однослойной мицеллы к двуслойной везикуле, обретающей способность расти, делиться (a) и захватывать крупные молекулы, в том числе несущие генетическую информацию (b).
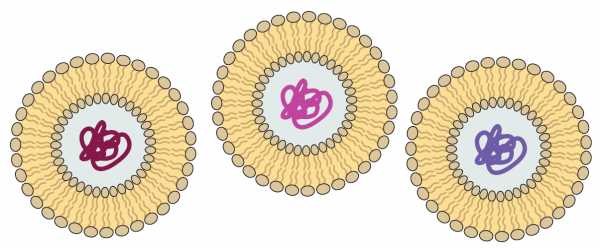
Компоненты первых везикул могли быть гораздо более простыми, чем фосфолипиды. На фотографиях — искусственно полученные везикулы из смеси карбоновых кислот и сложных углеводородов, найденной в знаменитом Мурчисонском метеорите (слева) и просто из жирной кислоты с 10 атомами углерода (справа).
Заодно сборка первых мембран структурировала живое вещество, разделив его на дискретные порции, то есть, собственно говоря, на клетки. Роль в этом процессе амфифильных молекул, отличающихся способностью к образованию пленок и пузырей, «вполне соответствует представлению о рождении Афродиты из пены морской» (Шноль, 1979).
При всем этом мы пока не знаем, в какой именно момент были «изобретены» первые биологические мембраны и из каких молекул они поначалу состояли. Судя по некоторым фактам, эволюция мембран была непростой и непрямой. Тут надо взглянуть на то, о чем мы пока еще не говорили — на разнообразие мембран у разных живых существ.
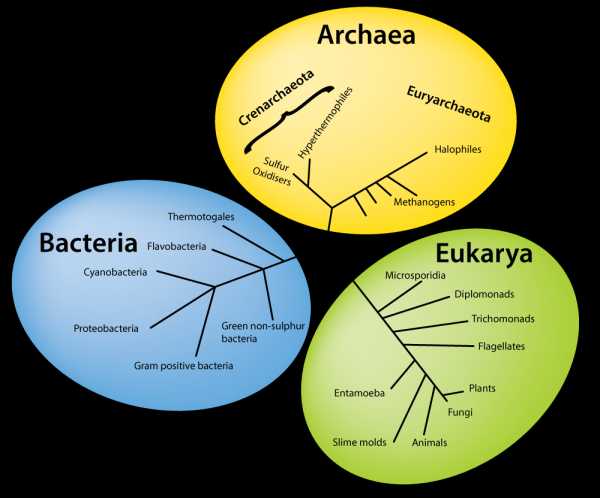
Со времен работ великого молекулярного биолога и микробиолога Карла Вёзе (Carl Richard Woese) общепризнано, что все клеточные организмы делятся на три эволюционные ветви: эукариоты, бактерии и археи. Эти ветви имеют ранг доменов, то есть могут включать по несколько царств. У эукариот есть клеточные ядра, у бактерий и архей нет. Кроме того, бактерии и археи никогда не бывают многоклеточными.
Оказалось, что принципы устройства клеточной мембраны, общие для эукариот и бактерий, не распространяются на архей. Устройство мембраны, свойственное эукариотам и бактериям, раньше считалось абсолютно всеобщим, но открытие архей опровергло это.

Сравнение компонентов эукариотных, бактериальных и архейных клеточных мембран показывает следующее:
● Архейные мембранные липиды представляют собой не сложные эфиры (с общей формулой R-CO-O-R), а простые эфиры (с общей формулой R-O-R).
● Углеводородные гидрофобные цепи у архей ветвятся за счет торчащих в стороны метильных групп.
● Самое поразительное — у некоторых родов архей (и только у них) мембрана представляет собой не бислой, а монослой из молекул с двумя гидрофильными головками и длинной гидрофобной цепью между ними.
Все эти химические особенности мембран полезны для жизни в экстремальных условиях, например при высокой температуре или высокой кислотности. И действительно, многие современные археи (но не все!) как раз в таких условиях живут. Значит, налицо просто далеко зашедшее приспособление?
Однако это не все отличия. Еще важнее то, что у бактерий с эукариотами и у архей для синтеза мембранных липидов используются разные оптические изомеры глицеролфосфата, то есть сложного эфира глицерина и фосфорной кислоты (Lombard et al., 2012). У большинства живых организмов в мембраны входит L-изомер глицеролфосфата, но у архей — D-изомер. И вот это уже гораздо труднее объяснить приспособлением к каким бы то ни было внешним условиям — ведь на «обычные» физико-химические свойства мембраны оптическая изомерия не влияет. К тому же показано, что мембрана, включающая оба изомера, будет физически неустойчивой, а ферменты, “работающие” с этими изомерами, различаются настолько, что проще всего предположить их совершенно независимое происхождение.
Может быть, общие предки бактерий, эукариот и архей вообще не имели никакой мембраны, то есть еще не были клетками (Koga et al., 1998)? Или мембрана у них была, но не липидная, а минеральная, железо-серная (Martin et al., 2003)? С другой стороны, генетические данные позволяют думать, что у общего предка всех клеточных форм жизни уже были кое-какие интегральные белки, приспособленные к работе в мембране и бесполезные без нее. В любом случае этот узел еще далеко не распутан.
evan-gcrm.livejournal.com
Гидрофобные взаимодействия в мембрана — Справочник химика 21
Образованные в результате такого гидрофобного взаимодействия соединения в дальнейшем связываются с гидрофобными частями полимера и образуют еще более малоподвижные молекулярные комплексы, которые могут укрупняться, образуя связь с уже имеющимися на поверхности мембраны молекулами неполярного вещества или их группами. Важным следствием такого гидрофобного взаимодействия является повышение числа свободных подвижных молекул воды в связанном слое, получаемых вследствие вытеснения некоторых молекул воды из моди- [c.221]Было высказано предположение [36], согласно которому стабильность структуры макромолекул и мембр-ан обеспечивается главным образом гидрофобными взаимодействиями углеводородных фрагментов, в результате чего молекулы липидов, белков и других соединений могут образовывать в водной цитоплазме олигомерные агрегаты и мембраны. Вместе с тем наиболее активные катализаторы, т. е. большинство ферментов, растворимы в воде. Таким образом, мембраны представляют собой сравнительно стабильные тонкие пленки, примыкаю щие к водным участкам клетки, в которых легко протекают химические реакции и которые содержат полярные молекулы, растворимые в воде. [c.355]
Гидрофобные взаимодействия. Биополимеры — белки и нуклеиновые кислоты — функционируют главным образом в водном окружении. Гидрофобные силы — силы специфического отталкивания между неполярными атомными группами и молекулами воды. Это энтропийный эффект, определяемый особенностями структуры воды как конденсированной системы. Гидрофобные взаимодействия играют важнейшую роль в формировании структуры белков, надмолекулярных систем (мембраны) и т. д. [c.58]
Низкая ионная электропроводность липидной мембраны, рассматриваемой как однородная среда, определяется низкой ди-, электрической проницаемостью (2—3) липидов, неблагоприятной для внедрения заряженных частиц. Коэффициент распределения частиц между липидной и водной фазами равен exp( — W/RT), где W — энергия частицы в липиде, отсчитанная от энергии в воде. Она складывается из электростатической энергии и энергии гидрофобного взаимодействия [c.351]
В состав клеточных мембран входят в основном белки и липиды, среди- которых преобладают фосфолипиды, составляющие 40—90 % от общего количества липидов в мембране. Строение биомембраны интенсивно изучается в настоящее время. В одной из моделей клеточная мембрана рассматривается как липидный бислой. В таком бислое углеводородные хвосты липидов за счет гидрофобных взаимодействий удерживаются друг возле друга в вытянутом состоянии во внутренней полости, образуя двойной углеводородный слой. Полярные группы липидов располагаются на внешней поверхности бислоя (рис. 14.2). [c.466]
Плазматическая мембрана состоит из двойного липидного слоя. Гидрофобные концы молекул фосфолипидов и триглицеридов направлены внутрь, а гидрофильные головки — наружу. Благодаря гидрофобным взаимодействиям между остатками жирных кислот, входящих в состав липидов, и электростатическому взаимодействию между гидрофильными головками мембрана стабилизируется. В двойной слой липидов встроены белки так называемые интегральные белки мембран. Они плавают в этом слое, будучи погружены в него частично, или же пронизывают его насквозь. Другие белки прикреплены к поверхности мембраны, и их называют периферийными белками (рис. 1.6). Некоторые мембраны, по-видимому, с одной или с обеих сторон покрыты сетью вытянутых белковых молекул. [c.23]
Вероятно, что при связывании макромолекулы часть мозаичной жидкостной структуры мембраны претерпевает такую деформацию, что молекула получает возможность проникнуть внутрь клетки. Эта деформация может быть вызвана локальными физическими силами, например, поверхностным натяжением или гидрофобным взаимодействием. Поскольку белок связывается с подвижным мембранным рецептором, процессы переориентации и вращения всего комплекса протекают очень быстро. [c.66]
Плазматическая мембрана состоит из двойного липидного слоя. Гидрофобные концы молекул фосфолипидов и триглицеридов направлены внутрь, а гидрофильные головки -наружу. Благодаря гидрофобным взаимодействиям между остатками жирных кислот, входящих в состав липидов, и электростатическому взаимодействию между гидрофильны- [c.44]
Внутри мембраны оказываются спрятанными углеводородные хвосты — гидрофобные группы. Этот гидрофобный скелет придает мембране важное свойство — она делается нерастворимой в воде. Но наличие поверхностных гидрофильных групп обусловливает тесное взаимодействие мембраны и водной среды и дает возможность протекать таким процессам, как переносы (юнов через мембрану от среды к клетке или в обратном направлении. Так сочетание гидрофобных и гидрофильных, т. е. по существу противоположных, свойств делает мембрану ценным и универсальным материалом природы. [c.159]
Понимание основных принципов, описывающих структуру воды и взаимодействие мембрана — вода, упрощает задачу тщательного отбора и синтеза новых перспективных полимеров для гиперфильтрационных мембран. Например, для гиперфильтрационных мембран из ацетата целлюлозы оказывается, что гидратация гидрофильных гидроксильных групп, образование водных оболочек около гидрофобных ацетатных групп и жесткость молекул целлюлозы оказывают совместное влияние на повышение вязкости (и, следовательно, на снижение е) воды, необходимое для практически полного выделения соли. [c.177]
Отсутствие взаимодействий мембрана—вода, характерное для гидрофобных материалов (таких как полиэтилен), приводит к более сильному межфазному поверхностному натяжению. Молекулы воды в этом случае образуют кластеры друг с другом, а не смачивают поверхность мембраны. Поскольку движение по каналам больших кластеров из молекул воды более затруднено, чем движение небольших кластеров или отдельных молекул, то проницаемость снижается с уменьшением взаимодействия мембрана — растворитель. [c.178]
Образованные в результате такого гидрофобного взаимодействия соединения связываются затем с гидрофобными частями материала мембраны и образуют еще менее подвижные молекулярные комплексы, которые могут укрупняться, соединяясь с уже имеющимися на поверхности мембраны молекулами неполярного вещества и их группами. Важным следствием такого гидрофобного взаимодействия является увеличение числа свободных подвижных молекул воды в связанном слое вследствие вытеснения некоторых молекул воды из модифицированных сфер неполярных молекул. Это должно привести к повышению селективности с ростом температуры, так как под де
www.chem21.info