Персональный сайт — Креатинин
КРЕАТИНИН
Креатин и креатинин – важные компоненты остаточного азота, в синтезе которых принимают участие аминокислоты аргинин, глицин и метионин. Известно два источника креатина в организме. Существует экзогенный креатин, т.е. креатин пищевых продуктов (мясо, печень), и эндогенный креатин, образующийся в процессе синтеза в тканях.
В почечной ткани при участии фермента трансамидиназы образуется предшественник креатина – гуанидин-уксусная кислота (гуанидинацетат), которая подвергается метилированию в печени. С током крови креатин доставляется из печени в мышечную ткань, где происходит его фосфорилирование под влиянием фермента креатинкиназы, образуется креатинфосфат. Макроэнерг креатинфосфат, образованный в митохондриях миоцитов, перемещается к миофибриллами, где происходит его разрушение с выделением энергии, а также остатка неорганического фосфора и молекулы воды. Образовавшийся креатинин является беспороговым веществом, который выделяется с мочой.
Спонтанный, т.е. самопроизвольный, гидролиз креатина ведет к образованию креатинина, который практически полностью выделяется с мочой.
Креатинин является конечным продуктом распада креатина, который вовлечен в энергетический обмен мышечной и других тканей. Концентрация креатинина в крови и моче зависит от мышечной массы и выделительной способности почек, а количество белков в рационе питания на его уровень не влияет. Определение креатина широко используется для диагностики заболевания почек.
Клинико-диагностическое значение определения креатинина.
При заболеваниях почек параллельно с нарушением выделения клубочками других азотистых продуктов обмена нарушается выделение креатинина и наступает задержка его в крови.
Креатининемия (гиперкреатининемия) – это повышение уровня креатинина в крови.
Увеличение уровня креатинина в сыворотке (плазме) крови обусловлено как усиленным образованием (продукцией), так и задержкой (ретенцией) этого метаболита в организме.
Продукционная креатининемия (гиперкреатининемия) – отмечается при кишечной непроходимости, острой жёлтой атрофии печени, хлоропривной азотемии (т.е. гиперазотемии вследствие уменьшения содержания осмотически активных ионов хлора), декомпенсации сердечно-сосудистой системы, пневмонии, лихорадочных состояния, мышечной дистрофии. Возрастание содержания креатинина в сыворотке (плазме) крови может быть вызвано изменением эндокринного баланса: при сахарном диабете, гипертиреозе, гипофункции надпочечников, акромегалии и гигантизме.
Ретенционная креатининемия (гиперкреатининемия) – обусловлена нарушением (острым и хроническим) функции почек любого происхождения и обычно наблюдается при уменьшении клубочковой фильтрации, поражении воспалительным процессом паренхимы почек, обтурации мочевых путей ниже уровня почек.
Креатининемия является как ранним показателем развивающейся недостаточности почек. Устойчивое повышение уровня креатинина в крови, как и возрастание концентрации в ней, указывает на нарушение функции почечного фильтра.
Снижение уровня креатинина в сыворотке (плазме) крови (гипокреатининемия) коррелирует с уменьшением мышечной массы (мышечные дистрофии и атрофии, параличи, парезы и др.), оно наблюдается при беременности, достигая наибольшей выраженности в первом и втором триместре.
В моче помимо эндогенного креатинина содержится экзогенный, поступающий в организм с мясной пищей. Поэтому уровень экскреции креатинина с мочой несколько зависит от характера питания.
Увеличение выведения креатинина с мочой отмечается при большой физической нагрузке (мышечной работе), лихорадочных состояниях, острых инфекционных заболеваниях (при которых происходит усиления цитолиза, т.е. повышение распада белков клеток), пневмонии, выраженной недостаточности функции печени. Увеличение секреции креатинина с мочой происходит при ряде эндокринных расстройств (акромегалии, гигантизме, сахарном диабете).
Уменьшение выведения креатинина с мочой наблюдается при голодании, длительном обездвижении больных (мышечная дистрофия), параличах, анемии, лейкозах, гипертиреозе, хронических заболеваниях почек, амилоидозе почек, голодании.
Параллельное определение концентрации креатинина в крови и моче значительно расширяет диагностические возможности оценки функционального состояния почек, поскольку позволяет получить информацию об интенсивности основных функций нефрона: фильтрации, реабсорбции, секреции, а также почечного кровообращения.
bioximia.narod.ru
Экзогенный и эндогенный креатинин — Лечение гипертонии
Липопротеины (липопротеиды) высокой и низкой плотности в крови: что это, норма, повышение
Многие годы безуспешно боретесь с ГИПЕРТОНИЕЙ?
Глава Института: «Вы будете поражены, насколько просто можно вылечить гипертонию принимая каждый день…
Читать далее »
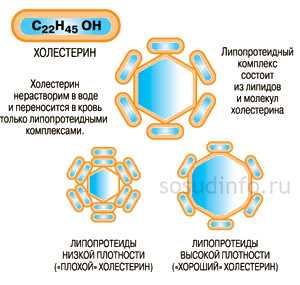
Липопротеины — сложные белково-липидные комплексы, входящие в состав всех живых организмов и являющиеся необходимой составной частью клеточных структур. Липопротеины выполняют транспортную функцию. Их содержание в крови — важный диагностический тест, сигнализирующий о степени развития заболеваний систем организма.
Это класс сложных молекул, в состав которых могут одновременно входить свободные триглицериды, жирные кислоты, нейтральные жиры, фосфолипиды и холестерин в различных количественных соотношениях.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Липопротеины доставляют липиды в различные ткани и органы. Они состоят из неполярных жиров, расположенных в центральной части молекулы — ядре, которое окружено оболочкой, образованной из полярных липидов и апобелков. Подобным строением липопротеинов объясняются их амфифильные свойства: одновременная гидрофильность и гидрофобность вещества.
Функции и значение
Липиды играют важную роль в организме человека. Они содержатся во всех клетках и тканях и участвуют во многих обменных процессах.
- Липопротеины — основная транспортная форма липидов в организме. Поскольку липиды являются нерастворимыми соединениями, они не могут самостоятельно выполнять свое предназначение. Липиды связываются в крови с белками — апопротеинами, становятся растворимыми и образуют новое вещество, получившее название липопротеид или липопротеин. Эти два названия являются равноценными, сокращенно — ЛП.
Липопротеины занимают ключевое положение в транспорте и метаболизме липидов. Хиломикроны транспортируют жиры, поступающие в организм вместе с пищей, ЛПОНП доставляют к месту утилизации эндогенные триглицериды, с помощью ЛПНП в клетки поступает холестерин, ЛПВП обладают антиатерогенными свойствами.
- Липопротеины повышают проницаемость клеточных мембран.
- ЛП, белковая часть которых представлена глобулинами, стимулируют иммунитет, активизируют свертывающую систему крови и доставляют железо к тканям.
Классификация
ЛП плазмы крови классифицируют по плотности (с помощью метода ультрацентрифугирования). Чем больше в молекуле ЛП содержится липидов, тем ниже их плотность. Выделяют ЛПОНП, ЛПНП, ЛПВП, хиломикроны. Это самая точная из всех существующих классификаций ЛП, которая была разработана и доказана с помощью точного и довольно кропотливого метода — ультрацентрифугирования.
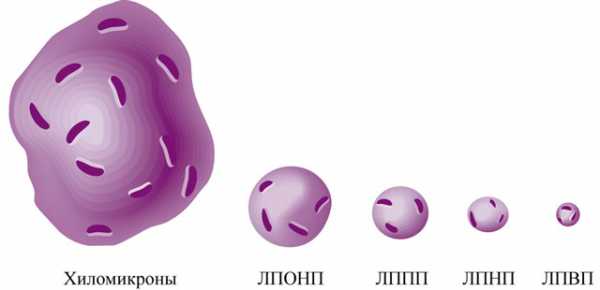
По размерам ЛП также неоднородны. Самыми крупными являются молекулы хиломикронов, а затем по уменьшению размера — ЛПОНП, ЛПСП, ЛПНП, ЛПВП.
Электрофоретическая классификация ЛП пользуется большой популярностью у клиницистов. С помощью электрофореза были выделены следующие классы ЛП: хиломикроны, пре-бета-липопротеины, бета-липопротеины, альфа-липопротеины. Данный метод основан на введении в жидкую среду активного вещества с помощью гальванического тока.
Фракционирование ЛП проводят с целью определения их концентрации в плазме крови. ЛПОНП и ЛПНП осаждают гепарином, а ЛПВП остаются в надосадочной жидкости.
Виды
В настоящее время выделяют следующие виды липопротеинов:
ЛПВП (липопротеины высокой плотности)
ЛПВП обеспечивают транспорт холестерина от тканей организма к печени.
ЛПВП содержат фосфолипиды, которые поддерживают холестерин во взвешенном состоянии и предупреждают его выход из кровяного русла. ЛПВП синтезируются в печени и обеспечивают обратный транспорт холестерина из окружающих тканей к печени на утилизацию.
- Увеличение ЛПВП в крови отмечают при ожирении, жировом гепатозе и билиарном циррозе печени, алкогольной интоксикации.
- Снижение ЛПВП происходит при наследственной болезни Танжера, обусловленной скоплением холестерина в тканях. В большинстве прочих случаев снижение концентрации ЛПВП в крови — признак атеросклеротического повреждения сосудов.
Норма ЛПВП отличается у мужчин и женщин. У лиц мужского пола значение ЛП данного класса колеблется в пределах от 0,78 до 1,81 ммоль/л, норма у женщин ЛПВП — от 0,78 до 2,20, в зависимости от возраста.
ЛПНП (липопротеины низкой плотности)
ЛПНП являются переносчиками эндогенного холестерина, триглицеридов и фосфолипидов от печени к тканям.
Данный класс ЛП содержит до 45% холестерина и является его транспортной формой в крови. ЛПНП образуются в крови в результате действия на ЛПОНП фермента липопротеинлипазы. При его избытке на стенках сосудов появляются атеросклеротические бляшки.
В норме количество ЛПНП составляет 1,3-3,5 ммоль/л.
- Уровень ЛПНП в крови повышается при гиперлипидемии, гипофункции щитовидной железы, нефротическом синдроме.
- Пониженный уровень ЛПНП наблюдается при воспалении поджелудочной железы, печеночно-почечной патологии, острых инфекционных процессах, беременности.
ЛПОНП (липопротеины очень низкой плотности)
ЛПОНП образуются в печени. Они переносят эндогенные липиды, синтезируемый в печени из углеводов, в ткани.
Это самые крупные ЛП, уступающие по размерам лишь хиломикронам. Они более, чем на половину состоят из триглицеридов и содержат небольшое количество холестерина. При избытке ЛПОНП кровь становится мутной и приобретает молочный оттенок.
ЛПОНП — источник «плохого» холестерина, из которого на эндотелии сосудов образуются бляшки. Постепенно бляшки увеличиваются, присоединяется тромбоз с риском острой ишемии. ЛПОНП повышены у больных с сахарным диабетом и болезнями почек.
Хиломикроны
Хиломикроны отсутствуют в крови у здорового человека и появляются только при нарушении обмена липидов. Хиломикроны синтезируются в эпителиальных клетках слизистой оболочки тонкого кишечника. Они доставляют экзогенный жир из кишечника в периферические ткани и печень. Большую часть транспортируемых жиров составляют триглицериды, а также фосфолипиды и холестерин. В печени под воздействием ферментов триглицериды распадаются, и образуются жирные кислоты, часть которых транспортируется в мышцы и жировую ткань, а другая часть связывается с альбуминами крови.
ЛПНП и ЛПОНП являются высокоатерогенными — содержащими много холестерина. Они проникают в стенку артерий и накапливаются в ней. При нарушении метаболизма уровень ЛПНП и холестерина резко повышается.
Наиболее безопасными в отношении атеросклероза являются ЛПВП. Липопротеины этого класса выводят холестерин из клеток и способствуют его поступлению в печень. Оттуда он вместе с желчью попадает в кишечник и покидает организм.
Представители всех остальных классов ЛП доставляют холестерин в клетки. Холестерин — это липопротеид, входящий в состав клеточной стенки. Он участвует в образовании половых гормонов, процессе желчеобразования, синтезе витамина Д, необходимого для усвоения кальция. Эндогенный холестерин синтезируется в печеночной ткани, клетках надпочечников, стенках кишечника и даже в коже. Экзогенный холестерин поступает в организм вместе с продуктами животного происхождения.
Дислипопротеинемия — диагноз при нарушении обмена липопротеинов
Дислипопротеинемия развивается при нарушении в организме человека двух процессов: образования ЛП и скорости их выведения из крови. Нарушение соотношения ЛП в крови — не патология, а фактор развития хронического заболевания, при котором уплотняются артериальные стенки, суживается их просвет и нарушается кровоснабжение внутренних органов.
При повышении уровня холестерина в крови и снижении уровня ЛПВП развивается атеросклероз, приводящий к развитию смертельно опасных заболеваний.
Этиология
Первичная дислипопротеинемия является генетически детерминированной.
Причинами вторичной дислипопротеинемии являются:
- Гиподинамия,
- Сахарный диабет,
- Алкоголизм,
- Дисфункция почек,
- Гипотиреоз,
- Печеночно-почечная недостаточность,
- Длительный прием некоторых лекарств.
Понятие дислипопротеинемия включает 3 процесса — гиперлипопротеинемию, гиполипопротеинемию, алипопротеинемию. Дислипопротеинемия встречается довольно часто: у каждого второго жителя планеты отмечаются подобные изменения в крови.
Гиперлипопротеинемия — повышенное содержание ЛП в крови, обусловленное экзогенными и эндогенными причинами. Вторичная форма гиперлипопротеинемии развивается на фоне основной патологии. При аутоиммунных заболеваниях ЛП воспринимаются организмом как антигены, к которым вырабатываются антитела. В результате образуются комплексы антиген — антитело, обладающие большей атерогенностью, чем сами ЛП.
- Гиперлипопротеинемия 1 типа характеризуется образованием ксантом — плотных узелков, содержащих холестерин и расположенных над поверхностью сухожилий, развитием гепатоспленомегалии, панкреатита. Больные жалуются на ухудшение общего состояния, подъем температуры, потерю аппетита, приступообразную боль в животе, усиливающуюся после приема жирной пищи.
- При 2 типе образуются ксантомы в области сухожилий стоп и ксантелазмы в периорбитальной зоне.
- 3 тип — симптомы нарушения сердечной деятельности, появление пигментации на коже ладони, мягких воспаленных язвочек над локтями и коленями, а также признаков поражения сосудов ног.
- При 4 типе увеличивается печень, развивается ИБС и ожирение.
Алипопротеинемия — генетически обусловленное заболевание с аутосомно-доминантным типом наследования. Заболевание проявляется увеличением миндалин с оранжевым налетом, гепатоспленомегалией, лимфаденитом, мышечной слабостью, снижением рефлексов, гипочувствительностью.
Гиполипопротеинемия — низкое содержание в крови ЛП, часто протекающее бессимптомно. Причинами заболевания являются:
- Наследственность,
- Неправильное питание,
- Сидячий образ жизни,
- Алкоголизм,
- Патология пищеварительной системы,
- Эндокринопатия.
Дислипопротеинемии бывают: органными или регуляторными, токсигенными, базальными — исследование уровня ЛП натощак, индуцированными — исследование уровня ЛП после приема пищи, препаратов или физической нагрузки.
Диагностика
Известно, что для организма человека избыток холестерина очень вреден. Но и недостаток этого вещества может привести к дисфункции органов и систем. Проблема кроется в наследственной предрасположенности, а также в образе жизни и особенностях питания.

Диагностика дислипопротеинемии основывается на данных анамнеза болезни, жалобах больных, клинических признаках — наличии ксантом, ксантелазм, липоидной дуги роговицы.
Основным диагностическим методом дислипопротеинемии является анализ крови на липиды. Определяют коэффициент атерогенности и основные показатели липидограммы — триглицериды,общий холестерин, ЛПВП, ЛПНП.
Липидограмма – метод лабораторной диагностики, который выявляет нарушения липидного обмена, приводящие к развитию заболеваний сердца и сосудов. Липидограмма позволяет врачу оценить состояние пациента, определить риск развития атеросклероза коронарных, мозговых, почечных и печеночных сосудов, а также заболеваний внутренних органов. Кровь сдают в лаборатории строго натощак, спустя минимум 12 часов после последнего приема пищи. За сутки до анализа исключают прием алкоголя, а за час до исследования — курение. Накануне анализа желательно избегать стресса и эмоционального перенапряжения.
Ферментативный метод исследования венозной крови является основным для определения липидов. Прибор фиксирует предварительно окрашенные специальными реагентами пробы. Данный диагностический метод позволяет провести массовые обследования и получить точные результаты.
Сдавать анализы на определение липидного спектра с профилактической целью, начиная с юности необходимо 1 раз в 5 лет. Лицам, достигшим 40 лет, делать это следует ежегодно. Проводят исследование крови практически в каждой районной поликлинике. Больным, страдающим гипертонией, ожирением, заболеваниями сердца, печени и почек, назначают биохимический анализ крови и липидограмму. Отягощенная наследственность, имеющиеся факторы риска, контроль эффективности лечения — показания для назначения липидограммы.
Результаты исследования могут быть недостоверны после употребления накануне пищи, курения, перенесенного стресса, острой инфекции, при беременности, приеме некоторых лекарственных препаратов.
Диагностикой и лечение патологии занимается эндокринолог, кардиолог, терапевт, врач общей практики, семейный врач.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для лечения гипертонии наши читатели успешно используют ReCardio. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Лечение
Диетотерапия играет огромную роль в лечении дислипопротеинемии. Больным рекомендуют ограничить потребление животных жиров или заменить их синтетическими, принимать пищу до 5 раз в сутки небольшими порциями. Рацион необходимо обогащать витаминами и пищевыми волокнами. Следует отказаться от жирной и жареной пищи, мясо заменить морской рыбой, есть много овощей и фруктов. Общеукрепляющая терапия и достаточная физическая нагрузка улучшают общее состояние больных.
Гиполипидемическая терапия и антигиперлипопротеинемические препараты предназначены для коррекции дислипопротеинемии. Они направлены на снижение уровня холестерина и ЛПНП в крови, а также на повышение уровня ЛПВП.
Из препаратов для лечения гиперлипопротеинемии больным назначают:
- Статины – «Ловастатин», «Флувастатин», «Мевакор», «Зокор», «Липитор». Эта группа препаратов уменьшает выработку холестерина печенью, снижает количество внутриклеточного холестерина, разрушает липиды и оказывает противовоспалительное действие.
- Секвестранты снижают синтез холестерина и выводят его из организма — «Холестирамин», «Колестипол», «Холестипол», «Холестан».
- Фибраты снижаю уровень триглицеридов и повышают уровень ЛПВП — «Фенофибрат», «Ципрофибрат».
- Витамины группы В.
Гиперлипопротеинемия требует лечения гиполипидемическими препаратами «Холестерамином», «Никотиновой кислотой», «Мисклероном», «Клофибратом».
Лечение вторичной формы дислипопротеинемии заключается в устранении основного заболевания. Больным сахарным диабетом рекомендуют изменить образ жизни, регулярно принимать сахаропонижающие препараты, а также статины и фибраты. В тяжелых случаях требуется проведение инсулинотерапии. При гипотиреозе необходимо нормализовать функцию щитовидной железы. Для этого больным проводят гормональную заместительную терапию.
Больным, страдающим дислипопротеинемией, рекомендуют после проведения основного лечения:
- Нормализовать массу тела,
- Дозировать физические нагрузки,
- Ограничить или исключить употребление алкоголя,
- По возможности избегать стрессов и конфликтных ситуаций,
- Отказаться от курения.
Видео: липопротеины и холестерин — мифы и реальность
Видео: липопротеины в анализах крови — программа «Жить здорово!»
infarkt.lechenie-gipertoniya.ru
Креатинин | Стероиды
 Креатинин — конечный продукт метаболизма креатинфосфата — вещества, участвующего в механизмах быстрого обеспечения энергетических потребностей мышечного сокращения.
Креатинин — конечный продукт метаболизма креатинфосфата — вещества, участвующего в механизмах быстрого обеспечения энергетических потребностей мышечного сокращения.
Креатинин образуется в мышцах результате неферментативного отщепления фосфатной группы от креатинфосфата, а также спонтанного превращения креатина в креатинин. Он продуцируется и поступает в кровь с постоянной скоростью, поэтому концентрация креатинина в сыворотке крови относительно стабильна и в норме определяется преимущественно общим объемом мышечной массы человека. У мужчин содержание креатинина несколько выше по сравнению с женщинами, что связано с относительно большей мышечной массой. Уровень креатинина сыворотки крови зависит от возраста (референсные значения для детей существенно ниже). Концентрация креатинина крови физиологически снижена у беременных женщин (на 40%) вследствие увеличения объема крови, повышения почечного плазмотока и фильтрации, и соответствующего роста клиренса креатинина, особенно во II и III триместрах беременности.
Креатинин выводится из крови почками. Он относится к так называемым «беспороговым» веществам: в норме креатинин свободно фильтруется в почечных клубочках и далее, не подвергаясь обратному всасыванию или дополнительной секреции в канальцах, полностью выводится с мочой из организма. Поэтому увеличение концентрации креатинина в сыворотке крови говорит об уменьшении уровня почечной фильтрации (снижении функции почек). Зная концентрацию креатинина сыворотки крови и количество выделенного с мочой креатинина за определенный промежуток времени, можно рассчитать объем плазмы крови, фильтрующейся в почечных клубочках в единицу времени (расчет объема клубочковой фильтрации по клиренсу эндогенного креатинина, или проба Реберга).
Следует отметить, что образование эндогенного креатинина в пожилом возрасте несколько уменьшается, и у пожилых пациентов степень тяжести болезни почек может оказаться выше, чем та, на которую указывает концентрация креатинина в сыворотке крови.
Вследствие высоких резервных возможностей почечной гемодинамики, креатинин не является чувствительным показателем заболеваний почек в ранней стадии и может оставаться на постоянном уровне при поражении значительной части нефронов. Поэтому этот тест обычно используют одновременно с определением мочевины тест №1.2.3), концентрация которой более чувствительна к функциональным изменениям состояния почек. В то же время, на уровень креатинина сыворотки в меньшей степени, чем на уровень мочевины, оказывает влияние характер пищи. Небольшое увеличение содержания креатинина в крови может вызвать повышенное поступление экзогенного креатина и креатинина с мясной пищей.
Исследование креатинина широко используется в лабораторной практике, во-первых, как один из биохимических показателей для диагностики гиперазотемий; во вторых, как клиренсовый показатель, то есть показатель фильтрационной способности почек, характеризующий степень очищения определенного объема крови, проходящего через почки от какого-либо вещества в одну минуту.
Содержание креатинина в крови закономерно повышается при почечной недостаточности, что имеет большое значение для ее диагностики. Следует отметить, что увеличение уровня креатинина и мочевины при ОПН – довольно поздние ее признаки. Повышение выявляется, когда поражено более 50% нефронов. При тяжелом нарушении функции почек содержание в крови креатинина может достигать очень высоких цифр – 800-900 мкмоль/л, а в отдельных случаях до 2650 мкмоль/л и выше. При неосложненных случаях ОПН концентрация креатинина в крови возрастает в сутки на 44-88 мкмоль/л, в случаях ОПН, сопровождающейся поражением мышц (обширная травма), уровень креатинина в крови возрастает более заметно в результате значительного увеличения скорости его образования. Уровни креатинина в крови и клубочковой фильтрации приняты как основные лабораторные критерии в классификации хронической почечной недостаточности (ХПН).
Следует помнить, что такие заболевания, как гипертиреоз, резко выраженные нарушения функций печени, недостаточность деятельности сердечно-сосудистой системы, воспалительные заболевания легких, лихорадочные состояния, закупорка мочевых путей, акромегалия, гигантизм, сахарный диабет, кишечная непроходимость, мышечная дистрофия, обширные ожоги, также могут сопровождаться повышением уровня креатинина в крови.
Показания к назначению анализа:
- Диагностика заболеваний почек.
- Заболевания скелетных мышц.
Референсные значения:
| Возраст | Креатинин, мкмоль/л |
| <1 года | 18-35 |
| 1-14 лет | 27-62 |
| Женщины, >14 лет | 53-97 |
| Мужчины, >14 лет | 62-115 |
Повышение значений:
- Нарушение функции почек (острое и хроническое) любой этиологии (нарушение перфузии почек, заболевание собственно почек, обтурация мочевых путей).
- Акромегалия и гигантизм.
- Гипертиреоз.
- Мясная диета.
Снижение значений:
- Пониженная мышечная масса тела.
- Беременность (особенно I и II триместры).
Связанные темы
Tags: биохимия крови
steroid.su
Креатин: чистая энергия
После осаждения белков крови в ней остается общее количество небелкового азота, который получил название остаточного азота. Это разные вещества, такие, как мочевина, азот аминокислот, мочевая кислота, креатин и креатинин, а также некоторые другие продукты обмена в меньших количествах. Определение количества креатина и продукта его дальнейшего преобразования креатинина очень важно для диагностики различных заболеваний.
Что такое креатин
Креатин — это продукт белкового обмена, который образуется при распаде аминокислот (глицина, аргинина, метионина) в печени и поджелудочной железе, откуда поступает в кровь, а затем в другие органы. Креатин содержится в различных тканях человека, впервые он был обнаружен французским ученым Шеврелем в 1835 году в экстракте из скелетных мышц.
Небольшая часть креатина распадается, превращаясь в креатинин. В тканях к креатину присоединяется фосфорильная группа АТФ, превращая его в креатинфосфат, являющийся запасным носителем энергии. Таким образом креатин участвует в энергетическом обмене. Креатин выполняет регуляторную роль во многих биохимических процессах: стимулирует биосинтез белков, активизирует процесс клеточного дыхания.
Процессы, которые идут в клетке с потреблением энергии, — сокращение мышц, активный транспорт ионов в нервные клетки сопровождаются расщеплением значительного количества креатинфосфата и накоплением креатина при постоянном уровне и небольших изменениях концентрации АТФ. Этот процесс помогает организму сберегать энергию.
В медицине определение содержания креатина и его производного креатинина в крови и моче служит для диагностики целого ряда заболеваний.
О чем говорит повышение уровня креатина в крови
Различают экзогенный и эндогенный креатин. Экзогенный креатин поступает в организм с белковыми продуктами (мясом, рыбой, молочными продуктами, орехами), а эндогенный синтезируется в печени и транспортируется с кровью в мышцы, где он является необходимым компонентом биохимических процессов.
В норме в цельной крови взрослого человека концентрации креатина составляет 153 — 305 мкмоль/л, в плазме крови — 15,25 — 76,25 мкмоль/л.
Повышение уровня креатина в крови (гиперкреатинемия) наблюдается как при избыточном его поступлении с пищей, так и при состояниях, сопровождающихся нарушением обмена веществ или выделением эндогенного креатина — при заболеваниях мышечной системы, кишечной непроходимости, поражениях печени и почек, ревматоидном артрите, сахарном диабете, повышенной функции щитовидной железы, некоторых эндокринных заболеваниях, сердечно-сосудистой недостаточности.
При высокой концентрации креатина в плазме крови (свыше 120 мкмоль/л) он начинает выделяться с мочой (креатинурия). Большие количества креатина в крови и в моче обнаруживаются при некоторых патологических процессах: мышечной дистрофии (обменных нарушениях в мышечной ткани), снижении тонуса мышц, воспалении мышц (миозитах). Физиологическая креатинурия (это входит в понятие нормы) нередко наблюдается у детей, у женщин в период беременности или кормления ребенка грудью, при избыточном употреблении мяса, рыбы, печени.
БАДы, содержащие креатин
Сегодня в некоторых видах спорта, пропагандирующих наращивание мышц, применяются специальные биологически активные добавки к пище (БАДы), содержащие креатин. В результате их применении стимулируется увеличение количества запасенного креатинфосфата в мышцах, который фактически является запасом энергии, поэтому у спортсменов повышается силовая выносливость.
Запасы креатинфосфата в мышцах можно увеличить и без БАДов. Количество его нарастает, когда организм постепенно адаптируется к нарастающим физическим нагрузкам. Таким образом количество креатинфосфата можно увеличить почти в два раза.
Процесс превращения креатинфосфата в АТФ резко повышает силовую выносливость при кратковременных физических нагрузках высокой интенсивности, например, при беге и плавании на короткие дистанции, прыжках, упражнениях с отягощением.
Выпускаются разные БАДы, содержащие креатин, но самым популярным является креатина моногидрат. Вполне естественно, что производители таких БАДов не указывают, кому можно, а кому нельзя их принимать, ведь это не лекарства и они не проходили соответствующие, предусмотренные для лекарств лабораторные и клинические исследования.
Поэтому прежде чем принимать БАДы с креатином, нужно пройти обследование, убедиться в том, что почки в состоянии выдержать дополнительную нагрузку. А еще лучше не принимать никакого спортивного питания, ведь не даром все виды допинга в спорте запрещены. А креатин — это допинг, так как увеличивает количество энергии.
Галина Романенко
www.luxemag.ru
Проба Реберга (клиренс эндогенного креатинина)
Определение клиренса эндогенного креатинина – исследование, применяемое для оценки уровня клубочковой фильтрации.
Синонимы русские
Скорость клубочковой фильтрации.
Синонимы английские
Test of renal function, creatinine clearance test, Rehberg test.
Метод исследования
Кинетический метод (метод Яффе).
Единицы измерения
Мкмоль/л (микромоль на литр), ммоль/сут. (миллимоль в сутки), мл (миллилитр), мл/мин. (миллилитр в минуту), % (проценты).
Какой биоматериал можно использовать для исследования?
Венозную кровь, суточную мочу.
Как правильно подготовиться к исследованию?
- Исключить из рациона алкоголь за 24 часа до анализа.
- Не принимать пищу в течение 12 часов до анализа.
- Не принимать мочегонные препараты в течение 48 часов до сбора мочи (по согласованию с врачом).
- Исключить физическое и эмоциональное перенапряжение за 24 часа до анализа.
- Не курить в течение 30 минут до анализа.
Общая информация об исследовании
Вся кровь человека сотни раз в день проходит через почки. Они пропускают жидкую часть крови через крохотные фильтры (нефроны), затем большая часть жидкости реабсорбируется обратно в кровь. Жидкие отходы, которые не реабсорбируются почками, удаляются из организма с мочой.
Креатинин (от греческого kreas – «плоть») – продукт распада креатинфосфата в мышечной ткани. Количество его в организме достаточно постоянно и зависит от мышечной массы человека. По химической структуре он является циклическим производным креатина.
Креатинин фильтруется из крови почками, и небольшое его количество активно выделяется с мочой. Канальцевая реабсорбция креатинина минимальна. Если фильтрующая способность почек недостаточна, то уровень креатинина в крови увеличивается. Зная уровни креатинина в моче и крови, можно вычислить клиренс креатинина, который отражает уровень клубочковой фильтрации. Клиренс креатинина (от англ. clearance – «очищение», т. е. очищение от креатинина, его выведение) – количество крови, которое почки могут очистить от креатинина за одну минуту. У здорового молодого человека он составляет около 125 мл в минуту, это значит, что его почки каждую минуту очищают от креатинина 125 мл крови.
Уровень клубочковой фильтрации – сумма уровней фильтрации во всех функционирующих нефронах. Этот показатель позволяет определить количество этих нефронов в почках. Он имеет важное клиническое значение, поскольку является основной характеристикой функции почек.
В случаях тяжелого нарушения функции почек клиренс креатинина повышается, поскольку при активной секреции креатинина выделяется его более крупная фракция.
Кетоновые кислоты, циметидин и триметоприм ограничивают канальцевую секрецию креатинина и снижают точность определения клубочковой фильтрации, особенно при тяжелой почечной недостаточности.
Клиренс креатинина можно определить двумя способами: измерением количества креатинина в крови человека и суточной моче. На практике чаще применяется анализ крови, поскольку это исследование удобнее для пациента.
Если у пациента низкий уровень клубочковой фильтрации, то лечащий врач разработает программу дополнительного обследования для выяснения причины этого патологического состояния. Основными причинами хронических болезней почек являются артериальная гипертония и сахарный диабет. Если они не выявлены, то необходимо дальнейшее обследование для выяснения причины заболевания почек.
Систематическое определение клиренса креатинина позволяет доктору следить за изменением функции почек пациента в динамике и корректировать медикаментозную терапию в зависимости от полученных данных.
Для чего используется исследование?
- Для оценки функции почек;
- для оценки динамики течения почечных заболеваний;
- для оценки функции почек у пациентов, принимающих нефротоксичные препараты;
- для выявления тяжелой дегидратации
Когда назначается исследование?
При выявлении у пациента болей в области почек, отеков вокруг глаз и на лодыжках, гипертонической болезни, пониженного количества мочи или проблем с мочеиспусканием, темной мочи, примеси крови в моче, синдрома Альпорта, амилоидоза, хронической почечной недостаточности, синдрома Кушинга, дерматомиозита, сахарного диабета, интоксикации сердечными гликозидами, генерализованных приступов тонико-клонических судорог, синдрома Гудпасчера, гемолитического уремического синдрома, гепаторенального синдрома, интерстициального нефрита, волчаночного нефрита, злокачественной артериальной гипертензии, мембранопролиферативного гломерулонефрита, тромбоцитопенической пурпуры, опухоли Вильмса (всё вышеперечисленное – факторы, оказывающие влияние на работу почек).
Что означают результаты?
Референсные значения
Креатинин в крови
| Пол | Возраст | Референсные значения |
| Мужской | Меньше 5 дней | 27 — 88 мкмоль/л |
| 5 дней – 1 месяц | 27 — 88 мкмоль/л | |
| 1 месяц – 1 год | 18 — 35 мкмоль/л | |
| 1-2 года | 27 — 62 мкмоль/л | |
| 2-12 лет | 27 — 62 мкмоль/л | |
| 12-17 лет | 44 — 88 мкмоль/л | |
| 17-51 год | 74 — 110 мкмоль/л | |
| Больше 51 года | 72 — 127 мкмоль/л | |
| Женский | Меньше 5 дней | 27 — 88 мкмоль/л |
| 5 дней – 1 месяц | 27 — 88 мкмоль/л | |
| 1 месяц – 1 год | 18 — 35 мкмоль/л | |
| 1-2 года | 27 — 62 мкмоль/л | |
| 2-12 лет | 27 — 62 мкмоль/л | |
| 12-17 лет | 44 — 88 мкмоль/л | |
| Больше 17 лет | 58 — 96 мкмоль/л |
Креатинин в моче
- Для женщин: 5,3 — 16 ммоль/сут.
- Для мужчин: 7 — 18 ммоль/сут.
Минутный диурез (моча)
| Возраст | Референсные значения |
| Меньше 2 дней | 30 — 60 мл |
| 3-10 дней | 1 — 300 мл |
| 11 дней – 2 месяца | 250 — 450 мл |
| 2 месяца – 1 год | 400 — 500 мл |
| 1-3 года | 500 — 600 мл |
| 4-5 лет | 600 — 700 мл |
| 6-8 лет | 650 — 1000 мл |
| 9-14 лет | 800 — 1400 мл |
| 15-60 лет | 600 — 1800 мл |
| Больше 61 года | 250 — 2400 мл |
Клубочковая фильтрация (моча)
- Для женщин: 75 — 115 мл/мин.
- Для мужчин: 95 — 145 мл/мин.
Канальцевая реабсорбция: 95-99 %.
Причины пониженного клиренса креатинина:
- острая почечная недостаточность,
- блок оттока мочи на уровне выходного отверстия мочевого пузыря,
- застойная сердечная недостаточность,
- дегидратация,
- хроническая почечная недостаточность,
- гломерулонефрит,
- шок,
- блок почек.
Причины повышенного клиренса креатинина:
- беременность,
- сахарный диабет, до развития диабетической нефропатии;
- большое количество белка в рационе.
Что может влиять на результат?
- Клиренс креатинина может увеличиваться при интенсивной физической нагрузке, предшествовавшей исследованию.
- Некоторые лекарственные препараты способствуют снижению клиренса креатинина (циметидин, триметаприм, прокаинамид, цефалоспорины, аминогликозиды и хинидин).
Важные замечания
- Клиренс креатинина снижается с возрастом (на 6,5 мл/мин. каждые 10 лет у людей старше 40 лет).
- Кетоновые кислоты, циметидин и триметоприм ограничивают канальцевую секрецию креатинина и снижают точность определения клубочковой фильтрации, особенно при тяжелой почечной недостаточности.
- Одним из основных ограничений использования результатов определения клиренса креатинина по суточному количеству мочи являются ошибочные результаты из-за неполного сбора мочи.
Также рекомендуется
- Клинический и биохимический анализ крови — основные показатели
- Креатинин в сыворотке
- Креатинин в суточной моче
- Мочевина в сыворотке
- Мочевина в суточной моче
Кто назначает исследование?
Врач общей практики, терапевт, нефролог, уролог.
Литература
- Post TW, Rose BD: Assessment of renal function: plasma creatinine; BUN; and GFR. In UpTo Date 9.1. Edited by BD Rose. 2001
- Kasiske BL, Keane WF: Laboratory assessment of renal disease: clearance, urinalysis, and renal biopsy. In The Kidney. Sixth edition. Edited by BM Brenner. Philadelphia, WB Saunders Company, 2000, pp 1129-1170
- Landry DW, Bazari H. Approach to the patient with renal disease. In: Goldman L, Schafer AI, eds. Cecil Medicine. 24th ed. Philadelphia, Pa: Saunders Elsevier
lekafarm.ru
Клиренс эндогенного креатинина (проба реберга-тареева)
Проба Реберга-Тареева позволяет судить о клубочковой фильтрации и канальцевой реабсорбции в почках. Проба основана на том, что креатинин фильтруется только клубочками, практически не всасывается и секре-тируется канальцами в незначительном количестве. Порядок проведения пробы следующий: больной утром мочится, выпивает 200 мл воды и затем натощак в состоянии полного покоя собирает мочу за точно определённое непродолжительное время (2 ч). Посередине этого периода времени берут кровь из вены. Определяют концентрацию креатинина в крови и моче, собранной за 2 ч. Рассчитывают коэффициент очищения (Коч) или клиренс эндогенного креатинина: Коч = (М/Пл.)хД (мл/мин), где М — концентрация креатинина в моче; Пл. — концентрация креатинина в плазме; Д — минутный диурез в мл/мин [равен количеству мочи, выделенной за 2 ч (мл), делённому на 120 мин). Коч выражает СКФ. Для определения СКФ можно исследовать мочу, собранную за сутки.
В норме СКФ составляет 120+25 мл/мин у мужчин и 95+20 мл/мин у женщин. Величины СКФ наиболее низки утром, повышаются до максимальных величин в дневные часы, и затем вновь снижаются вечером. У здоровых людей снижение СКФ происходит под влиянием тяжёлой физической нагрузки и отрицательных эмоций; возрастает после питья жидкости и приёма высококалорийной пищи.
СКФ — чувствительный показатель функционального состояния почек, её снижение считают одним из ранних симптомов нарушения функции почек. Уменьшение СКФ, как правило, наступает значительно раньше, чем снижение концентрационной функции почек и накопление в крови азотистых шлаков. При первичных клубочковых поражениях недостаточность концентрационной функции почек выявляют при резком снижении СКФ (приблизительно на 40-50%). При хронических пиелонефритах поражается преимущественно дистальный отдел канальцев, и фильтрация уменьшается позднее, чем концентрационная функция канальцев. Нарушение концентрационной функции почек и иногда даже незначительное повышение содержания в крови азотистых шлаков у больных с хроническим пиелонефритом возможно при отсутствии снижения СКФ.
На СКФ оказывают влияние экстраренальные факторы. Так, СКФ снижается при сердечной и сосудистой недостаточности, обильной диарее и рвоте, гипотиреозе, механическом затруднении оттока мочи (опухоли предстательной железы), поражении печени. В начальной стадии острого гломерулонефрита снижение СКФ происходит не только вследствие нарушения проходимости клубочковой мембраны, но и в результате расстройств гемодинамики. При хроническом гломерулонефрите снижение СКФ может быть обусловлено азотемической рвотой и диареей.
Стойкое падение СКФ до 40 мл/мин при хронической почечной патологии указывает на выраженную почечную недостаточность, падение до 15-5 мл/мин — на развитие терминальной ХПН (табл.).
Некоторые ЛС (например, циметидин, триметоприм) снижают тубуляр-ную секрецию креатинина, способствуя повышению его концентрации в сыворотке крови. Антибиотики группы цефалоспоринов, вследствие интерференции, приводят к ложноповышенным результатам определения концентрации креатинина.
Таблица Лабораторные критерии стадий ХПН
Повышение СКФ наблюдают при хроническом гломерулонефрите с нефротическим синдромом, в ранней стадии гипертонической болезни. Следует помнить, что при нефротическом синдроме величина клиренса эндогеного креатинина не всегда соответствует истинному состоянию СКФ. Это связано с тем, что при нефротическом синдроме креатинин выделяется не только клубочками, но и секретируется изменённым канальцевым эпителием, и поэтому Коч эндогенного креатинина может до 30% превышать истинный объём клубочкового фильтрата.
На величину клиренса эндогенного креатинина оказывает влияние секреция креатинина клетками канальцев почек, поэтому его клиренс может значительно превышать истинную величину СКФ, особенно у пациентов с заболеваниями почек. Для получения точных результатов чрезвычайно важно полностью собрать мочу за точно установленный промежуток времени, неправильный сбор мочи приведёт к ложным результатам.
В ряде случаев для повышения точности определения клиренса эндогенного креатинина назначают антагонисты Н2-гистаминовых рецепторов (обычно циметидин в дозе 1200 мг за 2 ч до начала сбора суточной мочи), которые блокируют тубулярную секрецию креатинина. Клиренс эндогенного креатинина, измеренный после приёма циметидина, практически равен истинной СКФ (даже у пациентов с умеренной и тяжёлой почечной недостаточностью).
Клиренс эндогенного креатинина быстро можно рассчитать по номограмме, приведённой на Рис. [Appel G.B., Neu H.C., 1977]. Для этого необходимо знать массу тела больного (кг), возраст (лет) и концентрацию креатинина в сыворотке крови (мг%). Первоначально прямой линией соединяют возраст пациента и его массу тела и отмечают точку на линии А. Затем отмечают концентрацию креатинина в сыворотке крови на шкале и соединяют её прямой линией с точкой на линии А, продолжая её до пересечения со шкалой клиренса эндогенного креатинина. Точка пересечения прямой линии со шкалой клиренса эндогенного креатинина соответствует СКФ.
Канальцевая реабсорбция. Канальцевую реабсорцию (КР) рассчитывают по разнице между клубочковой фильтрацией и минутным диурезом (Д) и вычисляют в процентах к клубочковой фильтрации по формуле: КР = [(СКФ-Д)/СКФ]х100. В норме канальцевая реабсорбция колеблется от 95 до 99% клубочкового фильтрата.
Канальциевая реабсорбция может значительно меняться в физиологических условиях, снижаясь до 90% при водной нагрузке. Выраженное снижение реабсорбции происходит при форсированном диурезе, вызванном мочегонными средствами. Наибольшее снижение канальцевой реабсорбции наблюдают у больных несахарным диабетом. Стойкое уменьшение реабсорбции воды ниже 97-95% наблюдают при первично и вторично сморщенной почке и хронических пиелонефритах. Реабсорбция воды может также уменьшаться при острых пиелонефритах. При пиелонефритах реабсорбция снижается раньше уменьшения СКФ. При гломерулонефритах реабсорбция снижается позднее, чем СКФ. Обычно одновременно со снижением реабсорбции воды выявляют недостаточность концентрационной функции почек. В связи с этим понижение реабсорбции воды в функциональной диагностике почек большого клинического значения не имеет.
Повышение канальцевой реабсорбции возможно при нефритах, нефротическом синдроме.
Обновлено: 2019-07-09 21:44:13
medn.ru
СКФ по методу Cockroft-Gault
Срок исполнения
Анализ будет готов в течение 1 дня (кроме дня взятия биоматериала). Вы получите результаты на эл. почту сразу по готовности.
Срок исполнения: 2 дня, исключая субботу и воскресенье (кроме дня взятия биоматериала)Подготовка к анализу
ЗаранееНе сдавайте анализ крови сразу после рентгенографии, флюорографии, УЗИ, физиопроцедур.
ВАЖНО: Уровень показателя в крови может значительно изменяться в течении суток, поэтому для сдачи анализа выберите интервал с 8.00 до 10.00.
Для проверки динамики показателя каждый раз выбирайте одинаковые интервалы сдачи анализа.
НаканунеЗа 24 часа до взятия крови:
Ограничьте жирную и жареную пищу, не принимайте алкоголь.
Исключите тяжёлые физические нагрузки.
От 8 до 14 часов до сдачи крови не принимайте пищу, пейте только чистую негазированную воду.
В день сдачи60 минут до забора крови не курить.
15-30 минут перед забором крови находиться в спокойном состоянии.
Информация об анализе
Расчётный, СКФ рассчитывается по концентрации креатинина в сыворотке крови, с учётом пола и веса пациента. Для оценки функции почек в лабораторной диагностике используют определение креатинина в сыворотке крови и рассчитывают скорость клубочковой фильтрации (СКФ). СКФ является наиболее точным показателем, который отражает функциональное состояние почек. С помощью данной формулы можно выявить незначительные нарушения функции почек даже при нормальном уровне креатинина.
Метод исследования — Расчётный, СКФ рассчитывается по концентрации креатинина в сыворотке крови, с учётом пола и веса пациента.
Материал для исследования — Сыворотка крови
Состав и результаты
СКФ по методу Cockroft-Gault
Для оценки функции почек в лабораторной диагностике используют определение креатинина в сыворотке крови и рассчитывают скорость клубочковой фильтрации (СКФ). Анализ концентрации содержания креатинина в сыворотке методом лабораторного исследования является обязательным. Определение концентрации содержания креатинина в сыворотке не является достаточным для оценки функции почек из-за зависимости от ряда факторов. Концентрация креатинина в сыворотке крови зависит от секреции, продукции и внепочечной экскреции креатинина. Образование креатинина, циркулирующего в крови, происходит в мышечной ткани. Средняя скорость образования креатинина также зависит от некоторых факторов. Так, например, средняя скорость образования креатинина выше у молодых лиц, мужчин и у лиц негроидной расы. В зависимости от возраста, пола и расы наблюдаются различия в концентрациях креатинина в сыворотке крови.
Образование креатинина снижается из-за мышечного истощения, что может приводить к понижению концентрации креатинина в сыворотке, чем можно было бы ожидать по уровню скорости клубочковой фильтрации у пациентов с белково-энергетической недостаточностью при хронической почечной недостаточности (ХПН). Употребление мяса влияет на образование креатинина, так как в процессе готовки мясных продуктов часть креатина переходит в креатинин. Из этого следует, что у пациентов, придерживающихся вегетарианских взглядов, а именно находящихся на низкобелковой диете, креатинин сыворотки крови ниже, чем можно было бы ожидать, исходя из уровня СКФ (Johnson C.A., et al.,2004).
Креатинин довольно свободно фильтруется в клубочках, также как и секретируется в проксимальных канальцах почек. Из этого следует, что количество креатинина, экскретированного в мочу, является суммой секретированного и профильтрованного креатинина. Клиренс креатинина (кКр) периодически завышает скорость клубочковой фильтрации, другими словами, величина кКр всегда выше СКФ. У здоровых лиц эти различия могут составлять от ~ 10% до ~ 40%, но больше и наиболее непредсказуемы различия у пациентов с хроническими заболеваниями почек. Некоторые распространенные лекарственные препараты, например, циметидин и триметоприм, ингибируют секрецию креатинина. У лиц с нормальной функцией почек внепочечная экскреция креатинина минимальна. И, напротив, у пациентов с хроническими заболеваниями почек внепочечная экскреция креатинина увеличивается. У больных с тяжелым снижением функции почек до двух третей общей суточной экскреции креатинина может происходить за счет его внепочечной элиминации.
Возможны значительные колебания СКФ при нормальном сывороточном креатинине, особенно у пожилых людей. По мере старения организма уменьшаются и мышечная масса, и клиренс креатинина (кКр), хотя при этом сывороточный уровень может оставаться неизменным, что, впрочем, не означает неизменную функцию. Таким образом, повышенный креатинин сыворотки не является чувствительным показателем сниженной СКФ. Креатинин сыворотки повышен только у 60% больных со сниженной СКФ. Другими словами, 40% лиц со сниженной скоростью клубочковой фильтрации имеют уровень креатинина в сыворотке крови в пределах нормы.
СКФ является наиболее точным показателем, который отражает функциональное состояние почек. Скорость клубочковой фильтрации может измеряться с применением экзогенных и эндогенных (инулин) маркеров фильтрации и рассчитываться по формулам, основанным на сывороточном уровне эндогенных маркеров (цистатин С, креатинин) или клиренсу эндогенных маркеров фильтрации (креатинина). Золотым стандартом измерения СКФ является клиренс инулина, который в стабильной концентрации присутствует в плазме, свободно фильтруется в клубочках, физиологически инертен, не секретируется, не синтезируется, не реабсорбируется, не метаболизируется в почках. Определение клиренса инулина, ровно как и клиренса экзогенных радиоактивных меток (99mTc-DTPA и 125I-иоталамата) труднодоступно и дорогостоящие в рутинной практике (Snyder S., et al., 2005).
В связи с этим разработан ряд альтернативных методов оценки скорости клубочковой фильтрации:
Проба Реберга-Тареева, которая помогает измерить 24-часовой клиренс креатинина. Для пробы Реберга-Тареева необходимо собрать мочу за определенный промежуток времени (24 часа), что часто обременительно для пациента и сопровождается ошибками. Данный метод оценки скорости клубочковой фильтрации не имеет преимуществ, в сравнении с расчетами по формулам. В то же время проба Реберга-Тареева для определения СКФ пригодится людям с отклонениями в мышечной массе или необычной диетой, так как эти факторы не принимались во внимание при разработке формул.
В ряде случаев, если уровень СКФ быстро меняется, то результаты могут быть ненадежными, т.к. анализ креатинина в сыворотке крови для оценки СКФ предполагает стабильное состояние пациента:
- при острой почечной недостаточности (ОПН),
- если мышечная масса необычно мала или велика — у истощенных лиц или атлетов,
- если потребление креатина с пищей необычно мало или велико — у вегетарианцев или у людей, употребляющих пищевые добавки с креатином.
Таким образом, проба Реберга-Тареева может дать лучшую оценку скорости клубочковой фильтрации, чем расчетные методы в следующих клинических ситуациях:
- беременность,
- младенческий или пожилой возраст,
- тяжелая белково-энергетическая недостаточность,
- очень маленькие или очень большие размеры тела,
- параплегия и тетраплегия,
- заболевания скелетных мышц,
- быстро меняющаяся функция почек,
- вегетарианская диета.
Расчетные методы оценки СКФ и кКр. Формулы для расчета скорости клубочковой фильтрации учитывают различные влияния на продукцию креатинина, они валидированы (их значения довольно точно совпадают со значениями эталонных методов оценки СКФ) и просты в применении. Для взрослых (старше 18 лет) наиболее широко применяется формула Cockroft-Gault и формула, полученная в исследовании MDRD (Modification of Diet in Renal Disease Study).
Формула Cockroft-Gault была разработана для оценки кКр, а не для СКФ. кКр всегда выше СКФ; следовательно, формулы, оценивающие кКр, могут недооценивать истинное состояние СКФ. Формула разработана в группе мужчин, для женщин предложен корректирующий коэффициент. В исследовании MDRD, крупнейшем исследовании, оценившем формулу Cockroft-Gault, в одной лаборатории, она завышала СКФ на 23%. Кроме того, формула Cockroft-Gault завышает кКр при уровне СКФ 60 мл/мин (Marx G.M., et al., 2004).
Таким образом, с помощью данной формулы можно выявить незначительные нарушения функции почек даже при нормальном уровне креатинина. Среди недостатков формулы можно выделить ее неточность при нормальных или незначительно сниженных значениях СКФ.
lab4u.ru