причины, симптомы и прогноз на выживаемость
Диффузная В крупноклеточная лимфома (ДВКЛ) — это группа опухолей лимфатической системы, в основе которой лежит трансформация В-лимфоцитов в злокачественные клетки.
Причины возникновения и группы риска
Причиной возникновения ДВКЛ является изменение В-лимфоцитов, т. е. нарушение структуры ДНК. Из-за этого клетки начинают бесконтрольно расти и размножаться, рассеиваясь по всему организму и поражая различные органы и системы. Почему возникают эти мутации, достоверно не установлено. Более того, есть много людей, у которых обнаруживаются характерные генетические поломки, но нет лимфомы. Данный вопрос продолжает изучаться.
В настоящее время принято говорить о факторах риска, которые повышают вероятность развития данного заболевания:
- Врожденные и приобретенные иммунодефициты: синдром Вискотта-Олдрича, Луи-Бара, СПИД, необходимость лечения, которое снижает иммунитет: цитостатики, иммуносупрессоры при трансплантации органов и др.
- Вирусные инфекции: ВИЧ, гепатит С, Т-лимфотропный вирус.
- Аутоиммунные заболевания: ревматоидный артрит, волчанка и др.
- Токсическое воздействие инсектицидов, гербицидов, бензола.
- Лечение посредством цитостатической и лучевой терапии.
Симптомы диффузной крупноклеточной В лимфомы
Крупноклеточная лимфома может проявляться множеством симптомов, но все их многообразие можно уложить в три синдрома:
- Увеличение лимфатических узлов — лимфаденопатия. Чаще всего, лимфома манифестирует безболезненным увеличением лимфатических узлов, которые можно обнаружить визуально или при пальпации. Но бывает так, что поражаются узлы, недоступные для осмотра и пальпации (например, в грудной или брюшной полости), тогда этого признака сразу может и не быть.
- Симптомы интоксикации: повышение температуры, не связанное с инфекцией, сильная потливость, потеря веса. Комбинацию этих признаков называют В-симптоматикой. Ее наличие имеет значение при определении стадии заболевания.
- Симптомы, которые развиваются, когда крупноклеточная лимфома переходит на другие органы и системы. Это могут быть боли в груди и кашель, боли в животе и нарушение стула. При поражении ЦНС развиваются головные боли, нарушение зрения и рвота. Из-за разрушения костного мозга снижается иммунитет, развивается анемия и склонность к опасным кровотечениям.
Классификация, формы и стадии диффузной лимфомы
Современная классификация крупноклеточной лимфомы базируется на клинических данных и степени распространенности опухолевого процесса.
Классификация Ann Arbor:
- 1 стадия. Поражение ограничено одной лимфатической зоной или одним экстралимфатическим органом или одним сегментом экстралимфатической ткани.
- 2 стадия. Поражено две и более зоны лимфатических узлов по одну сторону диафрагмы. При поражении внелимфатических органов или тканей обнаруживаются метастазы в регионарные лимфатические узлы.
- 3 стадия. Имеются единичные очаги поражения по обе стороны диафрагмы.
- 4 стадия. Имеются множественные очаги поражения экстралимфатических органов, либо ограниченное поражение экстралимфатических органов с отдаленными метастазами, либо поражение печени и костного мозга.
Классификация Ann Arbor дополняется модификацией Cotswold:
- А — нет В-симптомов.
- В — есть хотя бы один из В-симптомов.
- Е — есть локализованные экстранодальные очаги.
- S — лимфома поразила селезенку.
- X — имеется массивное опухолевое тканей и внутренних органов.
Диагностика диффузной крупноклеточной лимфомы
Диагноз неходжкинская лимфома выставляется на основании гистологического и иммуногистохимического исследования опухолевой ткани. Для того чтобы получить материал, проводят инцизионную или эксцизионную биопсию лимфатических узлов. Помимо этого, выполняют молекулярно-генетические и иммунофенотипические исследования, которые позволят определить вид опухоли, наличие тех или иных генетических изменений и подобрать оптимальный метод лечения.
Для определения стадии лимфомы проводят следующие исследования:
- Трепанобиопсия костного мозга.
- Методы лучевой диагностики — УЗИ, КТ, ПЭТ-КТ, МРТ.
- Также назначается ряд лабораторных анализов — развернутый анализ крови, определение маркеров парентеральных гепатитов, анализ на ВИЧ, биохимические исследования и др.
Лечение диффузной В-крупноклеточной лимфомы
Лечение диффузной лимфомы определяется исходя из следующих данных:
- Риски рецидива согласно IPI.
- Возраст пациента.
- Его состояние (сможет ли больной перенести высокодозную полихимиотерапию).
В качестве основных методов лечения крупноклеточной лимфомы применяется химиотерапия и в некоторых случаях облучение. Перед началом терапии фертильных пациентов обсуждается вопрос о криоконсервации гамет (половых клеток), поскольку лечение может вызвать бесплодие.

Главным критерием подбора терапии является международный прогностический индекс IPI, который включает следующие аспекты:
- Возраст. Младше 60 лет — 0 баллов, старше — 1 балл.
- Состояние пациента по ECOG (активность больного и способность к самообслуживанию). 1-2 балла по ECOG это 0 по IPI, и 3-4 балла по ECOG — это 1 балл по IPI.
- Уровень ЛДГ. В норме — 0 баллов по IPI, повышен — 1 балл.
- Стадия лимфомы. 1-2 — 0 баллов, 3-4 — 1 балл.
- Наличие более 1 экстранодальной зоны поражения. Нет — 0, да — 1.
Интерпретация IPI следующая:
- 0-1 балл — лимфома низкого риска.
- 2 балла — лимфома промежуточно низкого риска.
- 3 балла — лимфома промежуточно высокого риска.
- 4-5 баллов — лимфома высокого риска.
Пациенты из группы низкого и промежуточно-низкого риска начинают свое лечение с 6 циклов иммунохимиотерапии по протоколу R-CHOP-21. Эта схема, помимо цитостатиков, предполагает применение иммунотерапевтического препарата ритуксимаба. Такая схема позволяет добиться пятилетней выживаемости у 80% больных. Для пациентов с 3-4 стадией заболевания, лечение дополняется лучевой терапией на зоны массивного и экстранодального опухолевого поражения.
Лечение пациентов из групп промежуточно-высокого и высокого риска подбирается индивидуально с учетом возраста и состояния больного по шкале ECOG. Молодым пациентам с хорошим соматическим состоянием назначаются более агрессивные схемы лечения, предполагающие проведение высокодозной химиотерапии с трансплантацией гемопоэтических стволовых клеток (ГСК). При высоких рисках поражения нервной системы проводится несколько циклов интратекальной химиотерапии, когда препараты вводят в спинномозговой канал. Пожилым и слабым пациентам подбираются более щадящие схемы. Оценка эффективности лечения производится в середине циклов химиотерапии и после их окончания.
Восстановление после лечения крупноклеточной неходжкинской лимфомы
В целом, после того как у пациента диагностировали ремиссию, он должен регулярно наблюдаться у онколога. Сначала раз в три месяца, потом раз в полгода, а потом ежегодно. Если через пять лет после достижения ремиссии, у пациента нет признаков заболевания, его считают выздоровевшим и снимают с учета.
Рецидивы крупноклеточной лимфомы
При лечении диффузной В-крупноклеточной лимфомы долгосрочной ремиссии удается достичь в 70-80 % случаев, но у ряда пациентов возникает рецидив. Лечение рецидивов проводится по следующей схеме:
- Химиотерапия второй линии. Она должна подавить опухолевый рост, в то же время не нанося ущерба гемопоэтическим стволовым клеткам.
- Сбор ГСК.
- Высокодозная химиотерапия. Используются высокие дозы цитостатиков, которые уничтожают самые стойкие опухолевые клетки, но они же губят и кроветворение, поэтому чтобы его восстановить проводят следующий этап.
- Трансплантация гемопоэтических стволовых клеток, которая призвана восстановить кроветворение.
У пациентов из групп высокого риска, которые уже прошли аутологичную трансплантацию, и получили рецидив диффузной лимфомы, проводят аллогенную трансплантацию, т. е. используют стволовые клетки доноров. В этих случаях также есть шансы на полную ремиссию, но они не превышают 50%.
Осложнения диффузной В крупноклеточной лимфомы
Химиотерапия и лучевая терапия диффузной крупноклеточной лимфомы пагубно влияют не только на злокачественную опухоль, но и на все быстро делящиеся клетки. Это кроветворные клетки, эпителий кожи и слизистых оболочек и др. Поэтому в процессе лечения и восстановления большое внимание уделяется профилактике осложнений. В первую очередь, это борьба с инфекциями (бактериальными, вирусными, грибковыми), нарушением кровесвертывающей системы и работы пищеварительного тракта.
Помимо этого, в долгосрочной перспективе есть риск развития следующих осложнений:
- Возникновение других злокачественных опухолей: рак легкого, молочной железы, желудка, а также лейкозов и других видов лимфом. Наибольшие риски отмечаются в первые десятилетия после прекращения лечения.
- Кардиоваскулярные осложнения: нарушение работы миокарда, быстрый атеросклероз кровеносных сосудов, повреждение клапанов сердца и др.
- Поражение легких: пульмониты, пневмосклероз и пневмофиброз.
- Осложнение со стороны эндокринной системы: гипотиреоз, бесплодие, нарушение сперматогенеза.
Прогноз и профилактика крупноклеточной лимфомы
Прогноз течения диффузной В крупноклеточной лимфомы зависит от показателя IPI. Чем больше баллов, тем хуже прогноз. Для больных, имеющих 4-5 баллов (высокий риск), пятилетняя выживаемость колеблется в пределах 31%. При низких рисках пятилетняя выживаемость составляет около 91%.
Что касается специфической профилактики, то ее на сегодняшний день не существует, а все рекомендации для минимизации риска заболевания сводятся к ведению здорового образа жизни и правильному питанию.
Запись на консультацию круглосуточно
www.euroonco.ru
Диффузная В — крупноклеточная лимфома: прогноз
Лимфоидные новообразования образуются в связи со злокачественной трансформацией В-лимфоцитов в различных стадиях дифференцировки клеток. Поэтому В-клеточные опухоли лимфоидной системы наделены широким спектром гетерогенности.
Диффузная лимфома – самая распространенная неходжкинская лимфома. При выработке организмом аномальных В-лимфоцитов начинает развиваться эта опухоль. Лимфоциты В-клеточные в виде белых кровяных клеток предназначены для борьбы с инфекцией. Иногда опухолевые клетки оккупируют части тела, не состоящие из лимфоидной ткани. Тогда новообразования называются экстранодальными опухолями. Они быстро растут, не болят и находятся на шее, в паху или под мышками.
Развитие и проявление диффузной В-крупноклеточной лимфомы
Позднее опухоль проявляется дискомфортом:
- усталостью;
- ночной потливостью;
- высокой температурой;
- быстрой потерей веса.
Диффузная крупноклеточная В-клеточная лимфома (ДКВЛ) является гетерогенным заболеванием, что встречается у 40% всех НХЛ у взрослого населения.
Диффузные лимфомы наделены гетерогенностью: клинической, морфологической, цитогенетической и иммунофенотипической. В Классификации ВОЗ диффузные лимфомы находятся в отдельной клинико-морфологической категории, и они имеют свои особенности строения и клинического течения.
Информативное видео
Классификация диффузных лимфом
Классификация лимфом включает диффузные лимфомы, к которым относятся:
- диффузная крупноклеточная В-клеточная лимфома;
- диффузная мелкоклеточная лимфома;
- мелкоклеточная диффузная лимфома с расщепленными ядрами;
- смешанная (лимфома диффузная крупноклеточная и мелкоклеточная диффузная неходжкинская лимфома одновременно)
- ретикулосаркома;
- иммунобластная;
- лимфобластная;
- недифференцированная;
- лимфома Беркитта;
- неуточненные (неклассифицированные) типы диффузных лимфом:
- крупноклеточные лимфомы с промежуточными признаками ДКВЛ и лимфомы Беркитта;
- крупноклеточные лимфомы с промежуточными признаками ДКВЛ + лимфома Ходжкина.
Название «диффузная» лимфома получила в связи с тем, что при ней нарушается строение ЛУ. При распространении клеток по всей лимфатической системе происходит «диффузия». Новообразования образуются во всех группах ЛУ, либо в определенной зоне, где они растут и затем проявляются болевыми симптомами. Вначале опухоли можно прощупать в увеличенных лимфоузлах. Постепенно, даже при бессимптомных начальных стадиях, появляются «В-симптомы», по которым распознается онкология.
Диффузная крупноклеточная В-клеточная лимфома (ДКВЛ) разделена на подтипы:
- Первичная диффузная в крупноклеточная лимфома В-клеток средостения.
- Внутрисосудистая диффузная крупноклеточная неходжкинская лимфома.
- Лимфома с избытком гистиоцитов и Т-клеток.
- Кожно-первично-диффузная, с поражением кожи нижних конечностей.
- Диффузная b-крупноклеточная лимфома в сопровождении вируса Эпштейна-барра.
- Диффузная В-клеточная лимфома, возникающая на фоне воспаления.
Стадии ДКВЛ
Предполагаемого аналога диффузная b-клеточная крупноклеточная лимфома не имеет, поскольку его не смогли установить.
Диффузная неходжкинская лимфома из крупных В-клеток возникает de novo или развивается из зрелых клеток на фоне предшествующей лимфомы:
- из малых лимфоцитов/лимфолейкоза хронического;
- фолликулярной;
- из клеток зоны мантии.
Может трансформироваться и фолликулярная лимфома. Стадийность определяют в зависимости от степени поражения ЛУ и количества захваченных в процесс органов и тканей. При этом исследуются результаты КТ, МРТ, рентгена и иных методов диагностики.
Стадии диффузной крупноклеточной лимфомы:
- Стадия I – Поражены ЛУ одной группы на одной половине туловища.
- Стадия II – Поражены ЛУ двух и более групп над диафрагмой или ниже нее.
- Стадия III – Поражены лимфатические узлы с двух сторон диафрагмы.
- Стадия IV – Поражены внутренние органы за пределами ЛУ, онкоклетки обнаруживают в головном мозге, печени, костном мозге, легких.
Неходжкинская В-клеточная диффузная лимфома всегда растет быстро и агрессивно.
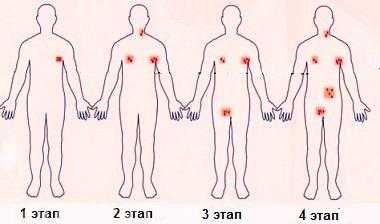
Этапы развития лимфом
Диффузная В — крупноклеточная лимфома, прогноз на выживание в течение 5 лет при адекватном своевременном лечении:
- благоприятный прогноз – у 95% пациентов;
- промежуточный прогноз – у 75% пациентов;
- неблагоприятный прогноз – у 60% пациентов.
Рецидивы происходят:
- на первый год жизни -80%;
- на второй год жизни – 5%.
Симптомы заболевания
Диффузная b клеточная лимфома средостения поражает людей в возрасте 25-40 лет, чаще страдают женщины. Опухоль проявляется кашлем, одышкой, дисфагией (нарушением глотания), отеком лица и шеи, болевыми симптомами и головокружением.
Все остальные подвиды В-крупноклеточной лимфомы проявляются аналогично, но у каждого пациента могут быть свои симптомы. Самый первый из них – увеличение ЛУ. Так организм пациента дает сигнал о появлении в ЛУ «клеток-чужаков».
Кроме этого:
- отекает печень или селезенка;
- вздувается живот;
- отекают конечности.
Неходжкинская крупноклеточная диффузная внутрисосудистая лимфома развивается с такими симптомами:
- онемением конечностей;
- слабостью;
- параличом лица, рук или ног;
- сильными головными болями;
- нарушением зрения;
- потерей равновесия;
- сильным похудением;
- появлением участков воспаленной кожи, их болезненностью.
Диагностика
За счет агрессивности диффузных лимфом диагноз ставят незамедлительно:
- первый этап – пациента осматривают, фиксируют жалобы;
- второй этап – исследуют анализы крови: клинический (выявляют уровень эритроцитов и лейкоцитов, тромбоцитов и скорость оседания эритроцитов — СОЭ) и биохимический (определяют уровень глюкозы, общих липидов, мочевины и прочих параметров)
- третий этап – исследуют материал биопсии;
- четвертый этап – проводят лучевую диагностику: КТ, МРТ и исследование рентгенограммы;
- пятый этап – проводят дополнительные исследования: иммуногистохимические, молекулярно-генетические и т.д.
Биопсия определяет состояние лимфоидной ткани, наличие в ней или отсутствие онкоклеток. Лучевая диагностика и дополнительные методы показывают локализацию лимфомы, стадию опухоли – подтверждается предварительный диагноз.
Лечение диффузной лимфомы
Лечение крупноклеточной диффузной лимфомы проводят с ограничением хирургического вмешательства. Чаще используются высокие дозы химиотерапии. Их вводят после трансплантации клеток костного мозга и стволовых клеток. Чтобы исключить осложнения пациентов госпитализируют.
Диффузная неходжкинская лимфома лечится химиотерапией и облучением, или комбинированными методами. За счет цитологического агента и дополнения облучения (или без него) получают высокий эффект от химии. Высокий лечебный эффект получают от удаления пораженного ЛУ. Операции помогают получить ткани для диагностики, но редко устраняют осложнения после лечения. Лечение диффузной b-крупноклеточной лимфомы кишечника выполняется приемлемым оперативным способом – хирургической резекцией.
Терапию проводят ведущими препаратами для химии – Ритуксимабом, Циклофосфамидом, Винкристином, Доксорубицином, Преднизолоном. Внутривенное введение препаратов способствует эффективному ответу организма на лечение. Отмечено, что пациенты, подвергавшиеся хирургической операции, а после получали химию, давали ответ на лечение более низкий, чем те, которых лечили химиопрепаратами и облучением.
Неходжкинская диффузная b-крупноклеточная лимфома эффективно лечится несколькими группами медицинских препаратов: антиметаболитами, иммуномодуляторами, антибиотиками, противоопухолевыми и противовирусными средствами.
Препаратами:
Из иммуностимуляторов чаще применяют Интерферон альфа. Пациентам с благоприятным прогнозом развития болезни (первой и второй степени) проводят лечение в два этапа по схеме ABVD препаратами: Блеомицин, Винбластин, Доксорубицин, Дакарбазин.
Пациентам с неблагоприятным прогнозом назначается интенсивная терапия:
- лечение по схемам АСОР или CHOP препаратами: Онковин, Циклофосфан, Доксорубицин;
- химиотерапия;
- лучевая терапия – уничтожают опухолевые клетки рентгеновскими лучами (на 1 и 2 стадиях). Доза – 40 Грэй. Лучи направляют непосредственно на пораженную область с целью уничтожения или повреждения клеток опухоли, сдерживания их роста.
Общепринятым стандартом, с помощью которого лечится диффузная крупноклеточная В-клеточная лимфома (4 стадия) является проведение шести курсов препарата Ритуксимаб. Длительность курса и комбинация препаратов меняется. Это зависит возраста и стабильности состояния пациентов, степени поражения.
Дополнительное лечение
- Рецидив-терапию проводят Ритуксимабом, Дексаметазоном, Цитарабином и Циспластином.
- Используют венозные устройства быстрого доступа пациентам, которым проводят много циклов химии. Их имплантируют для того, чтобы взять пробу на анализ или токсичность и сделать инъекцию.
- Пациента наблюдают каждые 3 недели даже при наличии временного улучшения.
От общего числа лимфом, 40% составляет диффузная крупноклеточная лимфома. Прогноз на выживание при данном заболевании составляет 40-50% пациентов.
Информативное видео
Будьте здоровы!
onkolog-24.ru
Диффузная В-крупноклеточная лимфома: прогноз и лечение
В онкологии крупноклеточная лимфома — злокачественная патология, возникающая в лимфатической системе, которая протекает в тяжелой форме с высокой агрессивностью. Крупноклеточные лимфомы могут развиваться как в лимфоузлах, так и в совокупности с тканями других органов. В 88% случаев развитие данной патологии происходит из B-лимфоцитов, в 10% случаев это могут быть T-лимфоциты, и только у 2% больных морфологический характер патологии остается неопознанным.
При распространении крупноклеточной лимфомы на костный мозг возникают сбои в синтезе тромбоцитов и эритроцитов, вследствие чего у пациентов снижаются показатели насыщенности кислородом и возникают спонтанные кровотечения. Местом локализации крупноклеточной лимфомы могут быть лимфатические узлы шейного отдела, брюшной полости, подмышечной области и внутренних органов. Лимфома данного типа относится к онкологическим заболеваниям с высоким показателем смертности, поэтому ее выявление должно быть максимально своевременным.

Причины
Современная наука в области онкологии пока не располагает точными знаниями о причинах того, почему может возникать лимфома крупноклеточная. Однако к наиболее вероятным факторам, которые могут спровоцировать крупноклеточную лимфому, относят:
- наследственность — передача атипичных генов возможна по родственной линии;
- иммунодефицитные болезни, например, ВИЧ-инфицирование или заболевания крови;
- наличие в организме других злокачественных образований;
- воздействие на организм ионизирующего излучения, постепенно вызывающего системные мутации на клеточном уровне;
- неблагоприятное экологическое окружение по месту жительства;
- профессиональная деятельность, предполагающая регулярный контакт с химическими и канцерогенными веществами.
Изначально патологический процесс возникает в лимфатических узлах, после чего выходит за пределы системы и распространяется по всему организму. Прогнозы при этом заболевании не однозначны, так как вероятность успешного излечения зависит от разных факторов.
Классификация
Диагностика и лечение онкологии может различаться в зависимости от вида патологии. Существует несколько типов крупноклеточных лимфом, к которым относятся:
- Диффузная лимфома;
- Анапластическая лимфома;
- Медиастинальная лимфома;
- Лимфосаркома;
- В-крупноклеточная.
Появление крупноклеточной лимфомы возможно в любом возрасте, при этом в первую очередь поражаются лимфатические узлы в области ЖКТ, брюшины и шеи. Развиваясь, лимфома распространяется на слюнные и щитовидную железы, а также в костный и головной мозг. По мере прогрессирования лимфомы, в патологический процесс вовлекаются почки, печень и легкие.
- Крупноклеточная диффузная лимфома относится к высокоагрессивным образованиям, способна поражать любую часть тела, при этом чаще ее выявляются в области лимфатических узлов шеи, паха и подмышек. К общим признакам неходжкинской лимфомы, как и других злокачественных новообразований, можно отнести сильное повышение температуры, стремительное похудение и усиленное потоотделение.
- С анапластической крупноклеточной лимфомой (АККЛ) могут столкнуться как мужчины, так и представительницы женского пола, преимущественно в возрасте от 40 до 60 лет. Выявить заболевание можно на начальных этапах, так как его развитие вызывает припухлость лимфоузлов и отечность кожи в области поражения. Во время пальпации пациенты могут жаловаться на болевой синдром. Обычной локализацией, как и в предыдущем случае, являются лимфатические узлы шеи, паха и подмышек.
- Медиастинальной называется лимфома, формирующаяся в медиастинальных лимфатических узлах (область средостения). Так как развивается данная опухоль рядом с такими важными органами как сердечная мышца, легкие и пищевод, течение данного заболевания несет серьезную угрозу. Прогноз для пациентов с данной патологией, в первую очередь, зависит от этапа развития на момент выявления.
- Одним из самых коварных видов онкологии является лимфосаркома, так как при возникновении болезни симптомы будут отсутствовать длительное время. Образуется аномалия из злокачественных клеток лимфоидных элементов. У каждого пятого пациента с данной патологией наблюдается развитие острого лейкоза. Прогноз выживаемости больных достаточно низкий даже при условии своевременного выявления. Только в 15% случаев возможно успешное излечение с длительной ремиссией.
- B-клеточные лимфомы также классифицируют как опухоли нехожкинского типа, бета-лимфоциты при этом являются первоисточником патологии. Главным отличием болезни является стремительное развитие с быстрым метастазированием. В группу повышенного риска попадают люди любого пола старшего возраста (от 40 до 60 лет).
Лечебные мероприятия напрямую зависят от разновидности онкопатологии.
Стадии
Чтобы выбрать наиболее оптимальный способ терапии, течение крупноклеточной лимфомы принято классифицировать на четыре стадии:
- Образование находится в пределах одного участка лимфоузлов;
- Раковое поражение захватывает две и более области лимфатических узлов;
- При наличии диффузной крупноклеточной лимфомы 3 степени можно наблюдать поражение узлов с обеих сторон диафрагмы;
- Патологический процесс на 4 этапе вовлекает находящиеся рядом органы и структуры.
Неходжкинские B-клеточные диффузные лимфомы всегда отличаются стремительным и агрессивным развитием, поэтому очень важно вовремя выявить заболевание, и как можно раньше начать адекватное лечение. Так как у людей, относящихся к группе 3-й стадии, имеется поражение лимфатических узлов по обеим сторонам диафрагмы, необходимо проводить клинические анализы регулярно, чтобы отслеживать дальнейшую динамику болезни.
Симптомы
Специфическая симптоматика крупноклеточных лимфом по большей мере зависит от их точного расположения. У больного при данной патологии возможны такие проявления:
- стремительное увеличение лимфоузлов;
- повышение температуры тела, особенно в ночное время суток;
- быстрая утомляемость и сонливость;
- усиленное потоотделение;
- быстрая и значительная потеря веса;
- нарушения в работе ЖКТ.

При наличии внутрисосудистой диффузной крупноклеточной b-клеточной лимфомы у больных наблюдаются такие признаки:
- паралич лица, конечностей;
- сильные головные боли;
- ухудшение зрения;
- потеря координации;
- появление воспаленных участков на теле.
Если поражена грудина или брюшная полость, появляется тяжесть в животе, затрудненное дыхание, частые болевые ощущения в области поясницы и может наблюдаться ректальное кровотечение.
На начальных этапах развития лимфомы клинические проявления часто отсутствуют, что в свою очередь становится причиной поздней диагностики.
Когда заболевание начинает поражать костные ткани, это значительно влияет на их функциональность и вызывает сильные боли. Появление сильной боли в области печени при данной болезни происходит у 80% пациентов, реже наблюдается поражение молочных и слюнных желез, надпочечников, глазниц и головного мозга. Так как аномалия может очень быстро развиваться, часто она приводит к смерти.
При первых признаках, независимо от их причины, необходимо немедленно пройти полное обследование.
Диагностика
При подозрении на развитие диффузной b-клеточной крупноклеточной лимфомы обязательно нужно провести ряд диагностических мероприятий. Оптимальные методы лечения рака могут быть назначены врачом только после постановки точного диагноза. В первую очередь доктор проводит внешний осмотр пациента, и на основании жалоб собирает анамнез. К инструментальным диагностическим исследованиям можно отнести:
- рентгенография — необходима для определения удаленных метастаз в мягких тканях и костных структурах;
- ультразвуковое исследование — позволяет точно определить, на какой стадии развития находится лимфома;
- биопсия — забор патологических частичек для дальнейшего гистологического исследования;
- спинномозговая и костномозговая пункция — нужна, чтобы определить вовлеченность костного мозга в патологический процесс;
- позитронно-эмиссионная томография — позволяет определить структуру образования и активность его клеток;
- компьютерная томография — необходима для выявления степени распространения злокачественных клеток рака;
- магнитно-резонансная томография — проводится для выявления удаленного метастазирования и вывода трехмерного изображения очага заболевания.

После того как будут получены результаты всех диагностических мероприятий доктор назначает курс лечения, основываясь на локализации лимфомы, стадии ее прогрессирования и общем состоянии здоровья пациента.
Лечение
Так как течение диффузной b-клеточной лимфомы отличается повышенной агрессивностью, сразу после обнаружения патологии нужно приступать к терапии. Обычно лечение начинается с применения низкодозированной химиотерапии, в ходе чего пациенту проводят не меньше чем шесть курсов приема цитостатических препаратов, направленных на устранение злокачественных клеток. При химиотерапии профилактика тошноты и других побочных эффектов проводится специальными препаратами. Также могут быть назначены высокие дозы химиотерапии. Оперативное вмешательство проводится не во всех случаях, но если лимфома распространилась на группу лимфатических узлов, проводится хирургическое устранение этого конгломерата.
Также врачи могут назначить лучевую терапию, подразумевающую облучение рентгеновским излучением пораженного участка. Облучение может быть назначено как в предоперационный период, так и после проведения хирургических манипуляций для устранения остаточных злокачественных клеток в зоне патологии, и предотвращения рецидива.

Если вышеописанные методы не дают ожидаемого результата, возможна костномозговая трансплантация. Также могут быть использованы гемопоэтические стволовые клетки, которые получают из эмбриональной печени. Пациент, которому будет выполнена пересадка, должен пройти иммуносупрессивную терапию как перед, так и после трансплантации.
Прогноз и профилактика
В случае раннего выявления диффузной лимфомы и проведения полноценного курса терапии прогноз для пациента вполне благоприятный. В случае когда болезнь была обнаружена уже на 4 стадии, шансы на выживание незначительные. К сожалению, из-за длительного отсутствия клинических признаков, выявление лимфомы чаще приходится на поздние этапы развития.
Так как точные причины образования крупноклеточных лимфом не изучены, специфической профилактики этой патологии нет. Чтобы снизить риск заболеваемости, стоит придерживаться некоторых правил:
- избавиться от вредных привычек;
- вести здоровый образ жизни;
- избегать контакта с вредными веществами;
- регулярно проходить медицинское обследование.
Успешность лечения во многом зависит от своевременности выявления патологии, поэтому если регулярно проходить плановое обследование в больнице, можно вовремя выявить недуг, что значительно увеличит шансы на выздоровление.
rakuhuk.ru
Симптомы, признаки, стадии и лечение диффузной В-крупноклеточной лимфомы

Вера Фомина
Наши женщины настолько суровы, что пьют чай для похудения вместе с тортом!
calendar_today 30 января 2017
visibility 326 просмотров
Лимфома b представляет собой злокачественное образование, поразившее лимфатическую систему больного. При данной патологии новообразования располагаются, как на самих лимфоузлах, так и на сторонних органах.
Крупноклеточная лимфома также относится к онкологическим аномалиям и делится на несколько видов:
- Ходжкинская лимфома;
- Неходжкинская.
Перерождения, происходящие в тканях лимфы при этом виде рака, разнятся по своей составляющей. Потому и терапия этих форм различается. Для эффективной борьбы с болезнью необходимо получить точный диагноз, по которому будет составлена схема лечения.
Симптомы
Диффузная б клеточная лимфома часто поражает людей от 25 до 40 лет. Лимфома b проявляется кашлем, отдышкой, дисфагией, отеками в область шеи, лица, головокружениями. Все остальные подтипы В клеточной лимфомы имеют аналогичные признаки, но у каждого больного выражаются они по своему.
Крупноклеточная лимфома имеет следующие признаки:
- Лимфатические узлы увеличиваются слишком быстро;
- Температура тела в течение дня выше нормы;
- Вялость, сонливость;
- Излишнее потоотделение;
- Масса тела резко уменьшается;
- Частые вирусные и простудные заболевания;
- Проблемы в работе желудочно-кишечного тракта.
Если болезнь проникла в брюшину, за грудину, то появляются проблемы с дыханием, боли в поясничном отделе, ощущение тяжести в животе.
- Симптомы общего недомогания выглядят так:
- Возникают проблемы с запоминанием;
- Появляется кожный зуд;
- Возникает лихорадка;
- Пропадает возможность полноценно работать;
- Донимает сильный кашель;
- В груди ощущается дискомфорт.
Признаки неходжкинской внутрисосудистой диффузной в крупноклеточной лимфомысостоят в следующем:
- Слабость;
- Паралич конечностей, лица;
- Сильный болевой синдром головы;
- Проблемы со зрением;
- Равновесие нарушается;
- Сильная потеря в весе;
- Появляются воспалительные участки на теле.
Когда крупноклеточная лимфома находится в начальной стадии, то аномалия не имеет никаких признаков. По этой причине на этом моменте необходимо провести рентгенодиагностику. Отрицательная черта патологии в том, что она проходит в брюшную полость, достигает брыжеечных узлов, таза. И пока образование будет увеличиваться в размерах, симптомы будут отсутствовать.

Из — за проблем с ЖКТ, больной будет быстро насыщаться едой, у него будут частые болевые симптомы в области живота. Может наблюдаться ректальное кровотечение и прободение. Кожа вся покроется сыпью. В случае, когда болезнь дошла до костей, их функциональность значительно снизится, связано это с сильными болями. Около 75% пациентов мучаются болями в печени, значительно меньше патология поражает яичники и яички, молочные и слюнные железы, надпочечники, глазницы и головной мозг.
Крупноклеточная диффузная лимфома считается самой распространенной неходжкинского типа. Лимфоциты бета – клеточные представляют собой белые клетки, которые отвечают за борьбу с инфекциями организма. Когда происходит сбой в здоровье человека, то начинает происходить выработка аномальных B –лимфоцитов, из которых и развивается данная опухоль. Диффузная крупноклеточная В клеточная лимфома относится к разнородным или гетерогенным болезням. Ею болеют сорок процентов взрослого населения. По МКБ диффузная лимфома б размещена в отдельной категории и имеет свое индивидуальное строение, клиническое течение.
Классификация
Классификация лимфом б по МКБ включает в себя:
- Диффузную мелкоклеточную лимфому;
- ДМЛ с расщепленным ядром;
- Смешанные диффузные лимфомы;
- Диффузную в крупноклеточную лимфому;
- Иммунобластому;
- Ратикулосаркому;
- Лимфобластому;
- Недифференцированную;
- Лимфому Беркета;
- И другие, неуточненные виды лимфом б.
Диффузные в в клеточные и крупноклеточные лимфомы делятся на подвиды:
- Внутрисосудистая диффузная крупноклеточная неходжкинская лимфома б;
- Первичная крупноклеточная лимфома В – клеток средостения;
- Кожно-первично-диффузная b-клеточная лимфома, поражающая дерму нижних конечностей;
- ДКВЛ, сопровождающаяся вирусом Эпштейна – Барра;
- Лимфома, возникшая на фоне воспалительных процессов;
- В клеточная лимфома маргинальной зоны.
Классификация болезни по международным показателям выявила, что аналогов диффузных КВЛ нет. Патология развивается на фоне имеющейся лимфомы или сама по себе.
- Зарождение болезни из малых лимфоцитов или хронического лимфолейкоза;
- Задействована клетка зоны мантии;
- На фолликулярном фоне.
Стадии болезни по мкб определяются по силе поражения лимфоузлов, количества пострадавших органов и тканей.
Стадии ДКВЛ
Стадии диффузной лимфомы:
- 1 стадия – лимфоузлы поражены на одной стороне туловища и принадлежат они к одной группе;
- 2 стадия – имеется поражение лимфатических узлов нескольких групп над диафрагмой и ниже;
- 3 стадия – с двух сторон диафрагмыимеется поражение ЛУ;
- 4 стадия – за пределами лимфосистемы охвачены внутренности, раковые клетки появляются в печени, костном и головном мозге, легких.
Важно! Неходжкинская диффузная лимфома растет быстро и имеет агрессивную форму. По этой причине, для того, что бы болезнь не переросла в последнюю стадию, необходимо проводить клинические анализы, плановое обследование.
Диагностика
Несмотря на то, что патологии такого вида свойственно быстро развиваться, активно расти, современная медицина в лечении онкологии сделала крупный скачек вперед и гарантирует благополучный исход болезни при своевременном ее выявлении и правильно проведенной терапии. Для исследования специалистам необходимо взять часть опухоли или поврежденного лимфатического узла. Далее образцы отправляются на морфологическое и иммуногистохимическое исследование. Такой анализ позволяет с высокой точностью диагностировать болезнь и составить схему лечения.
Помимо вышеуказанного исследования, будут назначены следующие:
- Осмотр пациента;
- Анализ крови;
- Лучевая диагностика при помощи МРТ, рентгенограммы и КТ;
- Биопсия.
Прогноз
Если диагностика показала хороший прогноз болезни, то терапия проводится по распространенной схеме СНОР — это общепринятая в онкологии лечение с применением химиотерапии. Длительность терапии состоит из шести курсов. Но все это индивидуально, каждому больному может понадобиться разное количество. В случае если лечение по схеме СНОР не имеет положительного результата, то назначают химиотерапию с использованием стволовых клеток. Прогноз при этом может быть неплохим, но риск, что результат будет отрицательным, остается.
При правильном лечении В – клеточной диффузной лимфомы, прогноз выживание в первые пять лет составляет:
- У 95% больных прогноз положительный;
- 75% пациентов имеют промежуточный прогноз;
- У 60% заболевших прогноз на выживаемость неутешительный.
- Рецидив болезни происходит у 80% на первом году жизни, у 5% больных на втором.
Полного излечения при этом виде онкологии не достигается, но жизнь можно продлить на пять, десять лет. По статистике, взрослые, с диагнозом диффузная В – крупноклеточная лимфома, на сорок процентов имеют шанс жить, у детей такая возможность составляет восемьдесят процентов.
Важно! Любая болезнь имеет благоприятный исход, если ее вовремя диагностировали.
rusmeds.com
В-крупноклеточные лимфомы у взрослых > Клинические протоколы МЗ РК
По течению заболевания, прогнозу и 5-ти летней выживаемости все лимфомы можно разделить на индолентные и агрессивные. Это условное деление имеет значение в выборе терапевтической тактики. Агрессивными лимфомами принято считать: фолликулярную лимфому IIIтипа, диффузную В-крупноклеточную лимфому, первичную медиастенальную лимфому, лимфому Беркитта[2].Агрессивные неходжкинские лимфомы — это наиболее распространенный подтип НХЛ, который характеризуется быстрым темпом роста опухоли в лимфатических узлах, селезенки, печени, костном мозге и/или других органах. Другие симптомы включают лихорадку, ночное потоотделение и потерю веса.
Последняя классификация лимфопролиферативных заболеваний была опубликована ВОЗ в 2016 году (смотреть Приложение 2, настоящего КП). Данная систематизация лимфом по группам основана как на морфологических особенностях, так и с учетом генетических и иммунофенотипических особенностей (более ранние классификации были основаны только с учетом морфологических характеристик)[3].
Фолликулярная лимфома, grade III (С82.2)[1]– это моноклональная опухоль из зрелыхВ-лимфоидных клеток, происходящих из фолликулярного центра лимфатических, имеющая иммунофенотип CD20+, CD10+/-, BCL-2+, BCL-6+, CD3-, CD5-, CD23+/-, CD43-, cyclin D1-[4].
Диффузная В-крупноклеточная лимфома (С83.3)[2] – это агрессивная В-крупноклеточная лимфома, морфологический субстрат представлен центробластами, иммунобластами, клетками с многодольчатыми ядрами, клетками с полиморфными/анаплазированными ядрами в различном количественном соотношении, что определяет морфологический вариант опухоли: центробластный, иммунобластный, анапластический.
Интраваскулярная (внутрисосудистая) диффузная В-крупноклеточная лимфома (С83.3)[3]— характеризуется избирательным ростом внутрь просвета капилляров, сосудов малого и среднего калибра, что приводит к их некротическим поражениям.Один из морфологических субвариантов В-крупноклеточной диффузной лимфомы [5].
Лимфобластная лимфома (С83.5)[4] – опухоль из Т- или В-клеточных предшественников, основную часть лимфобластных НХЛ составляют Т-клеточные опухоли, с пре- и интратимической стадиями Т-клеточной дифференцировки, т.е. из клеток-предшественниц [5].
Лимфома Беркитта (С83.7)[5]— высоко агрессивная лимфома из иммунологически зрелых В-клетокс преимущественно экстранодальной локализацией.
ДВККЛ, трансформированная (83.9) – данный вид лимфомы возникает как следствие трансформации зрелоклеточных индолентных НХЛ (в частности, лимфомы из малых лимфоцитов/хронического лимфолейкоза, фолликулярной лимфомы, лимфомы из клеток зоны мантии и некоторых других)[6].
Первичная медиастенальная лимфома (С85.1)[6] — представляет собой подтип диффузной В-клеточной лимфомы, локализующийся в переднем средостении и исходящий из вилочковой железы, а физиологические представители клеток лимфомы – В-клетки тимуса. Заболевание развивается на 3-5 декаде жизни преимущественно у женщин[5],[6].
ALK+ ДВККЛ (С88.9)[7](ранее известная как ALK+ плазмо-бластная лимфома) -это опухоль, образованная резко полиморфными атипичными клетками с фенотипом цитотоксических Т-лимфоцитов. ALK+ крупноклеточная лимфома является очень редкой формой злокачественного лимфопролиферативного процесса и составляет менее 1% всех ДВККЛ. Морфологически представлена тремя основными вариантами: обычным («классическим»), мелкоклеточным, лимфогистиоцитарным[6].
Т-клеточная богатая гистиоцитами крупно-клеточная лимфома (С96.3)[8]— вариант В-клеточной лимфомы со значительным количеством неопухолевых Т-клеток, в то время как неопластические В-лимфоциты составляют не более 10% клеток[5].
Соотношение кодов МКБ-10 и МКБ-9:
diseases.medelement.com
симптомы, стадии и прогноз на лечение
Материалы публикуются для ознакомления, и не являются предписанием к лечению! Рекомендуем обратиться к врачу-гематологу в вашем лечебном учреждении!
Соавторы: Марковец Наталья Викторовна, врач-гематолог
В-клеточная крупноклеточная лимфома относится к неходжкинской группе заболеваний. Этот тип В-клеточных лимфом является самым распространенным, но имеются и другие формы патологии. Их особенности и способы лечения стоит рассмотреть подробнее.Такое заболевание, как B-клеточная лимфома классифицируется, как неходжкинское. Его отличительной характеристикой является стремительное развитие с образованием опухолей и метастаз. Как результат, рак быстро распространяется по организму. Именно поэтому важно как можно раньше начать эффективное лечение.

Крупноклеточная В-лимфома
Характеристики заболевания
Преимущественно патология затрагивает людей старше 40-60 лет. Количество случаев заболевания — одно из наивысших в категории лимфом. Это заболевание нередко определяется, как В-клеточная лимфома кожи. Рассмотрим характеристики болезни более подробно.
Причины развития
Суть заболевания заключается в онкологическом процессе и неконтролируемой выработке В-лимфоцитов. В результате нарушаются внутренние процессы, возникает разбалансировка иммунной деятельности, затрагиваются органы и костные структуры. Крупноклеточная В-лимфома может быть спровоцирована следующими причинами:
- радиационное облучение;
- устойчивый иммунодефицит;
- контакт с токсическими веществами;
- аутоиммунные патологии;
- антидепрессантная терапия длительного течения;
- генетическая мутация;
- отравление пестицидами.

Одна из причин такого типа лимфомы — мутация клеток
Онкологические процессы зарождаются в лимфатических узлах, а затем выходят за пределы системы, могут поражать внутренние органы и кожу, то есть развивается диффузная крупноклеточная В-клеточная лимфома. Прогноз при таком диагнозе неоднозначный. Если лечение было начато рано и использовались наиболее эффективные мероприятия, пациенту можно значительно продлить жизнь.
Симптомы проявления
Чаще всего встречается именно диффузная В-клеточная крупноклеточная лимфома. Ее течение сопровождают такие симптомы:
- ночная потливость;
- анемическая бледность;
- кровотечения;
- тромбоцитопения;
- воспаление лимфоузлов;
- субфебрильная температура;
- потеря массы тела;
- образование опухолей;
- потеря работоспособности.
Прочитайте также статью Лимфома Беркета у детей — что это такое? на нашем портале.
Важно: заболевание может развиваться на базе лимфомы другого типа, поэтому поверхностных признаков недостаточно для постановки диагноза.
По мере прогрессирования болезни от начальной до четвертой стадии, симптомы усиливаются, образующиеся опухоли начинают давить на органы, метастазы проникают во все системы, что ведет к летальному исходу.
Виды и формы
Различают несколько типов В-лимфом:
- Маргинальной зоны (МАЛЬТ). Распространение из маргинальной зоны осуществляется по слизистым тканям.
- B-крупноклеточная лимфома. Проблема зарождается в лимфоузлах, существует вероятность экстранодального развития. Диффузная В-клеточная лимфома может быть медиастинальной или анапластической. В первом случе наблюдаются склеротические и некротические процессы, а во втором — системная опухолевая деятельность.
- Фолликулярная. Наименее опасная онкологическая патология.
- Мантийноклеточная. Развивается преимущественно у пожилых мужчин.
- Мелкоклеточная. Вялотекущее заболевание, слабо поддающееся терапии. Может переродится в опухолевую лимфому быстрого течения.

Виды и особенности заболевания
Важно: диффузная крупноклеточная В-клеточная лимфома АВС типа имеет наихудший прогноз, так как отличается низкой восприимчивостью к химиотерапии.
Диагностика и лечение
Диффузная крупноклеточная лимфома может быть диагностирована посредством проведения таких исследований:
- биохимическое;
- иммунологическое;
- цитологическое;
- гистологическое;
- рентгенографическое;
- биопсическое;
- МРТ и ПЭТ;
- КТ;
- УЗИ.
Для анализов берут кровь, образцы тканей пораженной области, пунктат спинного и костного мозга.
МРТ позволяет проанализировать состояние внутренних органов
В первую очередь диффузная B-клеточная лимфома лечится посредством прохождения полихимиотерапии. Для нее используют цитостатики и некоторые другие группы препаратов. Если ситуация запущенная, требуется вспомогательная лучевая терапия.

Для лечения применяют лучевую терапию
Радиотерапия может выступать как подготовка для хирургического вмешательства, а именно пересадки костного мозга. Так как облучение приводит к гибели не только раковых клеток, но и угнетению кроветворных структур, при одновременном сохранении риска развития рецидива, трансплантация является единственным выходом.
В целом, при диагнозе В-клеточная лимфома, прогноз достаточно благоприятный с показателем около 94-95% выживаемости. При осложненных формах болезни и неблагоприятном прогнозе процент выживаемости составляет около 60%, но сохраняется вероятность развития рецидива в пятилетний период.
Рекомендуем изучить похожие материалы:
- 1. Лимфома средостения
- 2. Причины наследственной серповидно-клеточной анемии
- 3. Лимфома Беркута у детей — что это такое?
- 4. Лимфома Ходжкина — заболевание, диагностика и прогноз на выздоровление
- 5. Симптомы Т-клеточной лимфомы, её виды и методы лечения
- 6. Диагностика фолликулярной лимфомы и её лечение
- 7. Классификация неходжкинских лимфом и как проходит лечение
moyakrov.ru
Как протекает и лечится диффузная в-крупноклеточная лимфома
Одной разновидностью неходжкинских лимфом является ее диффузная форма В-крупноклеточного типа. Патология отличается высокой уровнем злокачественности и активным ростом метастаз. Как правило, она поражает людей в возрасте 40–50 лет.
Определение
Диффузная лимфома представляет собой поражение лимфатической системы злокачественного характера, при котором клетки, отвечающие за иммунную защиту, начинают бесконтрольно продуцировать В-лимфоцитарные структуры. Патология может развиваться в качестве самостоятельного заболевания, или выступать в виде перерожденного образования из доброкачественных форм.

Виды
Для крупноклеточных лимфом характерна различная первичная локализация. В зависимости от этого, различают несколько основных форм заболевания:
- Маргинальной зоны. Основным местом локализации данного вида лимфомы является брюшная полость. Отличительной особенностью патологии является то, что она может протекать бессимптомно, до тех пор, пока опухоль не разрастется до объемных размеров.
- Крупноклеточная. Поражает, в основном, шею и органы, расположенные в области груди. Заболевание характеризуется увеличением региональных лимфатических узлов и их болезненностью. Патология отличается выраженной симптоматикой, которая характерна для заболеваний органов дыхания.
- Фолликулярная. Поражает область малого таза, спины и шеи. Отличается ранним проявлением специфических и общих симптомов, сопровождающихся резким повышением температуры тела.
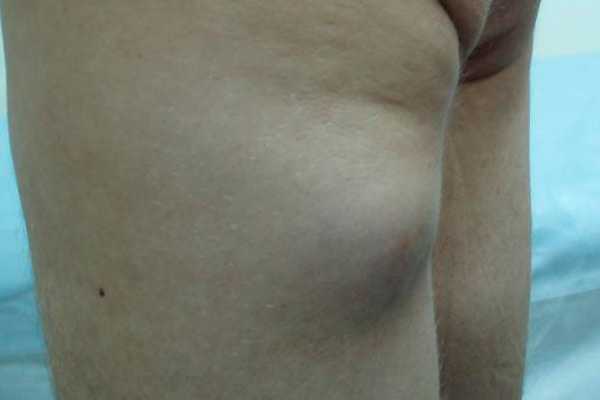
- Диффузная крупноклеточная В-клеточная лимфома. Данный вид является самым распространенным и диагностируется у 1/3 пациентов, с диагнозом неходжкинская лимфома. Характеризуется образованиями на кожных покровах, которые могут быть в виде бляшек или язв.
Подробное описание
Являясь самой распространенным видом патологии, диффузная В-клеточная опухоль отличается наиболее высокой степень злокачественности. Патология развивается путем распространения атипичных лимфоидных клеток, субстрат которых напоминает В-лимфоциты активированного типа.
Они отличаются высокой экспрессией общих и активированных антигенов. Чаще всего, опухоль развивается из В-лимфоцитов тимуса. Патология поражает, в основном, людей пожилого и среднего возраста.
У детей она диагностируется в 1,2% случаев. В детском возрасте и до 25 лет, опухоль имеет свойство обширно разрастаться на прилегающие ткани и органы, но не предрасположена к метастазированию.
Очаги разрастания диффузной В-крупноклеточной опухоли локализуются в лимфосистеме шейного или брюшного отдела. По мере развития опухоли, отмечается ее экстранодальное разрастание с поражением кожных покровов, органов ЖКТ, малого таза, щитовидной железы и головного мозга. На более поздних стадиях наблюдается образование вторичных опухолей в печени, легких и почках.
В-клеточный тип диффузных лимфом отличается инфильтрационным типом роста, при котором опухоль прорастает в сосуды, нервы, ткани дыхательных органов и костную ткань, приводя к их разрушению. На поздних стадиях отмечается тяжелое поражение костного мозга и лейкемизация.
Из-за высокого уровня злокачественности, заболевание отличается выраженными симптомами даже в начале заболевания. Благодаря этому, патологию часто диагностируют уже на I и II стадиях.

Формы
В зависимости от проявления клинической картины, различают несколько форм диффузной лимфомы:
- Медиастинальная. Для нее характерно диффузное прорастание в ткани и органы атипичной клеточной лимфоидной структурой. Выражается наличием множественных внутренних очагов некротического распада тканей и выраженным склерозом стромального типа.
- Анапластическая. Относится к системным формам, проявляющихся увеличением удаленных друг от друга групп лимфоузлов. Для нее характерно быстрое распространение на костную ткань, кишечник, селезенку или печень. В связи с высокой скоростью распространения вторичных опухолей, данная форма отличается высокой степенью летальности.
Из клеток мантийной зоны. Поражает, в основном, мужчин после 60 лет. Данный тип лимфомы отличается медленным развитием и ограниченным метастазированием. На ранних стадиях, патология проявляется лишь общими или системными симптомами.
Поэтому она чаще всего выявляется при обследованиях сопутствующих заболеваний. Несмотря на пассивность течения заболевания и эффективность лечения, выживаемость таких больных в течение 5 лет, составляет всего 6%.
- Маргинальная. Образуются в маргинальной зоне, быстро распространяясь по тканям лимфосистемы в отделы ЖКТ, щитовидную железу, костную ткань. Основная категория заболевших людей относится к пожилому возрасту.
Причины
Существуют множество причин, которые могут спровоцировать развитие опухоли диффузного В-крупноклеточного типа:
- наследственность;
- аутоиммунные патологии различного типа: рассеянный склероз, сахарный диабет, Витилиго и др.;
- пересадка почек;
- замена стволовых клеток;
- иммунодефицитные состояния;
- наличие герпесной инфекции;
- гепатиты;
- регулярное воздействие канцерогенных веществ;
- поражение вирусом Эпштейн-Барра;
- хронические патологии ЖКТ, при длительном отсутствии поддерживающей терапии;
- радиационное облучение;
- трансгенные мутации: моносомия, трисомия;
- длительная антидепресантная терапия.
Симптомы
Появление диффузной крупноклеточной опухоли сопровождается общими симптомами, к которым относятся:
- резкая потеря веса;
- ночная потливость;
- слабость;
- чрезмерная и быстрая усталость
- постоянное увеличение температуры тела, значение которой может варьироваться от небольших перепадов, до устойчивых высоких показателей;
- отечность лимфоузлов;
- бледность кожных покровов, которая обуславливается железодефицитной анемией.
В зависимости от формы патологии, по мере ее развития появляются новые специфические симптомы:
- При медиастальной форме появляется отдышка, приступы удушливого кашля, тяжесть и болезненность в области средостения. На фоне вовлечения в процесс поражения органов дыхания развивается дыхательная недостаточность.
- Анапластическая форма характеризуется поражением органов ЖКТ, поэтому увеличение опухоли сопровождается симптоматикой общих патологий желудка или кишечника. Появляется быстрое чувство насыщения, тошнота или рвота, изменение стула. В дальнейшем появляются боли в области ЖКТ и кровоточивость. При аппаратном обследовании отмечается сужение просветов органов.
Опухоль, развивающаяся из клеток мантийной зоны, проявляется различными симптомами в зависимости от пораженного органа. При поражении селезенки отмечается ее увеличение.
В дальнейшем, поражаются органы ЖКТ, что проявляется нарушением их работы и появление тошноты, запоров. При вовлечении в процесс легких наблюдается постоянная отдышка и сильный кашель.
- Маргинальная форма сопровождается увеличением селезенки и постоянной тяжестью в правой стороне подреберной части. Также, может присутствовать тошнота и рвота.

Диагностика
Для диагностирования данного вида заболевания, применяют следующие методы:
- Рентгенография. Позволяет определить наличие удаленных метастаз в костных и мягких тканях;
- Лимфоузловая биопсия. Представляет собой забор патологического материала, для изучения наличия раковых клеток и их характера;
- УЗИ. Предназначено для определения размеров образования;
- Костномозговая и спинномозговая пункция. Производится для определения вовлечения в раковый процесс костного мозга;
- ПЭТ. Позволяет увидеть не только структуру опухоли, но и рассмотреть активность ее клеток, а также клеток тканей вокруг образования;
- КТ. Предназначен для послойного определения структуры новообразования и выявления степени его распространения;
- МРТ. Выдает трехмерное изображение пораженных и здоровых тканей и выявляет удаленные метастазы.
В этом видео информация про диагностику и лечение болезни:
Лечение
Для лечения диффузной липомы В-крупноклеточного типа, применяют несколько стандартных методов:
- Лучевая терапия. Представляет собой облучение пораженной области рентгеновскими лучами. Применяется при ранних стадиях заболевания с дозой облучения не менее 40 Грей, при этом лучи направляются точечно, непосредственно на опухоль.
- Полихимиотерапия. Также как и лучевая терапия применяется для первой и второй стадии заболевания. На первой стадии проводят не менее 3 курсов терапии с использованием Блеомицина, Доксорубицина, Дакарбазина, Винбластина. Для второй стадии показано 6 курсов с применением Онковина, Доксорубицина, Циклофосфана.
- Химиотерапия. Представляет собой высокодозное лечение с использованием собственных стволовых клеток пациента.
Костномозговая пересадка. Используется при неэффективности других методов. Для пересадки берут костный мозг от доноров, полученный через аспирацию подвздошной кости или грудины. Также, могут быть использованы гемопоэтические стволовые клетки, полученные из эмбриональной печени.
Введение костного мозга проводят внутривенно. Это обеспечивает полную приживаемость вводимых клеток. Костная пересадка сопровождается иммуносупрессивной терапией, которая включает препараты: преднизолон, циклофосфамид и азатиоприн.

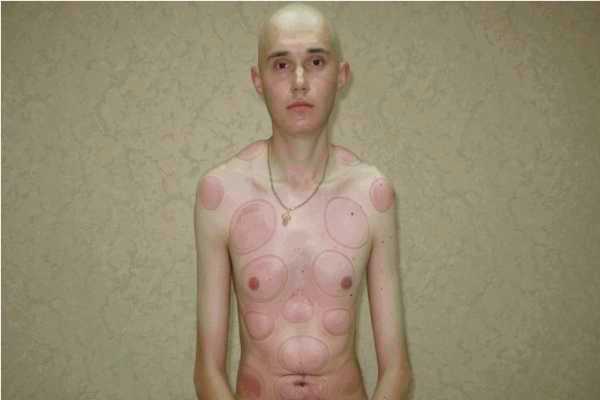
Фото запущенной стадии
Прогноз
Выживаемость пациентом при диффузной лимфоме ранних стадий составляет 95%.Основная особенность данного заболевания в том, что при отсутствии полной ремиссии, рецидивы наступают в 50% случаев.
Лечение на более поздних стадиях дает благополучные результаты только в 60% случаев. Но за 5 лет общая выживаемость от этого числа составляет всего 30%. При отсутствии лечения, патология быстро прогрессирует, что приводит к летальному исходу в течение нескольких лет у 97% заболевших.
Отзывы
Отзывы пациентов, показывают, что при своевременном обращении лимфома В-клеточного типа хорошо поддается лечению.
Предлагаем и вам поделиться своим отзывом о данном заболевании и особенностях его протекания, в комментариях к данной статье.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
stoprak.info